阿魏酸糖酯合成的研究进展
周 静,王 静,孙宝国
(北京工商大学食品添加剂与配料北京高校工程研究中心,北京100048)
阿魏酸糖酯合成的研究进展
周 静,王 静*,孙宝国
(北京工商大学食品添加剂与配料北京高校工程研究中心,北京100048)
阿魏酸糖酯类由于具有特殊的两亲结构以及在人体内起到的生理活性而广泛应用于医药、食品、化妆品等行业。综述了阿魏酸糖酯的化学和生物法合成,并比较了两者的优缺点,指出优化合成方法成为阿魏酸糖酯合成的研究热点。
阿魏酸糖酯,直接酯化法,酰氯法,DCC法,生物法
Abstract:Feruloylated glycosides are widely used in many commercial applications such as health care products and non-ionic surfactants in pharmaceuticals,cosmetics and food industries for their special amphipathic structures and physiological activity.The chemical and biological syntheses of feruloylated glycosides were described in this review,and the advantages and disadvantages of the two methods were compared.At present,the focus on the research that was how to improve the synthesis method,which was also pointed out in this review.
Key words:feruloylated glycosides;direct esterification method;carbonyl chlorides method;DCC method;biological syntheses
阿魏酸(Ferulic Acid,FA)是植物界天然存在的一种酚酸,1866年其活性化合物首次从伞形科植物阿魏中分离获得。在植物中阿魏酸主要通过酯键与细胞壁多糖和木质素交联或自身酯化,或醚化形成双阿魏酸,从而构成细胞壁的一部分[1]。阿魏酸糖酯(feruloylated glycosides)是阿魏酸羧基与糖中不同位置上的糖羟基酯化而形成的一类化合物。研究发现,阿魏酸具有活血化瘀、调节血脂、抗血栓、抗氧化、抗血小板聚集等功能[2],同时由于其中的酚羟基是优良的氢原子或电子的给予体,对能引起生物组织膜因产生过氧化作用而导致结构和功能损伤的过氧自由基、羟自由基具有明显的清除作用[3]。阿魏酸能被人体吸收并易于从尿中排出,不会在体内累积[4],因此在医学上有很高的应用价值。但是阿魏酸分子中的烷烃较短,含有双键,导致其亲水性较强,脂溶性较差,影响到其在体内的转运和利用,所以增大脂溶性一直是阿魏酸结构改造的重点[5],对阿魏酸进行修饰引起了研究人员的极大关注[6]。研究证实阿魏酸的一些衍生物表现出比阿魏酸更强的活性,因此合成生物活性更高的阿魏酸衍生物成为研究的重点,报道表明阿魏酸衍生物比阿魏酸具有更强的活性和较低的毒性[5,7-8]。Ou等[9]发现,阿魏酸糖酯的体外抗氧化能力显著高于阿魏酸和维生素C。阿魏酸,化学名称为4-羟基-3-甲氧基苯丙烯酸,其结构如图1所示,有顺式和反式两种[10],顺式为黄色油状物,反式为白色至微黄色斜方结晶,熔点为174℃;水溶性差,溶于热水、乙醇、乙酸乙酯和氯仿,微溶于乙醚,难溶于苯和石油醚[11-12]。阿魏酸分子中的活性基团有烯键、芳环、酚羟基和羧基,烯键能发生亲电加成反应生成醇、烷烃和卤化物等,芳环可以通过亲电取代反应引入卤素、硝基和磺基等,酚羟基可以通过中和、烷基化和酯化反应生成盐、醚和酯,羧基可以生成盐、酯、酰胺、酸酐,还能通过酰氯化生成酰氯[13]。阿魏酸糖酯类衍生物是将阿魏酸以酯键的形式引到糖的母体上的,通过这种结构修饰可以改善阿魏酸的脂溶性,提高其稳定性,并通过阿魏酸和糖之间可能存在的协同作用来提高修饰物的选择性和药效作用。目前阿魏酸糖酯的合成采用化学法和生物法。
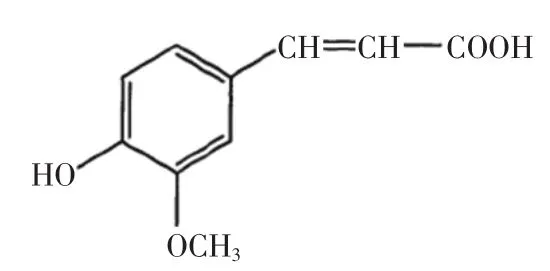
图1 阿魏酸的结构Fig.1 The structure of Ferulic Acid
1 化学合成法
阿魏酸糖酯的化学合成法主要有直接酯化法、酰氯法和二环己基碳二亚胺(DCC)催化法,其中酰氯法和DCC催化法是目前最常用的方法。
1.1 直接酯化法
直接酯化法是指阿魏酸在酸的催化下和糖中过量的羟基加热回流生成糖酯和水,达到反应的平衡。
虽然直接酯化法简单易行、反应迅速,但由于该反应为可逆反应,所以产率较低。为提高产物的转化率,生产中常采用溶剂共沸法,即在反应体系中加入与原料不反应的共沸试剂,如苯、甲苯等与水形成共沸体系,反应生成的水与共沸剂一起蒸出,经油水分离器两者分离,共沸剂返回反应体系继续以上循环,从而促使平衡向生成酯的方向移动。在直接酯化的反应体系中,通常采用硫酸、路易斯酸、对甲苯磺酸等质子型催化剂。近年来,阳离子交换树脂类催化剂因其反应条件温和、副产物少、产物后处理简单、不腐蚀设备[14],逐渐取代了质子型催化剂,促进了直接酯化法的推广和应用。
蓝志东等[15]以溶解在二甲亚砜中的阿魏酸和淀粉为原料,在对甲基苯磺酸的催化作用下合成了阿魏酸淀粉酯。对合成产物进行取代度分析,发现所合成的阿魏酸淀粉酯属于低取代度的产品,符合工业上生产重要变性淀粉的要求。对合成产物进行酶水解分析,发现阿魏酸淀粉酯具有抗α-淀粉酶水解的能力,减少了在肠胃中被淀粉酶水解的机会,能够通过胃部进入结肠,降低了结肠癌病变的可能性。张强等[16]以茯苓多糖为酯化剂,甲苯、二甲亚砜为共沸剂合成了阿魏酸茯苓多糖,并对其抗氧化性进行对比研究。结果显示,一定浓度下合成的阿魏酸糖酯抗氧化能力优于阿魏酸。
直接酯化法是可逆反应,可尝试通过加快反应速率、促进化学平移来改进合成方法,提高产率。如着重对催化剂进行研究,改进催化剂的专一性,增加其催化效率;开发高吸水性复合材料,提高吸水效率,促进反应平衡右移。同时,共沸体系中的有机溶剂多为含苯环类试剂,易造成严重的环境污染,今后的研究方向应尝试寻找对环境污染较小的有机甚至是无机试剂作为共沸试剂。
1.2 酰氯法
酰氯法是先将阿魏酸转化为酰氯,再与糖缩合生成酯的方法,其反应机理为亲核加成消除过程。酰氯属于亲核试剂,可由羧酸与三氯化磷、五氯化磷或氯化亚砜反应制得,其中氯化磷的沸点较低,适合于制备低沸点酰氯;氯化亚砜制备酰氯的反应其副产物都是气体,容易分离和提纯[17]。
酰氯法具有反应条件温和、所需的时间相对较短、后期处理简单、产率较高等优点。虽然酰氯法存在一些问题,比如酰氯需要现制现用,反应中必须保持无水干燥,产物纯化麻烦,合成路线偏长等,但是酰氯法的应用仍然较多。
李爱军等[18]先用三氯化磷将阿魏酸酰氯化,后与淀粉反应,成功地合成了淀粉阿魏酸酯。研究人员对合成的产物进行结肠微生物离体发酵实验,发现它不易被淀粉酶水解,在结肠微生物作用下,阿魏酸的释放率和释放速度大大高于麦麸膳食纤维,阿魏酸释放后对亚硝酸盐具有较强的清除能力,进而会减少结肠癌病变可能性。再者,淀粉阿魏酸酯能促进保加利亚乳杆菌和嗜热链球菌的繁殖,并使之在贮藏过程中维持较高的活力。
Richard等[19]采用酰氯法成功地合成甲基-6-氧-阿魏酰基-β-D-吡喃半乳糖苷、甲基-6-氧-阿魏酰基-β-D-吡喃葡萄糖苷、甲基-6-氧-阿魏酰基-β-D-呋喃阿拉伯糖苷,转化率分别达到95%、90%、73%。Petri等[20]利用酰氯法合成了一系列甲基阿魏酰基糖苷。Pauli等[21]将阿魏酸酰氯与阿拉伯糖基木聚糖和葡糖基木聚糖共价结合后脱保护基合成阿魏酰阿拉伯糖基木聚糖酯和阿魏酰葡糖基木聚糖酯,并从铜调节的人体低密度脂蛋白的抗氧化性能上将阿魏酸和结合态阿魏酸进行比较,结果发现,阿魏酸糖酯优于阿魏酸。
酰氯剂会与体系中存在的水反应失去亲和性,因而酰氯法要求反应体系无水,这对反应环境的要求较高,且反应较剧烈,很大程度上限制了酰氯法的应用。为使反应成功进行,除在反应前对试剂进行干燥处理外,还可在反应体系中加入分子筛,以保持体系的干燥状态。同时反应过程中产生大量二氧化硫,易造成环境污染,在实际生产中应注意尾气处理。
1.3 DCC催化法
DCC催化法是指阿魏酸羧基先被1,3-二环己基碳二亚胺(DCC)活化,再与糖羟基反应生成酯的反应。其作用机理如图2所示。
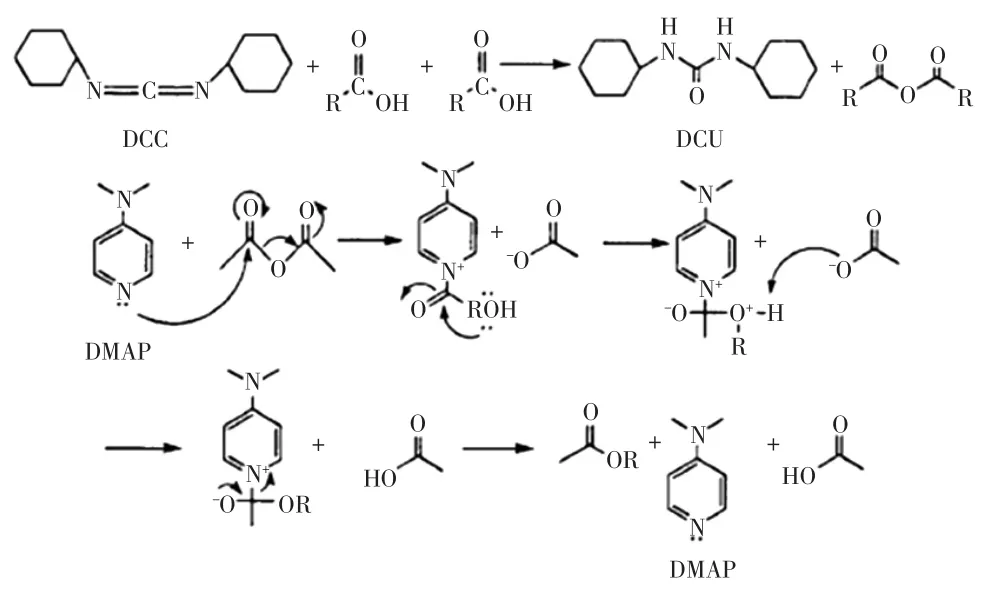
图2 DCC反应机理Fig.2 The mechanism of DCC
DCC与羧酸反应,两分子羧酸脱水生成酸酐,DCC得水生成1,3-二环己基脲(DCU),然后4-二甲氨基吡啶(4-DMAP)的吡啶氮原子进攻酸酐中的羰基碳,形成1-乙酰基-4-二甲氨基吡啶盐,其正离子与第一步产生的乙酸根离子形成一个不紧密的离子对。接着醇羟基的氧原子亲核进攻与吡啶相连的乙酰基碳原子,乙酸根离子立即夺取醇羟基的氢,氧把吡啶挤出去产生酯,同时重新生成4-DMAP,进行下一个循环[22]。
DCC是一种脱水剂,常用于催化酯化、酰胺化等反应[23],能减少体系中产物水的量,有利于反应向生成产物的方向进行。催化剂4-DMAP是超强亲核的酰化作用催化剂,其结构上供电子的二甲氨基与母环(吡啶环)的共振,能强烈激活环上的氮原子进行亲核取代反应,其活性约为吡啶的4~6倍[24]。该催化剂用量小,反应条件温和,在极性、非极性有机溶剂中均可进行,反应时间短,收率高,副反应少,三废少,因而被称为“超级催化剂”[25],近年来在酰化、烷基化、醚化、酯化及酯交换等多种反应中有广泛的应用。
缩水剂DCC、催化剂4-DMAP对高位阻、低反应活性的底物具有较高的活性,反应条件温和,可在低温下快速酰化,避免了反应过程中原料和产物的消旋化[26],溶剂选择广泛,操作简便,后处理简单,是在活性较弱的寡糖羟基上引入较大酰基的一种十分有效的方法。
Sonia等[27]以微晶纤维素和阿魏酸为原料,在DCC、DMAP的作用下均相合成了阿魏酰基微晶纤维素,并用抑制小鼠肝脏微粒体膜的脂质过氧化实验来评估产物的抗氧化能力,结果发现合成的产物是强的抗氧化剂。
与直接酯化法、酰氯法相比,DCC法对反应条件的要求较低,反应体系中同时存在脱水剂和催化剂,具有较高的反应活性,反应适用性强,因而该法可能会成为今后化工业上合成阿魏酸糖酯的主要方法。
2 生物合成法
由于传统的化学法进行得阿魏酸酯化修饰往往需要进行繁琐的保护和去保护,选择性差,有些反应条件苛刻,常需在高温、高压下进行,副反应多,对于某些糖很难实现。1980年以来,国内外研究人员开始研究应用生物手段合成非天然手性有机化合物。1984年生物催化剂和介质工程的研究取得了突破性进展,极大地推动了生物反应合成新化合物研究领域的发展。
选择性生物合成作为第三代生物技术的重要组成部分,是国际科技发展的前沿。利用生物反应,许多结构复杂的生物活性物质得以人工合成从而进行工业生产。该法不仅对结构具有化学选择性和非对映异构体选择性,而且还有严格的区域选择性和对映体选择性。
阿魏酸糖酯的生物合成法是指用生物技术来模拟植物体内的酶催化合成糖酯。目前,利用生物技术合成阿魏酸糖酯主要有生物酶催化和微生物细胞发酵两种方法。
用于催化合成阿魏酸糖酯的酶是阿魏酸酯酶。阿魏酸酯酶(E.C.3.1.1.73,Ferulic acid esterases,FAE)又称肉桂酸酯酶,是一类广泛存在于谷物中的胞外酶,1991年Faulds等首次从橄榄色链霉菌中分离得到。阿魏酸酯酶属于水解酶类的羧酸酯水解酶,是一种能打断阿魏酸甲酯、低聚糖阿魏酸酯和多糖阿魏酸酯中的酯键,将阿魏酸游离出来的酶[28-29]。根据其对人工合成的肉桂酸甲酯的专一性,阿魏酸酯酶可分为A、B、C、D四类[30]。A类阿魏酸酯酶的底物多含有甲氧基,特别是诸如阿魏酸和芥子酸之类含有间位甲氧基的酚类衍生物以及苯环上含有较大取代基的疏水性物质,大多数的A类阿魏酸酯酶只能催化水解O-5上的阿魏酸酯键。B类阿魏酸酯酶主要催化水解含有一到两个羟基的底物,比如p-香豆酸和咖啡酸,且能催化O-5或O-2的阿魏酸酯键。C类和D类阿魏酸酯酶对人工合成的羟基肉桂酸表现出范围较广的专一性,能够催化上述两种酯键,两者只是在催化分离5-5’阿魏酸二聚体的能力上有较小的差异。
阿魏酸酯酶可用于催化在水-有机溶剂混合体系或微乳液中发生的肉桂酸的酯化或酯基交换反应[31-32],而且生成阿魏酸糖酯的酯化反应只能用阿魏酸酯酶进行催化。从湿热侧孢霉中分离得到的C类阿魏酸酯酶被证明可以催化阿魏酸基团转移到L-阿拉伯糖和L-阿拉伯二聚糖上,实现了碳水化合物阿魏酰基化[33]。另外,Topakas等[34]在以己烷、丁醇和水的混合溶液为溶剂、嗜热侧孢霉阿魏酸酯酶的催化作用下将阿拉伯糖和阿魏酸进行了立体选择性酯化,反应得到了阿魏酸阿拉伯糖酯类衍生物,产率达到40%。
微生物细胞发酵生成糖酯又称整细胞生物转换合成,是指由活性细胞中多种酶联合起来进行连续的酶催化作用从而获得目的产物,这个过程经工业发酵来实现。通过发酵合成的糖酯化合物具有增强免疫、抗氧化、抗肿瘤性能,在医药行业备受瞩目,体现出了强于化学法的独特优势[35]。
以酶为催化剂进行选择性酯化可制得预期结构的糖酯,本质上属于有机合成,只是用生物酶替代了传统的有机试剂或催化剂。而发酵法得到的产物比通过其他方法获得的产物结构更为复杂,属于生物合成过程。所以,两者既存在差异,也具有一定的互补性。
目前,生物合成法的研究工作主要集中在实验室阶段,如何在保持酶活和酶立体选择性的基础上尽可能找到合适的反应体系,大大提高反应速率和转化率,将其应用到工业生产是我们亟待解决的难题。
3 展望
经过糖基修饰获得的阿魏酸糖酯类衍生物具有抗炎、抗氧化、清除自由基等作用,与阿魏酸相比,某些糖酯表现出更强的活性、较低的毒性和更强的适应性,在医药、食品、化妆品等方面有广阔的应用前景,所以阿魏酸糖酯的合成具有重要的理论意义和实际应用价值。
生物合成和化学合成的产品性能相似,但是相对于化学合成法的弱选择性,生物法可以以廉价的可再生材料为原料得到特定的糖酯类衍生物,且产量较高;可生物降解,不会造成二次污染;无毒或低毒;合成的糖酯一般不致敏,可用于化妆品和食品添加剂;可以利用工业废物进行生产,用于生物环境治理;由于结构多样,可能会在特殊领域得到应用。
虽然生物合成法在生产上更环保,合成的产物在应用上更广泛、性能上更优越,但是酶的活性不能得到充分发挥,产率不高,其经济成本约是化学合成的3~10倍,很大程度上影响了生物合成法在工业上的应用和推广。由于生物合成法代表了未来产业的发展方向,并且随着基因工程、蛋白质工程和发酵工程的发展可能使生物合成法得到优化,所以生物合成法清洁生产的优越性必将促进这一领域的突破性发展,所有这些都决定了将来阿魏酸糖酯的研究和生产必将在化学合成和生物法合成二者的优势互补中强势迈进。如何改进合成方法,将化学合成法、生物合成法以及其他方法进行优化结合,实现阿魏酸糖酯的安全高效生产,也成为了阿魏酸糖酯生产的研究热点。
[1]Ou Shi-yi,Zhang Jing.Antioxidant activity of enzymichydrolyzed productsfrom wheatbran[J].Food and Machinery,2005,21(6):17-19.
[2]Yu Yan-ying,Li xian-he,Cao Shu-wen,et al.Synthesis of genistein acetylferulic acid esters[J].NaturalProductand Development,2009,21(5):194-198.
[3]郑德勇,安鑫楠.植物抗氧化剂的研究概况与发展趋势[J].林产化学与工业,2004,24(3):113-118.
[4]Choudhury R,Srai SK,Dehnam E,et al.Urinary excretion of hydroxycinnamates and flavonoids after oral and intravenous administration[J].Free Radical Biology Medicine,1999,27(3-4):278-286.
[5]黄华永,沈海星,郑锦鸿.阿魏酸及其类似物的合成及其清除自由基活性研究[J].中国新药杂志,2006,15(6):454-458.
[6]唐于平,段金廒,范欣生,等.芳香酸类成分在活血化瘀方中的作用介析[J].世界科学技术-中医药现代化,2008,10(4):38-42.
[7]辛嘉英,郑妍,赵冠里,等.VE阿魏酸酯的酶法合成及抗氧化的研究[J].食品科学,2006,27(10):229-232.
[8]李宝泉,李念光,冯锋.阿魏酸酯类衍生物的合成及抗血小板聚集活性[J].中国药科大学学报,2009,40(6):486-490.
[9]Ou S,Kwok K.Ferulic acid:pharmaceutical functions,preparation and applications in foods[J].Journal of Food Science and Agriculture,2004,84(11):1261-1270.
[10]丁明玉,马帅武,刘德麟.阿魏酸的稳定性及其在川芎和当归药材中的存在形式[J].中草药,2004,35(1):28-30.
[11]周彩荣,石晓华,王海峰,等.反式阿魏酸在溶解中的溶解度[J].化工学报,2007,58(11):2705-2709.
[12]赵东平,杨文钰,陈兴福.阿魏酸的研究进展[J].时针国医国药,2008,19(8):1839-1841.
[13]张岳玲,韦长梅,王锦堂.阿魏酸的合成及其分子改造研究进展[J].淮阴师范学院学报,2003,2(1):50-53.
[14]陈洁,蒋建春,徐俊明.催化酯化反应中固体催化剂研究进展[J].精细石油化工进展,2009,10(3):32-37.
[15]蓝志东.阿魏酸及其衍生物的合成研究[D].广州:暨南大学,2001.
[16]张强,张黎明.阿魏酸茯苓多糖的抗氧化活性研究[J].现代食品科技,2011,27(9):1077-1080,1089.
[17]徐克勋.精细有机化工原料及中间体手册[M].北京:化学工业出版社,2002:291-294.
[18]李爱军,包惠燕,丘立达,等.淀粉阿魏酸酯的基本特性研究[J].食品科学,2001,22(8):29-32.
[19]Richard F Helm,John Ralph,Ronald D Hatfield.Synthesis offeruloylated and p-coumaroylated methylglycosides[J].Carbohydrate Research,1992,229:183-194.
[20]Petri Kylli,Paula Nousiainen,Peter Biely,et al.Antioxidant potential of hydroxycinnamic acid glycoside esters[J].Journal of Food Science and Agriculture,2008,56:4797-4805.
[21]Pauli Wrigstedt,Petri Kylli,Leena Pitkanen,et al.Syntheses and antioxidant activity of hydroxycinnamic acid xylan esters[J].JournalofFoodScienceandAgriculture,2010,58(11):6937-6943.
[22]Alfed H,Vazken A.Direct room temperature esterification of carboxylic acids[J].Tetrahedron Letters,1978,46:4475-4478.
[23]薄采颖,毕良武,王玉民,等.DCC及其在有机合成中的应用[J].化工时刊,2007,21(10):4-6,13.
[24]刘云.5-木糖酯类衍生物的合成及其增香效应研究[D].河南:河南农业大学,2010.
[25]曹志勇,吴光华.4-二甲氨基吡啶(DMAP)在医药合成中的应用[J].精细化工原料及中间体,2010(3):10-12
[26]Chongwei Yue,Josiane Thierry,Pierre Potier.2-phenyl isopropyl esters as carboxyl terminus protecting groups in the fast synthesis of peptide fragments[J].Tetrahedron Letters,1993,34(2):323-326.
[27]Sonia Trombino,Roberta Cassano,Ermelinda Bloise,et al.Design and synthesis of cellulose derivatives with antioxidant activity[J].Macromolecular Bioscience,2008,8:86-95.
[28]Kroon PA,Garcia-Conesa M T,Fillingham IJ,et al.Release of ferulic acid dehydrodimers from plant cell walls by feruloyl esterases[J].Journal of the Science of Food and Agriculture,1999,79(3):428-434.
[29]V F Crepin,C B Faulds,I F Connerton.Functional classification of the microbial feruloyl esterases[J].Microbiology and Biotechnology,2004,63:647-652.
[30]叶建华,杨红建.微生物阿魏酸酯酶及其应用[J].中国奶牛,2007,10:28-31.
[31]Vafiadi C,Topakas E.The feruloyl esterase system of Talaromyces stipitatus:Determining the hydrolytic and synthetic specificity of TsFaeC[J].Journal of Biotechnology,2006,125(2):210-221.
[32]Giuliani S,Piana C.Synthesis of pentylferulate by a feruloyl esterase from Aspergillus niger using water-in-oil microemulsions[J].Biotechnology Letters,2001,23(4):325-330.
[33]Vafiadi C,Topakas E,Christakopoulos P.Regioselective esterase-catalyzed feruloylation of L-arabinobiose[J].Carbohydrate Research,2006,341:1992-1997.
[34]Topakas E.Sporotrihum thermophile type C feruloyl esterase(StFaeC):purification,characterization,and its use for phenolic acid(sugar)ester synthesis[J].Enzyme Microb.Technol,2005,36:729-736.
[35]Singh P,Cameotra S S.Potential applications of microbial surfactants in biomedical sciences[J].Trends Biotechnol,2004,22(3):142-146.
Research progress in syntheses of feruloylated glycosides
ZHOU Jing,WANG Jing*,SUN Bao-guo
(Beijing Higher Institution Engineering Research Center of Food Additives and Ingredients,Beijing Technology and Business University,Beijing 100048,China)
TS201.2
A
1002-0306(2012)16-0392-04
2012-01-06 *通讯联系人
周静(1987-),女,在读硕士研究生,研究方向:食品科学。
北京市科技新星项目(2008B07)。

