流出道对糖尿病患者股腘动脉腔内成形术预后的影响
谭正力 宋希涛 郁正亚
(首都医科大学附属北京同仁医院血管外科,北京100730)
下肢动脉硬化闭塞症是血管外科常见疾病,治疗方法包括传统的动脉转流术和血管腔内治疗,由于后者具有创伤小、恢复快、可重复性等优点,目前已经在临床得到广泛应用[1]。糖尿病患者最终出现周围动脉硬化病变的概率是非糖尿病患者的5~10倍[2],泛大西洋学会联盟(Trans-Atlantic Inter-Societal Consensus,TASC)指南[3]已明确将糖尿病列为重要的动脉粥样硬化危险因素。股腘动脉是下肢动脉硬化闭塞症发生的常见部位,已知流出道条件的好坏是影响股腘动脉人工血管转流术预后的重要因素;但对腔内治疗预后的影响尚无定论。北美血管外科协会[4](Society for Vascular Surgery,SVS)在推荐下肢动脉疾病评估方法的同时考虑了远端血管的分流权重及各自的病变程度,对流出道进行了细致的评价并将其量化,提出流出道条件差对股腘动脉腔内成形术的预后有不良影响,但该方法目前尚未被广泛应用。
本研究旨在应用SVS流出道评分标准,研究术后流出道病变评分对糖尿病性下肢动脉硬化闭塞症患者股腘动脉腔内成形术后一期通畅率的影响。
1 资料和方法
1.1 一般资料
回顾性分析首都医科大学附属北京同仁医院2006年1月至2010年12月期间因下肢动脉硬化闭塞症进行股腘动脉介入治疗的2型糖尿病患者37例,共41条患肢,股腘动脉病变TASCⅡ分级限于A、B级。所有患者均经内科确诊为糖尿病,收集患者一般信息、下肢动脉硬化闭塞症相关内科疾病、下肢缺血Fontaine分期、踝 -肱指数(ankle brachial index,ABI)及动脉造影资料。股腘动脉病变严重程度采用TASCⅡ分级;远端流出道病变严重程度采用SVS标准,在介入治疗完成时通过数字减影血管造影(digital subtraction angiography,DSA)进行评估。股腘动脉流出道的SVS评分标准为:对胫前动脉、胫后动脉、腓动脉赋予部位相关权重分值为1,对各条血管赋予阻塞严重程度相关权重分值为0~3(见表1)。在各条血管分别将2者相乘,然后求和,再加基础值1,即得流出道评分。
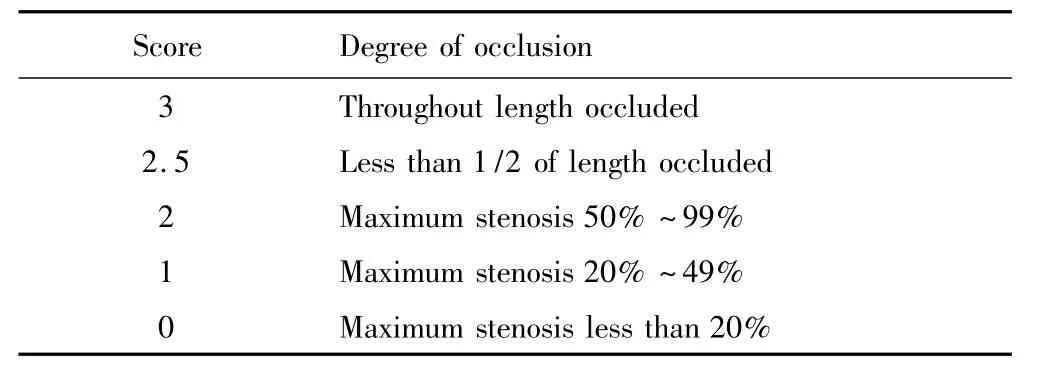
表1 流出道阻塞程度权重Tab.1 Weighting of runoff arteries-occlusion
1.2 患者入选及排除条件
1)入选条件:①有临床症状的下肢动脉硬化闭塞症患者,即间歇跛行(<100 m)、缺血性静息痛、溃疡或坏疽;②病变程度属于TASCⅡ A、B级;③无下肢动脉造影禁忌证。
2)排除条件:①有急性动脉栓塞;②既往接受髂、股腘或膝下胫腓动脉外科手术;③既往有下肢动脉外伤史;④合并免疫疾病或凝血系统异常。
1.3 治疗方法
对股腘动脉病变,均予单纯球囊扩张,当病变部位治疗后残余狭窄>30%,或出现动脉夹层时,一期植入金属裸支架(Smartcontrol,Cordis或 Maris,Invatec)。当胫前、胫后、腓动脉均已闭塞时,尽量同期实施单纯球囊扩张(Deep,Invatec),保证至少有1支通畅的动脉可直达足部。
患者于术前3 d口服氯吡格雷75 mg/d,或于手术当日顿服氯吡格雷300 mg,术后患者均长期口服阿司匹林100 mg/d,对于放置支架的患者加服氯吡格雷75 mg/d至术后6个月。所有患者的血糖、血脂、血压均经内科药物控制并定期监测。
1.4 随访
对所有符合条件的介入治疗患者进行定期随访,随访时间为术后1、3、6个月、1年,之后每年复查1次。电话通知到达随访时间点的患者来首都医科大学附属北京同仁医院复查,若患者出现下肢不适随时就诊。复查的常规内容包括患肢缺血的症状、体征、ABI。对再次出现缺血症状、体征或ABI较术后初值下降大于0.15的患者进一步行B超、CTA或DSA等影像学检查,以明确原股腘动脉介入治疗部位有无再狭窄或闭塞。随访终点定义为经治疗的股腘动脉节段发生再狭窄(管腔狭窄>50%)或闭塞。死亡及失访患者按“截尾”数据处理。
1.5 统计学方法
所有数据采用SPSS 16.0统计软件进行分析处理。应用Kaplan-Meier方法计算一期通畅率,Cox回归分析方法确定影响预后的相关危险因素。以P<0.05为差异有统计学意义。
2 结果
2.1 患者一般情况
所有患者均患有2型糖尿病,为内科确诊病例,高血压指血压大于140/90 mmHg(1 mmHg=0.133 kPa),高脂血症指总胆固醇大于5.7 mmol/L、三酰甘油大于1.7 mmol/L或低密度脂蛋白大于3.6 mmol/L,冠状动脉粥样硬化性心脏病(以下简称冠心病,存在心绞痛、心肌梗死、冠状动脉成形术或转流术病史),慢性充血性心力衰竭均经心内科专科医师确诊,肾功能不全指血肌酐浓度大于133 μmol/L。患者一般情况见表2。下肢缺血临床症状严重程度见表3,患肢TASCⅡ分级及流出道评分的分布情况见表4。
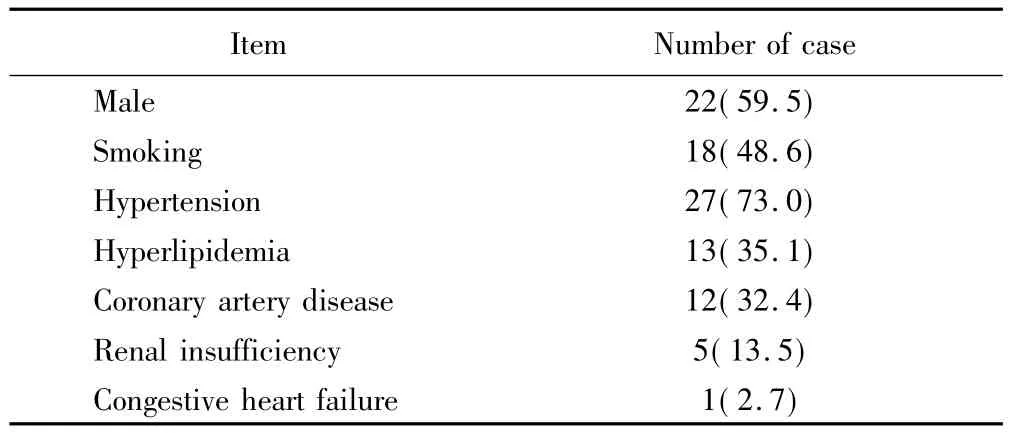
表2 患者一般情况Tab.2 Demographic information of patients n(%)

表3 下肢病变Fontaine分期Tab.3 Fontaine stage of lower extremity
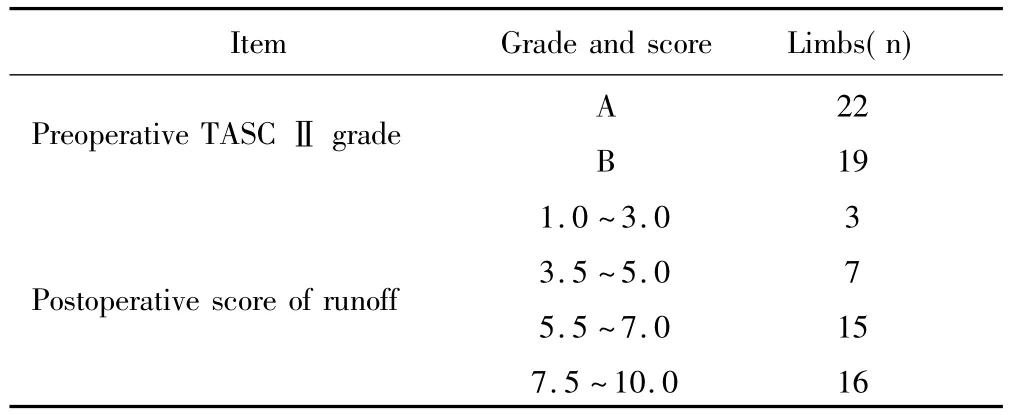
表4 股腘动脉病变解剖学分布Tab.4 Femoropopliteal artery lesions and its anatomy distribution
2.2 临床结果
41条患肢均进行了股腘动脉介入治疗,其中22条患肢(53.7%)一期植入金属裸支架,技术成功率100%,临床症状改善率93.7%,22条患肢(53.7%)成功进行膝下流出道血管球囊扩张,1例试行膝下血管扩张失败,术前 ABI平均值为0.39±0.03,术后ABI平均值为0.79±0.04。
随访时间1至48个月,中位随访时间12个月。随访率95.1%,1例患者(2.7%)因心血管疾病死亡,最后随访时间为术后 32个月;失访 1例(2.7%),最后随访时间为术后12个月。因上述2患者末次随访均未见股腘动脉再狭窄或闭塞,故按截尾数据处理。通过Kaplan-Meier方法计算,样本一期通畅率在1,3,6 个月,1,2,3 年,分别为 95.0%,92.5%,92.5%,77.4%,65.3%,45.5%,累积一期通畅率见图1。随访过程中,共4条患肢在股腘动脉闭塞后发生截肢(9.8%),其中3患肢流出道评分>7分。
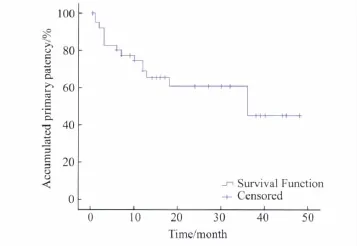
图1 累计一期通畅率Fig.1 Accumulated primary patency
Cox回归分析纳入的因素包括:流出道评分、性别、吸烟、高血压病、高脂血症、临床症状严重程度(是否属于FontaineⅢ、Ⅳ期)、TASCⅡ分级以及是否使用支架。各因素采用Wald backward模式进入Cox回归分析模型,发现只有流出道评分是影响一期通畅率的危险因素(RR=1.857,P=0.003,95%CI:1.230 ~2.806),详见表5。

表5 Cox回归分析结果Tab.5 Cox regression analysis(Wald backward model)
对所有患者根据流出道评分进行分层(流出道评分≤7与≥7.5),并行Kaplan-Meier分析,得到生存曲线(图2),Log-rank检验提示差异有统计学意义(P=0.002)。
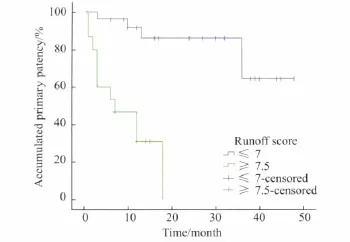
图2 流出道分组累积一期通畅率Fig.2 Accumulated primary patency of subgroup
3 讨论
本研究采用SVS评分标准,评估2型糖尿病患者股腘动脉腔内成形术后流出道评分对一期通畅率的影响。共纳入了37例患者,共计41条患肢,通过采用Cox回归分析法发现流出道评分的风险比为1.857,差异有统计学意义。说明在2型糖尿病合并股腘动脉硬化闭塞症患者中,流出道是影响股腘动脉腔内成形术预后的主要相关危险因素,流出道评分的分值越大,术后发生再狭窄或闭塞的可能性越大,一期通畅率越低。通过对流出道分层分析发现流出道评分≥7.5与<7相比,2组之间的累积一期通畅率明显不同,且结果差异有统计学意义,进一步说明了在股腘动脉成形术后,流出道条件差,预后明显不良。
我们选择糖尿病患者进行研究主要出于以下考虑:2型糖尿病与非糖尿病患者下肢动脉硬化闭塞症病变分布的特点有所不同,前者更多累及远端腘动脉、胫腓动脉及足部血管,而胫腓动脉恰恰是股腘动脉的流出道。与非糖尿病患者相比,股腘动脉成形术后,糖尿病仍会继续加重膝下流出道血管的动脉粥样硬化性病变,导致流出道恶化。
DeRubertis B G等[5]已经证实2型糖尿病既是下肢动脉硬化闭塞症重要的发病危险因素,也是影响其外科治疗效果的重要原因。因此在研究股腘动脉流出道对其介入治疗预后影响的作用时,应区分糖尿病人群与非糖尿病人群,以避免糖尿病因素对研究结果造成偏倚。
在股腘动脉腔内成形术治疗过程中,球囊在扩张狭窄或闭塞节段的同时也会因机械牵拉和压迫作用,对血管壁尤其是内膜造成损伤,并引起内膜增生,(内皮细胞和平滑肌细胞增生)以及细胞外基质的沉积。内膜增生受管腔内血流动力学影响,尤其是血流的剪切力和速度。血流剪切力越大,内膜增生越严重;而血流速度越慢,内膜增生越严重,相应的使管腔狭窄越重。流出道可影响股腘动脉腔内治疗部位的血流速度,进而影响内膜增生,最终对股腘动脉腔内成形术的预后产生影响。Heherlein C等[6]已经证实流出道条件差可促进内膜的增生。
此外,Ihnat D M等[7]提及在闭塞或再狭窄的病例中观察到流出道条件与初次治疗时相比发生了恶化。同时Salapura V等[8]也指出在股腘动脉腔内成形术后,流出道条件的恶化可降低通畅率,且早期的再狭窄或闭塞主要与初始流出道条件相关;而术后流出道条件的恶化,即流出道血管的新发病变与远期的通畅率降低有关。限于技术条件,本试验未能在所有发生再狭窄或闭塞的患者中取得造影资料,且样本量较小,故无法针对上述问题进行分析。
从本研究结果可以看出,流出道条件差与股腘动脉腔内成形术的预后相关,流出道评分越高,一期通畅率越低。通过病理生理学分析,可以看出2者存在因果关联。本研究的意义在于提示临床诊疗中应对流出道条件不良的患者加以区别对待:一方面在进行股腘动脉腔内成形术的过程中,应尽量同期改善流出道条件,降低流出道评分;另一方面在术后应对流出道评分高的患者加强随访,缩短随访间隔,及早发现治疗部位的再狭窄,争取在闭塞之前对其进行治疗。因为在进行腔内成形术时,闭塞性病变与狭窄性病变相比,前者治疗的难度增大,成功率降低且手术合并症发生率增高。
Fontaine分期反映了患肢缺血和血管病变严重程度,DeRubertis B G 等[9-11]证明重度缺血(FontaineⅢ、Ⅳ期)是降低糖尿病患者一期通畅率的危险因素。本研究发现缺血程度(FontineⅢ、Ⅳ期与Ⅱ期相比)对股腘动脉腔内成形术的一期通畅率影响无统计学意义(P=0.061,RR=2.610,95%CI:0.956 ~7.126),推测与本研究样本量过小有关,有待于增大样本量进一步考察。另外,本研究发现TASCⅡ分级(A级与B级相比)、是否使用支架、吸烟、高血压、高脂血症、性别等因素未影响股腘动脉腔内成形术后的一期通畅率。
本研究具有以下局限性:①样本量较小,会削弱某些所纳入影响因素的显著性,如上面提到的临床缺血症状,若样本量增加,其差异可能会有统计学意义。②患者就诊时病情偏重,处于FontaineⅢ、Ⅳ期的肢体所占比例较高,故更多的反映了重度缺血患者中的情况,不能完全代表轻度缺血患者中的情况。
股腘动脉流出道是影响糖尿病患者股腘动脉腔内成形术预后的主要危险因素,术后流出道评分数值越高,治疗部位再狭窄或闭塞的可能性越大,一期通畅率越低。本研究结果提示在糖尿病患者中,进行股腘动脉腔内成形术时应同期改善流出道;对于流出道条件差者,在术后应加强随访,及时纠正潜在病变,改善远期效果。
[1]Lee L K,Kent K C.Infrainguinal occlusive disease:endovascular intervention is the first line therapy[J].Adv Surg,2008,42:193-204.
[2]Dawson D L,Mills J L.Critical limb ischemia [J].Curr Treat Options Cardiovasc Med,2007,9(2):159-170.
[3]Norgren L,Hiatt W R,Dormandy J A,et al.Inter-Society Consensus for the management of peripheral arterial disease(TASC Ⅱ)[J].J Vasc Surg,2007,45:S5-7.
[4]Rutherford R B,Baker J D,Ernst C,et al.Recommended standards for reports dealing with lower extremity ischemia:revised version[J].J Vasc Surg,1997,26(3):517-538.
[5]DeRubertis B G,Faries P L,McKinsey J F,et al.Shifting paradigms in the treatment of lower extremity vascular disease:a report of 1000 percutaneous interventions[J].Ann Surg,2007,246(3):415-422.
[6]Hehrlein C,Chuang C H,Tuntelder J R,et al.Effects of vascular runoff on myointimal hyperplasia after mechanical balloon or thermal laser arterial injury in dogs[J].Circulation,1991,84(2):884-890.
[7]Ihnat D M,Duong S T,Taylor Z C,et al.Contemporary outcomes after superficial femoral artery angioplasty and stenting:the influence of TASCⅡclassification and runoff score[J].J Vasc Surg,2008,47(5):967-974.
[8]Salapura V,Blinc A,Kozak M,et al.Infrapopliteal run-off and the outcome of femoropopliteal percutaneous transluminal angioplasty[J].Vasa,2010,39(2):159-168.
[9]DeRubertis B G,Pierce M,Chaer R A,et al.Lesion severity and treatment complexity are associated with outcome after percutaneous infra-inguinal intervention[J].J Vasc Surg,2007,46(4):709-716.
[10]DeRubertis B G,Pierce M,Ryer E J,et al.Reduced primary patency rate in diabetic patients after percutaneous intervention results from more frequent presentation with limb-threatening ischemia[J].J Vasc Surg,2008,47(1):101-108.
[11]高明杰,华扬,贾凌云,等.应用超声检测糖尿病合并高血压患者大血管病变的特征[J].中国脑血管病杂志,2011,8(6):298-303.

