慢性乙型肝炎患者血清HBV DNA水平与HBsAg和HBeAg水平的相关性分析*
李筠竹 张振华 张亚飞 苏 倩 李 旭
我国慢性乙型肝炎(CHB)高发,乙型肝炎病毒(HBV)感染者约有9300 万。在CHB 的抗病毒治疗过程中,大部分患者HBsAg 和(或)HBeAg 很难转阴。临床上以HBV DNA、HBsAg 和HBeAg 的转阴作为评价抗病毒疗效的指标,但仅定性检测HBsAg和HBeAg,并不能动态反应其血清学变化。本研究采用Abbott 化学发光微粒子免疫分析法测定HBsAg 和 HBeAg 滴度,并分析 HBV DNA 水平与HBsAg 和HBeAg 滴度的相关性,旨在探讨测定HBsAg 和(或)HBeAg 滴度变化来推测HBV DNA水平变化的可行性。
对象与方法
一、研究对象 2010年8月至2011年3月在我科门诊及住院的CHB 患者951 例,男743 例,女208 例,年龄 2~80岁,中位数年龄为 38岁。所有患者的诊断标准均符合2010年修订的《慢性乙型肝炎防治指南》[1]。
二、检测方法 采用FQ-PCR 法检测血清HBV DNA 水平(上海科华生物工程股份有限公司);HBV DNA 检测线性范围为 103~108拷贝 /毫升。将HBV DNA 分成3 组:即<3 lg 拷贝/毫升、3~7 lg 拷贝/毫升和≥7 lg 拷贝/毫升组;采用CMIA 法检测 HBsAg 和 HBeAg 滴度(美国 Abbott公司)。根据试剂盒提供的标准判断结果。按照CMIA 检测试剂说明,将 HBsAg>0.05IU/mL 和HBeAg≥1.00 S/CO 判为阳性,前者为定量检测,后者为半定量检测。
三、统计学方法 采用SPSS 13.0 软件进行数据分析,HBV DNA 水平与HBsAg 和HBeAg 水平相关性采用Spearman 秩相关分析,多样本间中位数比较采用Kruskal-Wallis 检验,两组样本间中位数比较采用Mann-Whitney 检验,P<0.05 被认为差异有统计学意义。
结果
一、血清 HBV DNA 与 HBsAg 和 HBeAg 水平相关性分析 对951 例患者血清HBV DNA 与HBsAg和HBeAg滴度进行Spearman 秩相关分析,结果它们之间具有正相关性(r=0.45 和 0.49,P<0.05)。
二、不同HBV DNA 水平患者血清HBsAg 和HBeAg 滴度比较 对HBV DNA 载量分别为<3 lg拷贝/毫升、3~7 lg 拷贝/毫升和≥7 lg 拷贝/毫升3 组患者血清HBsAg 和HBeAg 滴度进行比较,发现各组之间差异有统计学意义(P<0.05),见表1。
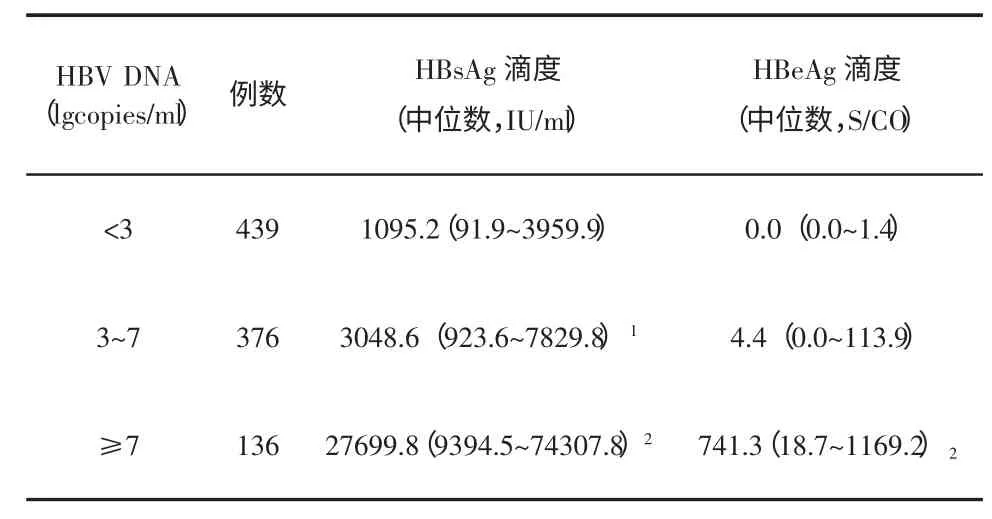
表1 不同HBV DNA水平患者血清HBsAg和HBeAg滴度比较
三、不同HBsAg 滴度患者血清HBV DNA 水平比较 将 HBsAg 滴度分成<1000 IU/ml、1000~10000 IU/mL 和≥10000 IU/mL3 组。三组之间HBV DNA 水平进行比较后发现,各组之间差异有统计学意义(P<0.05,表2)。经 Spearman 秩相关分析发现,在HBsAg≥10000 IU/ml 组患者,血清HBsAg滴度与 HBV DNA 水平呈正相关(rS=0.39,P<0.05)。

表2 不同HBsAg 滴度患者血清HBV DNA 水平比较
讨论
血清 HBV DNA 与 HBsAg 和 HBeAg 滴度是否存在相关性,国内外文献报道不一[2~6]。本文研究结果发现患者血清 HBV DNA 与 HBsAg、HBeAg 滴度呈正相关。分组后显示,在血清HBV DNA≥7 lg 拷贝/毫升和(或)HBsAg 滴度≥10000 IU/mL 患者下,HBV DNA 水平与HBsAg 滴度具有更好的一致性。在HBV DNA>3 lg 拷贝/毫升患者,HBV DNA水平与HBeAg 滴度呈正相关。
血清HBsAg 是HBV 感染的主要标志,常作为乙型肝炎的筛选和诊断。在血清中HBsAg 以小球形颗粒、丝状或杆状颗粒和Dane 颗粒三种形式存在,前两者不含核酸,不具有传染性,Dane 颗粒为病毒蛋白和部分双链rcDNA 组成,具有很强的传染性[7]。Deguchi[8]等认为HBsAg 滴度在一定程度上能够推测HBV DNA 复制水平。本研究结果显示,有些患者血清HBV DNA 与HBsAg 滴度不具有相关性,这可能是因为:(1)在一般情况下,非感染性HBsAg 颗粒与Dane 颗粒比例约为1∶103~105[9]。血清HBsAg滴度测定实际为三种颗粒总体的滴度,因此,只有双链rcDNA 水平达到一定程度和两种颗粒比例减小时,血清HBsAg 滴度与HBV DNA 水平才具有正相关性;(2)所有患者血清HBV DNA 与HBsAg 滴度的相关性较小,相关系数均为0.5 左右。本研究样本量仅为951 例,且选取患者时未剔除抗病毒治疗对HBV DNA 水平的影响因素,部分患者经过抗病毒治疗后HBV DNA 水平下降,造成病毒载量低的患者两者无明显相关性;(3)HBV DNA<3 lg 拷贝/毫升组HBV DNA 水平低于最低检测限,虽有实际测量值,但可能存在假阴性结果,造成实验误差;(4)HBV DNA 载量为 3~7 lg 拷贝 / 毫升时,其中 80.05%(301/376)HBsAg 滴度<10000 IU/ml,因而与HBV DNA 水平无相关性。
在HBV 复制过程中,HBeAg 滴度与HBV DNA水平应为正相关[5]。本研究结果表明,在HBV DNA载量为3~7lg 拷贝/毫升组和≥7lg 拷贝/毫升组,两者有相关性。对于分组后相关系数偏低的原因可能是因为:(1)本研究未区分HBeAg 阳性和HBeAg阴性患者,且部分患者经过抗病毒治疗后HBeAg 滴度下降;(2)Abbott CMIA 技术测定 HBeAg 滴度为半定量,可能会造成上述实验误差。
本实验结果与国内外文献报道有一定的差异,原因可能有以下几点:(1)检测试剂灵敏度不同;(2)HBsAg 存在 G145R 等突变[10];(3)荧光定量 PCR检测方法存在不足。本研究HBsAg、HBeAg 滴度的测定方法采用美国Abbott CMIA 技术,试剂灵敏度高,线性范围宽,是国际公认的定量检测试剂,且G145R 等变异不影响Abbott 试剂的检测灵敏度和线性范围[10]。
有文献指出,血清HBsAg 滴度测定由于其高度灵敏性及相对准确性,在未来预测及评估抗病毒治疗疗效中可能会起重要的作用[11]。血清HBeAg 和HBV DNA 水平均可以评估HBV 复制活跃程度,HBeAg 滴度在一定程度上可以推测HBV DNA 水平,且在评估CHB 进展程度上优于后者[12,13]。但部分患者血清HBsAg 滴度和HBV DNA 水平在抗病毒治疗过程中逐步下降。所以,在HBsAg 滴度和HBV DNA 都为低水平时,要综合血清HBsAg、HBeAg 滴度和HBV DNA 来评估抗病毒的疗效。
CHB 的发展过程是病毒、细胞和免疫系统相互作用的结果,监测HBsAg 滴度在一定程度上可以反映抗病毒疗效,而HBV DNA 水平和HBeAg 滴度都是衡量HBV 活动的一个重要的指标,综合HBsAg、HBeAg 和HBV DNA 水平能够更好地评估抗病毒疗效。本研究利用美国Abbott 试剂检测HBsAg、HBeAg 滴度,结果具有更高的准确性及可靠性,但没有剔除抗病毒治疗的影响,是本研究不足之处,有待于进一步分层研究。
[1]中华医学会肝病学分会和感染病学分会.慢性乙型肝炎防治指南(2010年版).实用肝脏病杂志,2011,14(2):81-89.
[2]雷建华,杨旭,罗红雨,等.血清 HBsAg 和HBeAg 阳性乙型肝炎患者HBsAg 滴度与HBV 复制水平的关系.中南大学学报,2006,31(4):548-551.
[3]蔡文品,赵春,吴惠洁,等.慢性乙型肝炎患者血清HBV DNA水平与肝纤维化指标的相关性.实用医学杂志,2009,25(2):72-73.
[4]Ozdil B,Cosar AM,Akkiz H,et al.Negative correlation between viral load and HBsAg levels in chronic HBV-infected patients.Arch Virol,2009,154(9):1415-1451.
[5]徐敬轩,谢而付,黄珮珺,等.慢性乙型肝炎患者血清中HBeAg、HBsAg 与 HBV DNA 的关系.检验医 学与 临床,2010,21(7):2337-2340.
[6]方红龙,吴金明,江宏峰,等.慢性乙型肝炎患者外周血HBsAg 与 HBV DNA 相关性分析.实用肝脏病杂志,2011,14(2):108-109.
[7]Louisirirotchanakul S,Kanoksinsombat C,The amboonlert A,et al.Mutation of the“a”determinant of HBsAg with discordant HBsAg diagnostic kits.Viral Immunol,2004,17(3):440-441.
[8]Deguchi M,Yamashita N,Kagita M,et al.Quantitation of hepatitis B surface antigen by an automated chem ilum inescent microparticle immunoassay.J Virol Methods,2004,115(2):217-222.
[9]Moucari R,Marcellin P.Quantification of hepatitis B surface antigen:a new concept for the management of chronic hepatitis B.Liver Int,2011,31(1):122-128.
[10]Werle lapostolle B,Bowden S,Locamini S,et al.Persistence of cccDNA during the natural history of chronic Hepatitis B decline during adefovir dipivoxil therapy.Gastroenterology,2004,126(7):1750-1758.
[11]赵秀英.血清HBsAg 定量检测及探讨-从检验者角度看HBsAg 定量.北京医学,2010,32(7):216-218.
[12]Liaw Y F.HBeAg seroconversion as an important end point in the treatment of chronic hepatitis B.Hepatol Int,2009,3(3):425-433.
[13]Yang HI,Lu S N,Liaw YF,et al.Hepatitis B e antigen and the risk of hepatocellular carcinoma.N Engl J Med,2002,347(1):168-174.

