玻璃体内注射贝伐单抗和贝伐单抗/曲安奈德联合用药治疗糖尿病性黄斑水肿疗效及安全性差异的荟萃分析
麻 南 李 丹 高付林 胡莲娜
糖尿病性黄斑水肿(diabeticmacular edema,DME)引起的视力丧失是糖尿病致盲的重要原因之一,20世纪80年代末开始,多采用格栅样激光光凝作为DME的首选治疗方案[1]。但是,有文献报道接受激光光凝的患者中只有17%获得了明显的视力提高(3行以上),而在弥漫性黄斑水肿的患者中激光光凝治疗效果更差[2]。近年研究发现,DME的发生发展与血管内皮生长因子(vascular endothelial growth factor,VEGF)关系密切,而玻璃体内注射抗VEGF药物(贝伐单抗等)可以有效地减轻水肿和提高视力。玻璃体内注射糖皮质激素(曲安奈德)最先是应用于眼内增殖性病变,近年发现其用于DME也能获得良好效果。两种药物作用机制不尽相同,且均有临床对照试验分别支持其对DME的治疗安全有效。近几年,贝伐单抗和贝伐单抗联合曲安奈德哪一种更适合用于治疗DME逐渐成为眼科临床医师争论的焦点,针对玻璃体内注射贝伐单抗对比贝伐单抗联合曲安奈德(intravitreal bevacizumab versus intravitreal bevacizumab plus intravitreal triamcinolone acetonide,IVB versus IVB/IVT)的临床对照试验在国内外也多有开展。本文通过Cochrane系统评价的方法对相关临床对照研究数据进行系统评价,旨在探讨二者治疗DME的疗效和安全性方面的差异。
1 资料与方法
1.1 资料收集方法
1.1.1 纳入标准 (1)收集国内外1966年至2011年10月发表与未发表的以DME患者作为研究对象、治疗方案采用玻璃体内注射IVB和IVB/IVT相比较的所有临床对照研究,研究中进行分组时考虑到患者年龄、性别及糖尿病病史等因素,排除人为因素造成的偏倚;(2)结果观察包括以下指标:中央黄斑厚度(central macular thickness,CMT)、最佳矫正视力(bestcorrected visual acuity,BCVA)并换算为最小分辨视角的对数值(logarithm of the minimum angle of resolution,logMAR)视力、随访期内发生何种并发症或其他不良反应;(3)研究病例数不低于20眼。
1.1.2 排除标准 (1)原始文献临床研究设计不合理(如对照组设计不合理、未对患者糖尿病病情进行评估、样本资料交代不全、诊断或疗效判断不规范等);(2)原始文献的研究对象未对治疗的有效性进行评价;(3)重复发表的文献。
1.2 检索策略 计算机检索 Medline(1966年至2011年 10月)、EMbase(1966~2010年)、Cochrane图书馆(2010年)、中国生物医学文献数据库CBM(1979~2010年)。手工检索中、英文已发表的资料和会议论文,并查阅文章所附参考文献。
1.3 资料提取及质量评价 由有经验的评价员独立选择临床研究并提取资料,主要内容包括:(1)一般资料:文题、作者、日期和文献来源;(2)研究特征:研究对象、地点、干预措施和质量控制;(3)结果测量:CMT、BCVA以及发生何种并发症或其他不良反应。
根据改良的Jadad评分量表,按照随机分配的方法、分配方案的隐藏、盲法及失访记录四个方面来评价纳入资料的方法学质量:1~3分为低质量研究,4~7分为高质量研究[3]。
1.4 统计学处理 阅读文献,按Meta分析要求整理数据,建立数据库并核校数据。对纳入文献进行异质性检验,若纳入的各研究无异质性(即P≥0.1,I2<50%),采用固定效应模型进行分析,反之则用随机效应模型。Meta分析采用RevMan5.1进行,CMT和BCVA为计量资料以加权均数差(weighted mean deviation,WMD)作为效应尺度,提取各组资料的均数和标准差进行合并分析;随访期内发生的不良反应为计数资料以合并比值比(odds ratio,OR)作为效应尺度。合并效应的统计检验结果以Z值表示,根据Z值对应得到P值,P<0.05表示两种治疗方案的差异有统计学意义。敏感性分析采用排除1~2项低质量研究后重新分析的方法,发表性偏倚采用倒漏斗图表示。
2 结果
2.1 纳入的研究概况 初检得到相关文献55篇,发表时间(未发表文献为研究时间)为2006~2011年。经阅读文题、摘要、全文后,51篇由于研究目的与本系统评价不符、重复发表或为动物实验等原因而被排除。最终纳入4篇临床对照研究文献[4-7]进行系统评价。
纳入的研究包括局限性黄斑水肿、弥漫性黄斑水肿及黄斑囊样水肿的患者,各研究的样本量为60~100眼,随访时间为3~9个月,病情资料连续且均在研究中依照均衡的原则进行分组。纳入文献的Jadad评分结果为3~4分,均为中、低质量研究。4个临床对照研究共计321眼,其中IVB组163眼,IVB/IVT组158眼,各项研究中两组间研究对象的年龄、性别、糖化血红蛋白水平及糖尿病病史等方面的差异均无统计学意义。
2.2 IVB与IVB/IVT对比治疗DME的疗效差异
2.2.1 CMT 纳入的4篇文献均报道了研究对象治疗前和随访期内的CMT,异质性检验统计值I2=97%,P<0.05,为异质性研究。采用随机效应模型分析,IVB治疗组与IVB/IVT治疗组的患者CMT降低幅度的差异为-28.72 μm(95%CI,-90.68~33.25 μm),合并效应统计值Z=0.91,P=0.36。故以CMT作为指标衡量IVB和IVB/IVT治疗DME的疗效时,两组差异无统计学意义(图1)。
2.2.2 BCVA 纳入的4篇文献均报道了研究对象治疗前和随访期内的BCVA并换算为logMAR视力。Meta分析显示,异质性检验统计值I2=92%,P<0.05,为异质性研究。采用随机效应模型分析,IVB治疗组与IVB/IVT治疗组的患者BCVA提高幅度的差异为-0.03(95%CI,-0.14~0.09),合并效应统计值Z=0.45,P=0.65,故以BCVA作为指标衡量IVB和IVB/IVT治疗DME的疗效时,两组差异也无统计学意义(图2)。
2.2.3 敏感性分析 删除Jadad评分较低的一项研究[6]后,重新进行Meta分析。以CMT作为分析指标,采用随机效应模型分析,IVB治疗组与IVB/IVT治疗组的患者CMT降低幅度的差异为-14.49 μm(95%CI,-87.56 ~58.59 μm),Z=0.39,P=0.70,两组差异无统计学意义;以BCVA为分析指标,采用随机效应模型分析,IVB治疗组与IVB/IVT治疗组的患者 BCVA提高幅度的差异为0.00(95%CI,-0.13~0.13),合并效应统计值Z=0.02,P=0.98,两组差异无统计学意义。与删除前结果相同,显示本评价结果较稳定。
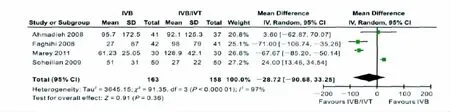
Figure 1 Meta-analysis of CMT in DME patients after IVB or IVB/IVT treatmentIVB和IVB/IVT治疗后DME患者CMT的Meta分析
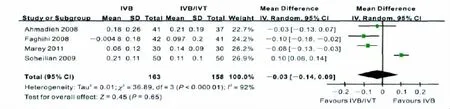
Figure 2 Meta-analysis of BCVA in DME patients after IVB or IVB/IVT treatmentIVB和IVB/IVT治疗后DME患者BCVA的Meta分析
2.2.4 潜在的发表性偏倚 分别以CMT和BCVA为分析指标,作倒漏斗图,因入选研究的个数较少,分布趋势不明显,但倒漏斗图显示趋势对称,提示发表性偏倚不大。
2.3 并发症及其他不良反应 纳入的所有研究均记录了随访期内发生的并发症和不良反应,包括一过性前房反应、眼压升高(>21 mmHg,1 kPa=7.5 mmHg)等;前者均在1周内自愈,后者多经降眼压药物治疗后获得控制。IVB/IVT治疗组有2.5%患者(4眼/158眼)在随访期内发生了晶状体混浊,而在IVB治疗组未见报道。总体上,IVB组发生不良反应的比例为11.7%(19眼/163眼),而IVB/IVT治疗组的比例为22.8%(36眼/158眼)。随访期内发生不良反应的异质性检验统计值I2=0,为同质性研究,采用固定效应模型进行分析,OR为0.41(95%CI,0.22 ~0.78),Z=2.74,P=0.006,IVB 治疗组和IVB/IVT治疗组发生不良反应的差异具有显著统计学意义(图3)。即IVB/IVT治疗组发生不良反应的比例是IVB治疗组的2.44倍(95%CI,1.28~4.55倍)。
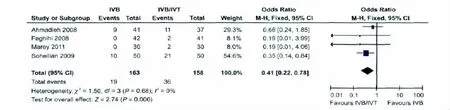
Figure 3 Meta-analysis of adverse events in DME patients after IVB or IVB/IVT treatment IVB和IVB/IVT治疗后DME患者发生不良反应的Meta分析
3 讨论
黄斑区激光格栅样光凝是20世纪80年代以来应用于DME患者的经典治疗方案,但疗效不尽如人意,主要表现在激光光凝提高患者视力效果有限,且对局部解剖结构的破坏性无法避免。近年研究发现,DME的发病机制与VEGF及白细胞介素-6、白细胞介素-8等细胞因子有密切关系,上述细胞因子的局部高表达可能通过破坏细胞吞饮作用、激活视网膜细胞蛋白激酶C通路等途径引起局部血管内皮细胞增殖和血管通透性增加[8-10]。21世纪初至今已有多个临床机构尝试将玻璃体内注射贝伐单抗或曲安奈德应用于DME的治疗。贝伐单抗作为人源化单克隆抗VEGF抗体的全长,对所有VEGF的异构体均有抑制作用,而曲安奈德的抗DME效应与其抗炎作用及抗 VEGF作用有关[11]。近几年来,IVB和IVB/IVT两种治疗方案何者更适合用于治疗DME更是成为国内外眼科医师争论的焦点,多家研究机构为此进行了临床对照研究。不同研究机构报道的结果不尽相同,因此本文通过Cochrane系统评价的方法,收集发表和未发表的相关临床对照研究数据,进行Meta分析,旨在探讨二者在治疗DME的疗效和安全性方面的差异。
CMT和BCVA是可量化的评价DME疗效的指标。本系统评价中,针对CMT和BCVA的Meta分析结果表明:IVB/IVT治疗与单纯IVB治疗相比,既未能更好地减轻患者的黄斑水肿程度,又未获得更好的BCVA。
在安全性方面,研究中报道的不良反应主要是一过性前房反应和眼压升高,IVB/IVT治疗组发生不良反应的比例是IVB治疗组的2.44倍(95%CI,1.28~4.55倍)。其中,眼压升高均发生于IVB/IVT治疗组。玻璃体内注射糖皮质激素引起眼压升高的机制不明,有研究报道发生的几率与年龄、接受注射前是否患有青光眼、患者的糖尿病病情、给药剂量以及使用的药物载体等因素有关[12]。虽然IVB/IVT联合治疗有可能引起眼压升高,但纳入的文献均提到此不良反应多为轻症、且可用药物控制,IVB/IVT联合治疗用于DME是安全的。值得注意的是,Gillies等[13]报道了接受IVT有潜在的引起白内障发生和进展的风险。本系统评价纳入的研究中也在IVB/IVT治疗组中发现了有2.5%(4眼/158眼)患者随访期内发生了晶状体混浊。此不良事件并未发生于单纯IVB治疗组,但研究者并未就此做出进一步的探讨,提示在尚未明确曲安奈德与白内障发生发展的关系时,将IVT应用于DME患者仍应抱着小心谨慎的态度。
为了弥补单一机构进行临床对照研究的局限性,2011年隶属于美国哈佛大学医学院的糖尿病视网膜病变研究小组利用互联网组建数据库并呼吁相关研究机构加入,以期扩大玻璃体内给药治疗DME相关研究的样本量[14]。近年来国内学者也开始尝试将玻璃体内注射药物应用于DME的治疗,姚进等[15]报道了21例DME患者在接受玻璃体内注射曲安奈德后水肿减轻和视力提高。Wang等[16]研究报道单纯IVB和IVB/IVT联合治疗两组患者在CMT和BCVA方面的差异均无统计学意义,但由于随访至3个月的病例数较少,并未纳入本系统评价。
总之,由于目前完成的IVB和IVB/IVT联合治疗DME的临床对照研究多为中低质量研究且样本量较小,导致基于这些临床研究的本文结论的可信度受到源于统计学方面的局限。但从目前已完成的临床对照研究结果来看,单纯IVB治疗和IVB/IVT联合治疗DME在降低CMT和提高BCVA方面二者疗效相仿,单纯IVB治疗的安全性优于IVB/IVT联合治疗。关于二者谁更适合作为DME的治疗方案,尚需更多前瞻性、多中心、大样本的临床随机对照试验数据支持。
1 Blumenkranz MS.Optimal current and future treatments for diabeticmacular oedema[J].Eye,2010,24(3):428-434.
2 Lee CM,Olk RJ.Modified grid laser photocoagulation for diffuse diabeticmacular edema.Long-term visual results[J].Ophthalmology,1991,98(10):1594-1602.
3 Jadad AR,Moore RA,Carroll D,Jenkinson C,Reynolds DJ,Gavaghan DJ,et al.Assessing the quality of reports of randomized clinical trials:is blinding necessary[J]?Control Clin Trials,1996,17(1):1-12.
4 Marey HM,Ellakwa AF.Intravitreal bevacizumab alone or combined with triamcinolone acetonide as the primary treatment for diabeticmacular edema[J].Clin Ophthalmol,2011,5:1011-1016.
5 Soheilian M,Ramezani A,Obudi A,Bijanzadeh B,Salehipour M,Yaseri M,et al.Randomized trial of intravitreal bevacizumab alone or combined with triamcinolone versus macular photocoagulation in diabeticmacular edema[J].Ophthalmology,2009,116(6):1142-1150.
6 Faghihi H,Roohipoor R,Mohammadi SF,Hojat-Jalali K,Mirshahi A,Lashay A,et al.Intravitreal bevacizumab versus combined bevacizumab-triamcinolone versus macular laser photocoagulation in diabeticmacular edema[J].Eur J Ophthalmol,2008,18(6):941-948.
7 Ahmadieh H,Ramezani A,Shoeibi N,Bijanzadeh B,Tabatabaei A,Azarmina M,et al.Intravitreal bevacizumabwith or without triamcinolone for refractory diabeticmacular edema:a placebocontrolled,randomized clinical trial[J].Graefes Arch Clin Exp Ophthalmol,2008,246(4):483-489.
8 Hofman P,Blaauwgeers HG,Tolentino MJ,Adamis AP,Nunes-Cardozo BJ,Vrensen GF,et al.VEGF-A induced hyperpermeability of blood-retinal barrier endotheliumin vivois predominantly associated with pinocytotic vesicular transport and not with formation of fenestrations[J].Curr Eye Res,2000,21(2):637-645.
9 Sohn HJ,Han DH,Kim IT,Oh IK,Kim KH,Lee DY,et al.Changes in aqueous concentrations of various cytokines after intravitreal triamcinolone versus bevacizumab for diabeticmacular edema[J].Am J Ophthalmol,2011,152(4):686-694.
10 Witkin AJ,Brown GC.Update on nonsurgical therapy for diabeticmacular edema[J].Curr Opin Ophthalmol,2011,22(3):185-189.
11 Fraser-Bell S,Kaines A,Hykin PG.Update on treatments for diabeticmacular edema[J].Curr Opin Ophthalmol,2008,19(3):185-189.
12 Yamashita T,Uemura A,Kita H,Sakamoto T.Intraocular pressure after intravitreal injection of triamcinolone acetonide following vitrectomy for macular edema[J].J Glaucoma,2007,16(2):220-224.
13 Gillies MC,Simpson JM,Billson FA,Luo W,Penfold P,Chua W,et al.Safety of an intravitreal injection of triamcinolone:results from a randomized clinical trial[J].Arch Ophthalmol,2004,122(3):336-340.
14 Diabetic Retinopathy Clinical Research Network;Writing Committee,Aiello LP,Beck RW,Bressler NM,Browning DJ,Chalam KV,Davis M,et al.Rationale for the diabetic retinopathy clinical research network treatment protocol for center-involved diabeticmacular edema[J].Ophthalmology,2011,118(12):e5-14.
15姚 进,蒋 沁,袁南荣.曲安奈德玻璃体腔内注射治疗糖尿病黄斑水肿[J].眼科新进展,2007,27(3):201-203.
16 Wang YS,Li X,Wang HY,Zhang ZF,Li MH,Su XN.Intravitreal bevacizumab combined with/without triamcinolone acetonide in single injection for treatment of diabeticmacular edema[J].Chin Med J(Engl),2011,124(3):352-358.

