4-叔丁基碘苯合成
程庆龙
(辽宁职业学院,辽宁 铁岭 112000)
4-叔丁基碘苯合成
程庆龙
(辽宁职业学院,辽宁 铁岭 112000)
主要对电致磷光材料5-[4-二(4-叔丁基苯)胺基]苯基-吡啶-2-甲酸的重要中间体4-叔丁基碘苯的合成进行了研究。在参照文献的基础上,提出了用叔丁基苯和4-叔丁基苯甲酸合成4-叔丁基碘苯的两种方法。其最佳工艺条件是,浓硫酸与亚硝酸钠的物料比为2.0∶1,反应温度为5℃。研究结果表明,叔丁基苯和4-叔丁基苯甲酸两种方法的产率分别可达42.1%和29.4%。与4-叔丁基苯甲酸方法相比,叔丁基苯方法是一条更简单、更有效的合成4-叔丁基碘苯方法。
叔丁基碘苯;叔丁基苯;电致发光材料中间体;合成
前 言
自2001年牛津大学Burn研究组最先报道高效率的树枝状共轭芳基铂-卟啉配合物新型电致磷光材料以来,树枝状电致磷光材料的研究十分活跃。其中,树枝状三芳胺环金属配合物由于具有潜在的优良载流子传输性和发光性能,引起了研究者的关注。很多研究者开始投入到了对其中间体叔丁基苯的研究与应用,尤其是对叔丁基碘苯的研究与应用。
1 实验部分
1.1 主要试剂及仪器
1.1.1 主要试剂
叔丁醇、水合肼、无水氯化钙,天津市博迪化工有限公司;无水乙醇,莱阳市康德化工有限公司;碳酸氢钠,济南化工厂分厂;三氯化铝,天津光复精细化工研究所;苯,国药集团化学试剂有限公司;浓盐酸、浓硫酸,莱阳市双双化工有限公司;碘化钾、亚硝酸钠、浓硝酸、氯化钠、钯碳,莱阳经济技术开发区精细化工厂;无水硫酸镁,天津市北方天医化学试剂厂;分子筛,天津市福晨化学试剂厂。以上试剂均为分析纯。
1.1.2 仪器
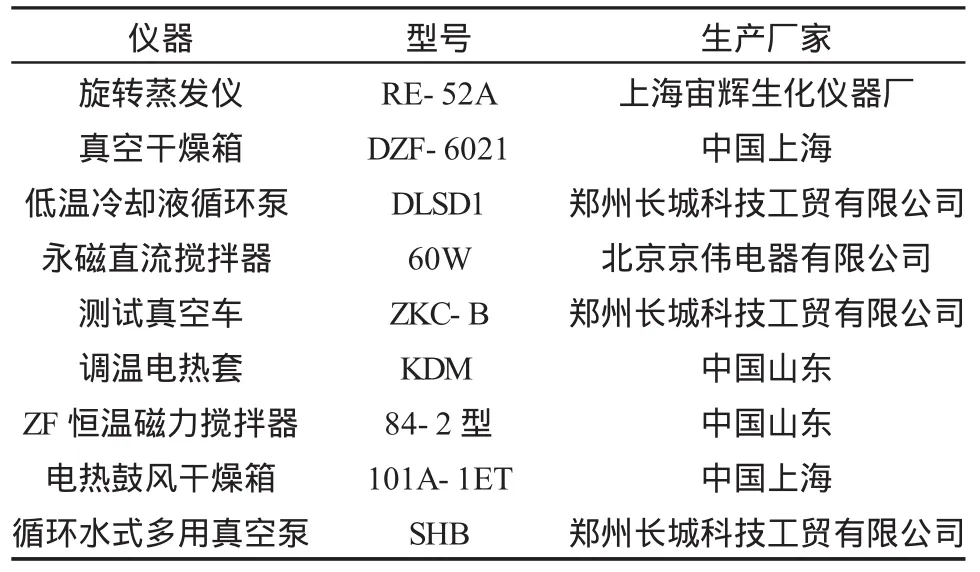
表2 实验所用主要仪器设备一览表Table 2 The main equipment used in the experiment
1.2 合成路线


表3 中间体和目标化合物的编号、名称和结构式Table 3 The serial number,name and structural formula of intermediates and target compounds
1.3 实验过程
1.3.1 叔丁基氯(Inter-M1)的合成
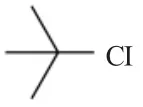
在100mL圆底烧瓶中放置24.8g叔丁醇加入84mL浓HCl,不断振荡10~15min后转入分液漏斗。静止待明显分层后,分去水层。有机层分别用水,5%碳酸氢钠溶液水各5mL洗涤。产品用无水CaCl2干燥后转入蒸馏烧瓶中,加入分子筛作为沸石,接瓶置于冰水浴中,在水浴上蒸馏收集50~51℃馏份。
1.3.2 叔丁基苯(Inter-M2)的制备

向配有冷凝管、水浴锅、搅拌器及尾气吸收装置的三口烧瓶中投入苯84.0mL和无水AlCl34.2g,搅拌下滴加定量的叔丁基氯17.2g,控制一定的反应温度,30min滴加完毕,保温反应一定时间,用稀盐酸中和反应液并洗涤2~3次,分出油相,经无水MgSO4干燥后,常压蒸馏至无馏分馏出为止,回收原料苯,再经常压蒸馏,收集166~171℃的馏份,得8g无色液体,产率66.3%。
1.3.3 4-叔丁基硝基苯(Inter-M3)的制备
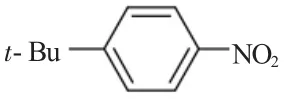
将10mLHNO3和18.5mL浓H2SO4混合液滴加到 16.67g(0.125 mo1)叔丁基苯中(约 20min),在 20℃下反应2h,溶液慢慢倒入冰水中,用氯仿萃取(30mL×3)。有机相依次用饱和 NaHCO3溶液(50mL×3),水(50mL×2)洗涤,无水 Mg2SO4干燥。过滤,常压蒸馏出三氯甲烷,然后减压蒸馏得18.2g浅黄色液体,收率80%。1HNRM(300MHz,CDCl3):δ8.1(d,2HJ=6.87),7.5(d,2HJ=6.84),1.4(s,9H).IR v/cm-1152913691298。
1.3.4 4-叔丁基苯胺(Inter-M4)的制备
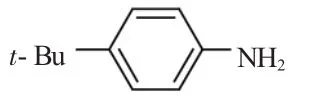
在250mL三口瓶中,加入18.2g(0.1 mo1)4-叔丁基硝基苯,50mL无水乙醇和0.7g5%Pd-C,搅拌。50℃下滴加25 mL水合肼 (约30min),回流反应10h。过滤除去Pd-C,滤液蒸馏出乙醇后,倒入30 mL水中,用苯萃取(20mL×2)。有机相用饱和食盐水洗涤,无水MgSO4干燥。过滤,常压蒸馏回收苯,最后减压蒸馏得11.9g黄色液体,收率79.8%。1HNRM(300MHz,CDCl3):δ7.2(d,2HJ=8.4),6.7(d,2HJ=8.4),3.5 (s,2H),1.3 (s,9H).IR v/cm-13412335213901363829。
1.3.5 4-叔丁基碘苯(Inter-M5)的制备
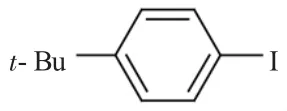
将11.54g(0.083mo1)4-叔丁基苯胺加入到100mL三口瓶中,再加入20mL水和10mL浓硫酸组成的溶液,搅拌成白色糊状物,冰盐浴冷却,滴加6.3g(0.091mo1)亚硝酸钠溶于20mL水的溶液,用淀粉碘化钾试纸指示终点,然后加入15.3g(0.091mo1)碘化钾和15mL水组成的溶液。室温放置3h,再在沸水浴上加热0.5h,冷却,分离出油层。油层用10%NaOH溶液洗涤至呈碱性,水蒸气蒸馏,馏出液油层依次用5%亚硫酸氢钠溶液和饱和食盐水洗涤,无水氯化钙干燥,减压蒸馏得16g黄色液体,收率74%。1HNRM(400MHz,CDCl3):δ7.4(d,2HJ=8.4),7.2(d,2HJ=8.4),1.5(s,9H)。
2 结果与讨论
2.1 叔丁基氯的合成
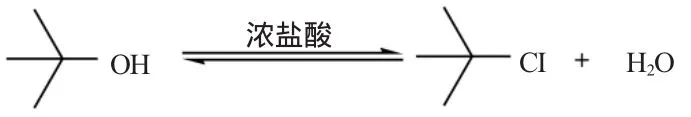
叔丁基氯的合成为一个可逆反应,在查阅相关文献得知浓盐酸与叔丁醇的物料比(3∶1时最好),反应振荡的时间以及粗产品的干燥时间对产率有重要影响。
2.1.1 干燥时间对反应的影响
在确定固有原料物料比及反应温度的情况下,干燥的时间太短或太长都对反应不利,干燥时间太短干燥不完全,太长则容易造成产物被吸附无法分离也不利于实验的多次进行。从表4中发现粗产品干燥6h收率最高。图1是干燥时间与反应收率之间的关系图。

表4 干燥时间的影响Table 4 The effect of drying time
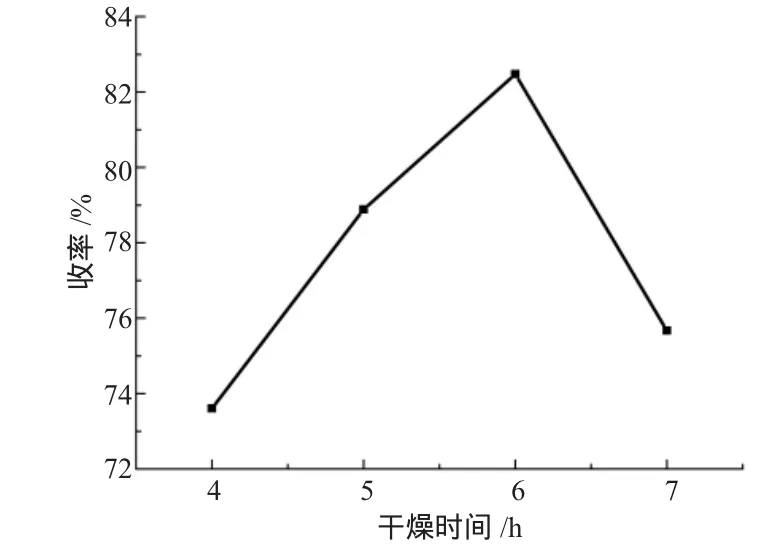
图1 干燥时间与反应产率之间的关系图Fig.1 The relationship between drying time and yield
2.1.2 振荡时间对反应的影响
在确定固有原料比、反应温度等条件的情况下,振荡时间的长短对反应有重要的影响[1]。在实验过程中我们分别振荡 5min,10min,15min以及20min进行反应。由表5可知反应振荡15min以后变化不大,当振荡时间为15min时最合适。图2是振荡时间与收率之间的关系。

表5 振荡时间对收率的影响Table 5 The effect of oscillation time on the yield

图2 振荡时间与收率的关系Fig.2 The relationship between oscillation time and yield
2.2 叔丁基苯的合成
为了探究叔丁基苯合成时的各种因素的影响,在查阅相关文献的基础上我们设计了一个四要素三水平L9(34)正交实验来进行研究[2]。所选的因素及水平如表6、7所示。
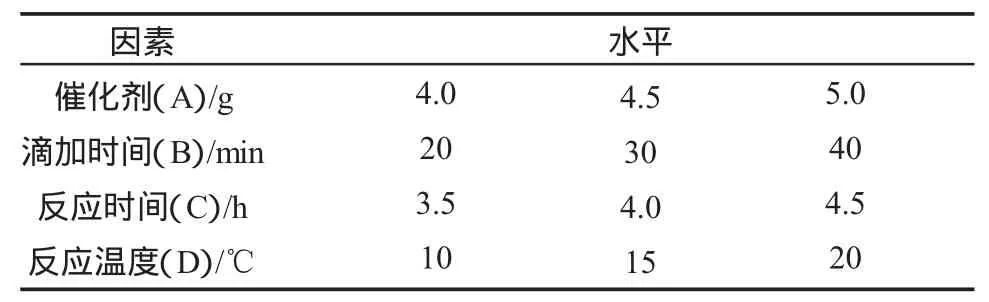
表6 正交实验所选的因素和水平Table 6 The orthogonal experiment factors and level
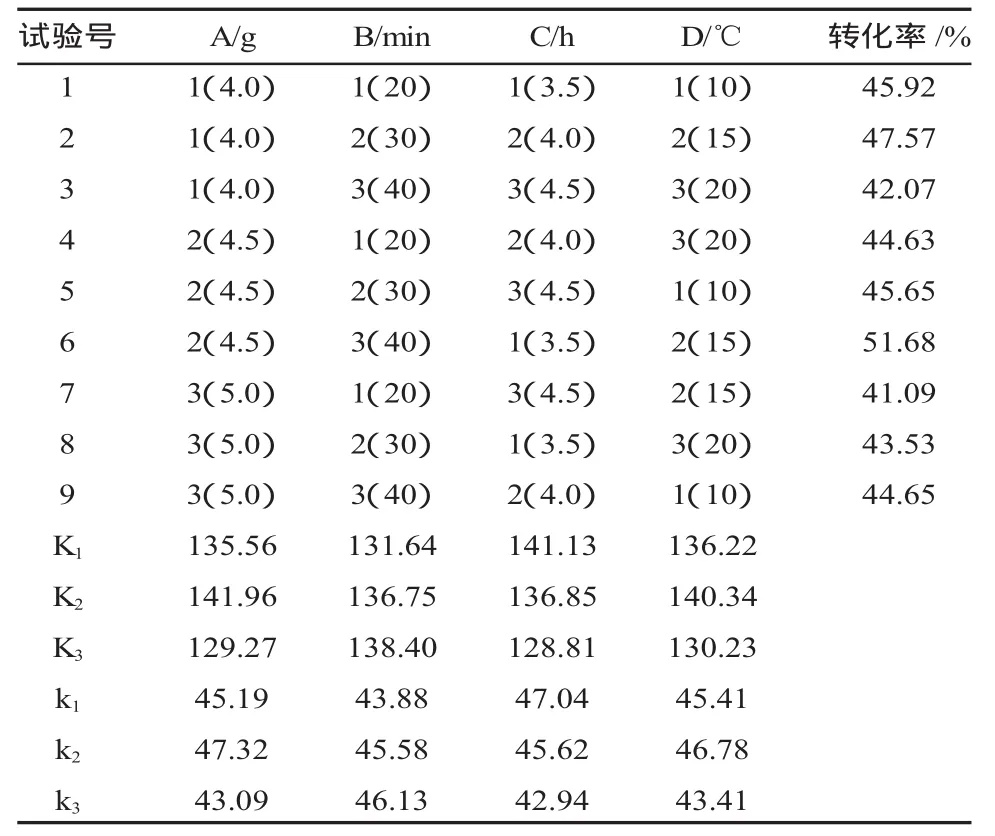
表7 正交实验的结果与分析表Table 7 The orthogonal experiment results and analysis
从图3上可以了解各因素对转化率的影响趋势,能够得出分析因素的主次。直观上很容易看出,一个因素对转化率影响大,是主要的,那么这个因素不同水平相应的转化率之间差异就很大;一个因素对转化率影响不大,是次要的,相应的转化率之间的差异就小。反应在图上,各点散布范围大的因素是主要的,散布范围小的是次要的。从图上我们可以看出主次关系为:
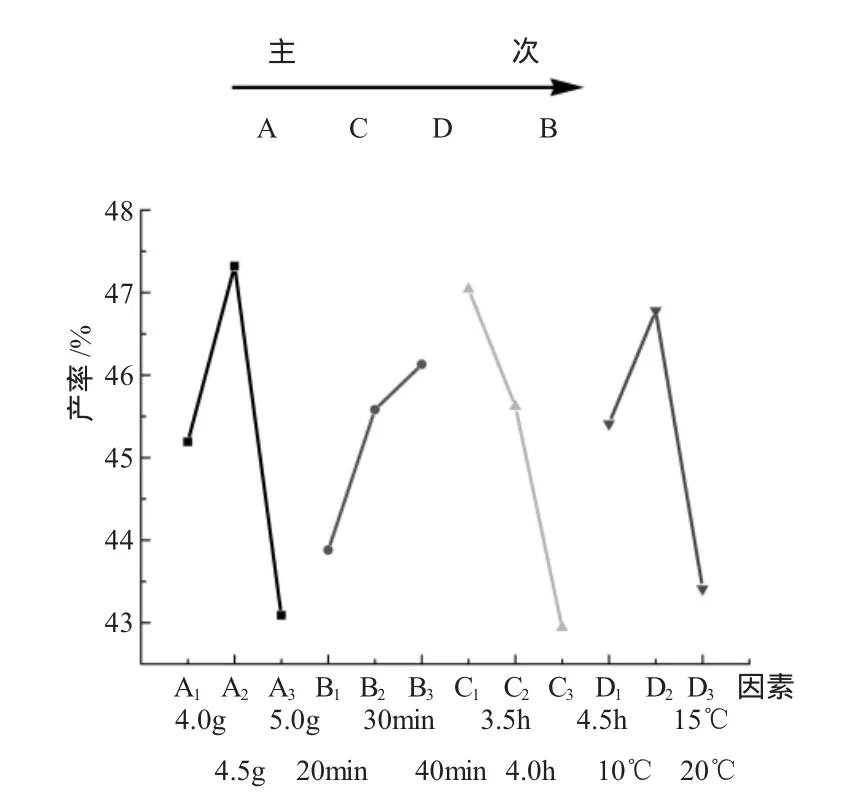
图3 转化率与四因素之间的关系Fig.3 The relationship between conversion rate and the four factors
2.2.1 催化剂的用量对反应的影响
催化剂的用量是实验的一个重要影响因素[3],在滴加时间、反应时间以及控制温度不变的情况下,加入不同量的催化剂,发现催化剂的用量过多或者过少都不利于反应的进行:催化剂用量过少反应不完全,过多则造成产物无法顺利分离收率下降。从表中可见催化剂用量为4.5g(A2)时收率最高。图3中第一条线(自左向右)显示的是催化剂的用量与收率之间的变化关系。
2.2.2 滴加时间对反应的影响
在叔丁基氯与苯合成叔丁基苯的过程中,叔丁基氯的滴加时间是一个很重要的影响因素。在固定原有原料比、反应温度和反应时间的情况下,滴定时间过少或者过晚都对实验不利,滴的太快则容易产生大量的副产物,滴定的太慢则太浪费反应时间。在查阅文献[15]的基础上我们得知,滴定的温度在10~20℃之间,从表中可见滴定的最佳时间为40min(B3)。图3中的第二条线(自左向右)显示的是滴加时间与收率之间的变化关系。
2.2.3 反应时间对反应的影响
在叔丁基苯的合成反应中,叔丁基氯向苯中滴定结束以后,我们需要其反应一段时间。在反应温度、滴加时间以及固有原料比都固定的情况下,反应时间太长则会产生大量的副产物。从表中可见当反应时间为3.5h(C1)时反应的收率最高。图3中的第三条线(自左向右)显示的是反应时间与收率之间的变化关系。
2.2.4 反应温度对反应的影响
在叔丁基苯的合成过程中,反应温度对反应有重要的影响。在固有的原料比、催化剂用量、滴定时间和反应时间都确定的前提下,反应的温度过高或者过低都会对反应不利,如果温度过低则反应无法进行,过高则会造成副产物较多。从表中可见当反应温度为15℃(D2)时反应的收率最高。图3中的第四条线(自左向右)显示的是反应时间与收率之间的变化关系。
2.2.5 结论小结
由以上讨论我们可以得到如下结论:(1)催化剂的用量为4.5g时收率最高;(2)滴加时间越长收率越高。做过的反应中以40min为最好,还应进一步探索更长时间的情况;(3)静置反应时间以3.5h转化率最好;(4)反应温度为15℃时产率最高。综合起来以A2B3C1D2为最佳工艺条件。
2.3 叔丁基硝基苯的合成
2.3.1 浓硫酸的用量对反应的影响
浓硫酸在反应过程中既是吸水剂也是催化剂,在固有原料比、反应温度及滴加时间等不变的情况下,其用量的多少对反应有着及其重要的影响:加入过少反应不完全,过多则将混合物氧化。从表8中得知当浓硝酸的用量为10mL,叔丁基硝基苯的用量为浓硫酸的加入量为18.5mL时收率最高。图4为浓硫酸的用量与收率的关系图。
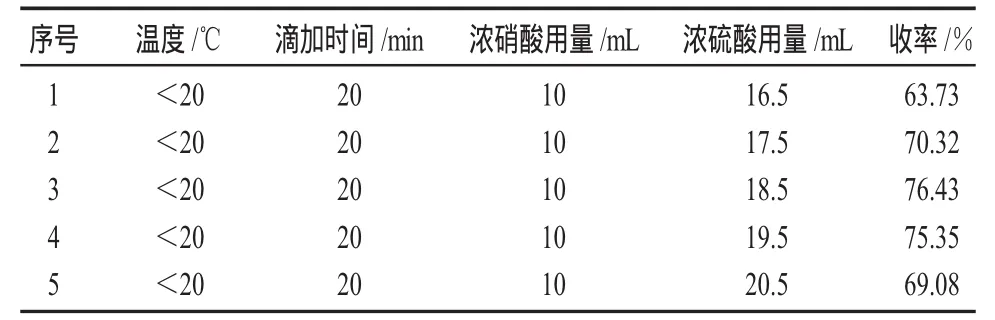
表8 浓硫酸的用量对反应的影响Table 8 The effect of amount of concentrated sulfuric acid on the reaction
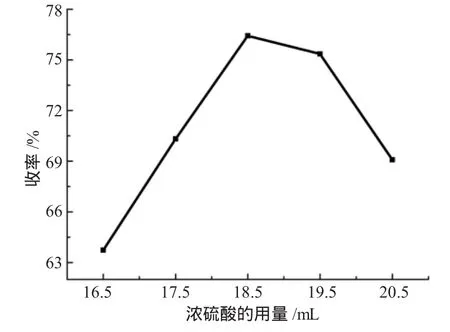
图4 浓硫酸的用量与收率的关系Fig.4 The relationship between amount of concentrated sulfuric acid and the yield
2.4 叔丁基苯胺的制备
2.4.1 滴定时间对反应的影响
4-叔丁基硝基苯与水合肼合成叔丁基苯胺的反应为催化加氢反应[4]。在固有原料比、反应温度、催化剂用量等条件不变的情况下,滴定的时间对其反应有重要影响:时间太短,则反应不完全,会生成大量副产物;滴定的时间太长,产率难以提高且浪费时间。为此我们必须找到最佳的滴定时间。从表9中我们可以看出,滴定的时间为30min以后收率变化不大,30min为最佳滴定时间。图5为滴定时间与收率的关系图。
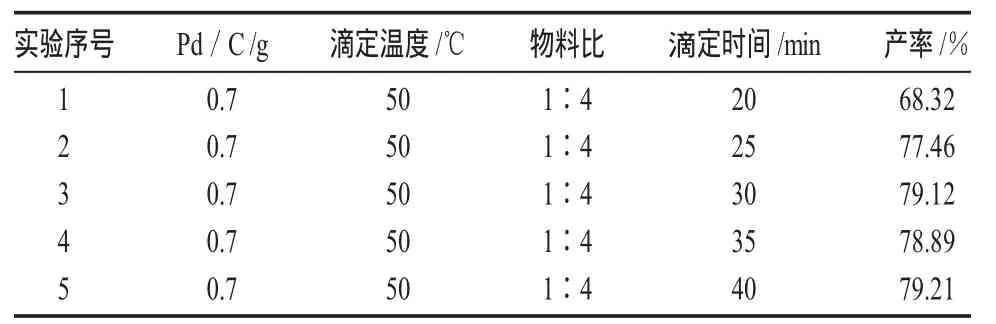
表9 滴定时间对反应的影响Table 9 The effect of titration time on the reaction
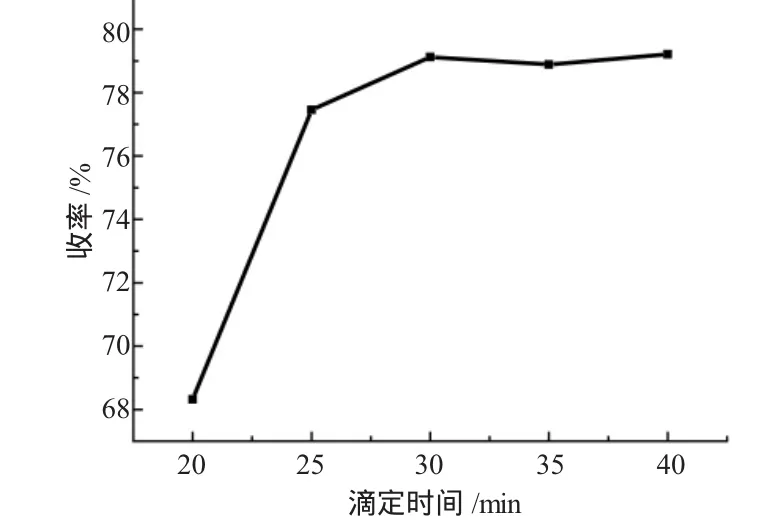
图5 滴定时间与收率的关系Fig.5 The relationship between titration time and the yield
2.5 目标产物的制备及其表征
2.5.1 反应温度对反应的影响
在4-叔丁基碘苯的合成反应中,伯芳胺在低温及强酸(主要是盐酸或硫酸)水溶液中,与亚硝酸作用生成重氮盐的反应称为重氮化反应。在保持物料比、静置时间等条件不变的情况下,反应温度对反应有重要影响,温度过高或者过低都会造成反应收率过低[5]。从表10中我们可以看出当反应温度为5℃时反应收率最高。图6为反应温度与收率的关系。
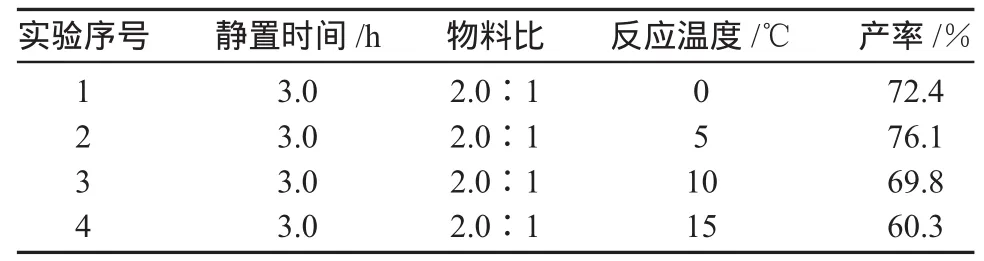
表10 反应温度对反应收率的影响Table 10 The effect of temperature on reaction yield

图6 反应温度与收率的关系Fig.6 The relationship between temperature and yield
2.5.2 浓硫酸与亚硝酸钠的物料比对反应的影响
亚硝酸钠与叔丁基苯胺的反应为重氮化反应[6],亚硝酸钠与浓硫酸混合生成亚硝酸,其与苯环上的硝基发生重氮化反应生成重氮苯硫酸盐。反应时浓硫酸的用量对反应有重要的影响,一般过量,一部分与亚硝酸钠作用生成亚硝酸,一部分与产物结合,多下来的酸是使溶液保持一定的酸度。亚硝酸不能过量,因为它的存在会加速重氮盐本身的分解。在保持反应温度、静置时间等条件不变的情况下,我们对浓硫酸与亚硝酸钠的物料比对反应的影响进行了研究。从表11中我们可以看出,浓硫酸与亚硝酸钠的物料比在2.0∶1以后变化不大,故当物料比为2.0∶1时收率最佳。图7为浓硫酸与亚硝酸钠的物料比与收率的关系。

表11 浓硫酸与亚硝酸钠的物料比与收率的的关系Table 11 The effect of ratio of concentrated sulfuric acid to sodium nitrite on the yield
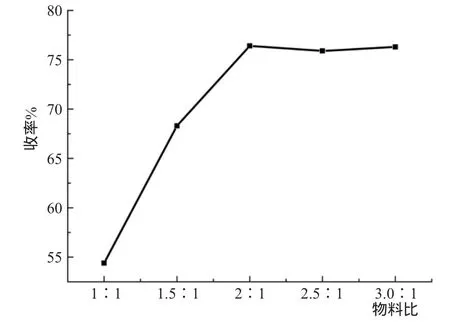
图7 浓硫酸与亚硝酸钠的物料比与收率的关系Fig.7 The relationship between the ratio of concentrated sulfuric acid to sodium nitrite and yield
3 结论
(1)本文最终设计合成出了4-叔丁基碘苯。
(2)本文对叔丁基苯的合成的影响因素进行了研究,得到了其影响因素的主次关系。其影响因素从主到次的顺序为:催化剂的用量、反应时间、反应温度、滴加时间。
(3)对目标化合物的工艺条件进行了初步探索,并得到了较佳的工艺条件。合成叔丁基氯的较佳工艺条件是:以浓盐酸和叔丁醇为原料,按照物料比为3∶1的比例,室温条件下振荡15min,随后干燥6h。叔丁基氯与苯合成叔丁基苯的最佳反应条件是:在15℃的温度下,以4.5g的AlCl3为催化剂,滴定40min并反应3.5h。叔丁基苯胺合成的最佳反应条件:浓硝酸10mL,浓硫酸的用量为18.5mL,滴20min,反应2h,然后以精馏乙醇为溶剂加热回流10h。
(4)目标产物的最佳合成工艺条件是,浓硫酸与亚硝酸钠的物料比为2.0∶1反应温度为5℃。在此条件下,我们合成的4-叔丁基碘苯纯度高,收率为76.4%(文献值为 74%)。
[1]HREHA R D,GEORGE C P,HALDI A,et al.2,7-Bis(diarylamino)-9,9 -dimethylfluorenes as Hole-Transport Materials for Organic Light-Emitting Diodes [J].Advanced Functional Materials,2003,13(12):967~973.
[2]CHEN C H,SHEN W J,JAKKA K.Synthesis and characterization of spiro(adamantane-2,9′-fluorene)-based triaryldiamines:thermally stable hole-transporting materials[J].Synthetic Metals,2004,143(2):215~220.
[3]SATO Y,ICHINOSAWA S,OGATA T.Blue-emitting organic EL devices with a hole blocking layer[J].Synthetic Metals,2000,111:25~29.
[4]YAMASHITA K,MORI T,MIZYTANI T.EL properties of organiclight-emitting-diodeusingTPD derivativeswith diphenylstylyl groups as hole transport layer [J].Thin Solid Films,2000,363(1~2):33~36
[5]HUANG T H,LIN J T,TAO Y T,et al.Benzo[a]aceanthrylene Derivatives for Red-Emitting Electroluminescent Materials[J].Chemstry of Materials,2003,15(25):4854~4862.
[6]SHIROTA Y.Organicmaterials for electronic and optoelectronic devices[J].Journal of Materials Chemistry 2000,10(1):1~25.
Synthesis of 4-Tert-butyl-iodobenzene
CHENG Qing-long
(Liaoning Vocational College,Tieling 112001,China)
The 4-tert-butyl-iodobenzene is synthesized which is a key intermediate of 5-[4-(4-tert-butyl phenyl)amino]phenyl-pyridine-2-acid.Based on the literature,two ways for synthesizing 4-tert-butyl-iodobenzene are proposed,one is using tert-butyl benzene and the other is using 4-tert-butyl benzoic acid.The results show that the yields of these two methods were up to 42.1%and 29.4%respectively.And compared to the 4-tertbutyl benzoic acid method,the tert-butyl benzene is a simpler,more efficient synthesis method.The optimum conditions are as follows:the material ratio of concentrated sulfuric acid to sodium nitrite is 2.0∶1 and the reaction temperature is 5℃.
Tert-butyl-iodobenzene;tert-butyl benzene;electroluminescent intermediates materials;synthesis
TQ 242.2
A
1001-0017(2012)01-0039-06
2011-08-26
程庆龙(1964-),男,汉族,辽宁省昌图县人,高级讲师,理学学士学位,研究方向:基础化学教学与应用化学。

