离子液体1-烷基-3-甲基咪唑四氟硼酸盐在水溶液中的聚集行为
付素珍 陈庆德 沈兴海
(北京大学化学与分子工程学院,放射化学与辐射化学重点学科实验室,北京分子科学国家实验室,北京100871)
离子液体1-烷基-3-甲基咪唑四氟硼酸盐在水溶液中的聚集行为
付素珍 陈庆德 沈兴海*
(北京大学化学与分子工程学院,放射化学与辐射化学重点学科实验室,北京分子科学国家实验室,北京100871)
采用等温滴定量热法、静态荧光猝灭法和电导法系统研究了典型离子液体1-烷基-3-甲基咪唑四氟硼酸盐([Cnmim][BF4])在水溶液中的聚集行为,获得了胶束形成的临界胶束浓度(cmc),摩尔焓变(ΔHmic),摩尔吉布斯自由能变(ΔGmic),摩尔熵变(ΔSmic)以及不同浓度时[Cnmim][BF4]胶束的平均聚集数等基本参数.发现这类离子液体的聚集为熵驱动,阳离子的烷基链越长,ΔGmic越负,聚集更容易发生.此外,结合[Cnmim]X(X=Cl-,Br-)的相关研究发现,阳离子相同时,体积越大和疏水性越强的阴离子与头基的结合能力越强,能有效地降低头基之间的静电排斥,降低cmc,利于胶束的形成.对于[C12mim][BF4],添加剂β-环糊精(β-CD)的加入可使cmc增大, ΔHmic和ΔSmic减小,而KBF4则可使cmc和ΔHmic减小,ΔSmic增大.
离子液体;1-烷基-3-甲基咪唑四氟硼酸盐;等温滴定量热;荧光;电导
1 引言
室温离子液体(room temperature ionic liquids, RTILs),简称离子液体,是一类完全由有机阳离子、无机或有机阴离子构成的,在室温或接近室温下呈液态的有机盐.1离子液体的种类繁多,1-烷基-3-甲基咪唑四氟硼酸盐([Cnmim][BF4])是一类常用的亲水性离子液体,在化学反应,2,3分离过程,4,5材料制备,6,7电化学8,9等研究领域具有广阔的应用前景.
在对[Cnmim][BF4]的研究中,人们注意到其在水溶液中具有一些特殊的现象.Dorbritz等10利用质谱研究[C4mim][BF4]水溶液时发现存在[C4mim] [BF4]2和[C4mim]2[BF4]3小聚集体.Katayanagi等11在测定[C4mim][BF4]-水体系中[C4mim][BF4]的偏摩尔焓、偏摩尔熵和化学势时发现,[C4mim][BF4]在摩尔分数为0.015处出现不连续变化的现象.Malham等12在利用表面热系数法研究此体系时也发现了类似的现象.Archer等13利用绝热量热仪对[C8mim][BF4]在水中的溶解行为进行研究时,观察到浓度为0.05 mol·L-1时的溶解热突变.这些特殊的现象可能是由于[Cnmim][BF4]在水中聚集形成胶束的缘故.虽然已有文献报道了[C4mim][BF4]14和[C12mim][BF4]15在水中的临界胶束浓度(cmc),但目前对[Cnmim][BF4]在水溶液中的聚集行为还缺乏系统的研究,尤其是聚集过程中的热力学参数明显缺乏.等温滴定量热(isothermal titration calorimetry,ITC)法是一种快速灵敏的量热技术,能够同时测定胶束形成的cmc,摩尔焓变(ΔHmic),摩尔吉布斯自由能变(ΔGmic),摩尔熵变(ΔSmic),16该法在研究离子液体在水中聚集行为的独特作用已引起了人们的关注.17-20对[Cnmim][BF4]在水溶液中聚集行为的热力学研究将为离子液体的分子设计和进一步应用提供理论依据.
本文采用ITC、静态荧光猝灭法和电导法系统研究了[Cnmim][BF4](n=4,6,8,10,12)在水溶液中的聚集行为,获得了胶束形成的cmc,ΔHmic,ΔGmic, ΔSmic以及不同浓度时[Cnmim][BF4]胶束的平均聚集数(Nagg)等基本参数,并进一步研究阴、阳离子以及添加剂β-环糊精(β-CD)、四氟硼酸钾(KBF4)对其聚集行为的影响.
2 实验部分
2.1 试 剂

图1 [Cnmim][BF4]分子的结构式Fig.1 Molecular structure of[Cnmim][BF4]
[Cnmim][BF4](n=4,6,8,10,12),[Cnmim]Br(n= 8,10,12),[Cnmim]Cl(n=8,10),分析纯,购于中国科学院兰州化学物理研究所;其中[Cnmim][BF4]的结构如图1所示.β-CD、KBF4、二苯甲酮均为分析纯,北京化学试剂公司产品;芘为色谱纯,Fluka公司产品;甲醇为色谱纯,天津四友精细化学公司产品.除β-CD经三次重结晶处理外,其余试剂在使用前未经进一步纯化.荧光猝灭实验所用到的试剂均进行了检测,未发现干扰实验的杂质.实验用水为三次蒸馏水.
2.2 仪器和实验方法
电导测定:采用FE30(Mettlet Toledo,瑞士)电导率仪测定[Cnmim][BF4](n=4,6,8,10,12),[Cnmim] Br(n=8,10,12),[Cnmim]Cl(n=8,10)水溶液的电导率.
等温滴定量热测定:采用Nano ITC2G等温滴定量热仪(TA,美国)测定上述离子液体在水中聚集过程的热力学参数.样品池体积为952 μL,搅拌速度为250 r·min-1,以水为参比,以高浓度的离子液体水溶液为滴定剂,向纯水、5×10-3mol·L-1β-CD和1× 10-2mol·L-1KBF4水溶液中滴定.所有样品均经过15 min真空除气的预处理.
荧光测定:参考文献21,22中的方法,用1.0×10-6mol·L-1芘的水溶液分别配制不同浓度的离子液体水溶液,备用.在一系列容量瓶中分别加入不同量的二苯甲酮-甲醇溶液,氮气吹干;用所配制的离子液体水溶液定容,超声波振荡45 min,利用F-4500 (Hitachi,日本)荧光分光光度计测定芘的荧光光谱,并计算Nagg.激发波长为334 nm,激发狭缝宽度为2.5 nm,发射狭缝宽度为1 nm.
所有实验均在298.15 K下进行.
3 结果与讨论
3.1 离子液体[Cnmim][BF4]水溶液的电导率测定

图2 [Cnmim][BF4]水溶液的电导率随浓度变化曲线Fig.2 Conductivity curves of the aqueous solutions of[Cnmim][BF4](a)[C4mim][BF4](□),[C6mim][BF4](■);(b)[C8mim][BF4](○),[C10mim][BF4](●),[C12mim][BF4](Δ)
图2是[Cnmim][BF4](n=4,6,8,10,12)水溶液电导率随其浓度变化的曲线.这些曲线均可分为两直线部分,其交点所对应的浓度即是该离子液体在水中的cmc,两条直线斜率之比即为离子液体解离度α.23所测得的数据均列于表1中.其中我们测得[C4mim][BF4]在水中的cmc(912 mmol·L-1)与小角中子散射结果(920 mmol·L-1)14基本相符;[C12mim] [BF4]在水中的cmc(8.70 mmol·L-1)与表面张力方法测定结果(9.2 mmol·L-1)基本一致.15同时还发现: [Cnmim][BF4]随着阳离子咪唑烷基链长度的增加,其cmc和α值均减小;其中,lgcmc与烷基链上碳原子数nC之间存在如下线性关系:这与传统阳离子表面活性剂体系类似.24

3.2 离子液体[Cnmim][BF4]水溶液的等温滴定量热测定
ITC可以直接测得胶束形成的cmc和ΔHmic,根据质量作用模型,由公式(2)、(3)可分别计算得到胶束形成的ΔGmic和ΔSmic.16,17,25

其中α由电导法测得,xcmc是表面活性剂浓度为cmc时的摩尔分数.
目前,利用ITC测定表面活性剂胶束化过程的热力学参数,主要采用稀释模式,即利用高浓度胶束溶液向水中滴定.该过程的热量变化分为三个阶段,利用三直线法可获得cmc与ΔHmic.26此方法同样适用于离子液体类表面活性剂体系.17图3(a)即为298.15 K时利用ITC测定[C12mim][BF4]在水中形成胶束过程的滴定热功率随时间变化的谱图,可以看出该过程为吸热.图3(b)则为每个热流峰对应的摩尔焓ΔHm随浓度的变化趋势,利用三直线法即可得到[C12mim][BF4]在水中胶束化过程的cmc与ΔHmic,根据公式(2)、(3)计算得ΔGmic和ΔSmic.所有测得的热力学参数列于表1中.
3.2.1 离子液体的阴、阳离子对其聚集行为的影响
由表1可以看出ITC测得的cmc数值及其随烷基碳链长度(nC)的变化趋势(图4a)与电导法测定结果相符.[Cnmim][BF4](n=4,6,8,10,12)在水中聚集形成胶束的ΔHmic较小,ΔSmic为较大的正值.尽管离子液体自身从单体分子到形成胶束的过程是熵减,但离子液体周围水的有序结构瓦解,因而体系的无序性增加,整体表现为熵增,17,19,25故[Cnmim][BF4]胶束化过程为熵驱动.以ΔHmic,-TΔSmic和ΔGmic对nC作图(图4b)发现,随着阳离子烷基链长度的增加,-TΔSmic和ΔGmic均线性降低,即聚集更容易发生.这是由于碳氢单元的增加既增强了烷基碳链的疏水性,又增强了烷基链间的以及烷基链与离子间的范德华力.27从热力学角度来看,烷基链的疏水效应引起的熵增是这类离子液体聚集的主要驱动力.

表1 电导法和ITC法所测离子液体水溶液的相关参数Table 1 Parameters obtained from conductivity and ITC methods for the aqueous solutions of ionic liquids

图3 (a)[C12mim][BF4]水溶液的滴定热功率随时间变化谱图;(b)[C12mim][BF4]水溶液稀释过程的摩尔焓变ΔHmic随浓度的变化Fig.3 (a)ITC heat-flow curve and(b)plot of mole enthalpy change ΔHmicversus concentration during the titration of the aqueous solution of[C12mim][BF4]
目前,文献17,23中已有[Cnmim]Cl和[Cnmim]Br在水中形成胶束的cmc以及与[Cnmim]Cl聚集相关的热力学参数的报道.为了系统地研究阴离子对离子液体胶束形成的影响,本文还利用ITC和电导法测定了[Cnmim]X(X=Cl-,Br-)在水中聚集的相关参数.我们测得的数据与文献已有结果基本一致.由表1可以发现:当阳离子相同时,我们所研究阴离子(Cl-,Br-,BF4-)体积越大和疏水性越强,α值越小,即阴离子与头基的结合能力越强,从而能有效地降低头基之间的静电排斥,降低cmc,利于胶束的形成.
3.2.2 添加剂对[C12mim][BF4]聚集行为的影响
由表1可以看出,当水中含5×10-3mol·L-1β-CD时,[C12mim][BF4]的cmc从8.30×10-3mol·L-1增加至1.00×10-2mol·L-1.这可能是β-CD和疏水烷基链的相互作用,使离子液体胶束原有的结构被破坏,由于β-CD的包合作用消耗了部分单体分子从而使得cmc增大.28我们研究中发现[C12mim][BF4]与β-CD形成包合物为放热反应,因而水中少量的β-CD可导致[C12mim][BF4]聚集的焓效应增强.由表1可以看出,与纯水中相比,[C12mim][BF4]在β-CD水溶液中聚集过程的熵效应略微减弱.
当水中含有KBF4时,[C12mim][BF4]的cmc降低.其原因主要是:一方面BF-4离子作为[C12mim] [BF4]胶束的反离子,因静电作用而接近带电荷的胶束表面,并屏蔽其表面电荷,降低相电位,减少胶束扩散双电层的厚度,从而使胶束较易形成,cmc值降低.29,30另一方面K+离子因水化作用,打破离子液体单体周围液态水的“冰山结构”,从而引起较大的熵增,使得离子液体更易自聚集形成胶束,从而降低胶束的cmc.31因此,KBF4对[C12mim][BF4]聚集行为的影响主要是由于反离子效应和熵增效应.

图4 [Cnmim][BF4]胶束形成时的(a)cmc和(b)热力学参数(ΔHmic,-TΔSmic,ΔGmic)随烷基碳链长(nC)的变化Fig.4 (a)Value of cmc and(b)plots of the thermodynamic parameters of micellization versus the alkyl length(nC)of the imidazolium cations of[Cnmim][BF4]
3.3 荧光猝灭法测定离子液体[Cnmim][BF4]胶束
的平均聚集数
胶束平均聚集数即缔合成胶束的表面活性剂分子(或离子)数,是胶束大小的量度.静态荧光猝灭法是测定Nagg的常用方法.32以[Q]表示猝灭剂的浓度,[S]表示表面活性剂的浓度,I、I0分别表示有、无猝灭剂存在时的荧光强度,则[S]和Nagg存在以下关系式:33

若固定表面活性剂的浓度[S],实验测定ln(I0/I)随[Q]的变化,由直线斜率和cmc即可求得Nagg.
芘与二苯甲酮组成的探针-猝灭体系是测定离子液体胶束聚集数的一个强有力工具.34本文采用此体系测定[Cnmim][BF4]胶束的聚集数.图5是[C12mim][BF4]水溶液中芘的荧光光谱随猝灭剂浓度的变化情况,其中373 nm处的ln(I0/I)与猝灭剂浓度具有很好的线性关系(图5的插图).根据公式(4)则可计算得到Nagg.
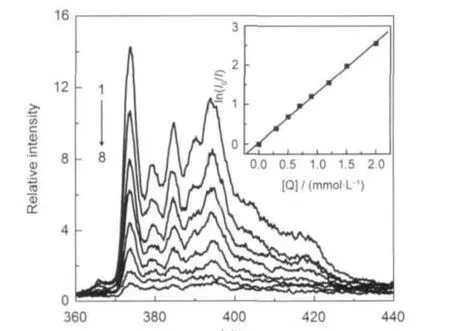
图5 猝灭剂浓度[Q]对[C12mim][BF4]水溶液中芘的荧光光谱的影响Fig.5 Effect of quencher concentration[Q]on the fluorescence emission spectra of pyrene in the aqueous solution of[C12mim][BF4][Q]/(mmol·L-1):(1)0,(2)0.3,(3)0.5,(4)0.7,(5)0.9,(6)1.2,(7)1.5,(8)2.0;The inset shows the plot of ln(I0/I)at λ=373 nm versus the concentration of quencher[Q].

图6 [Cnmim][BF4]胶束的平均聚集数(Nagg)与其浓度的关系Fig.6 Plots of the average aggregation number(Nagg) versus the concentration of[Cnmim][BF4] (□)[C4mim][BF4],(■)[C6mim][BF4],(○)[C8mim][BF4], (●)[C10mim][BF4],(Δ)[C12mim][BF4]
图6为[Cnmim][BF4](n=4,6,8,10,12)胶束的Nagg随其浓度的变化规律,可以看出这些曲线有类似的形状,且Nagg随浓度增加幅度的转折点与本文利用电导法以及量热法测得的cmc基本相符.虽然静态荧光猝灭法是测定胶束聚集数的常用方法,但本文在低于cmc的一定浓度范围内,利用公式(4)也可获得较合理的结果,这可能是由于[Cnmim][BF4]在水中出现预胶束化的缘故.35当[Cnmim][BF4]在水中形成胶束后,继续增加浓度会使胶束溶液的整体极性增大,烷基链间的相互作用减弱,体系中的胶束处于解离-聚合的动态平衡中.36因此,在胶束浓度大于cmc之后,随着浓度的增加,Nagg的增加趋于平缓.
4 结论
本文采用ITC和电导法系统研究了典型离子液体[Cnmim][BF4]在水溶液中的聚集行为,获得了胶束形成的cmc,ΔHmic,ΔGmic,ΔSmic等一系列热力学参数.进一步研究离子液体的阴,阳离子以及添加剂β-CD,KBF4对其聚集行为的影响,发现这类离子液体在水中聚集形成胶束的过程为熵驱动;随着烷基侧链的增长,ΔGmic越负,ΔSmic越大,聚集更容易发生;而当阳离子相同时,阴离子的体积越大,cmc越小,越有利于离子液体的聚集.对于[C12mim][BF4],由于与烷基侧链的包合作用消耗部分单体分子,添加剂β-CD的加入使其cmc增大,而KBF4主要是由于反离子效应和熵增效应而降低其cmc.此外,以芘为探针,利用静态荧光猝灭法测定了[Cnmim][BF4]胶束的Nagg随其浓度的变化规律.
(1) Welton,T.Chem.Rev.1999,99,2071.
(2) Endo,T.;Kato,T.;Nishikawa,K.J.Phys.Chem.B 2010,114, 9201.
(3) Yang,Y.K.;Qiu,S.Q.;He,C.G.;He,W.J.;Yu,L.J.;Xie,X. L.Appl.Surf.Sci.2010,257,1010.
(4) Shokouhi,M.;Adibi,M.;Jalili,A.H.;Hosseini-Jenab,M.; Mehdizadeh,A.J.Chem.Eng.Data 2010,55,1663.
(5)Wang,Y.;Han,J.A.;Xie,X.Q.;Li,C.X.Cent.Eur.J.Chem. 2010,8,1185.
(6) Du,P.;Liu,S.N.;Wu,P.;Cai,C.X.Electrochim.Acta 2007, 52,6534.
(7) Qiu,Z.M.;Texter,J.Curr.Opin.Colloid Interface Sci.2008, 13,252.
(8) Shangguan,X.D.;Tang,H.S.;Liu,R.X.;Zheng,J.B.J.Anal. Chem.2010,38,1510.
(9) Trombetta,F.;de Souza,M.O.;de Souza,R.F.;Martini,E.M. A.J.Appl.Electrochem.2009,39,2315.
(10) Dorbritz,S.;Ruth,W.;Kragl,U.Adv.Synth.Catal.2005,347, 1273.
(11) Katayanagi,H.;Nishikorbritz,K.;Shimozaki,H.;Miki,K.; Westh,P.;Koga,Y.J.Phys.Chem.B 2004,108,19451.
(12) Malham,I.B.;Letellier,P.;Turmine,M.J.Phys.Chem.B 2006, 110,14212.
(13)Archer,D.G.;Widegren,J.A.;Kirklin,D.R.;Magee,J.W. J.Chem.Eng.Data 2005,50,1484.
(14) Bowers,J.;Butts,C.P.;Martin,P.J.;Vergara-Gutierrez,M.C.; Heenan,R.K.Langmuir 2004,20,2191.
(15) Dong,B.;Li,N.;Zheng,L.Q.;Yu,L.;Inoue,T.Langmuir 2007,23,4178.
(16) Bouchemal,K.;Agnely,F.;Koffi,A.;Djabourov,M.;Ponchel, G.J.Mol.Recognit.2010,23,335.
(17)Bai,G.Y.;Lopes,A.;Bastos,M.J.Chem.Thermodyn.2008, 40,1509.
(18)Guan,W.;Wang,H.;Li,L.;Zhang,Q.G.;Yang,J.Z. Thermochim.Acta 2005,437,196.
(19) Luczak,J.;Jungnickel,C.;Joskowska,M.;Thoming,J.;Hupka, J.J.Colloid Interface Sci.2009,336,111.
(20) Stodghill,S.P.;Smith,A.E.;O'Haver,J.H.Langmuir 2004,20, 11387.
(21) Fang,Y.;Liu,X.F.;Xia,Y.M.;Yang,Y.;Cai,K.;Suh,J.M.; Cho,H.Y.Acta Phys.-Chim.Sin.2001,17,828.[方 云,刘雪峰,夏咏梅,杨 扬,蔡 琨,徐廷穆,赵宪英.物理化学学报,2001,17,828.]
(22) Molina-Bolivar,J.A.;Hierrezuelo,J.M.;Ruiz,C.C.J.Colloid Interface Sci.2007,313,656.
(23) Vanyur,R.;Biczok,L.;Miskolczy,Z.Colloid Surf.APhysicochem.Eng.Asp.2007,299,256.
(24) Klevens,H.B.J.Am.Oil Chem.Soc.1953,30,74.
(25) Zhao,G.X.Physcal Chemistry of Surfacatants;Peking Universtity Press:Beiijing,1991;pp 137-143.[赵国玺.表面活性剂物理化学.北京:北京大学出版社,1991:137-143.]
(26) Bouchemal,K.;Agnely,F.;Koffi,A.;Djabourov,M.;Ponchel, G.Drug Discov.Today 2008,13,960.
(27) Tokuda,H.;Hayamizu,K.;Ishii,K.;Susan,M.;Watanabe,M. J.Phys.Chem.B 2005,109,6103.
(28)Sehgal,P.;Sharma,M.;Larsen,K.L.;Wimmer,R.;Otzen,D. E.;Doe,H.J.Dispersion Sci.Technol.2008,29,128.
(29) Kresheck,G.C.J.Phys.Chem.B 2009,113,6732.
(30) Fernandes,R.M.F.;Marques,E.F.;Silva,B.F.B.;Wang,Y.J. J.Mol.Liq.2010,157,113.
(31) Du,J.;Jiang,B.Y.;Xie,J.Q.;Zeng,X.C.J.Dispersion Sci. Technol.2001,22,529.
(32) Chandra,A.K.;Turro,N.J.;Lyons,A.L.;Stone,P.J.Am. Chem.Soc.1978,100,4964.
(33) Russell,J.C.;Wild,U.P.;Whitten,D.G.J.Phys.Chem.1986, 90,1319.
(34)Wang,J.J.;Wang,H.Y.;Zhang,S.L.;Zhang,H.H.;Zhao,Y. J.Phys.Chem.B 2007,111,6181.
(35) Hadgiivanova,R.;Diamant,H.J.Phys.Chem.B 2007,111, 8854.
(36) Goodchild,I.;Collier,L.;Millar,S.L.;Prokes,I.;Lord,J.C. D.;Butts,C.P.;Bowers,J.;Webster,J.R.P.;Heenan,R.K. J.Colloid Interface Sci.2007,307,455.
April 12,2011;Revised:May 3,2011;Published on Web:May 20,2011.
Aggregation Behavior of 1-Alkyl-3-methylimidazolium Tetrafluoroborate Ionic Liquids in Aqueous Solutions
FU Su-Zhen CHEN Qing-De SHEN Xing-Hai*
(Beijing National Laboratory for Molecular Sciences,Radiochemistry and Radiation Chemistry Key Laboratory of Fundamental Science,College of Chemistry and Molecular Engineering,Peking University,Beijing 100871,P.R.China)
The aggregation behavior of 1-alkyl-3-methylimidazolium tetrafluoroborate([Cnmim][BF4])ionic liquids in aqueous solutions was investigated by isothermal titration calorimetry(ITC),fluorescence quenching,and conductivity methods.The critical micelle concentration(cmc),the changes of the enthalpy(ΔHmic),the Gibbs free energy(ΔGmic),and the entropy(ΔSmic)for the micelle formation and the mean aggregation number of the micelles at different concentrations were obtained.We found that entropy was the principle driving force leading to the micellization of these types of ionic liquids.The increase in alkyl chain length led to a decrease in ΔGmic,favoring the formation of micelles.Furthermore, by combining with the aqueous solution data for[Cnmim]X(X=Cl-,Br-),the effect of anions on the aggregation behavior of the ionic liquids was investigated.The increase in the hydrophobicity and the volume of the anions favored the formation of micelles when the ionic liquids contained identical cations. This is believed to result from the decrease in electrostatic repulsion between the head groups in the micelles because of the relatively strong binding between the anions and the cations.With respect to [C12mim][BF4],the addition of β-cyclodextrin(β-CD)caused an increase in its cmc and a decrease in ΔHmicand ΔSmic;while the presence of KBF4caused a decrease in cmc and ΔHmic,and an increase in ΔSmic.
Ionic liquids;1-Alkyl-3-methylimidazolium tetrafluoroborate;Isothermal titration calorimetry;Fluorescence;Conductivity
O645
*Corresponding author.Email:xshen@pku.edu.cn;Tel:+86-10-62765915.
The project was supported by the National Natural Science Foundation of China(20871009)and Fundamental Research Funds for the Central Universities,China.
国家自然科学基金(20871009)和中央高校基本科研业务费专项资金资助项目

