不同温度烧制介孔碳作为直接甲醇燃料电池催化剂载体
徐群杰 李金光 李巧霞
(上海电力学院能源与环境工程学院,上海200090)
不同温度烧制介孔碳作为直接甲醇燃料电池催化剂载体
徐群杰*李金光 李巧霞
(上海电力学院能源与环境工程学院,上海200090)
以嵌段共聚物P123为模板制备介孔氧化硅SBA-15,并以此SBA-15为模板,以蔗糖为碳源在不同的温度下(600-900°C)制备介孔碳CMK-3.采用浸渍还原法,以硼氢化钠为还原剂,制备介孔碳载Pt电催化剂,即20%(w)Pt/CMK-3.利用循环伏安法(CV)、计时电流法等测试电催化剂对甲醇的催化氧化性能及稳定性.预吸附单层CO溶出伏安法研究测试催化剂抗CO中毒能力.结果表明在烧制温度为900°C时制备的介孔碳载Pt催化剂具有最好的催化性能和稳定性,而在烧制温度为700°C时制备的介孔碳载Pt催化剂对CO有较低的溶出电位.
介孔碳;甲醇;Pt;CO溶出
1 引言
直接甲醇燃料电池(DMFC)是将甲醇与氧反应的化学能转化为电能的一种发电装置.由于DMFC燃料易得、易于储存和携带、理论比能量高、近乎零污染等优点而受到越来越多的关注.1-3然而DMFC发展仍然存在许多需要克服的难题,如阳极催化剂活性不易提高并且很容易被CO等中间体毒化,电解质膜材料价格昂贵且伴有的甲醇渗透现象会显著降低电池寿命,这些问题均需要得到有效解决.而其中阳极催化剂性能的提高尤为重要.
由于DMFC阳极催化剂多采用贵金属Pt,因此一般将其负载在比表面积大的载体上以提高其分散性并增加催化剂的耐机械冲击性能.目前常用的碳载体有碳纳米管、4碳纳米纤维、5Vulcan XC-726和有序介孔碳.7其中介孔碳具有规则的孔道结构,很好的水热稳定性,同时具有较大的比表面积和孔隙率而受到更多的关注.Salgado等7,8将Pt及PtRu合金采用蚁酸还原法负载在介孔碳上,其对甲醇的催化活性均比在Vulcan XC-72上的活性高,同时具有更负的CO氧化电位,而经过浓硝酸功能化处理的介孔碳由于具有大量的含氧官能团能够有效提高Pt的分散性.Chen等9将Pt负载在以酚醛树脂为碳源的介孔碳上,认为所制备的介孔碳的孔壁中相互贯穿的小的介孔和介孔通道能够有效提高Pt的分散性,并且所制备的催化剂对乙醇氧化表现出更好的催化活性和稳定性,对乙醇中C―C键的断裂有较高的反应活性.然而自Ryoo等10以MCM-48为模板合成介孔碳以来,在合成介孔碳的温度上少有研究,一般都为在特定温度下制备介孔碳并负载催化剂进行研究,如Shanahan等11以酚醛树脂为碳源,在2600°C的高温下制备了石墨化的介孔碳,发现负载的阴极催化剂有更好的稳定性,Chen等9在900°C碳化酚醛树脂,而Salgado等7则选择在700°C碳化蔗糖,虽说他们所使用的碳源有所不同,但介孔碳的碳化温度的选择及其对介孔碳负载的催化剂催化性能的影响却不可忽视.
本实验在不同温度下烧制介孔碳并用于负载单Pt催化剂,测试其对甲醇的催化性能,并研究了其CO溶出曲线,考察了抗CO中毒性能.
2 实验部分
2.1 介孔碳的制备
SBA-15的制备:12将1.0 g嵌段共聚物P123 (EO20PO70EO20,Mav=5800,BASF公司)、7.5 g水与30 g 2 mol·L-1的盐酸混合,控温在35-40°C范围搅拌至表面活性剂全部溶解,然后加入2.08 g正硅酸乙酯(分析纯,国药试剂),在相同温度下继续搅拌24 h.将所得到的混合溶液在100°C烘箱中水热反应1 d,然后在550°C下焙烧6 h除去有机结构导向剂,得到SBA-15.
CMK-3的制备:将1 g SBA-15,1.25 g蔗糖, 0.14 g硫酸,5 g水,强力超声20 min,先控温100°C烘6 h,然后再控温160°C烘6 h.将得到的黑褐色的物质进行研磨,然后以相同的配比,再加入0.8 g蔗糖、0.09 g硫酸和5 g水,重复100、160°C各烘6 h,并再次进行研磨后,在石英管式炉中(GWG-1/1400,东南大学自动化仪表研究所)氮气气氛下分别控温600、700、800、900°C焙烧6 h.最后用10%(w)氢氟酸(HF)浸润洗涤以除去二氧化硅模板,得到介孔碳CMK-3.13
2.2 Pt/MC的制备
将一定量的CMK-3、H2PtCl6溶液、柠檬酸钠加入水溶液中,控制金属的碳载量为20%(w),在水浴中超声震荡0.5 h,滴加0.1 mol·L-1NaOH水溶液调节溶液的pH值,滴加10 mL 0.1 mol·L-1NaBH4的水溶液作为还原剂,反应3 h,抽滤,水洗至滤液中无氯离子,80°C真空干燥12 h.
2.3 工作电极的制备
电化学分析使用三电极体系,其中铂片电极为辅助电极,饱和甘汞电极(SCE)为参比电极,文中所述电位均相对于SCE.将直径d=3 mm的玻碳电极用粒径0.05 μm的Al2O3粉磨至镜面.称取2 mg Pt/ MC溶于1 mL无水乙醇,加入120 μL Nafion(5%)溶液,超声震荡0.5 h,取5.6 μL分散液滴在玻碳电极上,晾干,用上海辰华仪器公司CHI 660D电化学工作站测其电化学性质.电极表面Pt载量为28 μg· cm-2.电解液为0.1 mol·L-1HClO4+0.5 mol·L-1CH3OH的混合溶液.
用预吸附单层CO溶出实验(CO-tripping)研究催化剂在0.1 mol·L-1HClO4溶液中氧化CO催化活性.高纯氮对电解质除氧,分别以100和10 mV·s-1扫描电极表面,使电极表面达到稳定,然后向电解质中通入CO(纯度为99.9999%)0.5 h,使电极表面上CO的吸附达到饱和,停止通CO,再用高纯氮除去溶液中的CO,然后进行循环伏安扫描,扫描速率为10 mV·s-1.
3 结果讨论
3.1 介孔碳的表征

图1 SBA-15及CMK-3-900的氮气脱附曲线(A)及相应的孔径分布曲线(B)Fig.1 Nitrogen desorption isotherms(A)and pore size distribution curves(B)of SBA-15 and CMK-3-900 T in CMK-3-T is temperature(°C).

图2 不同温度烧制的介孔碳的紫外可见光谱图(A)和傅里叶变换红外光谱图(B)Fig.2 UV-Visibe spectra(A)and Fourier infrared(FTIR)spectra(B)of different CMK-3 in different temperaturss ε:molar absorption coefficient
采用JW-K比表面积分析仪和孔隙率测定仪(北京精微高博科学技术有限公司),测试了所制备的介孔氧化硅SBA-15和900°C烧制的介孔碳的比表面积和孔径,实测结果见图1.从图1A中可以看出SBA-15和CMK-3的N2脱附等温线属于IV型曲线,而且带有H1型滞后,具有圆柱型孔道介孔材料的典型特征,同时从图1B中可以看出CMK-3是SBA-15很好的反相复制品,其孔径分布相近.软件计算的SBA-15的比表面积为527.9 m3·g-1,平均孔径为10 nm,介孔碳的比表面积为825 m3·g-1,平均孔径为13.8 nm.
采用U-3310紫外可见分光光度计(日本,日立公司)和傅里叶变换红外(FTIR-8400S)光谱仪(日本,岛津公司)测试了不同烧制温度的介孔碳在不同波长下的吸收,测试结果见图2.
从图2A中可以看出,600°C到800°C烧制的介孔碳在200 nm附近有强的吸收峰,对应于―COOH,而900°C烧制的碳样在200 nm处的吸收峰降低很多,说明―COOH减少很多.从B图中可以看出3200-3400 cm-1处为缔合的―OH的宽吸收带,并且随烧制温度的提高其量减少,2300 cm-1处可能为―C≡N的吸收峰,1620 cm-1处可能为―C=O的吸收峰,这与紫外-可见图中的羧基吸收峰相对应.
图3是采用德国BRUKER公司U型X射线小角散射系统测试介孔硅及介孔碳的SAXS谱图,扫描范围0.2°-2.8°.从图中可以看出介孔硅SBA-15有三个较明显的衍射峰,分别对应于(100)、(110)和(200)晶面,证明SBA-15具有高度有序的六方介孔结构.12而CMK-3-900则只存在一个较为明显的(100)衍射峰,表明其为二维六方相介孔结构.
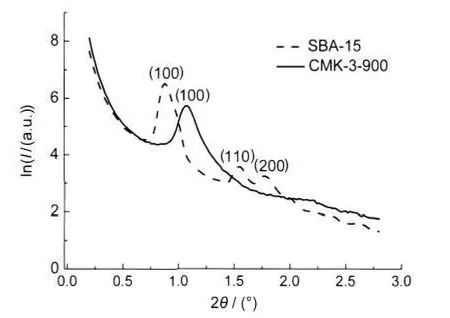
图3 介孔硅SBA-15及介孔碳CMK-3-900的小角X射线散射(SAXS)谱图Fig.3 Small-angle X-ray scattering(SAXS)survey spectra of SBA-15 and CMK-3-900
3.2 催化剂的表征及测试
3.2.1 循环伏安曲线
图4是不同温度烧制的介孔碳负载20%(w)Pt催化剂后对甲醇的循环伏安曲线,扫面速率为50 mV·s-1.从图中可以看出,所制备的催化剂都在0.6 V附近出现甲醇的氧化峰,峰电流相差很大,900°C制备的介孔碳所负载的催化剂对甲醇有最好的催化效果,同时随着介孔碳制备温度的降低,其负载的催化剂对甲醇的催化效果缓慢降低,对比紫外-可见光谱及傅里叶变换红外光谱图,发现并没有某一官能团的量呈现规律性的变化,推测原因可能是低温制备的介孔碳具有更低的导电性,同时可能存在部分羰基吸附在Pt的活性位上,导致了整体催化效果的降低,而制备的温度越低,其羰基的比例愈大,14也即Pt的活性位被占据得更多,其催化效果更低.从表1中可以看出随着介孔碳制备温度的提高,其正扫与回扫过程中甲醇的氧化峰电流密度比值If/Ib呈下降趋势,根据Birss的理论,15这两个峰电流密度的比值可以看作反应过程中含碳积聚物的比例,16比值越大说明其越能抵抗CO的毒化.于是从表中可以看出虽然高温条件制备的介孔碳负载的催化剂具有较高的催化性能,但是相对于低温条件,其If/ Ib比值下降,从一定角度说明低温制备的介孔碳中所含有的羧基或其它基团能够提高Pt的抗CO中毒能力.
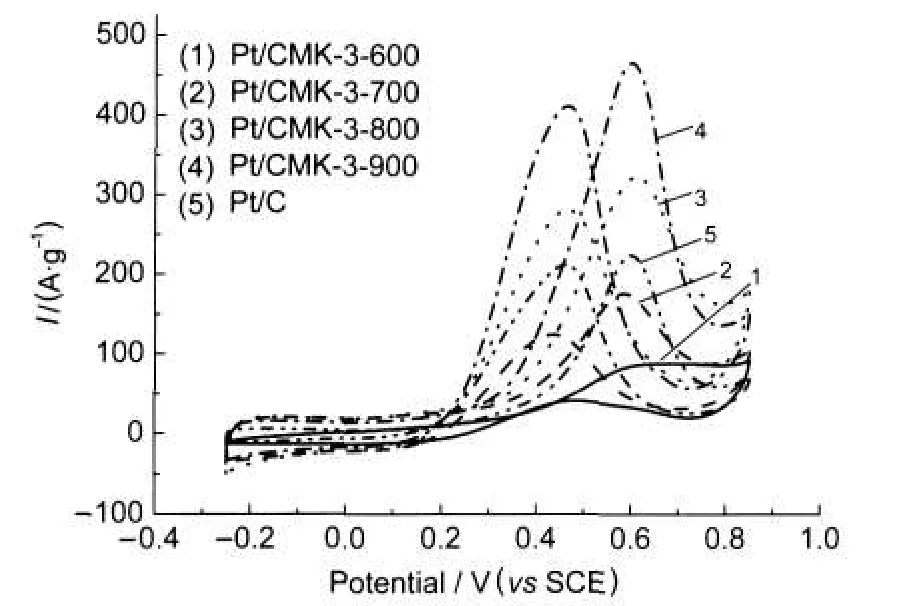
图4 不同温度烧制的介孔碳负载20%(w)Pt催化剂及Pt/C在0.1 mol·L-1HClO4+0.5 mol·L-1CH3OH溶液中的循环伏安曲线Fig.4 Voltammetric curves of 20%(w)Pt supported on different mesoporous carbon and Pt/C in 0.1 mol·L-1 HClO4+0.5 mol·L-1CH3OH
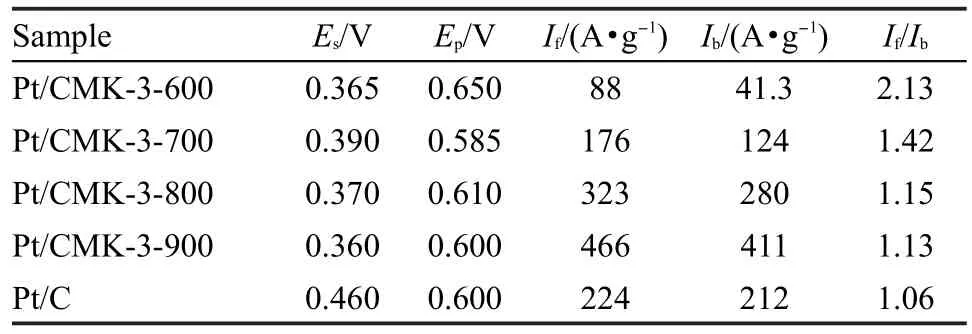
表1 不同介孔碳负载的Pt对甲醇氧化活性的对比Table 1 Comparison of the oxidation activity of Pt loaded on different mesoporous carbon and Pt/C
采用活性炭Vulcan XC-72为载体,以浸渍还原法制备了Pt/C,测试其对甲醇的催化活性,列于图4中做对照.发现Pt/C的If/Ib比值最低,说明介孔碳中的某些含氧官能团能够提高Pt催化剂的抗CO中毒能力.
3.2.2 计时电流曲线
图5是上述制备的催化剂在0.6 V下,0.1 mol· L-1HClO4+0.5 mol·L-1CH3OH溶液中的计时电流曲线.从图中可以看出高温制备的介孔碳负载的催化剂对甲醇具有更好的催化效果,但是随着反应时间的延长,其催化效果降低,这主要是由于甲醇在被氧化的同时,生成了类似CO的有毒性物种吸附在Pt的活性位置上,毒化了催化剂.但仍可以看出, 600°C制备的介孔碳所负载的催化剂的催化效果降低的不明显,可以认为羰基已占据了可以被甲醇氧化所生成的毒性物种占据的Pt的活性位,17而未被羰基占据的Pt的某些晶面或者位置无法吸附毒性物种.Pt/C催化剂的催化活性衰减得更加厉害.
3.2.3 预吸附单层CO后的循环伏安测试

图5 0.1 mol·L-1HClO4+0.5 mol·L-1CH3OH溶液中不同温度制备介孔碳负载Pt(20%(w))催化剂及Pt/C在0.6 V下的计时电流曲线Fig.5 Chronoamperomery curves of 20%(w)Pt supported on different mesoporous carbon and Pt/C in 0.1 mol·L-1HClO4+0.5 mol·L-1CH3OH at 0.6 V(vs SCE)
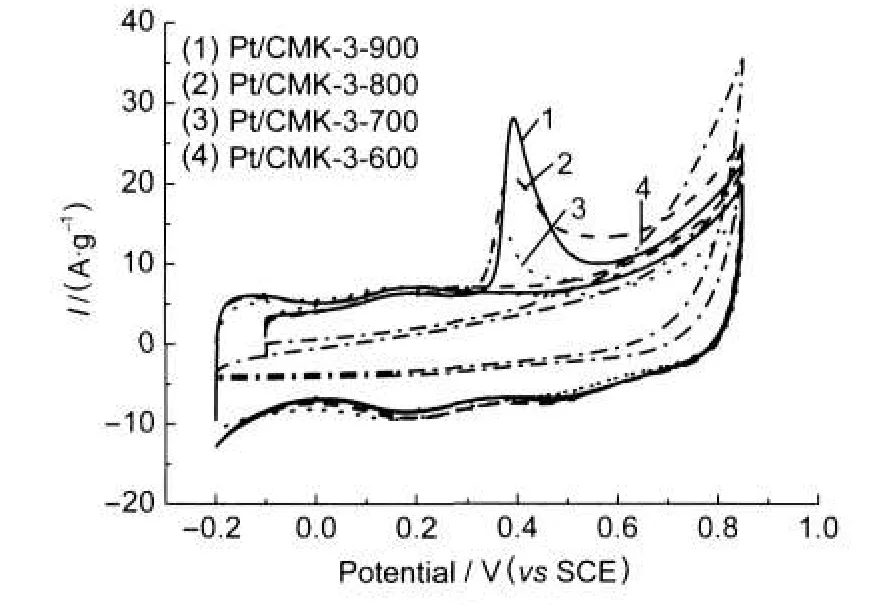
图6 预吸附单层CO的介孔碳负载Pt催化剂在0.1 mol·L-1HClO4溶液中的溶出循环伏安曲线Fig.6 CO striping voltammetric curves of Pt/CMK-3 in 0.1 mol·L-1HClO4
图6是预吸附单层CO的催化剂在0.1 mol·L-1HClO4溶液中的循环伏安溶出曲线.从图中可以看出在0.2 V附近有一个小的氧化峰,可以归为介孔碳的双电层电容性质.18不同温度下介孔碳负载的催化剂的CO溶出氧化峰大约在0.4 V,而且随着介孔碳制备温度的降低,其氧化峰的峰值有所降低,但是CO溶出氧化峰更加提前,可以推测Pt活性位上羧基的吸附有助于CO的溶出.其CO氧化峰值的降低,也可以认为是因为Pt的活性位已经被羧基所占据,只能吸附更少的CO,从而也导致了CO氧化峰峰值的下降,但从CO的起始溶出电位看,700°C制备的介孔碳负载的Pt催化剂对CO具有较低的起始溶出电位.
在第二圈的扫描中,可以看出-0.2-0 V有一个较为明显的H的氧化峰,而且随着介孔碳制备温度的下降其峰值减小.Pt/CMK-3-600在0.4 V附近仅有一个低峰,在高电位下出现一个强的氧化峰,则是Pt对氧的强氧化峰.
通过对催化剂的COads氧化峰的积分计算可得电化学活性面积(EAS),19其计算公式如下:

其中,Q代表在Pt上电氧化CO的总电量,v为扫描速率.从图中可积分CO氧化峰的面积得出,[Pt]代表电极上铂的负载量(为0.0283 mg·cm-2),0.42代表在纯铂上氧化CO所需的电荷密度.20
通过计算可以得知Pt/CMK-3-900、Pt/CMK-3-800及Pt/CMK-3-700的电化学比表面积为46.3、43.0、31.4 m2·g-1.计算结果表明高温条件下烧制的介孔碳所负载的催化剂对CO有更好的电氧化活性.
4 结论
以介孔氧化硅SBA-15为模板,在不同温度下以蔗糖为碳源制备了介孔碳CMK-3,通过浸渍还原法制备了Pt/CMK-3,采用循环伏安法研究了其催化氧化甲醇的活性,结果表明高温制备的介孔碳所负载的催化剂对甲醇有高的催化活性,而低温制备的介孔碳负载的催化剂的催化性能有所下降,但通过研究其计时电流曲线和CO溶出曲线,可以初步判断低温制备的介孔碳中所含有的部分羧基可以使CO的溶出电位提前,为今后开发抗毒性的催化剂提供参考.
(1)Wang,R.H.;Tian,C.G.;Wang,L.;Wang,B.L.;Zhang,H.B.; Fu,H.G.Chem.Commun.2009,3104.
(2) Sun,Z.P.;Zhang,X.G.;Liang,Y.Y.;Tong,H.;Xue,R.L.; Yang,S.D.;Li,H.L.J.Electroanal.Chem.2009,633,1.
(3)Reshetenko,T.V.;Kim,H.T.;Kweon,H.J.Electrochim.Acta 2008,53,3043.
(4) Zhou,C.;Wang,H.;Peng,F.;Liang,J.;Yu,H.;Yang,J. Langmuir 2009,25,7711.
(5)Liu,H.J.;Wang,X.M.;Cui,W.J.;Dou,Y.Q.;Zhao,D.Y.; Xia,Y.Y.J.Mater.Chem.2010,20,4223.
(6) Xu,Q.J.;Zhou,X.J.;Li,Q.X.;Li,J.G.Acta Phys.-Chim.Sin. 2010,26,2135.[徐群杰,周小金,李巧霞,李金光.物理化学学报,2010,26,2135.]
(7) Salgado,J.R.C.;Alcaide,F.;Álvarez,G.;Calvillo,L.;Lázaro, M.J.;Pastor,E.J.Power Sources 2010,195,4022.
(8) Salgado,J.R.C.;Quintana,J.J.;Calvillo,L.;Lazaro,M.J.; Cabot,P.L.;Esparbe,I.;Pastor,E.Phys.Chem.Chem.Phys. 2008,10,6796.
(9) Chen,M.H.;Jiang,Y.X.;Chen,S.R.;Huang,R.;Lin,J.L.; Chen,S.P.;Sun,S.G.J.Phys.Chem.C 2010,114,19055.
(10) Ryoo,R.;Joo,S.H.;Jun,S.J.Phys.Chem.B 1999,103,7743.
(11)Shanahan,P.V.;Xu,L.B.;Liang,C.D.;Waje,M.;Dai,S.;Yan, Y.S.J.Power Sources 2008,185,423.
(12) Zhao,D.Y.;Feng,J.L.;Huo,Q.S.;Melosh,N.;Fredrickson, G.H.;Chmelka,B.F.;Stucky,G.D.Science 1998,279,548.
(13) Jun,S.;Joo,S.H.;Ryoo,R.;Kruk,M.;Jaroniec,M.;Liu,Z.; Ohsuna,T.;Terasaki,O.J.Am.Chem.Soc.2000,122,10712.
(14) Parsons,R.;VanderNoot,T.J.Electroanal.Chem.1988,257,9.
(15) Sirk,A.H.C.;Hill,J.M.;Kung,S.K.Y.;Birss,V.I.J.Phys. Chem.B 2004,108,689.
(16) Liu,Z.L.;Ling,X.Y.;Su,X.D.;Lee,J.Y.J.Phys.Chem.B 2004,108,8234.
(17) Howard,F.D.;Peng,X.D.;Viswanathan,R.;Stair,P.C.; Trenary,M.;Fan,J.Surface Science Letters 1993,285,L455.
(18) Cui,X.Z.;Cui,F.M.;He,Q.J.;Guo,L.M.;Ruan,M.L.;Shi, J.L.Fuel 2010,89,372.
(19) Lee,E.P.;Peng,Z.;Cate,D.M.;Yang,H.;Campbell,C.T.; Xia,Y.J.Am.Chem.Soc.2007,129,10634.
(20) Pozio,A.;De Francesco,M.;Cemmi,A.;Cardellini,F.;Giorgi, L.J.Power Sources 2002,105,13.
March 17,2011;Revised:May 12,2011;Published on Web:June 23,2011.
Preparation of Mesoporous Carbon at Different Temperatures as a Catalyst Support for Direct Methanol Fuel Cells
XU Qun-Jie*LI Jin-Guang LI Qiao-Xia
(Department of Thermal Power and Environmental Engineering,Shanghai University of Electric Power, Shanghai 200090,P.R.China)
Using mesoporous SiO2(SBA-15)as templates and sugar as a carbon precursor,mesoporous carbon(CMK-3)was prepared at different temperatures(600-900°C).20%(w)Pt/CMK-3 was then prepared by impregnation reduction with sodium borohydride as a reductant.Cyclic voltammetry(CV)and chronoamperometry were applied to study the catalytic performance and stability toward methanol oxidation for the as-prepared catalyst.CO striping voltammetry was used to determine its anti-poisoning capability toward CO.The results show that the Pt/CMK-3 prepared at 900°C had the best catalytic performance and stability toward methanol but at a carbonization temperature of 700°C the Pt catalyst had a lower stripping potential to CO.
Mesoporous carbon;Methanol;Pt;CO striping
O643
*Corresponding author.Email:xuqunjie@shiep.edu.cn;Tel:+86-21-35303892.
The project was supported by the National Natural Science Foundation of China(20873031),Innovation Program of Shanghai Municipal Education Commission,China(10ZZ116),Key Project of Shanghai Committee of Science and Technology,China(09230501400,10160502300)and Talent
Development Fund of Shanghai,China.
国家自然科学基金项目(20873031),上海市教委科技创新重点项目(10ZZ116),上海市科委能力建设项目(09230501400,10160502300)和上海市人才发展基金资助

