磁性BiVO4可见光催化材料的制备及光催化性能
刘坤杰 常志东 李文军 车 平 周花蕾
(北京科技大学化学与生物工程学院化学系,北京 100083)
磁性BiVO4可见光催化材料的制备及光催化性能
刘坤杰 常志东*李文军*车 平 周花蕾
(北京科技大学化学与生物工程学院化学系,北京 100083)
采用水相沉淀法,以Fe3O4粒子为核心,令BiVO4沉淀附着于其上,制备了一种更易于从溶液中分离的磁性BiVO4可见光催化材料,以XRD、SEM、UV-Vis DRS、低温氮吸附-脱附等对其进行了表征。结果表明制备的磁性BiVO4为单斜白钨矿型,颗粒呈片状,粒径比普通BiVO4有所增大,在可见光区的吸收更强,吸收边红移程度随Fe3O4含量增加而增大,但比表面积并没有明显改变。并以可见光(λ≥400 nm)为光源,以亚甲基蓝溶液模拟染料废水,考察了其可见光催化活性,发现与纯BiVO4相比,磁性BiVO4具有更为良好的催化性能。通过考察各催化剂的DRS图谱以及暗反应后亚甲基蓝的浓度,发现这种降解效率上的提高是禁带宽度(Eg)降低、可见光吸收增加和对亚甲基蓝吸附量增大综合作用所导致的。这种吸附量的提升与比表面积无关,本工作以等电点的影响来解释此原因。
BiVO4;可见光催化剂;等电点;光催化
0 引 言
利用半导体材料光催化降解工业废水中的有机污染物是一项具有发展前景的新兴技术。其中,TiO2是应用最为广泛的光催化剂之一,其活性高,降解效果好,但因为禁带宽度较大(Eg=3.2 eV),对激发光能量要求高,因此只能在紫外光的照射下表现出催化活性,而太阳光谱中紫外光所占不到5%,这就限制了TiO2对太阳能这种清洁能源的利用。为了克服这一缺点,人们对TiO2的修饰改性进行了大量研究工作,虽然取得了一定成果,但其在可见光域的催化活性仍没有很大提高。近年来,人们另辟蹊径开发出许多新型可见光响应光催化剂,如、等。其中,BiVO4因其制备简单、光降解效果好、无毒的特性得到了广泛关注。BiVO4是一种环境友好的半导体物质,其可见光催化性在上世纪90年代已有报道[4]。早先制备BiVO4多采用固相法[4],后来又发展出水相沉淀法[5-6]、水热法[7-8]、溶胶凝胶法[9]、超声法[10]等,其中以沉淀法和水热法最为常见。为了提高BiVO4的光催化活性,人们对其进行了掺杂改性研究,目前多以掺杂金属离子为主。Xu等[11-13]制备了过渡金属及稀土元素掺杂的 BiVO4催化剂,Ge[14-15]考察了 Pt-BiVO4、Pd-BiVO4的光催化活性,Long等[16]则对Co3O4-BiVO4进行了研究,均发现经过掺杂改性的BiVO4的可见光催化活性有所提高。但是这些掺杂改性都是以改善催化剂的催化性能为目的,并不解决BiVO4的回收分离问题。在以往关于BiVO4降解水体污染物的文献中,BiVO4催化剂多以粉末形式悬浮在水体中进行光催化,因为其颗粒较轻不易沉降,分离往往比较困难,耗时耗力[5]。虽然也有将BiVO4制成膜固定在载体上的技术,但是这种方法比较麻烦而且需要载体[17-18]。为了解决这个问题,希望能够制备出一种易于从水体中分离并拥有良好可见光催化性能的BiVO4催化剂,在完成催化降解后,能够方便快捷地将其从反应体系中分离出来。为此本工作采用水相沉淀法,制备了一种具有磁性的BiVO4催化材料,以一种典型的水体污染物亚甲基蓝为降解对象,考察了磁性钒酸铋的可见光催化性能,并讨论了各因素对催化效果的影响。
1 实验部分
1.1 试 剂
硝酸铋[Bi(NO3)3·5H2O],偏钒酸铵(NH4VO3),氨水(NH3·H2O),硝酸(HNO3),三氯化铁(FeCl3·6H2O),硫酸亚铁(FeSO4·7H2O),均为分析纯。文中用水均为去离子水。
1.2 磁性BiVO4催化剂的制备
1.2.1 Fe3O4的制备
将 FeCl3·6H2O(1.5mmol)和 FeSO4·7H2O (7.5 mmol)混合,以定量水溶解使总Fe浓度为0.05 mol·L-1,在超声振荡的条件下滴加氨水调节pH=10,50℃恒温水浴静置2 h,以磁铁分离出磁性粒子,水洗,50℃干燥。
1.2.2 磁性BiVO4的制备
称取0.584 9 g偏钒酸铵溶解于100 mL热水(90℃左右)中,冷却后备用,硝酸铋2.425 4 g先以3 mL浓硝酸和少量水溶解,再将溶液体积调整为100 mL。向偏钒酸铵溶液中定量加入制备好的Fe3O4,Fe3O4的用量分别占BiVO4理论产量的10%、20%、30%(w/w),在超声振荡的条件下将硝酸铋溶液逐滴加入到偏钒酸铵溶液中去,使反应生成的BiVO4沉淀附着于Fe3O4颗粒核心上。用浓氨水将pH值调节为4,90℃水浴热搅拌6 h。抽滤,洗涤,80℃烘干,450℃灼烧1 h。所得的产品分别标记为BiVO4(Fe3O410%),BiVO4(Fe3O420%)和BiVO4(Fe3O430%)。
1.3 催化剂的晶型及形貌表征
XRD分析采用日本理学公司D/max-RB 12kW旋转阳极X射线衍射仪,辐射源采用Cu Kα射线(λ=0.154 06 nm),工作电压 40 kV,工作电流100 mA,采用系统自带在固体探测器,石墨单色器滤波,闪烁计数器记录X射线强度,扫描范围2θ= 10°~90°。以德国ZEISS公司SUPRA 55型场发射扫描电子显微镜(FE-SEM,加速电压10 kV)和Philips CM200-FEG型透射电镜(TEM,加速电压200 kV)进行形貌分析,在北京彼奥德公司SSA-4200全自动物理吸附仪上进行比表面积测定,采用BET方法计算样品的比表面积。以北京普析通用仪器有限责任公司TU-1901型紫外-可见分光光度计测量样品的漫反射光谱 (硫酸钡作为标准参比样品),扫描范围400~800 nm。
1.4 等电点的测量
以去离子水将制备的BiVO4和磁性BiVO4产品配制成1 mg·L-1的稀悬浊液,并用HCl和氨水调节一系列的pH值(pH=1、4、7、10、13),利用NANO ZS(型号:ZEN 3600,英国Malvern Instrument Ltd.)纳米粒度和电位仪测量ζ电位,求得各物质的等电点[19]。
1.5 光催化实验
以亚甲基蓝溶液模拟工业废水,考察磁性BiVO4的光催化性能。将30 mL浓度为10 mg·L-1的亚甲基蓝溶液置于小烧杯中,加入0.2 g制备好的样品,振荡后在黑暗中静置12 h使样品吸附完全。以100 W白炽灯为光源,用滤光片使得只有λ≥400 nm的可见光通过。液面与光源的距离为10 cm。每2 h取上清液于721型分光光度计上λ= 664 nm处检测亚甲基蓝的吸光度。在低浓度范围内,吸光度与浓度有良好的线性对应关系,且遵守朗伯-比尔定律,因此由吸光度的变化可监测溶液中亚甲基蓝的浓度。
2 结果与讨论
2.1 样品的磁性
图1是水溶液中的磁性BiVO4(Fe3O410%)经磁铁分离后的情况与普通BiVO4的对比。将永磁铁置于烧杯底部3 min后磁性BiVO4悬浊液即可变澄清透明,而普通的BiVO4放置同样的时间依然是混浊的悬浊液。由此可见,制备的产品具备较好的磁性,利用磁铁可达到比一般BiVO4更优良的分离效果。

2.2 样品的XRD分析
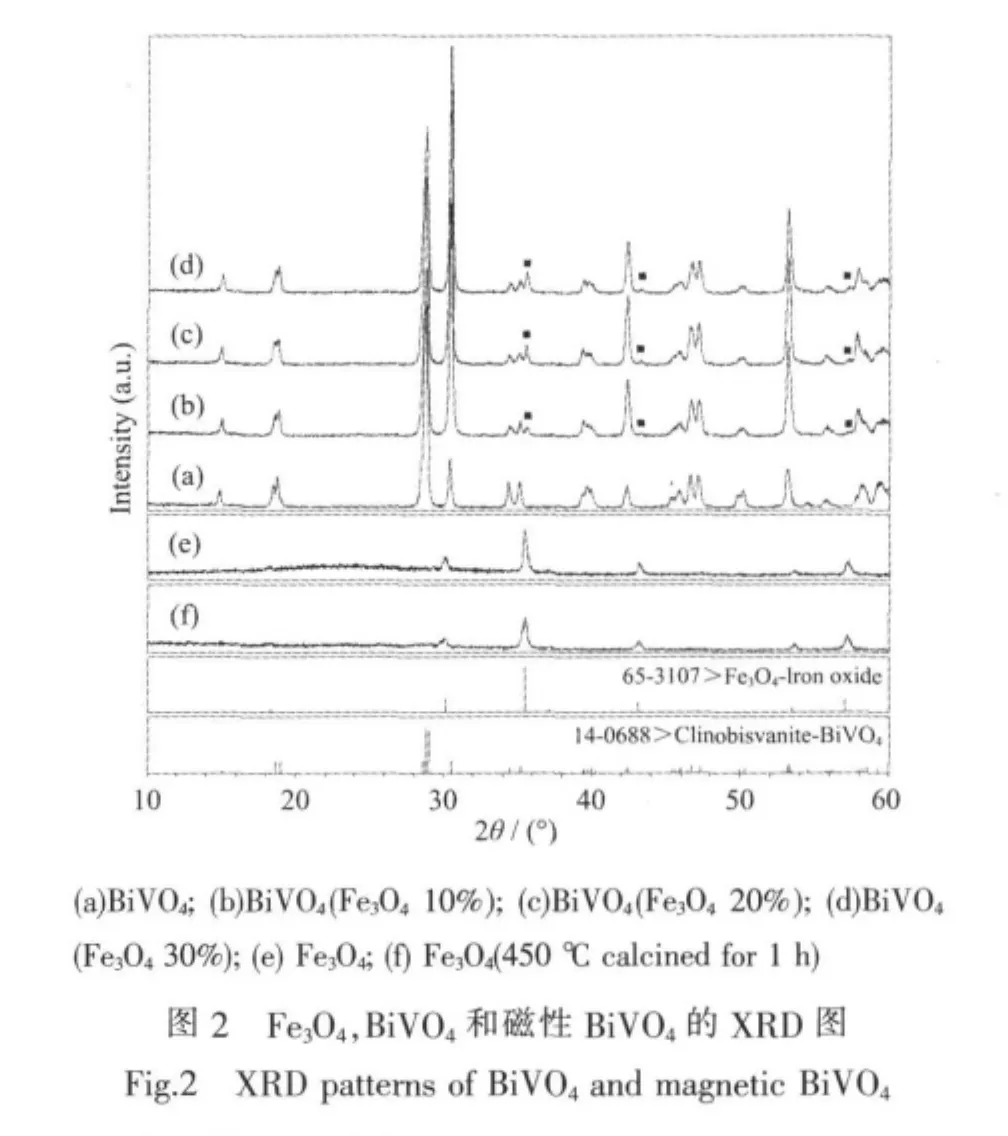
图 2为制备的 Fe3O4、BiVO4、磁性 BiVO4的XRD图。Fe3O4的特征峰与Fe3O4的PDF(65-3107)完全吻合,为立方尖晶石相,且经过1 h的450℃热处理后其晶型未发生改变,也无新物质生成。BiVO4有3种晶型结构:单斜白钨矿型、四方白钨矿型和四方锆石型。其中,单斜白钨矿型BiVO4的光催化活性最好[20]。因此,制备的BiVO4的晶型为单斜白钨矿型是保证其光催化活性的重要条件。从图2可以看出,纯BiVO4和磁性BiVO4在28.6°、30.5°、34.1°和53.1°处均出现了明显的衍射峰,且在19.0°、35.2°和46.0°处出现了单斜白钨矿结构的标志性双峰[18,21]。通过对照标准PDF卡片(14-0688)得知,制备的BiVO4和磁性BiVO4的晶型都属于单斜白钨矿结构,Fe3O4并未进入BiVO4晶格而使其晶型结构发生改变。因为与Fe3O4的衍射峰发生重叠的缘故,磁性 BiVO4在35.45°、43.35°、57.3°处出现了衍射峰,同时,30.5°、47.15°、53.1°附近的峰也有所增强,如图中标示。
2.3 样品的形貌表征

图3为BiVO4和磁性BiVO4的SEM照片。由图可见,加入Fe3O4磁性粒子的BiVO4在形貌上与纯BiVO4有很大区别。纯BiVO4样品的颗粒呈近似椭圆形,粒径在200 nm左右,有较明显的团聚现象。而磁性BiVO4的颗粒较大,呈方片状,粒径在2~5 μm,有枝晶细微结构,团聚情况有所改善。随着Fe3O4含量升高,磁性BiVO4的粒径也逐渐增大,形状也变得更加规则。
为了更细致地考察磁性BiVO4的形貌,将样品超声分散处理后进行了TEM表征。图4是制备的磁性BiVO4(Fe3O410%)的TEM照片。因为Fe3O4是磁性物质,比无磁性的BiVO4能够吸引更多的电子,因此,在磁性BiVO4的TEM照片中,Fe3O4粒子呈现较深的颜色,BiVO4则呈现较浅的颜色。

2.4 样品的比表面积分析
BET法测得 BiVO4、BiVO4(Fe3O410%)、BiVO4(Fe3O420%)和BiVO4(Fe3O430%)的比表面积分别为11、10、10、9 m2·g-1。可以看出,磁性BiVO4的比表面积与纯BiVO4相差不多。物质的吸附量与其比表面积有很大关系,一般来说,比表面积越大吸附量也就越大。很显然磁性BiVO4在这一方面并不占优势。
2.5 样品的UV-Vis吸收光谱
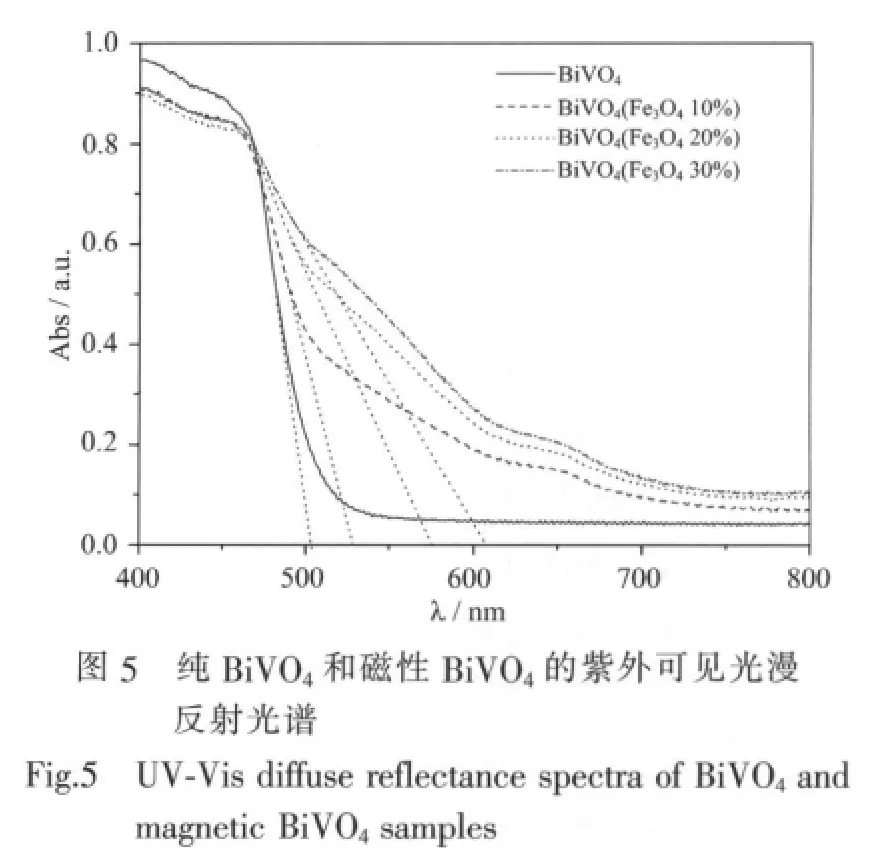
纯BiVO4和磁性BiVO4的紫外可见光漫反射光谱见图5。所有样品在可见光区均有吸收,但后者在可见光区的吸收更为明显,吸收边的红移程度随Fe3O4含量增加而逐渐变大,样品的颜色也逐渐加深,从柠檬黄过渡到橙红色。由图中的曲线的吸收边可以确定纯BiVO4和磁性BiVO4的禁带宽度,计算公式为:

其中λg表示漫反射边延长线与横轴交点处的波长(单位:nm),Eg为物质的禁带宽度(单位:eV)[22]。半导体物质是否具有可见光催化活性,Eg的大小是一个关键因素。计算所得BiVO4、BiVO4(Fe3O410%)、BiVO4(Fe3O420%)和BiVO4(Fe3O430%)的Eg分别为2.45、2.32、2.19、2.10 eV。可见,增大Fe3O4含量可以降低催化剂的禁带宽度,并使样品在可见光区的吸收增强。这对提高催化剂的光催化活性是有利的。可见光吸收增强,光子的利用率将增大,更多的光子被吸收从而激发BiVO4价带上的电子;Eg降低,BiVO4价带上的电子将更易于被激发越过禁带跃迁至导带,在导带和价带分别形成光生电子和光生空穴,二者都可生成强氧化性的羟基自由基(OH·),从而将亚甲基蓝分子氧化降解[23]。
2.6 样品的等电点
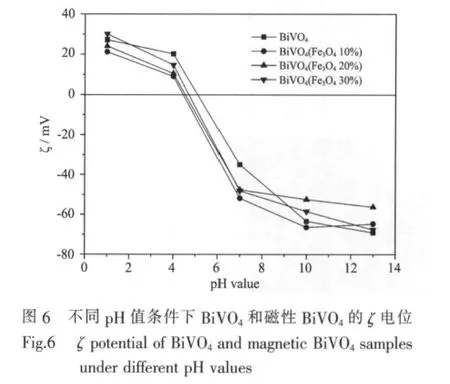
对不同pH值的产品溶液做ζ电位表征,以pH对ζ电位作图,结果如图6。当溶液达到某个pH值时粒子表面电位为零,这个特定的pH值即为等电点[24]。
由图 6可以得出 BiVO4,BiVO4(Fe3O410%),BiVO4(Fe3O420%)和BiVO4(Fe3O430%)的等电点分别为5.10,4.44,4.54,4.70,Fe3O4的引入导致了催化剂等电点的降低。在中性的亚甲基蓝溶液中,磁性BiVO4比普通BiVO4表面带有更多的负电荷。亚甲基蓝是一种阳离子染料,在水溶液中形成一价有机阳离子型季胺盐离子基团[25-27],更易于吸附在带有更多负电荷的磁性BiVO4粒子表面。而催化剂表面吸附的亚甲基蓝分子增多,光催化反应也就更容易进行,这对提高催化剂对亚甲基蓝的降解效率是有利的。
2.7 样品的可见光催化活性
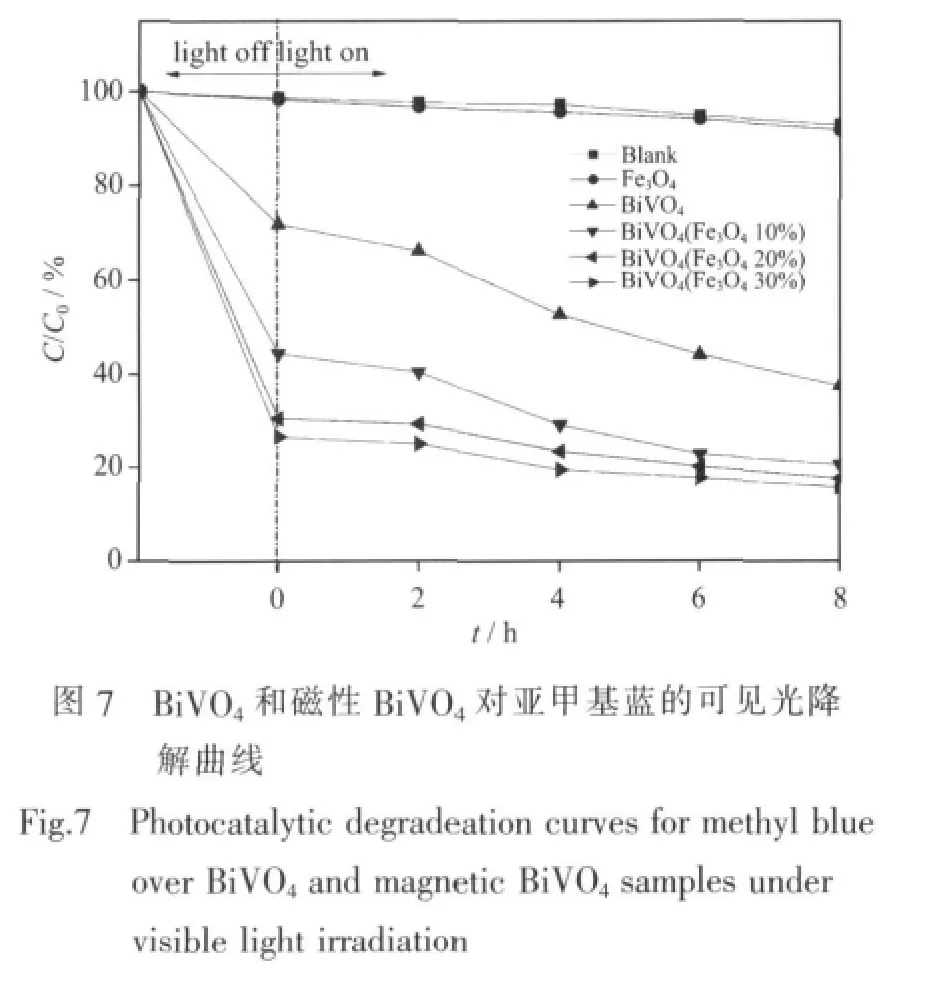
图7为空白样、BiVO4和磁性BiVO4对亚甲基蓝的可见光降解曲线,纵座标表示某时间亚甲基蓝浓度(C)与初始浓度(C0)的比值。从图中可以看出,8 h光照前后空白样的亚甲基蓝浓度几乎无变化,可见其没有发生光降解作用。只加入Fe3O4的溶液在黑暗中静置后以及光照后亚甲基蓝的浓度也几乎不变,说明Fe3O4并不吸附亚甲基蓝,也没有可见光催化性。加入BiVO4的溶液,暗反应后亚甲基蓝的浓度下降了一些,光降解实验结束后则降至42%左右,这表明单纯的BiVO4可以吸附一定量的亚甲基蓝,并具有一定的可见光催化活性。而加入磁性BiVO4的溶液,不仅暗反应后亚甲基蓝的浓度大幅度下降,8 h光降解后的亚甲基蓝浓度也降至20%左右,降解效率比纯BiVO4有很大提高。对比BiVO4和磁性BiVO4暗反应前后溶液中亚甲基蓝的浓度可得知,虽然Fe3O4本身并不吸附亚甲基蓝,但其加入却会使BiVO4催化剂对亚甲基蓝的吸附有所增加。结合2.4与2.6的检测结果来看,这种吸附量的提升应归因于掺入Fe3O4的BiVO4其等电点比纯BiVO4有所降低,与比表面积并没有关系。同时,由2.5可知磁性BiVO4的Eg比纯BiVO4的小,在可见光区的吸收也比纯BiVO4强,因此光催化活性更高。催化剂表面吸附的亚甲基蓝分子增加、对可见光的吸收增强、禁带宽度降低都有利于改善催化剂的降解效果。虽然在质量相同的情况下磁性BiVO4材料中能够起到催化作用的BiVO4的含量比纯BiVO4少是不利因素,但在Fe3O4含量不超过10%时,这些有利因素仍能带来8 h光降解效率比纯BiVO4大幅度提高的表观结果。但当Fe3O4的含量达到30%时,因对亚甲基蓝无吸附降解作用的Fe3O4增多,催化剂的吸附量的增加已经很有限,且对亚甲基蓝的降解效率也无明显提高。这是因为,虽然Fe3O4含量增大有利于降低Eg提高催化剂的催化活性,但同时因BiVO4的含量降低,导致能够产生光催化作用的活性中心减少,进而影响了降解效率的提高。
3 结 论
采用沉淀法制备出一种全新的磁性BiVO4可见光催化材料。利用磁铁可以将其从反应后的溶液中较好地分离出来,解决普通BiVO4在水体中不易沉降分离的问题。且磁性BiVO4对亚甲基蓝的降解效率也比 BiVO4有较大提高,这不仅是因为磁性BiVO4的Eg比纯BiVO4的小,在可见光区的吸收比纯BiVO4强,其对亚甲基蓝的吸附量比后者有所增加也是原因之一。但这种吸附量的提升的原因并不是磁性BiVO4的比表面积增大,而是由于其等电点比普通BiVO4有明显降低,在溶液中更易于吸附亚甲基蓝分子,使光催化降解反应更易发生的缘故。Fe3O4的含量综合考量应以占BiVO4质量的10%为最佳。
[1]Zhang L W,Fu H B,Zhang C,et al.J.Solid State Chem., 2006,179:804-811
[2]Huang C M,Pan G T,Li Y C M,et al.Appl.Catal.A:General,2009,358:164-172
[3]Yin J,Zou Z G,Ye Y H.Chem.Phys.Lett.,2003,378:24-28 [4]Kudo A,Ueda K,Kato H,et al.Catal.Lett.,1998,53:229-230
[5]Zhang X,Ai Z H,Jia F L,et al.Mater.Chem.Phys.,2007, 103(1):162-167
[6]Kohtani S,Koshiko M,Kudo A,et al.Appl.Catal.B:Environ., 2003,46:573-586
[7]Liu J B,Wang H,Wang S,et al.Mater.Sci.Eng.B,2003, 104:36-39
[8]Gotic M,Music S,Ivanda M,et al.J.Mol.Struct.,2005,744-747(1):535-540
[9]Jing H Q,Endo H,Natori H,et al.J.Euro.Cera.Soc., 2008,28:2955-2962
[10]Zhou L,Wang W Z,Liu S W,et al.J.Mol.Catal.A:Chem., 2006,252(1/2):120-124
[11]Xu H,Wu C D,Li H M,et al.Appl.Surf.Sci.,2009,256: 597-602
[12]Xu H,Li H M,Wu C D,et al.J.Hazard.Mater.,2008,153: 877-884
[13]Xu H,Li H M,Wu C D,et al.Mater.Sci.Eng.B,2008, 147:52-56
[14]Ge L.Mater.Chem.Phys.,2008,107:465-470
[15]Ge L.J.Mol.Catal.A:Chem.,2008,282:62-66 [16]Long M C,Cai W M,Cai J,et al.J.Phys.Chem.B,2006, 110(41):20211-20216
[17]Francois R,Andre′L,Michel D.Chem.Mater.,2006,18: 771-777
[18]Galembeck A,Alves O L.Thin Solid Films,2000,365:90-93
[19]QIU Yong-Liang(丘永樑),CHEN Hong-Ling(陈洪龄), WANG Xiao-Zu(汪效祖),et al.J.Chem.Eng.Chinese Univer.(Gaodeng Huaxue Gongcheng Xuebao),2005,19(1): 129-133
[20]Tokunaga S,Kato H,Kudo A.Chem.Mater.,2001,13(12): 4624-4628
[21]Zhou L,Wang W Z,Zhang L,et al.J.Phys.Chem.C,2007, 111:13659-13664
[22]ZHANG Ai-Ping(张爱平),ZHANG Jin-Zhi(张进志).J.Mol. Catal.(Fenzi Chuihua),2010,24(1):51-56
[23]GE Lei(戈磊),CUI Li-Shan(崔立山),et al.J.Chinese Ceram.Soc.(Guosuanyan Xuebao),2008,36(3):320-324
[24]Subramanian S,Noh J S,Schwarz J A.J.Catal.,1988,114: 433-439
[25]Faria P C C,Órfão J J M,Pereira M F R.J.Water Res., 2004,38:2043-2052
[26]Lazaridis N K,Karapantsios T D,Georgantas D.J.Water Res.,2003,37:3023-3033
[27]ZHAO Li-Yan(赵立艳),WANG Xue-Kai(王学凯),GUO Yu-Guo(郭玉国),et al.Acta Physico-Chimica Sinica(Wuli Huaxue Xuebao),2003,19(10):896-901
Visible-Light-Driven Magnetic BiVO4Photocatalyst:Synthesis and Photocatalytic Performance
LIU Kun-Jie CHANG Zhi-Dong*LI Wen-Jun*CHE Ping ZHOU Hua-Lei
(Department of Chemistry,School of Chemistry and Bioengineering,University of Science and Technology,Beijing,100083,China)
A visible-light-driven photocatalyst-magnetic BiVO4-was synthesized by an aqueous deposition method and characterized by XRD,SEM,UV-Vis DRS and low temperature nitrogen adsorption-desorption.The results show that magnetic BiVO4photocatalysts have monoclinic scheelite structure and increase visible-light absorption. The BET specific surface area is a little lower than that of BiVO4.The photocatalytic activity of magnetic BiVO4photocatalysts was investigated in methylene blue solution under visible-light irradiation.The photocatalytic activity of magnetic BiVO4photocatalysts is better than that of the pure one because of the reduction of Eg,the enhancement of absorption in visible light region and increasement of adsorption of methylene blue.The increased adsorption of methylene blue is explained in terms of the lower isoelectric point of magnetic BiVO4than pure BiVO4.
BiVO4;visible-light-driven photocatalyst;isoelectric point;photocatalysis
O614.53+2;O614.51+1;O643
A
1001-4861(2011)08-1465-06
2011-01-19。收修改稿日期:2011-03-30。
国家自然科学基金(No.20876015)资助项目。
*通讯联系人。E-mail:zdchang@ustb.edu.cn,wjli@sas.ustb.edu.cn,Tel:010-62332468

