大环配合物[Ni((14)4,11-二烯-N4)]I2 和[Co((14)4,11-二烯-N4)]I2 的合成
刘云华,殷彩霞,张 仙,刘海龙,赵 艳,赵红梅 ,卜玉涛
(1.云南农业大学基础与信息工程学院,云南 昆明 650201;2.云南大学化学科学与工程学院,云南 昆明 650091;3.云南农业大学经济管理学院,云南 昆明 650201)
近年来大环金属配合物的独特理化性质及其特殊的生物学功能(如吸氧性能[1]、磁性[2~4]、催化作用[5~9]、核酸切割活性、抑菌抗菌活性等[10~13])得到了广泛的研究。由于这类化合物类似于生物体内发现的大环金属配合物(如血红蛋白和叶绿素a,均为卟啉类大环金属配合物),因此,对这类化合物的合成和特性进行研究,可以提供生物机能的有关信息。
作者在此合成了镍/钴大环配合物[5,7,7,12,14,14-六甲基-1,4,8,11-四氮环-(14)4,11-二烯合镍/钴碘化物],即[Ni((14)4,11-二烯-N4)]I2和[Co((14)4,11-二烯-N4)]I2,并对其结构进行了验证。
合成路线如图1所示。
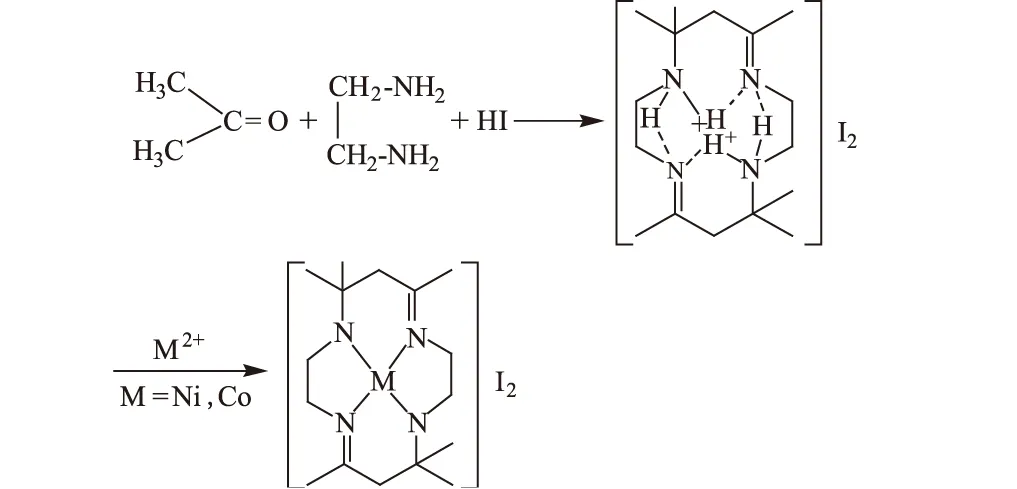
图1 合成路线
1 实验
1.1 试剂与仪器
丙酮、冰醋酸、氯化镍、氯化钴、无水乙醇、无水乙二胺、氢氧化钠、氢碘酸。
BIO-RADFTS-40型傅立叶红外变换光谱仪;BrukerDRx-500型核磁共振仪(甲醇、吡啶作溶剂,TMS为内标)。
1.2 方法
1.2.1 醋酸镍和醋酸钴的制备
将氯化镍/氯化钴与氢氧化钠溶液反应,得氢氧化镍/氢氧化钴沉淀,抽滤,将沉淀溶于醋酸,再减压蒸馏,得绿色醋酸镍[(Ni(OAc)2·4H2O]结晶/淡红色醋酸钴[(Co(OAc)2·4H2O]结晶。
1.2.2 大环配体[(14)4,11-二烯-N4]2HI的合成
方法Ⅰ:在250 mL烧杯中加入10 mL无水乙醇、13.2 mL无水乙二胺,置于冰浴中冷却,慢慢滴加36 mL 47%的氢碘酸,再加入30 mL丙酮,搅拌均匀,继续置于冰浴中冷却3 h使晶体析出完全,抽滤得白色晶体,真空干燥0.5 h,称重,得白色针状晶体19 g,产率36.0%,m.p. 145~148 ℃[14]。
方法Ⅱ:在250 mL烧杯中加入13.2 mL无水乙二胺,置于冰浴中冷却,慢慢滴加36 mL 47%的氢碘酸,放置3 h,有大块透明结晶,然后加入30 mL丙酮,微热使之溶解,此时有大量白色晶体析出,放置1 h,抽滤,红外灯下不停搅拌,干燥,得白色针状晶体20 g,产率37.8%。
1.2.3 大环配合物[Ni((14)4,11-二烯-N4)]I2和[Co((14)4,11-二烯-N4)]I2的合成
在装有冷凝管、搅拌器的100 mL三颈瓶中,加入20 mL甲醇、和配体等摩尔的醋酸镍,慢慢加热并搅拌,使其溶解,再加入大环配体[(14)4,11-二烯-N4]2HI,搅拌,回流1~1.5 h,趁热过滤,将滤液浓缩至有晶体析出,浓缩液在冰浴中冷却1 h左右,重结晶提纯,干燥,称重,得亮黄色大环配合物[Ni((14)4,11-二烯-N4)]I22 g,产率20.26%[15,16]。
将醋酸镍换成醋酸钴,实验步骤同上,同法制得紫红色大环配合物[Co((14)4,11-二烯-N4)]I23 g,产率30.4%。
2 结果与讨论
2.1 波谱分析(表1)
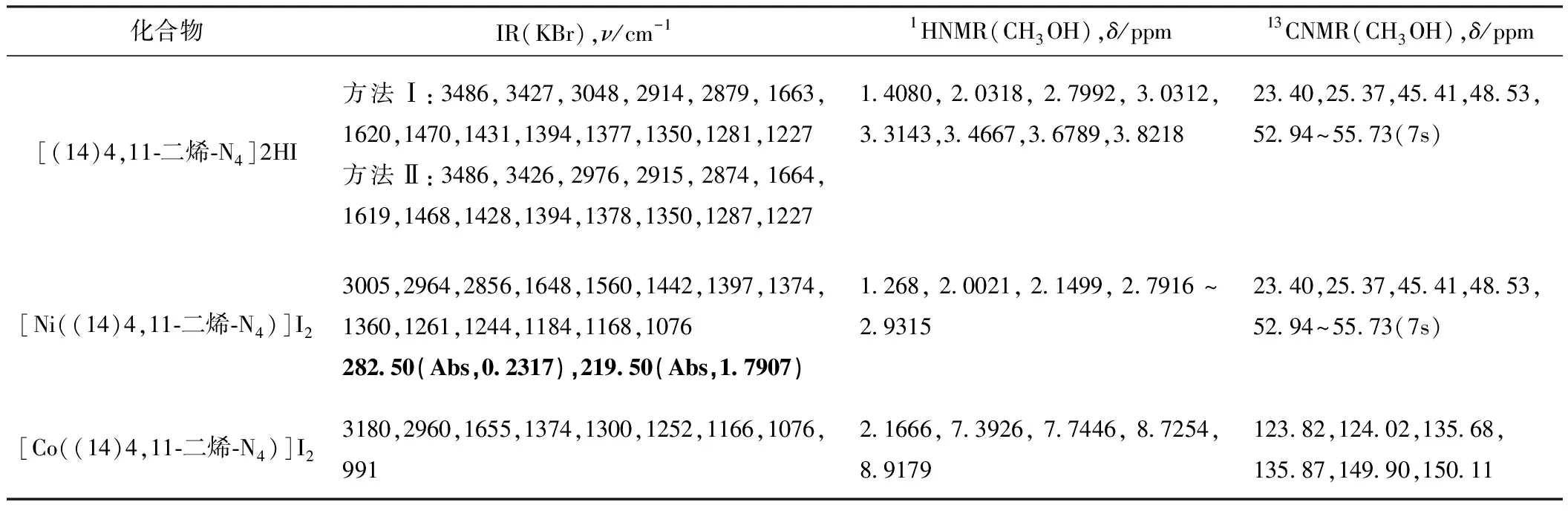
表1 化合物的波谱分析
2.2 讨论
2.2.1 合成反应历程分析(图2)
反应历程为在酸性条件下,丙酮缩合成4-甲基-3-戊烯-2-酮,然后与乙二胺发生亲核加成,反应生成β-氨基酮,这个分子的胺基与另一分子的羰基合成大环配体,然后大环配体与镍/钴离子反应生成大环金属配合物。
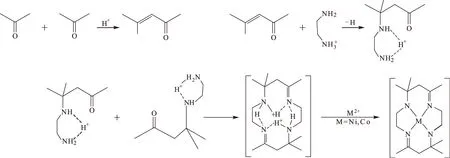
图2 合成反应历程
本合成路线原料易得,反应条件易于控制。尤其是丙酮羟醛缩合所得产物不用分离,直接在体系中与乙二胺加成后缩合,简化了操作。
2.2.2 合成大环配体[(14)4,11-二烯-N4]2HI的影响因素
(1)氢碘酸的量要加够,该反应是在酸性条件下进行,氢碘酸既起催化又起反应作用。若氢碘酸量不足,则反应慢且不完全,但滴加氢碘酸要慢,因为滴加太快会放出大量热而导致飞溅,还伴有大量白烟,有安全隐患。
(2)潮湿大环配体[(14)4,11-二烯-N4]2HI在空气中极易变色,甚至呈黄褐色,为此可在红外灯下不停搅拌,直到干燥为止,该方法比真空干燥更好。
(3)方法Ⅰ与方法Ⅱ相比,方法Ⅱ少用了无水乙醇,过量的无水乙二胺和氢碘酸可溶解在丙酮中,得到的大环配体([(14)4,11-二烯-N4]2HI更纯。
3 结论
在酸性条件下,丙酮缩合成异丙基丙酮,再与乙二胺反应生成β-氨基酮,再与另一酮基缩合得到[(14)4,11-二烯-N4]2HI,最后分别与Ni(OAc)2·4H2O和Co(OAc)2·4H2O进行反应,得到大环配合物[Ni((14)4,11-二烯-N4)]I2和[Co((14)4,11-二烯-N4)]I2,其结构经IR、1HNMR、13CNMR验证。
参考文献:
[1] 邓凡政,汤跃群.钴(Ⅱ)大环配合物的合成与吸氧性能研究[J].长沙水电师范学院学报(自然科学版),1994,9(4):375-378.
[2] 刘焕, 潘志权, 冷士良, 等. 不对称大环双核铜(Ⅱ)配合物[Cu2(C23H26Cl2N4O2)](ClO4)2的合成、晶体结构及磁性(英文) [J].无机化学学报,2011,27(3):590-594.
[3] 倪中海,张丽芳,崔爱莉,等.氰根桥联大环配合物的合成、结构与磁性研究[J].中国科学B辑:化学,2009,72(9):910-917.
[4] 阎世平,程鹏,夏庆,等.双核Cu(Ⅱ)、Ni(Ⅱ)与N-氧化-2,6-二甲酰吡啶Schiff碱大环配合物的合成和表征[J].高等学校化学学报,1993,14(2):164-166.
[5] 梁汝萍,赵庆琦,向华,等.大环镍配合物/Nafion膜修饰电极对一氧化氮的电催化氧化及测定[J].分析试验室,2001,20(5):53-55.
[6] 贾东方,林美容,房芳,等.带有苯酚侧臂的四氮大环配合物的光谱特性[J].天津大学学报,2001,34(2):256-260.
[7] 贾东方,林美容,房芳,等.二氧四胺大环配合物光谱特性与其催化活性关系的研究[J].光谱学与光谱分析,2002,22(1):99-102.
[8] 张浩明,陈展虹.过渡金属大环配合物电催化氧还原[J].新疆教育学院学报,1991,(4):79-82.
[9] 梁汝萍,邱建丁,黄婷婷,等.同时测定多巴胺和肾上腺素的大环镍膜修饰电极[J].分析测试学报,2002,21(6):31-34.
[10] 李凤莲,石硕,姚天明.大环配合物在核酸切割中的应用[J].化学通报,2008,71(10):731-738.
[11] 王银平,吴起峰,夏雨佳,等.Ho(Ⅲ)希夫碱大环配合物的合成、晶体结构及对DNA的切割活性[J].高等学校化学学报,2010,12(12):2344-2348.
[12] 朱早龙,刘景旺,达文燕,等.稀土姜黄素大环配合物的合成、表征及其荧光性质和抑菌活性研究[J].化学通报,2009,72(1):59-64.
[13] 王临艳.稀土大环配合物抗菌性研究[J].中国社区医师(医学专业),2010,12(1):94.
[14] Curtis N F.Macrocyclic coordination compounds formed by condensation of metal-amine complexes with aliphatic carbonyl compounds[J].Coordination Chemistry Reviews,1968,3(3):47.
[15] Curtis N F,House D A.Structure of some aliphatic Schiff-base complexes of nickel(Ⅱ) and copper(Ⅱ)[J].Chem and Ind,1961,(42):1708-1709.
[16] Merrell Philip H,Urbach F L,Arnold Michael.Synthesis and characterization of a macrocyclic nickel complex.An experiment to conclude an advanced inorganic or analytical course[J].J Chem Educ,1977,54(9):580-582.

