TSHR和 RASSF1A基因甲基化与乳头状甲状腺癌的相关性△
南方医科大学珠江医院内分泌科 (广州 510282)
戴亚丽 蔡德鸿* 陈 宏 张 振 张 桦 李 静
肿瘤的发生与原癌基因激活和抑癌基因失活,并最终引起基因表达异常有关。基因表达异常可能通过基因机制(Genetic mechanism)和表基因机制(Epigenetic mechanism)[1]来完成。 DNA甲基化是一种表观遗传修饰,对维持染色体的结构、X染色体的失活、基因印记和肿瘤的发生发展都起重要的作用,主要发生在启动子区 CpG位点[2]。正常组织的肿瘤抑癌基因不发生甲基化,当肿瘤抑癌基因发生甲基化后,就不能正常转录、翻译合成抑癌蛋白及发挥抑癌作用,细胞就有可能发生单克隆增生形成肿瘤。
乳头状甲状腺癌(Papillary thyroid carcinoma,PTC)是甲状腺最常见的恶性肿瘤,目前国外有研究报道甲状腺癌的发生也与抑癌基因启动子甲基化的发生密切相关[3],本研究选择了两种抑癌基因:促甲状腺激素受体(Thyroid stimulating hormone receptor,T SHR)和 RASSF1A基因,采用甲基化特异性 PCR(Methylation-specific PCR,M SP)法 ,对 PTC及对照组织进行研究,来探讨 PTC的发生机制。
对象和方法
1 研究对象 研究组为我院甲乳外科 2007~2009年收治的 50例 PTC患者(PTC组),男 15例,女35例,平均年龄 (40± 12)岁;对照组为我院甲乳外科同期收治的 32例良性甲状腺肿瘤患者,其中结节性甲状腺肿 20例,甲状腺腺瘤 12例;男 9例,女 23例,平均年龄(37±12)岁。两组均为新鲜手术标本,经病理检查确诊,标本切除后迅速转移至-80℃冰箱保存。
2 方 法
2.1 组织 DNA的提取:使用 QIAamp DNA Mini Kits 51304基因组提取试剂盒(美国 Qiagen公司)按说明书提取基因组 DNA,紫外分光光度仪检测其含量和纯度。
2.2 DNA甲基化修饰:使用 Cp GenomeTMDNA Modification Kit S7820(CHEMICON公司 )试剂盒对提取的 DNA进行亚硫酸氢钠处理和纯化。
2.3 甲基化特异性 PCR(MSP)扩增:两种抑癌基因的甲基化引物与非甲基化引物序列参照文献[4,5],见表 1,由上海生工公司合成。 PCR反应体系 25 μ l,上下游引物各 1 μ l(10pmol/μ l),甲基化修饰后的 DNA 2 μ l,所 用 试 剂 盒 为 2× PCR master mix K0171(Fermentas公司)。 2%琼脂糖凝胶电泳检测 PCR扩增产物。
两种抑癌基因 PCR(甲基化与非甲基化)扩增条件:95℃预变性 5min,95℃变性 30s,65℃(TSHR基因)/60℃(RASSF1A基因 )退火 30s,72℃延伸 30s,循环 30个周期,最后 72℃延伸 5min。
2.4 抑癌基因克隆及测序:每个抑癌基因各随机选取 2例 PTC及 2例对照组织(均包含甲基化标本及未甲基化标本各 1例),首先进行 PCR扩增,克隆后再测序。
2.5 统计学方法:采用 SPSS13.0统计软件,以Pearsoni2检验分析两个抑癌基因 PTC组与对照组间甲基化差别;PTC组 TSHR与 RASSF1A基因甲基化的相关性用 Spearman相关分析;以 Pearsoni2检验分析 PTC组两个抑癌基因启动子甲基化和主要的临床病理参数的关系,P<0.05为有统计学差异。

表1 PCR所用引物序列及片段大小
结 果
1 两种抑癌基因启动子甲基化分析:PTC患者中,发现 34/50例(68.0%)TSHR基因、30/50例(60.0%)RASSF1A基因启动子发生了甲基化;对照组患者中,7/32例(21.9%)TSHR基因、10/32例(31.3%)RASSF1A基因启动子发生甲基化;PTC组 TSHR基因和 RASSF1A基因启动子甲基化率均显著高于对照组,差异有统计学意义(P<0.05)(图 1,2)。
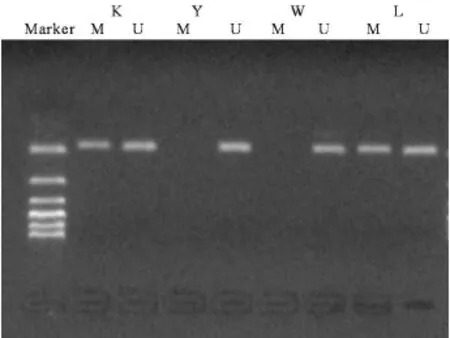
图1 TSHR基因启动子 M SP电泳图(Marker:100bp DN A标记物,K、L:PTC组,Y、W:对照组,U:非甲基化条带,M:甲基化条带)
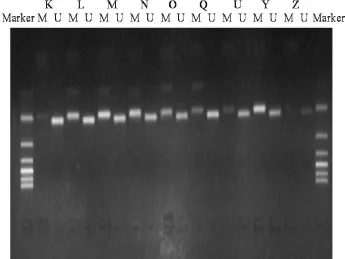
图2 RASSF1A基因启动子 M SP电泳图(Marker:100 bp DN A标记物,K、L、M、N、O、Q:乳头状甲状腺癌,上排 U、Y、Z:对照组织标本,下排 U:非甲基化条带,M:甲基化条带)
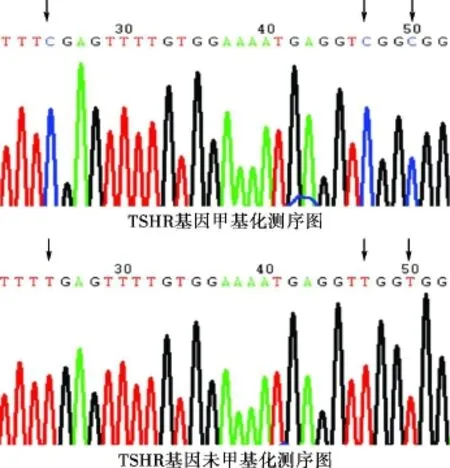
图3 测序图(TSHR基因启动子甲基化者 CpG岛中的 C仍为 C,未甲基化者 C均转变为 T)
2 测序结果:两个基因启动子发生了甲基化的,其所有 CpG位点碱基均发生了改变,即甲基化引物扩增产物中的 CpG位点的 C仍然保持 C,而非甲基化引物扩增产物中的 CpG位点中的 C转变为 T(图 3,4)。
3 PTC组 TSHR和 RASSF1A基因甲基化间的关系:PTC组织中 TSHR和 RASSF1A基因启动子均甲基化的为 26/50;TSHR甲基化而 RASSF1A基因未甲基化的为 8/50;TSHR未甲基化而 RASSF1A基因甲基化的为 4/50;TSHR和 RASSF1A基因启动子均未甲基化的为 12/50。计算 r=0.490(P=0.000),提示 PTC组 TSHR和 RASSF1A两个抑癌基因甲基化之间存在显著相关性。
4 两个抑癌基因甲基化与患者临床病理资料之间的关系:结合患者的临床病理资料,TSHR和RASSF1A基因甲基化与患者的年龄、性别、临床分期均未见相关性;TSHR基因与患者是否伴有淋巴结转移相关,RASSF1A基因与患者是否伴有淋巴结转移无关 ,见表 2。
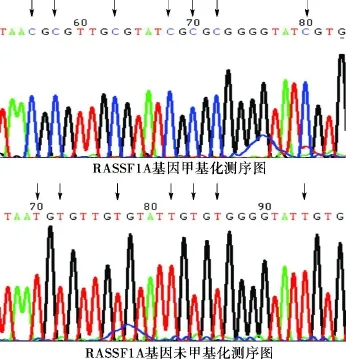
图4 测序图(RASSF1A基因启动子甲基化者 CpG岛中的 C仍为 C,未甲基化者 C均转变为 T)
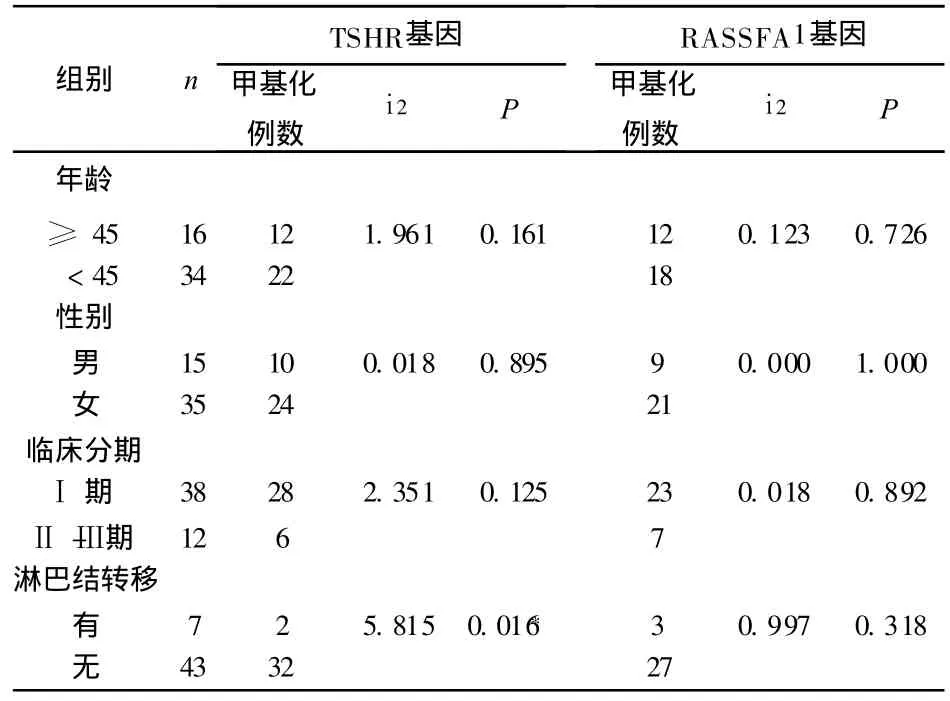
表2 两个抑癌基因启动子甲基化和主要临床病理参数的关系
讨 论
表基因机制主要指 DNA 5’CpG岛胞嘧啶甲基化改变[1],引起基因表达异常。肿瘤中 DNA甲基化异常表现为基因中散在的 CpG位点甲基化普遍下降和区域性 CpG岛高甲基化并存及细胞总的甲基化能力升高。目前人们已在多种肿瘤(乳腺癌、卵巢癌、结肠癌、肾癌、鼻咽癌等)的发生中证实抑癌基因启动子区的甲基化与肿瘤的发生密切相关[6],有关甲状腺肿瘤与抑癌基因甲基化的关系,国外也有相关报道。
Jason等[5]对 32例 PTC患者和 27例对照组采用MSP方法进行研究,发现 T SHR在癌组织的甲基化率为 34%,在对照组中为 7%,两者存在显著统计学差异,并且在甲状腺癌组发现了 TSHR甲基化的肿瘤复发率高,未发生甲基化的肿瘤复发率低,他们认为抑癌基因启动子区的甲基化是甲状腺癌的一个恶性标记。Schagdarsurengin等[7]采用 MSP法 ,对 13例 PTC,10例滤泡型甲状腺癌,9例未分化甲状腺癌,6例髓样甲状腺癌,12例结节性甲状腺肿及 10例滤泡型腺瘤进行研究,发现 PTC患者 TSHR启动子甲基化率为58%,未分化甲状腺癌为 86%,而在对照组达到 80%,T SHR启动子甲基化率仅在未分化癌中较其他甲状腺癌高。唐建东[8]等用 M SP法在 PTC组织中发现RASSF1A基因启动子甲基化的发生率为 55.9%(19/34),癌旁组织中甲基化的发生率为 23.5%(8/34),认为甲基化可能与 PTC发生发展有关。
我们使用 MSP法,检测了 50例 PTC和 32例对照 TSHR和 RASSF1A基因启动子甲基化情况,发现了两种抑癌基因启动子的甲基化频率在 PTC中明显高于对照组(P<0.05);测序结果证实了两个基因启动子 CpG岛的所有 CpG位点均发生了甲基化。有研究发现多个抑癌基因启动子甲基化在肿瘤的发生发展中有协同作用,多个抑癌基因甲基化对信号转导通路的影响可能较单一基因甲基化更为重要[5]。我们进一步对两种抑癌基因甲基化之间相关性进行分析,发现T SHR和 RASSF1A之间存在关联性,这可能是由于两种抑癌基因的作用环节相同:TSHR基因和RASSF1A基因都主要作用于信号传导[9]。 PTC组两种抑癌基因启动子甲基化,均与肿瘤的临床分期无关,提示两种抑癌基因启动子甲基化可能在甲状腺肿瘤的早期阶段既已发生;但 TSHR基因启动子甲基化率在有淋巴结转移的 PTC高于无淋巴结转移的病例,提示该抑癌基因启动子甲基化在甲状腺癌的恶性进展中可能发挥一定作用。仅从我们的研究结果表明,在 PTC中两种抑癌基因启动子的高甲基化可能抑制了抑癌基因的表达,使得抑癌基因对 PTC的抑制作用减少,从而促进了 PTC的发生和发展,另 TSHR基因和RASSF1A基因在 PTC的发生中可能起到协同作用。因此,我们的研究提供了证据:在 PTC中异常的抑癌基因启动子甲基化可能是抑癌基因沉寂的一个重要机制。
总之,我们在 PTC的研究显示了 TSHR和RASSF1A两种基因异常的甲基化在 PTC中是一种较普遍的现象,可能是基因沉寂的一个潜在分子通路,与 PTC的发生、发展有一定联系。虽然 DNA甲基化是一个复杂的过程,许多细节尚未明了,但随着对这一领域研究的深入以及对于肿瘤发生机制的逐渐明释,我们相信它对于肿瘤早期预测与干预以及预后评估等将会有重要作用。
[1]Byun DS,Lee M G,Chae KS,et al.Frequent epigenetic inactivation of RASSF1A by aberrant promoter hypermethylation in human gastric adenocarcinoma[J].Cancer Res,2001,61(19):7034-7038.
[2]Partha M,Rakesh S.DNA methylation and cancer[J].J Clin Oncol,2004,22(15):4632-4642.
[3]Xing M,Usadel H,Cohen Y,et al.Methylation of the thyroid-stimulating hormone receptorgene in epithelial thyroid tumors-a marker of malignancy and a cause of gene silencing[J].Cancer Res,2003,63(5):2316-2321.
[4]Jason A,Chun-Yang Fan,ChunlaiZou,etal.Methylation status of genes in papillary thyroid carcinoma[J].Arch Otolaryngol Head Neck Surg,2007,133(10):1006-1011.
[5]Schagdarsuregin U,Gimm O,Cuong Hoang-Vu C,et al. Frequent epigenetic silencing ofthe CpG island promoter of RASSF1A in thyroid carcinoma[J].Cancer Res,2002,62(12):3698-3701.
[6]刘桂芝,吴逸明,杨继要,等.非小细胞肺癌组织中RASSF1A和 P16基因启动子甲基化研究 [J].陕西医学杂志,2007,5(36):515-520.
[7]Schagdarsurengin U,Gimm O,Dralle H,et al.CpG island methylation of tumor-related promoters occurs preferentially in undifferentiated carcinoma[J].Thyroid,2006,16(7):633-642.
[8]唐建东,欧阳军,栗夏莲,等.甲状腺乳头状癌组织中RASSF1A基因启动子甲基化与临床病理学的关系 [J].天津医药,2007,35(12):887-889.
[9]Tommasi S,Dammann R,Jim SG,et al.RASSF3 and NORE1: identification and cloing of two human homologuesoftheputativetumorsuppressorgene RASSF1[J].Oncogene,2002,21(17):2713-2720.

