晶态锂离子固体电解质的最新研究进展
王伟国,李卫东,马文强,侯新儒
(延安大学 物理与电子信息学院,陕西 延安 716000)
晶态锂离子固体电解质的最新研究进展
王伟国,李卫东,马文强,侯新儒
(延安大学 物理与电子信息学院,陕西 延安 716000)
锂离子电解质是高功率密度和能量密度、长循环寿命和安全性能良好的锂离子电池的关键材料之一,对锂电池的发展起着非常重要的作用。简单介绍了几种主要类型锂离子晶态固体电解质材料的研究情况,并详细概括了最近晶态锂离子固体电解质的研究热点材料——类石榴石结构的 Li5La3M2O12(M=Ta,Nb)锂离子导体,最后对以 Li5La3M2O12(M=Ta,Nb)锂离子导体为代表的晶态锂离子固体电解质的研究做出了展望。
锂离子电池;晶态锂离子固体电解质;Li5La3M2O12(M=Ta,Nb)
锂离子电池自20世纪90年代初实现商业化以来,因其自身的优越性能而得到了迅速的发展,已经在汽车交通、手机通信、笔记本电脑以及数码摄像等多个领域中得到了广泛的应用。但是目前主要使用的锂离子电池的电解质主要是含有可燃性液体有机物,这给锂离子电池在使用中带来了很大的安全隐患,在一定程度上限制了其应用范围的继续扩大。虽然聚合物电解质在一定程度上缓解了这个问题,然而由于聚合物电解质本身在使用过程中容易出现“脱水现象”以及与锂或其他高电位插层材料的电化学性能不稳定等问题决定了这种材料并不是一种完美的解决方案。而使用不可燃晶态锂离子固体电解质不仅能排除电池内部短路和液体电解质泄漏的问题,还能彻底解决由于电解液造成的安全隐患问题。另外,在高温环境下的工作更是其它两种电解质体系所不具备的。正是基于以上这些优点,近年来国际上对晶态锂离子固体电解质的研究和开发十分 活 跃[1]。
本文在简要介绍了几种主要的晶态锂离子固体电解质材料(LISICON结构、NASICON结构、钙钛矿结构)的基础上重点介绍一下最近的研究热门——类石榴石结构的 Li5La3M2O12(M=Ta,Nb)电解质。
1 具有 LISICON结构的锂离子固体电解质
对 Li4GeO4进行掺杂调控导致其结构向 γ-Li3PO4结构的转变,进而形成了所谓的 LISICON(lithium super ionic conductor)结构,其典型的代表物质是有 MIT的 Hong博士研究报道的Li14Zn(GeO4)4材料[2],这种材料以 Li11Zn(GeO4)4形成了坚固的三维网络结构,而剩下的三个间隙 Li+则可以通过上面的网络结构进行扩散迁移。对 LISICON结构锂离子导体的研究主要集中在掺杂以及探索新的制备烧结方法两个方面:通过掺杂提高晶体结构的稳定性、改善Li+的扩散通道以及弱化骨架和迁移的Li+之间的相互作用来提高电导率[3];通过采用新的制备方法和烧结工艺的改进,改善了LISICON陶瓷样品的颗粒形貌并提高了材料的离子电导率。如冯守华[4]等人利用微波加热合成 LISICON结构的快离子导体 Li2+2xZn1-xGeO4。当 x=0.75时即 Li3.5Zn0.75GeO4,在 100℃下的锂离子电导率可以达到0.13 S/cm。最近对LISICON类型材料的改性主要是硫代LISICON(thio-LISICON)。
固体电解质的研究,通过半径比较大的 S离子取代氧离子可以显著增大晶胞尺寸,扩大离子传输瓶颈尺寸,使 LISICON型固体电解质的离子电导率有了大幅度提高[5]。
2 具有 NASICON结构的锂离子固体电解质
NASICON(Na super Ionic Conductor)结构的锂陶瓷电解质具有非常高的离子导电率,其母体为NaZr2P3O12,组成可用通式 Li(A2B3O12)来表示。A、B分别指的是四价(Ti、Zr或 Sc等)和五价(P、Si或Mo)阳离子。在这种结构是由 AO6八面体和BO4四面体共用顶角形成[A2(PO4)3]刚性结构,锂离子就在该三维隧道结构中迁移扩散[6-10]。但是锂离子在传输通道中迁移时存在骨架收缩和离子迁移的协同运动,只有当传输通道与迁移离子的半径匹配到一定程度时才能有利于锂离子的迁移。用锂离子取代钠离子得到化合物Li3Zr2Si2PO12的离子电导率比母体材料 Na3Zr2Si2PO12约下降了大约三个数量级,其直接原因是NASICON结构中适合于Na+的传输通道相对于半径比较小的 Li+来说太大了,反而不利于 Li+的传输扩散[11]。
对 NASICON型固体电解质材料的电学性质的改善方面主要以掺杂为主:1)用半径较小的 Ti4+替代 Zr4+来减小Li+的传输通道半径,明显改善Li+的电导率,化合物LiTi2P3O12在室温下的电导率可以达到 10-6S/cm;2)用化学价态比较低的阳离子 Al3+、La3+、Cr3+、Fe3+和 In3+分别取代其中的Zr4+或 P5+来提高载流子的浓度;3)通过掺杂提高陶瓷的烧结性能,降低晶粒边界电阻,进而提高该材料的导电性[12]。尽管通过掺杂可以改善具有 NASICON结构的导锂陶瓷电解质的传输通道,产生锂离子间隙或者空位,同时也可以降低材料的孔隙率和晶界电阻[13],从而大幅度改善材料的锂离子电导率。但是这类材料一般情况下对金属锂不稳定,容易在低电位被还原产生电子电导,这极大地影响了这类材料在全固体锂离子电池中的应用前景。
3 具有钙钛矿结构的锂离子固体电解质
钙钛矿结构的一般通式为 ABO3,这类物质一般情况下具有很多的 A位置空位,锂离子可以比较容易借助于这些空位扩散迁移,因而其中锂空位的浓度以及锂离子的浓度对锂离子的电导率有着非常重要的影响[14]。最具典型的 ABO3型锂离子固体电解质是由 Belous等人[15]通过三价的 La3+和单价的锂离子 Li+共同取代 CaTiO3中的二价 Ca2+而得到钙钛矿结构化合物 La2/3-xLi3xTiO3(0.04<x<0. 167,LLTO),其中A位格点并没有完全被三价的La3+和半径较小的单价锂离子 Li+所占据,空位的数量为(1/3+x),锂离子则通过 La3+周围的通道(有四个氧原子组成的四边形)在空位间进行迁移扩散。钙钛矿结构化合物 La2/3-xLi3xTiO3的晶体结构不仅和锂离子数目(或者说锂离子空位)相关,而且还和样品的制备方法有关,这使得在同一种物质在不同的制备方法下锂离子的活性是不相同的。如用柠檬酸络合法制备的 LLTO材料较用传统固相法制备的 LLTO材料具有更高的锂离子活性和离子电导率[16]。LLTO型锂离子导体材料的结构随着锂离子含量的变化而变化,目前已发现的晶体结构大致有 四种:立 方 结构[17,18]、四方结构[19,20]、正交结构[21,22]和 六 角 结 构[23]。
在电学性质方面,LLTO材料体系在室温下的锂离子电导率随锂含量的增加表现出先增加后减小的性质。当锂含量达到 0.11(La0.56Li0.33TiO3)时,在室温条件下晶粒电导率最高可以达到 1×10-3S/cm,接近于固溶体 Li4-xGe1-xPxS4(x=0.75)在室温下的锂离子电导率。对LLTO型锂离子固体电解质材料电学性质的研究主要集中在结构元素的掺杂或部分元素的替代改善锂离子的扩散通道和提高载流子锂离子的含量进而提高锂离子电导率。譬如(1)用离子半径比较大的 Ba2+、Sr2+来取代A格点上的La3+[24,25],或用离子半径较小的Pr3+取代 A格点上的 La3+,结果发现前两种掺杂可以提高离子电导率而后面的 Ca掺杂则不利已锂离子的扩散[26];(2)Al3+,Ta5+,Nb5+取 代 或 部 分 取 代 B位 格点 上 的Ti4+[27-29]。尤其是Al3+的取代,不仅可以改善锂离子的扩散通道和提高载流子的浓度,而且 Al-O键的束缚能要强于Ti-O,通过强化B-O键来相对减弱了氧离子对 A格点上锂离子的束缚,从而提高了离子电导率。
最近又有新的研究将晶体结构中的部分氧离子O2-用 F-取代,虽然后者的离子半径小于前者,会减小离子扩散的瓶颈尺寸,但是 B-F之间的键能大于B-O键能,在某种程度上降低了 A-O之间的键强,减小了O对A格点上的离子的束缚,提高了材料的锂离子电导。当 F的掺杂量为0.072时(La0.56Li0.258TiO2.928F0.072),室 温体 晶 粒 电 导 率 可以达到1.59×10-3S/cm,相对于母体 La2/3-xLi3xTiO3(LLTO,x=0.11)提高了将近 50%[30]。
尽管 LLTO材料的锂离子电导率非常高,但是
这类电解质含有容易变价的钛离子,与金属锂接触时在低电位(1.7 V)下将Ti4+被还原为 Ti3+,产生电子电导,成为锂离子和电子的混合导体[31],另外这种材料的晶界电阻非常高,大约是晶粒电阻的50倍,使得 LLTO材料总的离子电导率大约在 10-5S/cm,这在一定程度上限制了这类固体电解质在锂离子电池中的应用。最近研究还发现这种材料暴露在空气中易吸附空气中的水蒸气和二氧化碳,产生新的化合物 (Li0.3-xHx)La0.57TiO3且伴 随 着 Li2CO3的生成[32],其具体的反应过程可以表示为:
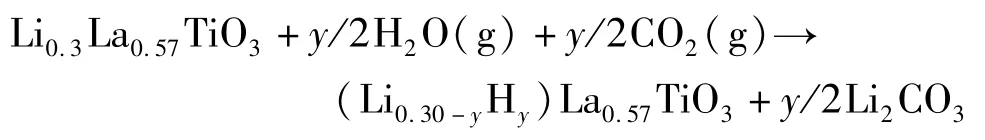
4 类石榴石结构的锂离子固体电解质
针对前面介绍的几种无机固体电解质不足之处,很多离子学研究工作者们多年来不断地研究和设计新型的锂离子导体材料,使其满足分解电压比较高、与金属锂比较稳定不产生电子电导并具有非常好的室温电导率。最近,Weppner等人[33-35]报道了一类基于母相为 Li5La3Ta2O12的新 型锂离子导体,该类型氧化物锂离子电解质具有类石榴石结构(空间群I213),其中,La3+离子占据八配位的十二面体位置,而 Ta5+离子则与O2-离子形成 TaO6八面体。与理想的(SiO4)3型石榴石结构中的简单SiO4四面体不同的是,在 Li5La3Ta2O12中,由于单胞中 Li+离子浓度高(同理想石榴石结构相比,每个单胞中有16个额外 Li+离子分布),因此,Li+离子在晶格中的占位比较复杂,目前对其还没有很清晰的认识。Cussen[36]根据中子衍射的结果拟合分析认为,不管是四面体中心24 d位置还是八面体中心的48 g位置都是部分占据的,大约有 80%的24 d和40%的48 g格点被锂离子所占据,换句话说大约有20%和60%的空位没有被锂离子所占据,正是因为在 Li5La3M2O12(M=Ta,Nb)中有如此多的锂空位,为锂离子的迁移提供了迁移的通道,从而使得Li5La3M2O12(M=Ta,Nb)在室温情况下有较好的锂离子电导率,而且锂离子扩散传输的方向是三维的。
电性能研究结果显示,纯 Li5La3Ta2O12在室温下 Li离子电导率可达 3.4×10-6S/cm[33],而电子电导至少要低两个量级,表现出典型的纯锂离子导电特性。同时,Li5La3Ta2O12还具有很高的化学稳定性(分解电压 >6 V),同目前已实用化的正极材料LiCoO2在900℃以下不发生反应[37]。尤其有意义的是同钙钛矿结构的锂离子电解质 LLTO相比,Li5La3Ta2O12中不含可变价的 Ti离子,作为电解质使用时没有因阳离子变价而产生电子电导的问题。电学性质改善方面,对 La位进行部分二价阳离子替代(如Ca2+,Sr2+,Ba2+等)后,Li5La3Ta2O12能够在保持化学稳定性不变的情况下大幅度提高导电性能,如部分 Ba掺杂的多晶 Li6BaLa2Ta2O12室温下的Li离子电导率可达 4×10-5S/cm[37,38],可同钙钛矿型LLTO多晶电解质相比较,而比薄膜化的 LiPON高一个量级以上。此外,该类型电解质的另一个显著优点是晶界电阻非常低,适量的 Sr2+、Ba2+掺杂甚至能使晶界电阻降低至总电阻的 10~14%。在M的格点位置,用三价 In3+来部分取代 M5+[39],来实现增加晶格常数和载流子浓度进而改善材料的电导率目的。尤其是在 化合物 Li5+xLa3-xBaxTa2O12中当 x=1时对应的化合物Li6La2BaTa2O12在室温下的电导率可以达到 4×10-5S/cm,而且在几种与对金属 Li稳定的无机晶体电解质中仅仅低于分解电压为0.45 V的二维锂离子导体Li3N。最近Thangadurai等人进一步用 Zr4+来取代 M5+得到Li7La3Zr2O12锂离子导体[40],该材料在 18℃的温度下,晶粒电导率可以达到4×10-4S/cm,总的电导率可以达到2.3 ×10-4S/cm,与现在通用的有机液体电解质的电导率 10-3S/cm相比已经很接近了,大大提升了无机晶态固体电解质在全固体锂离子电池中的应用潜力。
5 发展展望
就目前的研究而言,对锂离子无机晶态固体电解质的研究主要集中在如何提高优化它们的离子电导率和电化学稳定性方面。在电学性能改善方面,主要集中在以下三个方面:1)通过掺杂调控锂离子的传输通道尺寸使其和锂离子的半径大小想匹配;2)弱化锂离子和骨架离子之间的键合力;3)调节锂空位使其和锂离子浓度的比例适中。其中最有希望应用于锂离子电池电解质当属具有类石榴石结构的锂离子导体Li5La3M2O12(M=Ta,Nb),这类材料不管是离子电导率(室温总电导率 10-4S/cm)、分解电压(高于6 V)以及与电池电极材料的稳定性方面(与 LiCoO2(1173 K)以及熔融的金属 Li保持稳定)均优于其它种类的锂离子电池电解质材料。但是这类材料最高的电导率仍然与现在业已商业化的有机液体电解质的电导率相比还要低一个数量级左右。因此,必须进一步改善锂离子的传输能力,提高其锂离子的电导率。作者认为可能的途径如下:(1)用半径比较大、化合价比较低的离子取代化合物Li7La3Zr2O12的镧离子来调控离子扩散通道半径和锂离子(空位)浓度;(2)采用 sol-gel的方法取代目前所采用的固相反应,优化烧结工艺,来提高材料的致密度;(3)用离子半径大的硫离子取代化合物Li7La3Zr2O12中的氧离子,从而得到更大的锂离子传输通道,得到更高的锂离子室温电导率。
[1]Thangadurai V,WeppnerW.Recent progress in solid oxide and lithium ion conducting electrolytes research[J].Ionics,2006,12(1):81-92.
[2]Robertson A D,West A R,Ritchie A G.Review of crystalline lithium-ion conductors suitable for high temperature battery applications[J].Solid State Ionics,1997,104(1-2):1-11.
[3]Kanno R,Murayama M,Inada Taro.A self-assembled breathing interface for all-solid-state ceramic lithium batteries[J].Electrochem and Solid-State Lett,2004,7(7):A455-A458.
[4]冯守华,庞广生,徐如人.微波诱导合成固体快离子导电材料[J].高等学校化学学报,1996,17(10):1495-1499.
[5]吴显明,李新海,许名飞,等.锂离子固体电解质的研究回顾[J].电源技术,2003,27(S1):255-259.
[6]Leo C J,Chowdari B V R,Subba G V,et al.Lithium conducting glass ceramic with Nasicon structure[J].Mater Res Bull,2002(37):1419-1430.
[7]Aatiq A,Menetrier M,Croguennec L,et al.On the structure of Li3Ti2(PO4)3[J].Mater Chem,2002,12(10):2971-2978.
[8]Masquelier C,Wurm C,Carvajal R,et al.A powder neutron diffraction investigation of the two rhomobohedral NASICON analogues:γ-Na3Fe2(PO4)3and Li3Fe2(PO4)3[J].Chem Mater,2000(12):525-532.
[9]París M A,Martínez-Juárez A,Iglesias JE,et al.Phase transition and ionicmobility in LiHf2(PO4)3with NASICON structure[J].Chem Mater,1997,9(6):1430-1436.
[10]Takada K,Tansho M,Yanase I,et al.Lithium ion conduction in LiTi2(PO4)3[J].Solid State Ionics,2001,139(3-4):241-247.
[11]Arbi K,Lazarraga M G,Chehimi BD,et al.Lithium mobility in Li1.2Ti1.8R0.2(PO4)3compounds(R=Al,Ga,Sc,In)as followed by NMR and impedance spectroscopy[J]. Chem Mater,2004,16(2):255-262.
[12]Aono H,Suqimoto E,Sadaoka Y,et.al,Ionic conductivity of solid electrolytes based on lithium titanium phosphate[J].Electrochem Soc,1990,137(4):1023-1027.
[13]庞明杰,王严杰,曹涯路,等.锂快离子导体 Li3-2x(Al1-xTix)2(PO4)3的合成与表征[J].材料科学与工程学报,2005,23(5):545-548.
[14]Stramare S,Thangadurai V,Weppner W.Lithium lanthanum titanates:A review[J].Chem Mater,2003,15(25):3974-3990.
[15]Belous A G.Lithium ion conductors based on the perovskite La2/3-xLi3xTiO3[J].JEuropean Ceram Soc,2001,21(10-11):1797-1800.
[16]李景新,温兆银,许晓雄,等.柠檬酸络合法制备 La0.56Li0.33TiO3锂离子导电材料[J].无机材料学报,2007,22(3):432-436.
[17]Inaguma,Liquan Y,Itoh C,et.al.High ionic conductivity in Lithium Lanthanum Titanate[J].Solid State Commun,1993,86(10):689-693.
[18]Ban CW,Choi G M.The effect of sintering on the grain boundary conductivity of lithium lanthanum titanates[J]. Solid State Ionics,2001,140(3-4):285-292.
[19]Crosnier-Lopez M P,Duroy H,Calage Y,et al.New A-deficient perovskites in the series LixLa2/3Ti1-xFexO3(0. 12<x<0.33)and La(2+x)/3Ti1-xFexO3(0.5<x<1)[J].Mater Res Bull,2001,36(3-4):651-660.
[20]Bhuvanesh N S P,Bohnke O,Duroy H,et al.Topotactic H+/Li+ion exchange on La2/3-xLi3xTiO3:New metastable perovskite phases La2/3-xTiO3-3x(OH)xand La2/3-xTiO3-3x/2obtained by further dehydration[J].Mater Res Bull,1998,33(11):1681-1691.
[21]París M A,Sanz J,León C,et.al.Limobility in the orthorhombic Li0.18La0.61TiO3perovskite studied by NMR and impedance spectroscopies[J].Chem Mater,2000,12,(6):1694-1701.
[22]Inaguma Y.Katsumata T,Itoh M.Crystal structure of a lithium ion-conducting perovskite La2/3-xLi3xTiO3(x=0.05)[J].Solid State Chem,2002,166(1):67-72.
[23]Alonso JA,Sanz,J,Santamarl'a J,etal.On the location of Li+cations in the fast Li-Cation conductor La0.5Li0.5TiO3perovskite[J].Angew Chem Int Ed,2000,39(3):619-621.
[24]Morata-Orrantia A,García-Martín S,Alario-Franco M Á.New La2/3-xSrxLixTiO3solid solution:Structure,Microstructure,and Li+conductivity[J].Chem Mater,2003,15(1):363-367.
[25]Varaprased A M,Shashi Mohan A L,Chakrabarty D K,et al.Structure and dielectric studies of some perovskitetype titanates[J].Phys C:Solid State Phys,1979,12(3):465-467.
[26]Morales O,West A R.Phase diagram,crystal chemistry and Lithium ion conductivity in the perovskite-type system,Pr0.5+xLi0.5-3xTiO3[J].Solid State Ionics,1996,91(1-2):33-43.
[27]Morata-Orrantia A,Garcl'a-Martl'n S,Mora'n E,et al.A new La2/3-xLixTi1-xAlxO3solid solution:structure,microstructure,and Li+conductivity[J].Chem Mater,2002,14(7)2871-2875.
[28]Mizumoto K,Hayashi S.lithium ion conduction in A-site deficient perovskites R1/4Li1/4TaO3(R=La,Nd,Sm and Y)[J].Solid State Ionics,1999,116(3-4),263-269.
[29]Garcl'a-Martl'n S,Rojo JM,Tsukamoto H,et al.Lithium-ion conductivity in the novel La1/3-xLi3xNbO3solid solution with perovskite-related structure[J].Solid State Ionics,1999,116(1-2):11-18.
[30]Li JX,Wen Z Y,Xu X X,et al.Lithium-ion conduction in the anion substituted La2/3-xLi3x-yTiO3-yFyelectrolyte with perovskite-type structure[J].Solid State Ionics,2005,176(29-30):2269-2273
[31]Birke P,Scharner S,Huggins R A.Electrolytic stability limit and rapid lithium insertion in the fast-ion-conducting Li0.29La0.57TiO3perovskite-type compound[J].J Electroehem Soc,1997,144(6):L167-L169.
[32]Boulant A,Bardeau J F,Jouanneaux A,et al.Reaction mechanisms of Li0.30La0.57TiO3powder with ambient air:H+/Li+exchange with water and Li2CO3formation[J]. Dalton Trans,2010,39(6):3968-3975.
[33]Thangadurai V,Schwenzel J,Weppner W.Tailoring ceramics for specific application:A case study of the development of all-solid-state lithium batteries[J].Ionics, 2005,11(1):11-23.
[34]Thangadurai V,Kaack H,Weppner W J F.Novel Fast Lithium Ion Conduction in Garnet-Type Li5La3M2O12(M=Ta,Nb)[J].Am Ceram Soc,2003,86(3):437-440.
[35]Thangadurai V,Adams S.Weppner W.Crystal structure revision and identification of Li+-ion migration pathways in the garnet-like Li5La3M2O12(M =Nb,Ta)oxides[J].Chem Mater,2004,16(16):2978-3006.
[36]Edmund JC.The structure of lithium garnets:cation disorder and clustering in a new family of fast Li+conductors[J].Chem Commun,2006,412-413.
[37]Thangadurai V,Weppner W.Investigations on electrical conductivity and chemical compatibility between fast lithium ion conducting garnet-like Li6BaLa2Ta2O12and lithium battery cathodes[J].JPower Sources,2005,142(1-2):339-344.
[38]Thangadurai V,and WeppnerW.Li6ALa2Ta2O12(A=Sr,Ba):Novel Garnet-Like Oxides for Fast Lithium Ion Conduction[J].Adv Funct Mater,2005,15(1):107-112.
[39]Thangadurai V,and Weppner W.Effect of sintering on the ionic conductivity of garnet-related structure Li5La3Nb2O12and In- and K-doped Li5La3Nb2O12[J].J Solid State Chem,2006,179(4):974-984.
[40]Murugan R,Thangadurai V,and WeppnerW.Fast Lithium Ion Conduction in Garnet-type Li7La3Zr2O12[J].Angew Chem Int Ed,2007,46(41):7778-7781.
[责任编辑 贺小林]
New Development of the Crystalline Lithium-ion Solid Electrolytes
WANGWei-guo,LIWei-dong,MAWen-qiang,HOU Xin-ru
(College of Physics and Electronic Information,Yan an University,Yan an 716000,China)
Lithium-ion electrolyte is one of the keymaterials in the lithium-ion secondary batteries of high power density and energy density,long cycle life and the better safety performance,playing an important role in the development of the lithium-ion secondary batteries.The progress of the several kinds of the lithium-ion crystalline solid electrolyte was presented and further the investigation of the garnet-like lithium ion conductor Li5La3M2O12(M=Ta,Nb),attractingmany groups attentions for its excellent electrical performance and electrochemistry stability,was summarized in detail.Finally,the possible development of the crystalline lithium-ion solid electrolyte based on the Li5La3M2O12(M=Ta,Nb)was suggested.
lithium-ion secondary batteries;crystalline lithium-ion solid electrolyte;Li5La3M2O12(M=Ta,Nb)
TM 912.9
A
1004-602X(2011)01-0032-05
2010 -01 -07
陕西省自然科学基金(2010JQ6007,2010JK917);延安大学专项基金(YD2009-2)
王伟国(1981-),男,河南洛阳人,延安大学讲师,博士。

