RP-HPLC法测定天山雪莲口服液中绿原酸及芦丁
贾丽华, 凯赛尔·阿不拉
(1.新疆生产建设兵团医院,新疆乌鲁木齐 830002;2.新疆维吾尔自治区食品药品检验所,新疆 乌鲁木齐 830004)
天山雪莲口服液是以菊科风毛菊属植物天山雪莲(Sau-ssurea involucrataKar.et Kir.)Sch.-Bp.为原料,运用现代技术研制而成的纯天然单味口服制剂。本品收载于《国家中成药标准汇编》经络肢体脑系分册[1],其测定方法为以芦丁作对照,用紫外分光光度法测定总黄酮量,缺乏专属性。文献报道天山雪莲中的紫丁香苷为其有效成分之一,其质量分数为0.232 mg/g[2]。曾经采用高效液相色谱法,对天山雪莲口服液中紫丁香苷的测定进行了研究,以进一步探索专属性较强的质量控制方法。然而天山雪莲口服液中紫丁香苷量较低,平均每1 mL 含0.03 mg[3],不适宜作含测指标。天山雪莲药材主要含芦丁、槲皮素、高车前素、柯伊利素、木犀草素等黄酮类,大苞雪莲碱等倍半萜内酯类,挥发油类,还有绿原酸、紫丁香苷、多糖等成分[2-9]。高车前素、柯衣利素及大苞雪莲碱等无对照品可供用于测定。天山雪莲药材中绿原酸及芦丁的定量测定已收载于《中国药典》2005年版一部[5-6],为保证天山雪莲口服液质量的可控性,采用HPLC法对其所含成分绿原酸和芦丁同时进行了测定,该方法简单易行,重复性好,可用于天山雪莲口服液的质量控制。
1 仪器与试药
1.1 仪器 Waters高效液相色谱仪,包括Waters 1525双元高压泵,Waters 2487双通道紫外检测器,Waters 717自动进样器,Brezee色谱工作站;BP211D电子天平(赛多利斯公司);KLZ-UP高端超纯水机(台湾艾柯成都康宁实验专用纯水设备厂)。
1.2 试药 绿原酸对照品(中国药品生物制品检定所,批号:110753-200212供含量测定用)。芦丁对照品(中国药品生物制品检定所,批号:0880-9705供定量测定用)。甲醇为色谱纯(Fisher公司),水为超纯水,其他试剂均为分析纯。天山雪莲口服液(新疆天山雪莲制药有限公司,批号20040208, 20040628, 20040804, 20040921, 20050606,20050711,20050824,20050930)
2 方法与结果
2.1 色谱条件 Waters Symmetry shieldTMRP18(4.6 mm ×150 mm,5 μm,Ireland);以乙腈为流动相 A,0.4% 磷酸溶液为流动相B,按表1进行梯度洗脱;体积流量为1.0 mL/min,柱温为30 ℃;检测波长为340 nm[5];进样:10 μL 测定。在以上色谱条件下,与其它组分分离度良好,见色谱图1。

表1 流动相洗脱程序
2.2 对照品溶液制备 分别精密称取120℃减压干燥至恒重的芦丁,和绿原酸对照品各适量,加50%甲醇制成每1 mL含芦丁100 μg、绿原酸40 μg的混合溶液,作为对照品溶液。
2.3 供试品溶液的制备 精密量取本品10 mL,置25 mL
量瓶中,加50%甲醇稀释至刻度,摇匀,滤过,取续滤液,用微孔滤膜(0.45 μm)滤过,作为供试品溶液。
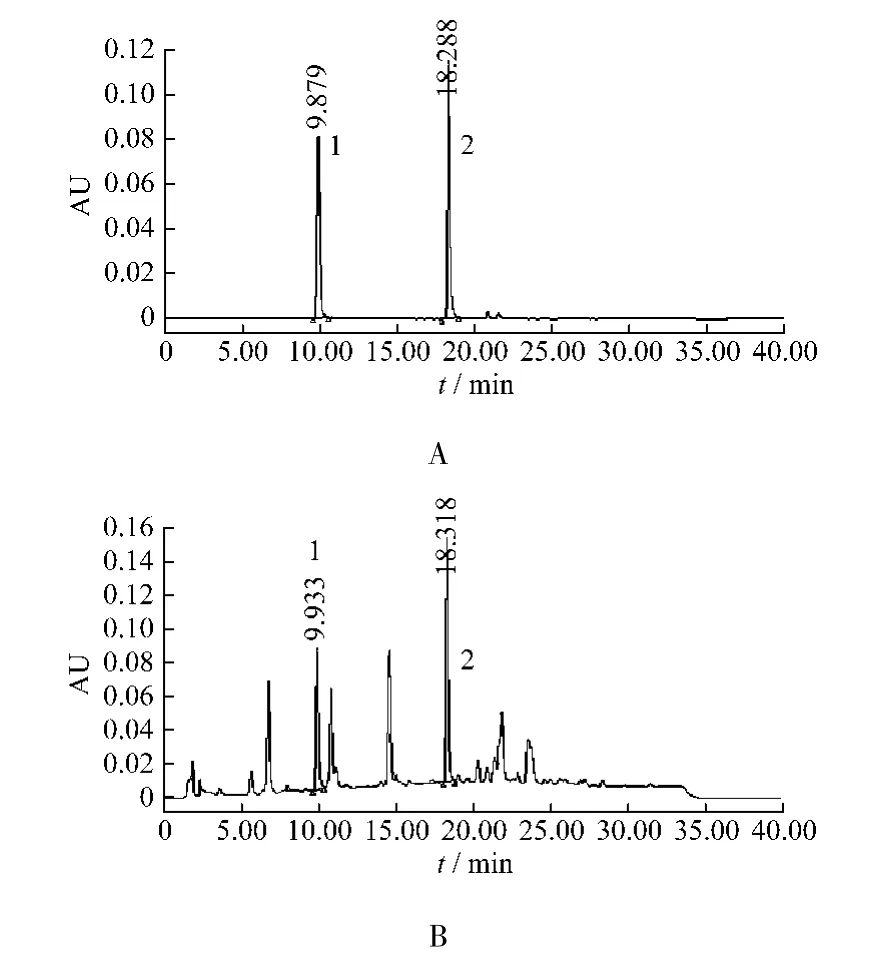
图1 绿原酸及芦丁对照品(A)和样品(B)HPLC色谱图
2.4 标准曲线及线性关系考察 精密称取绿原酸对照品10.19 mg及120℃干燥至恒重的芦丁对照品10.56 mg,置10 mL棕色量瓶中,加50%甲醇适量溶解并定容至刻度,摇匀,制成每1 mL含绿原酸1.019 mg及芦丁1.056 mg的贮备液,精密吸取此贮备液 0.1、0.2、0.4、0.6、0.8、1.0、1.2、1.4 mL置10 mL棕色量瓶中,加50%甲醇至刻度,摇匀,制成每 1 mL 含绿原酸0.010 19、0.020 38、0.040 76、0.061 14、0.081 52、0.101 9、0.122 28、0.142 66 mg 及芦丁 0.010 56、0.021 12、0.042 24、0.063 36、0.084 48、0.105 6、0.126 72、0.147 84 mg的系列浓度对照品溶液,分别进10 μL,以进样量X(μg)为横坐标,峰面积的积分值Y为纵坐标进行线性回归。各组分回归方程,相关系数,线性范围见表2。
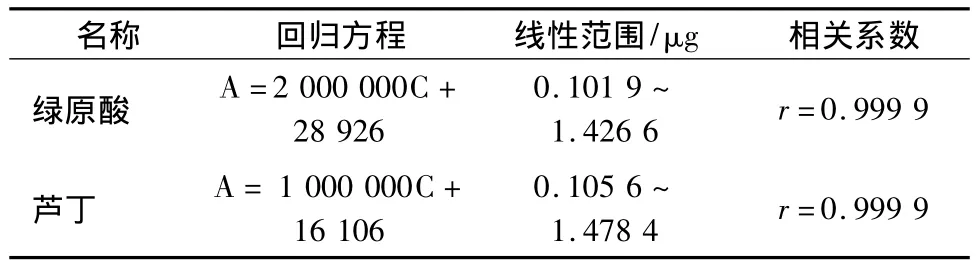
表2 标准曲线
2.5 精密度试验 取绿原酸与芦丁混合对照品溶液10 μL,连续进样6次,测定峰面积,结果绿原酸的 RSD为0.34%,芦丁的RSD为0.16%,显示精密度良好。
2.6 重复性试验 取同一样品(20050930),按2.3项下的方法分别制备6份供试品溶液,按测定法进行测定,结果绿原酸,芦丁质量浓度分别为 0.106 mg/mL,0.289 mg/mL,RSD分别为1.66%,1.73%。结果表明,该方法重复性良好。
2.7 稳定性试验 精密吸取同一供试品溶液(20050930),分别放置 0、4、8、12、16 h 后进样,每次 10 μL,测定峰面积,结果绿原酸和芦丁RSD分别为1.23%、0.14%。表明供试品溶液室温在16 h内稳定。
2.8 回收率试验 取已测定的(20050930)样品共9份5.0 mL,每份按高、中、低分别加入各对照品溶液,按2.3项下操作,计算回收率,结果见表3。
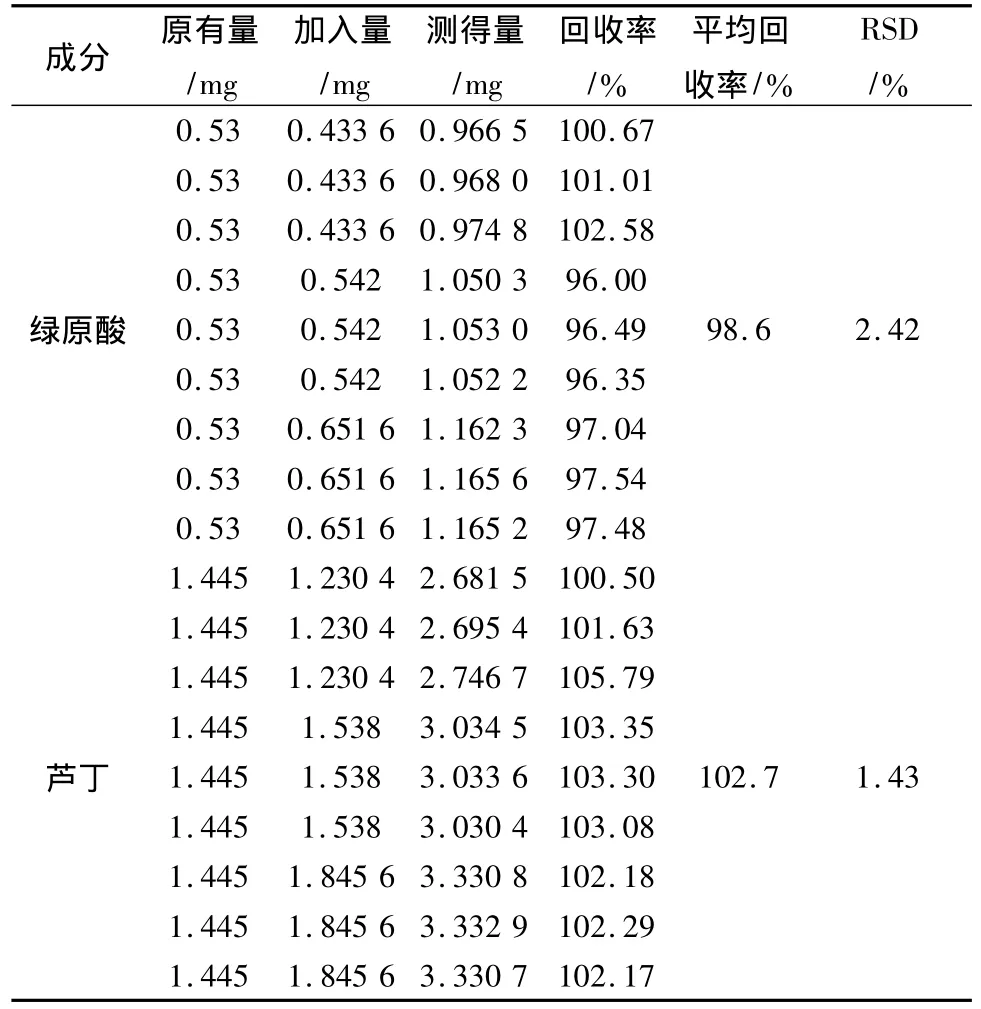
表3 加样回收实验
2.9 样品测定 取8批天山雪莲口服液,按2.3项下的样品处理方法及2.1项下的色谱条件进行测定,每批样品平行制备2份,每份进样2次,每次进样10 μL,结果见表4。
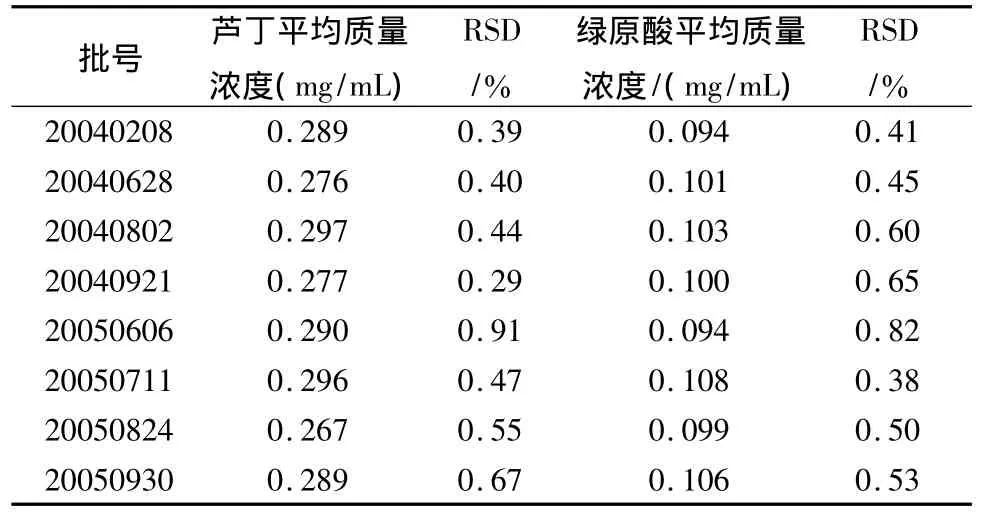
表4 样品测定结果(n=4)
3 讨论
3.1 本实验曾参考中国药典2005年版一部天山雪莲药材[5]项下HPLC中的流动相系统,不能同时满足芦丁和绿原酸的分离,而在本实验条件下绿原酸和芦丁的分离度良好。
3.2 流动相选择试验中比较了甲醇-0.4% 磷酸溶液(38∶62,35 ∶65),乙腈-0.4% 磷酸溶液(13 ∶87,15 ∶85)等,发现绿原酸、芦丁和相邻杂质分离度不佳,以乙腈-0.4% 磷酸溶液进行梯度洗脱,达到完全分离。因此最终确定进行梯度洗脱。
[1]国家药品监督管理局编.国家中成药标准汇编.经络肢体脑系分册[S].2002:560-563.
[2]俞敏倩,陈建民.高效液相色谱法测定11种雪莲花中芦丁及紫丁香苷[J].色谱,2001,19(3):243-244.
[3]凯赛尔·阿不拉,苏来曼·哈力克,王新宇.HPLC测定雪莲口服液中紫丁香苷的含量[J].中国中药杂志,2006,31(22):1895-1897.
[4]李君山,蔡少青.雪莲花类药材的化学和药理研究进展[J].中国药学杂志,1998,33(8):449-452.
[5]国家药典委员会.中华人民共和国药典:2005年版一部[S].北京:化学工业出版社,2005:36-37.
[6]苏来曼·哈力克,凯赛尔·阿不拉.RP-HPLC测定不同产地不同采集期天山雪莲中绿原酸和芦丁的含量[J].中草药,2007,38(9):1412-1414.
[7]欧 元,袁晓凡.天山雪莲HPLC指纹图谱研究[J].中草药,2008,39(1):105-108.
[8]李 燕,郭顺星.新疆雪莲化学成分的研究[J].中国中药杂志,2007,32(2):162-163.
[9]张富昌,赵文军.新疆雪莲的超临界萃取及气相色谱-质谱分析[J].时珍国医国药,2007,18(8):1821-1823.
[10]陈发奎主编.中药有效成分含量测定[M].北京:人民卫生出版社,2007:11.
[11]刘晓秋主编.中成药分析实验[M].北京:中国医药科技出版社,2006.

