元胡炮制前后UPLC指纹图谱研究
张 虹, 王 麟, 陈相涛, 袁 珂*
(1.浙江农林大学天然药物研发中心,浙江 临安311300;2.河南中医学院药学院,河南 郑州 450008)
元胡炮制前后UPLC指纹图谱研究
张 虹1, 王 麟2, 陈相涛1, 袁 珂1*
(1.浙江农林大学天然药物研发中心,浙江 临安311300;2.河南中医学院药学院,河南 郑州 450008)
目的 建立元胡炮制前后的UPLC指纹图谱。方法 将元胡趁鲜切片,加醋后烘干得醋制元胡。元胡生、制品各10批,采用ACQUITY UPLC®BEH C18色谱柱,PDA检测器,以0.2%甲酸水溶液-0.1%甲酸甲醇溶液为流动相进行梯度洗脱,选择色谱图出峰数目最多,各色谱峰分离度较好的297 nm为检测波长,柱温30℃,体积流量0.3 mL/min。结果 以延胡索乙素作为参照,确定元胡生品有32个共有色谱峰,元胡制品有23个共有色谱峰。结论 从整体上显示了生、制品的特征,炮制后多种未知成分的量下降或消失。建立的UPLC指纹图谱方法为元胡生、制品的质量控制提供有效手段。关键词:UPLC;元胡;炮制;指纹图谱
中药指纹图谱是采用一定的分析手段,得到能够标示其化学特征的色谱图[1],它是一种综合的鉴定手段,是建立在中药化学成分系统研究的基础上,主要用于分析评价中药材、中药饮片及中药制剂的真实性、优良性和稳定性,具有“整体性”和“模糊性”两大特点[2]。
延胡索为罂粟科植物Corydalis yanhusuoW.T.Wang的干燥块茎,又称元胡,为常用理气止痛药,具有活血、利气、止痛的功能。用于胸胁、脘腹疼痛,经闭痛经,产后瘀阻,跌扑肿痛等症[3]。历代对元胡的炮制有生用、炒、醋炙、酒炙、醋煮、盐炙等,现多采用醋炙、醋煮和醋蒸,部分地区沿用酒炙和盐炙。《中国药典》2010年版载有生元胡和醋元胡。元胡为浙八味之一,主产于磐安、东阳一带。多年来因元胡药材产地加工过程多由药农自己完成、且加工方法不规范,导致药材质量存在一定差异,造成目前药源质量不稳定和市售元胡饮片质量无法正确评估的混乱局面。
元胡作为临床常用药,其药材的HPLC指纹图谱已有报道,但建立元胡生、制品UPLC指纹图谱鉴定技术的研究尚未见文献报道。为综合评价和分析饮片质量,本实验建立元胡生、制品UPLC指纹图谱,以全面、客观地分析评价元胡所含内在化学成分的种类和数量,为元胡药材及元胡饮片的综合质量控制提供参考,以确保药材及饮片品质的一致性,疗效的可靠性。
1 仪器与试药
1.1 仪器 ACQUITY UPLCTM超高效液相色谱仪系统(美国Waters公司),配备二元溶剂管理器、自动进样器和PDA检测器;Masslynx色谱工作站。舒美KQ2200DE数控超声仪,AUTO SCIENCE溶剂过滤装置,森信DGG-9240A型干燥箱,Millipore公司Milli-Q 超纯水仪(Bedford,MA,USA)。
1.2 试剂 延胡索乙素对照品(中国药品生物制品检定所,批号:110726-200409);甲醇为色谱纯;甲酸为分析纯;水为娃哈哈纯净水。
1.3 样品 元胡药材(生品)采集于磐安、东阳不同的时间,经浙江林学院楼炉焕教授鉴定为罂粟科植物元胡的新鲜块茎。制元胡通过炮制工艺优选,对元胡鲜品进行一体化加工。以元胡趁鲜切片的厚度、加醋量和干燥温度为考察因素,每个因素设定三个水平,以延胡索乙素为指标,采用正交实验设计,优选出延胡索醋炙的最佳工艺,即将元胡鲜品采用抢水洗的方法除去外表泥沙,沥干水分即可趁鲜切片4 mm,以加醋量40%的米醋少量多次喷淋的方法,喷淋后将其用保鲜膜覆盖闷润,至醋被吸尽,然后在50℃下干燥得到醋制元胡。所测样品详见表1。
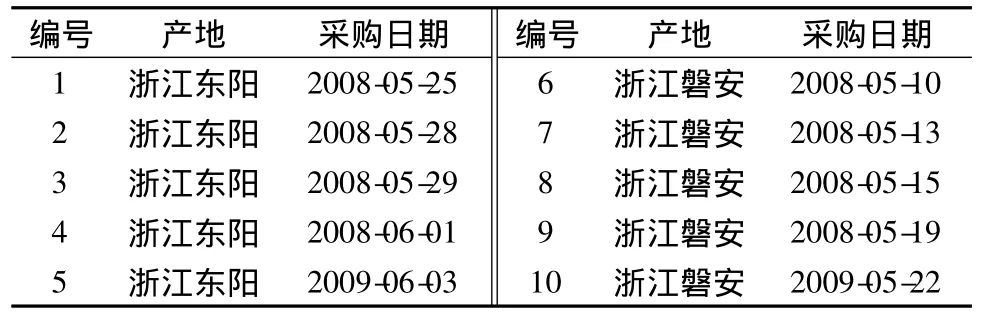
表1 元胡生品来源Tab.1 Sample resoures of Corydalis Rhizoma
2 方法与结果
2.1 对照品溶液的制备 精密称取一定量的延胡索乙素对照品,置量瓶中,加甲醇溶解并定容,配制成浓度为46 μg/mL的对照品溶液。
2.2 样品溶液的制备 取元胡生品、制品粗粉各0.5 g甲醇(1∶20)溶液50 mL,冷浸1 h,加热回流1 h。放冷,滤过,蒸干滤液,残渣加甲醇溶解转移至25 mL量瓶中,并稀释至刻度,摇匀,过0.45 μm 微孔滤膜作为供试液。
2.3 色谱条件 色谱柱为Waters公司ACQUITY UPLC®BEH C18色谱柱(50 mm ×2.1 mm,1.7 μm);流动相A为0.2%甲酸水溶液,B为0.1%甲酸甲醇溶液;梯度洗脱程序见表2。柱温:30℃;体积流量:0.3 mL/min;检测波长 297 nm;进样量为 10 μL。

表2 流动相梯度洗脱程序Tab.2 Procedure of gradient elution with mobile phase
2.4 指纹图谱方法学考察
2.4.1 精密度试验 取同一供试品溶液(5号生品)连续进样6次分析,比较各主要特征峰相对保留时间和相对峰面积,结果RSD值小于3.0%,表明仪器精密度良好,符合指纹图谱分析要求。
2.4.3 重复性试验 取同一批样品(5号生品)6份,每份约0.2 g,精密称定,按上述供试液制备方法制备后分别进样进行测定,比较各主要特征峰的相对保留时间和相对峰面积,结果RSD值小于3.0%,表明方法的重复性良好,符合指纹图谱分析要求。
2.4.4 稳定性试验 取同一供试品溶液(5号生品),分别在 0、1、2、4、8、12、24 h 进样分析,比较各主要特征峰相对保留时间和相对峰面积,结果RSD值小于3.0%,表明供试品溶液在24 h内稳定。
2.5 元胡生品指纹图谱共有模式的建立及相似度比较
2.5.1 元胡生品指纹图谱共有模式的建立及特征峰的标定 按供试液制备方法制备供试液,按照确定的色谱条件分别进样进行UPLC测定,记录UPLC图谱,在25 min内出现32个共有峰,通过对照品UPLC图谱确定,其中10号峰为延胡索乙素。以延胡索乙素作为参照峰,其他依次标记为1、2……32。各特征峰的相对峰面积及相对保留时间均具有较好的重复性。元胡生品的特征指纹峰的相对保留时间的RSD均低于0.5%,符合《中药注射剂指纹图谱研究的技术要求》[4]的要求,元胡生品的对照指纹1, 10的叠加图见图2,各主要特征峰的相对峰面积见表3。
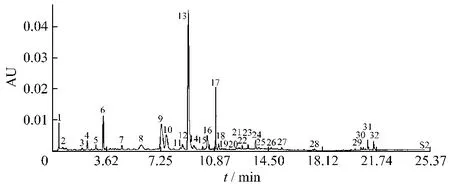
图1 元胡生品的对照指纹图谱Fig.1 Compared fingerprint of Corydalis Rhizoma
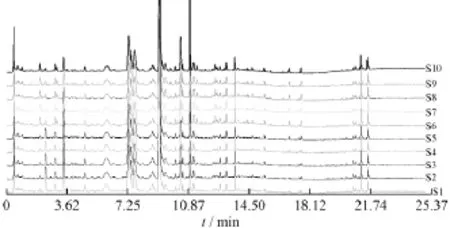
图2 元胡生品10批供试品的共有模式图Fig.2 Intercommunity pattern of Corydalis Rhizoma
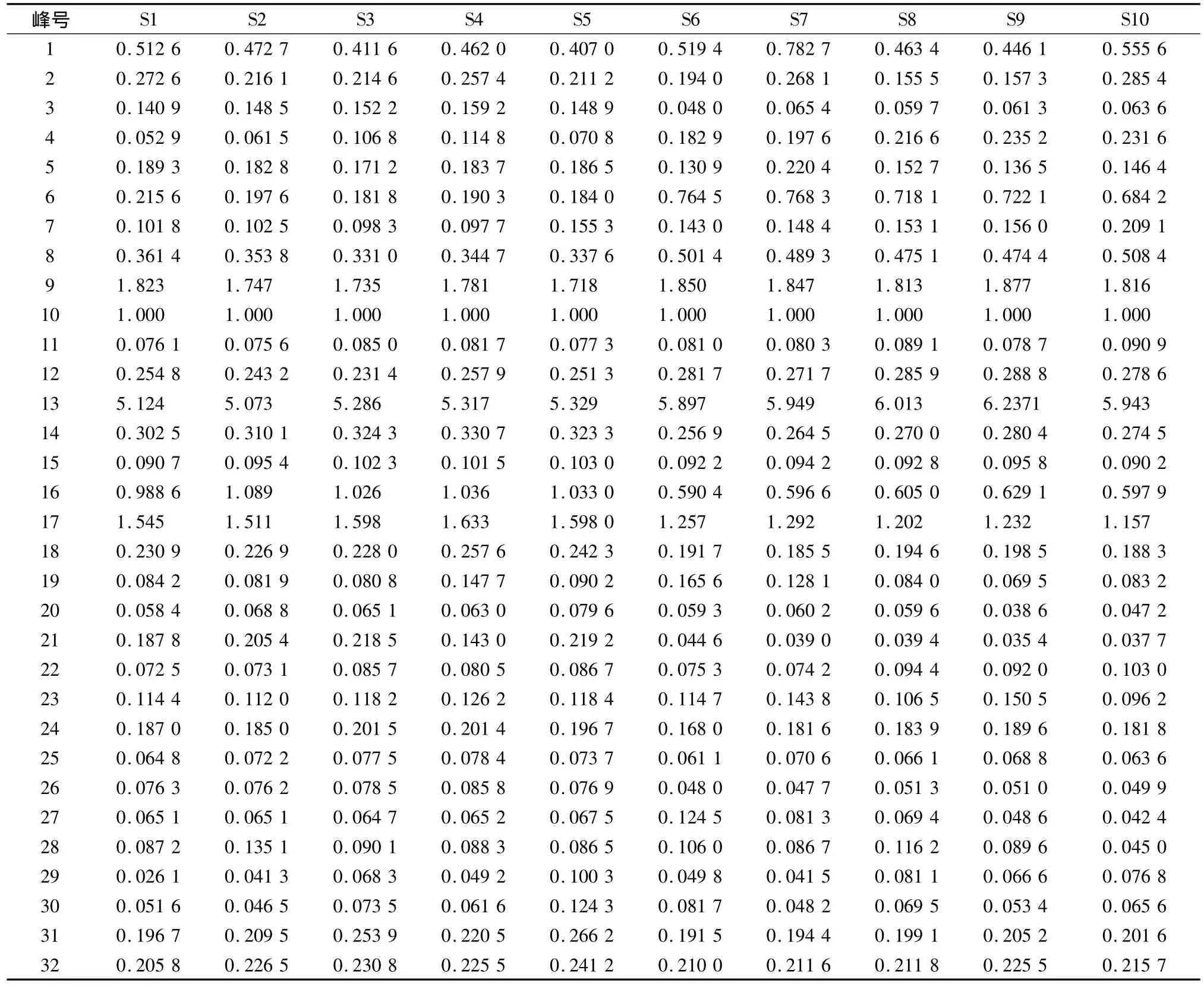
表3 元胡生品指纹图谱主要特征峰的相对峰面积Tab.3 Relative peak area of Corydalis Rhizoma
2.5.2 不同产地及批次元胡生品的相似度比较利用中药色谱指纹图谱相似度评价系统,对10批产地及批次的元胡生品进行相似度评价,结果见表4。实验结果表明10批元胡生品具有良好的相似度。

表4 10批元胡生品的相似度计算结果Tab.4 Similitude degree result of Corydalis Rhizoma
2.6 元胡制品指纹图谱共有模式建立及相似度比较
2.6.1 元胡制品指纹图谱共有模式的建立及特征峰的标定 按供试液制备方法制备供试液,按照确定的色谱条件分别进样测定,记录UPLC图谱,25 min内有23个共有峰,通过对照品UPLC图谱确定,其中11号峰为延胡索乙素。以延胡索乙素作为参照峰,其他依次标记为1、2……23。各特征峰的相对峰面积及相对保留时间均具有较好的重复性。元胡制品的特征指纹峰的相对保留时间的RSD均低于0.5%,符合《中药注射剂指纹图谱研究的技术要求》[4]的要求。元胡制品的对照指纹图谱见图3,特征指纹峰的共有模式的10批供试品的叠加图见图4,各主要特征峰的相对峰面积见表5。
2.6.2 不同产地及批次元胡制品药材样品的相似度比较 利用中药色谱指纹图谱相似度评价系统,对10批元胡制品进行相似度评价,结果见表6,实验结果表明每个产地的5批药材制品相似度较好,东阳产元胡炮制后较生品出现了6号非共有峰。
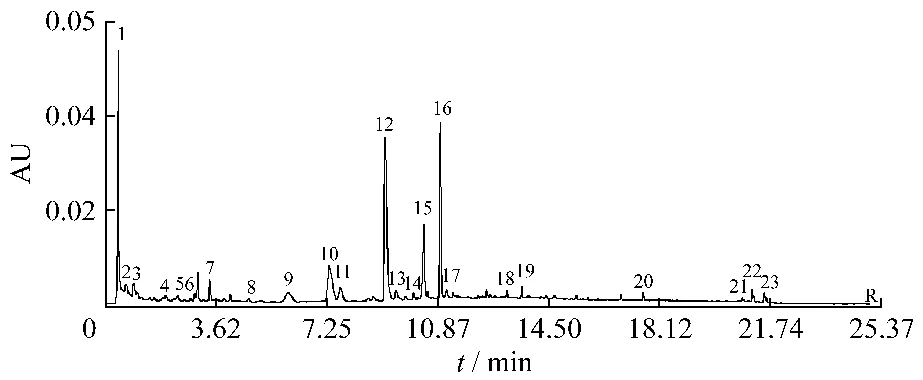
图3 元胡制品的对照指纹图谱Fig.3 Fingerprint of processed Corydalis Rhizoma

图4 元胡制品10批供试品共有模式图Fig.4 Intercommunity pattern of processed Corydalis Rhizoma
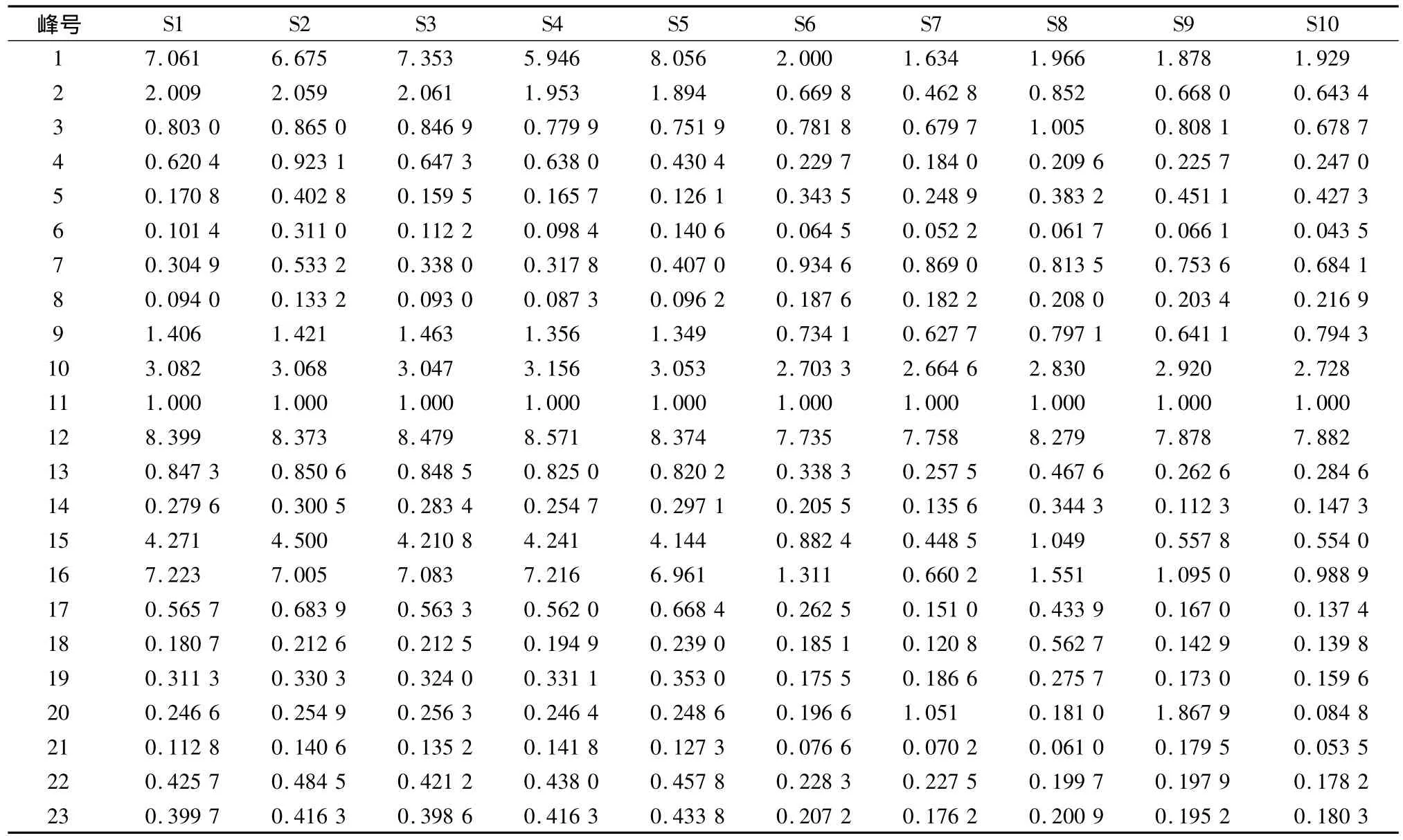
表5 元胡制品指纹图谱主要特征峰的相对峰面积Tab.5 Relative peak area of processed Corydalis Rhizoma

表6 10批元胡制品的相似度计算结果Tab.6 Similitude degree result of processed Corydalis Rhizoma
3 讨论
3.1 根据指纹图谱对元胡提取液进行分析,结果表明,按照药典方法以甲醇-氨水(20∶1)作为提取溶剂,可以使元胡中的生物碱游离,进而增加其溶出度,且此方法提取10批生品样品的相似度均大于0.9,说明采用现有提取工艺制备的样品,每个批次间一致性较好,该方法可用于元胡提取液的质量控制。
3.2 本实验对元胡提取液指纹图谱的色谱条件进行了优化。延胡索乙素为元胡镇痛的主要成分,故作为参比峰。采用二极管阵列检测器(PDA),在分析时进行全波长紫外扫描,并在不同波长下获取数据,经比较后表明297 nm色谱图峰形最好,出峰数目最多,各色谱峰相互之间分离度较好,故检测波长选定在297 nm波长下确定元胡生、制品的指纹图谱。
3.3 采用不同比例的甲醇-水梯度系统进行洗脱,结果表明,甲醇在较低波长下吸收度较强,梯度洗脱时基线漂移严重,且色谱峰无法成形,而在酸性条件下有较好的色谱峰分离,经过多次调整甲酸的比例,最后选取0.2%甲酸水-0.1%甲酸甲醇作为流动相。
3.4 从表6中所列相似度结果可以看出,每个产地元胡制品的相似度较接近,但两个产地元胡制品色谱图的相似度间有较大的差异,经对比两产地制品的对照图谱发现,二者的差异主要表现在磐安产元胡制品的色谱图中的6号(如图3)色谱峰较东阳产元胡制品色谱图中的6号色谱峰峰高较高,峰面积较大,除此,二者基本相似。
3.5 将元胡生品和制品的对照指纹图谱进行比较发现,炮制后色谱峰的数目发生变化(生品为32个色谱峰,制品为23个色谱峰),另外有些保留时间相同的色谱峰的峰面积也发生了一定的变化,如制品的7号色谱峰(tR为3.417 min)和生品的6号色谱峰(tR为3.42 min)保留时间相同,但峰面积相对变小,这一成分结构和药效将有待于进一步研究。
4 小结
4.1 传统的HPLC指纹图谱由于液相色谱柱效较低,分离时间较长,一般都在1 h以上[5-6],不能满足高通量分析的要求,制约着液相色谱指纹图谱在实际质量控制中的应用。而超高效液相色谱的出现解决了这一技术难题,UPLC指纹图谱技术能大大缩短样品运行的时间[7],作为理想的中药质量控制的手段,有着广阔的应用前景。
4.2 本研究通过建立元胡生、制品的UPLC指纹图谱,对10批生、制品进行了指纹图谱测定。测定结果显示,不同生品供试品与制品供试品的色谱概貌一致,整体分离度较好,生品供试品有32个共有峰,相似度均大于0.99,制品供试品有23个共有峰,相似度均大于0.82,具有自身化学条码特征,建立的共有模式比较可靠,能反映其内在的化学成分种类和数量,以此作为控制元胡生品、制品质量的方法,元胡生品与其对照指纹图谱的相似度不得低于0.9,制品与其对照指纹图谱相似度不得低于0.8,此方法比较科学有效。
[1]谢培山.中药色谱指纹图谱鉴别的概念、属性、技术与应用[J].中国中药杂志,2001,26(10):653.
[2]谢培山.中药色谱指纹图谱[M].北京:人民卫生出版社,2005,2:12.
[3]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:130-131.
[4]国家药品监督管理局.中药注射剂指纹图谱研究的技术要求(暂行)[J].中成药,2000,22(10):671-675.
[5]Xu Lina,Xu Han,Qi Yan,et al.Multiple compounds determination and fingerprint analysis of Lidanpaishi Tablet and keli by highperformance liquid chromatography[J].Anal Chim Acta,2009,633(1):136-148.
[6]Ye Ji,Zhang Xi,Dai Weixing,et al.Chemical fingerprinting of Liuwei Dihuang Pill and simultaneous determination of its major bioactive constituents by HPLC coupled with multiple detections of DAD,ELSD and ESI-MS[J].J Pharm Biomed Anal,2009,49(3):638-645.
[7]Zhou Dayong,Zhang Xiuli,Xu Qing,et al.UPLC/Q-TOFMS/MS as a powerful technique for rapid identification of polymethoxylated flavones inFructus aurantii[J].J Pharm Biomed Anal,2009,50(1):2-8.
UPLC fingerprint of crude and processed Corydalis Rhizoma
ZHANG Hong1, WANG Lin2, CHEN Xiang-tao1, YUAN Ke1*
(1.Research and Development Certer of Natural Medicine,Zhejiang Agriculture and Forestry University,Lin’an 311300,China;2.College of Pharmacy,Henan University of Traditional Chinese Medicine,Zhengzhou 450008,China)
AIMTo establish the fingerprint of crude and processedCorydalis Rhizomaby UPLC.METHODSTen batches of slicedCorydalis Rhizomawere added vinegar and boiled to dryness as the processed along with another ten batches of unprocessedCorydalis Rhizomafor experiment.The UPLC analysis was carried out on an ACQUITY UPLC®BEH C18column,with a detector of PDA and the mobile phase consisting 0.2%formic acid water-0.1%formic acid methanol in gradient mode.The detection wavelength was set at 297 nm that more peaks can be detected.The column temperature was 30 ℃,and flow rate was 0.3 mL/min.RESULTSThirty-two and twenty-three co-possessing peaks were selected as the fingerprint peaks of crude and processedCorydalis Rhizoma,respectively,based on the peak area of corydalis B as reference peak.CONCLUSIONThe method of UPLC fingerprint can display the feature of crude and processedCorydalis Rhizoma.After processing various chemical constituents are reduced and disappeare.It provides the effective means for quality control of crude and processedCorydalis Rhizoma.
UPLC;Corydalis Rhizoma;processed;fingerprint
R284.1
A
1001-1528(2011)07-1093-05
2010-06-02
浙江省科技厅重点项目(2007C23024)
张 虹(1982—),女,讲师,主要从事中药饮片炮制研究。
* 通信作者: 袁珂,女,教授,主要从事天然药物活性成分研究。Tel: ( 0571) 63743607,E-mail: yuan_ke001@163.com

