6种常用抗肿瘤药物致小鼠肝损害程度的比较研究Δ
叶冬梅,陈晓宇,兰顺,李重勤(.广西壮族自治区人民医院,南宁市 5300;.桂林医学院药学系,桂林市 54004)
顺铂、卡铂、紫杉醇、多西紫杉醇、吉西他滨及长春瑞滨是临床上常用的广谱抗肿瘤药。顺铂、卡铂分别与其余4种药物组成的化疗方案广泛应用于肺癌、乳腺癌等疾病的治疗,其疗效在化疗中的地位相近。6种药物在消化系统、肾脏及造血系统的毒副作用有明显差异,而在肝脏损害方面,临床中的发生率和严重程度在不同的文献报道中有较大差异[1,2]。为了明确不同化疗药物致肝损害的严重程度差异,本文进行了疗效近似的上述6种药物之间致肝损害程度的比较实验研究,为临床合理用药及防治药物肝损害提供实验依据,以保证患者进行积极抗肿瘤治疗的同时最大限度地减少药物对正常机体组织的损害。
1 仪器与材料
1.1 仪器
数显恒温水浴锅(金坛市医疗仪器厂);Baujahr 2000低温离心机(上海博星基因芯片有限公司);紫外-可见分光光度计(美国惠普公司);Bx50F4光电显微镜(日本Olympus公司)。
1.2 试药
顺铂注射液(批号:20080901,规格:30 mg∶6 mL)、注射用吉西他滨灭菌粉末(批号:20090407,规格:每瓶200 mg)、长春瑞滨注射液(批号:20090101,规格:10 mg∶1 mL)均购自江苏豪森药业股份有限公司;卡铂注射液(齐鲁制药有限公司,批号:20090429,规格:100 mg∶10 mL);紫杉醇注射液(哈药集团生物工程有限公司,批号:2009041,规格:30 mg∶5 mL);多西紫杉醇注射液(深圳万乐制药有限公司,批号:20091001,规格:20 mg∶0.5 mL);丙二醛(MDA)、超氧化物歧化酶(SOD)、还原型谷胱甘肽(GSH)检测试剂盒(南京建成生物工程研究所提供,批号:20091026);直接胆红素(D-BIL)试剂盒(批号:EE953)、碱性磷酸酶(ALP)试剂盒(批号:EG979)、天门冬氨酸氨基转移酶(AST)试剂盒(批号:EF246)、丙氨酸氨基转移酶(ALT)试剂盒(批号:EF250)均由日本和光纯药工业株式会社提供。
1.3 动物
昆明种小鼠,♂,体重(20±2)g,广西医科大学实验动物中心提供,许可证号:SCXK桂2003-0005。
2 方法
2.1 供试药液的制备
取顺铂注射液5 mL,用生理盐水稀释至15 mL,得浓度为1.7 mg·mL-1的顺铂供试药液;取卡铂注射液10 mL,用5%葡萄糖注射液稀释至15 mL,得浓度为6.7 mg·mL-1的卡铂供试药液;取紫杉醇注射液5 mL,用生理盐水稀释至10 mL,得浓度为3.0 mg·mL-1的紫杉醇供试药液;取多西紫杉醇注射液0.5 mL,用5%葡萄糖注射液稀释至12 mL,得浓度为1.7 mg·mL-1的多西紫杉醇供试药液;取注射用吉西他滨灭菌粉末200 mg,用生理盐水稀释至9 mL,得浓度为22.2 mg·mL-1的吉西他滨供试药液;取长春瑞滨注射液1 mL,用5%葡萄糖注射液稀释至18 mL,得浓度为0.56 mg·mL-1的长春瑞滨供试药液。
2.2 分组与给药
根据预实验结果,取小鼠70只,10只为生理盐水组作正常对照,其余按临床常用剂量给药分为顺铂组(17 mg·kg-1)、卡铂组(67 mg·kg-1)、紫杉醇组(30 mg·kg-1)、多西紫杉醇组(17 mg·kg-1)、吉西他滨组(222 mg·kg-1)、长春瑞滨组(5.6 mg·kg-1),每组10只,尾静脉注射给予相应药物,给药量均为0.2 mL,给药时间为10~20 s。
2.3 肝功能生化指标检测
注射给药第3天时,各组小鼠眼眶取血(取标本前1天禁食),3000 r·min-1离心10 min,分离血清,测定其中D-BIL、ALP、AST、ALT水平。
2.4 肝组织氧化及抗氧化指标检测
注射给药第3天时,取各组小鼠肝组织0.2 g(取标本前1天禁食),加4℃生理盐水在冰浴下制成10%(W/W)肝组织匀浆,将匀浆在4 ℃离心10 min(4000 r·min-1),取上清液,考马斯亮蓝法检测总蛋白含量,按试剂盒方法测定肝组织匀浆中MDA、GSH含量和SOD活性。
2.5 肝组织病理学检查
取同一部位肝组织一小块,用10%甲醛固定,石蜡包埋,切片,苏木精-伊红(HE)染色,光电显微镜下观察。如果肝细胞内有圆形空泡,并将细胞核推向细胞外周,即为肝细胞脂肪变性;出现肝细胞肿胀,细胞核团缩、溶解或碎裂,镜下仅能见到支持肝细胞的网状支架及缺损的小叶结构,为肝细胞坏死[3]。
2.6 数据处理
3 结果
3.1 肝功能生化指标检测结果
D-BIL值:与生理盐水组比较,顺铂、卡铂和紫杉醇无明显改变,多西紫杉醇、吉西他滨、长春瑞滨显著升高(P<0.01),三者之间比较无显著性差异。ALT值:与生理盐水组比较,顺铂组明显升高(P<0.01),其余5个药物组无明显变化。AST值:与生理盐水组比较,6个药物组均明显升高(P<0.05或P<0.01),其中顺铂组明显高于其它5个药物组(P<0.01)。ALP值:与生理盐水组比较,6个药物组均明显升高(P<0.01),其中卡铂组明显低于其它5个药物组(P<0.01)。各组小鼠血清中D-BIL、ALP、AST、ALT水平比较见表1。
表1 各组小鼠血清中D-BIL、ALP、AST、ALT水平比较(,n=10)Tab 1 Comparison of D-BIL,ALP,AST and ALT activities in mice serum among those group(s,n=10)
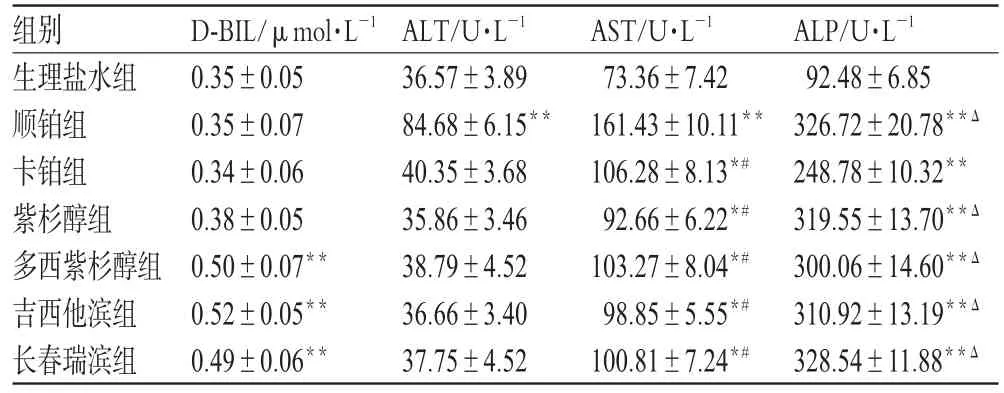
表1 各组小鼠血清中D-BIL、ALP、AST、ALT水平比较(,n=10)Tab 1 Comparison of D-BIL,ALP,AST and ALT activities in mice serum among those group(s,n=10)
与生理盐水组比较:*P<0.05,**P<0.01;与顺铂组比较:#P<0.01;与卡铂组比较:ΔP<0.01vs.normal saline group:*P<0.05,**P<0.01;vs.cisplatin group:#P<0.01;vs.carboplatin group:ΔP<0.01
3.2 肝组织氧化及抗氧化指标检测结果
与生理盐水组比较,6个药物组MDA含量均明显升高,GSH含量均明显降低(P<0.05或P<0.01),多西紫杉醇组和吉西他滨组SOD活性明显降低(P<0.05)。各组小鼠肝组织中MDA、GSH、SOD活性比较见表2。
表2 各组小鼠肝组织中MDA、GSH、SOD活性比较(,n=10)Tab 2 Comparison of MDA,GSH and SOD activities in hepatic tissue among those group(s,n=10)
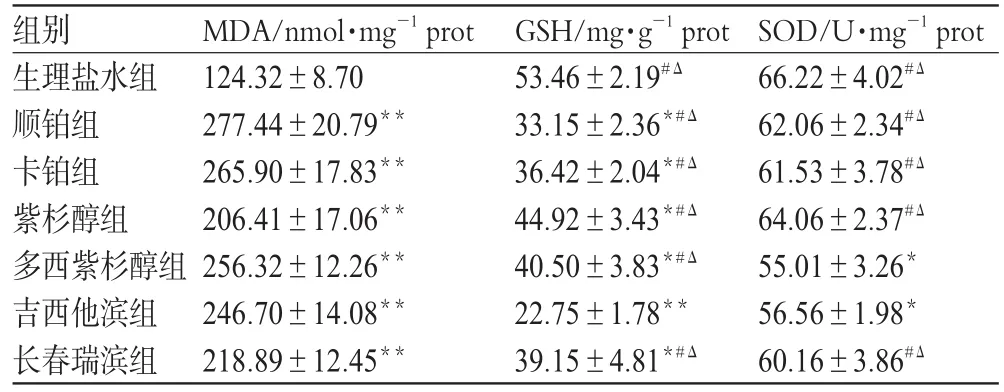
表2 各组小鼠肝组织中MDA、GSH、SOD活性比较(,n=10)Tab 2 Comparison of MDA,GSH and SOD activities in hepatic tissue among those group(s,n=10)
与生理盐水组比较:*P<0.05,**P<0.01;与多西紫杉醇组比较:#P<0.05;与吉西他滨组比较:ΔP<0.05vs.normal saline group:*P<0.05,**P<0.01;vs.docetaxel group:#P<0.05;vs.gemcitabine group:ΔP<0.05
3.3 肝组织病理学变化
6个药物致肝细胞脂肪变性程度排序为:多西紫杉醇>吉西他滨≈顺铂>紫杉醇≈长春瑞滨>卡铂;致肝细胞坏死程度排序为:吉西他滨≈多西紫杉醇>长春瑞滨>顺铂≈紫杉醇>卡铂。肝细胞瘀胆最严重者为吉西他滨和多西紫杉醇(二者比较无显著性差异),发生率均为40%,其次为长春瑞滨;顺铂、卡铂和紫杉醇组均未出现肝细胞瘀胆。各组小鼠肝组织病理学变化比较见表3,病理切片图见图1。
4 讨论
实验结果表明,顺铂、卡铂、紫杉醇、多西紫杉醇、吉西他滨及长春瑞滨6种常用抗肿瘤药物在给药第3天均出现肝功能生化指标与病理组织形态的改变,综合上述指标考察,6种药物致肝损害程度排序为吉西他滨≈多西紫杉醇>长春瑞滨>顺铂≈紫杉醇>卡铂。
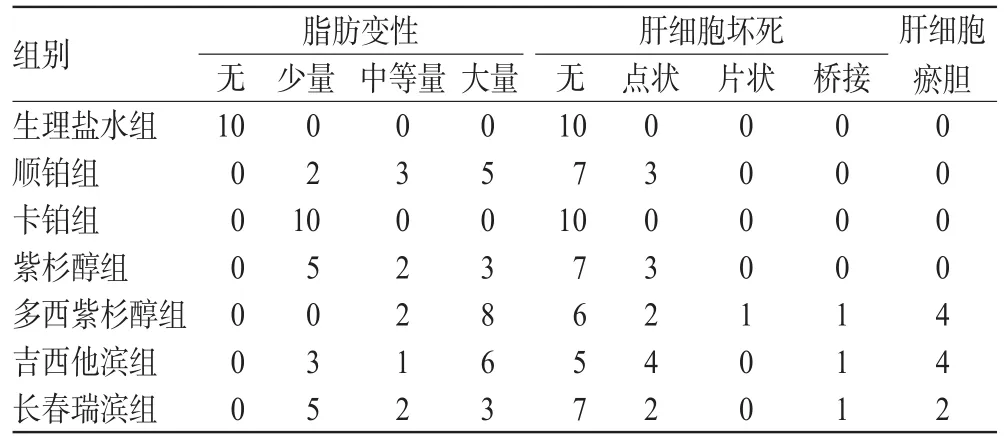
表3 各组小鼠肝组织病理学变化比较(只,n=10)Tab 3 Comparison of pathological changes of hepatic tissue(number,n=10)
图1 各组小鼠肝组织病理切片图A.生理盐水组;B.顺铂组;C.卡铂组;D.紫杉醇组;E.多西紫杉醇组;F.吉西他滨组;G.长春瑞滨组Fig 1 Pathological sections of hepatic tissueA.normal saline group;B.cisplatin group;C.carboplatin group;D.paclitaxel group;E.docetaxel group;F.gemcitabine group;G.vinorelbine group
6种药物的肝组织脂质过氧化物MDA水平较生理盐水组明显升高,抗氧化成分GSH水平明显降低,符合药物诱导肝脏损伤的氧化应激反应机制,即药物诱导的肝脏损伤与药物的代谢异常有密切关系。药物本身含有的及其经细胞色素P450(CYP450)酶系代谢产生的自由基、亲电子基、氧基等有害活性物质,通常与GSH结合而解毒,并不产生肝损害;而多种原因可导致这些有毒活性物质的产生超过了肝内GSH代偿水平,使肝组织抗氧化防御体系(GSH等)功能下降,引发脂质过氧化,肝组织脂质过氧化链式反应的终产物之一MDA升高,导致肝脏氧化应激损伤,轻者为脂肪变性(具有可逆性),重者可发生中毒性肝细胞坏死[4,5]。
护肝辅助治疗可有效地预防化疗药物所致的肝损害[6,7]。鉴于氧化应激反应在化疗性肝损伤的作用,建议临床上在使用上述6种药物化疗期间应及早使用抗氧化剂,通过其与过氧化物及自由基结合,拮抗氧化剂对巯基的破坏,保护细胞膜中含巯基的蛋白质和含巯基酶,减轻化疗对肝脏的毒副作用。
[1]李文军.紫杉醇不良反应文献综述[J].药物流行病学杂志,2002,11(4):187.
[2]钟佩红,董兰菊.紫杉醇卡铂联合化疗毒副反应的观察与护理[J].基层医学论坛,2008,12(6):481.
[3]武忠弼,周晓军.超微病理诊断学[M].上海:上海科学技术出版社,2003:205.
[4]李钦民,韩 真.药物性肝病发病机制的研究进展[J].实用肝脏病杂志,2005,8(2):124.
[5]卡萨瑞·特道.毒理学:毒物的基础科学[M].北京:人民卫生出版社,2005:419.
[6]罗朝利.还原型谷胱甘肽的临床应用[J].中国药房,2003,14(12):756.
[7]郑 滢,宋方闻,庄学龙,等.复方甘草酸苷治疗抗肿瘤药导致肝损害的疗效观察[J].中国药房,2005,16(3):207.

