地尔硫 中间体的合成工艺改进
李长思 ,王永超 ,俞健钧 ,戴振亚 *,尤启冬 *,王德峰
1中国药科大学药物化学教研室,南京 210009;2江苏德峰医药化工有限责任公司,南通 226531
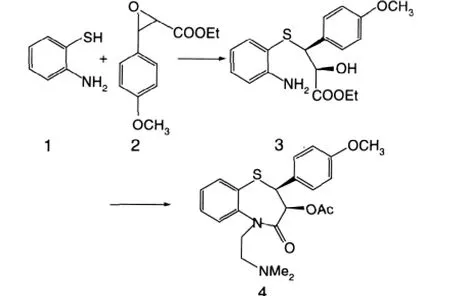
图1 地尔硫的一般合成路线
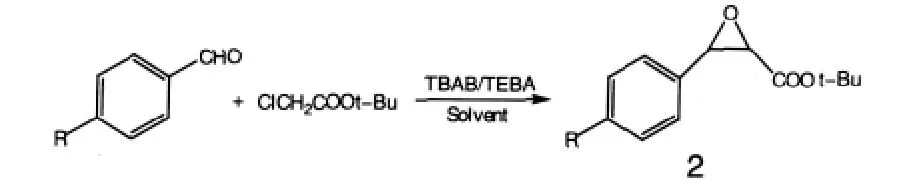
图2 Darzen's反应制备化合物2
本研究利用相转移催化的方法对Darzens反应进行可行性探索,发现在液液和固液相转移催化下,氯乙酸乙酯和甲酯都不能和对甲氧基苯甲醛反应,而氯乙酸叔丁酯可以发生反应;随后又对四正丁基溴化铵 (TBAB)与苄基三乙基氯化铵(TEBA,Makosza催化剂)这两个催化剂进行试验比较,发现TEBA效果略佳 (TEBA,产率70%;TBAB,产率63%);再在 TEBA 催化下,从二氯甲烷(CH2Cl2)、甲苯(tolune)、四氢呋喃(THF)中筛选出THF为最佳反应溶剂(表1);在 TEBA-THF/KOH 催化体系下,本实验用5种不同取代的苯甲醛与氯乙酸叔丁酯进行了平行比较(表2),共得到5种 α,β-三元酸酯目标产物,其结构经核磁共振氢谱表征确证。
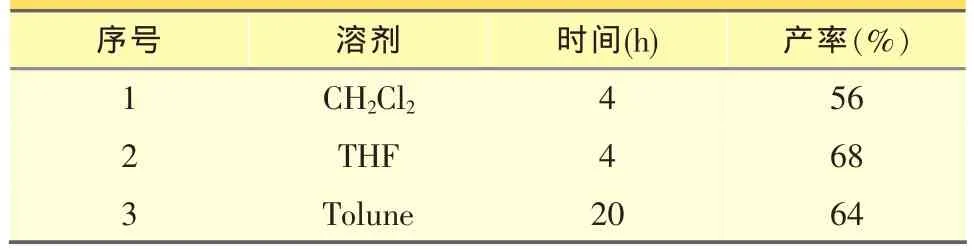
表1 溶剂筛选
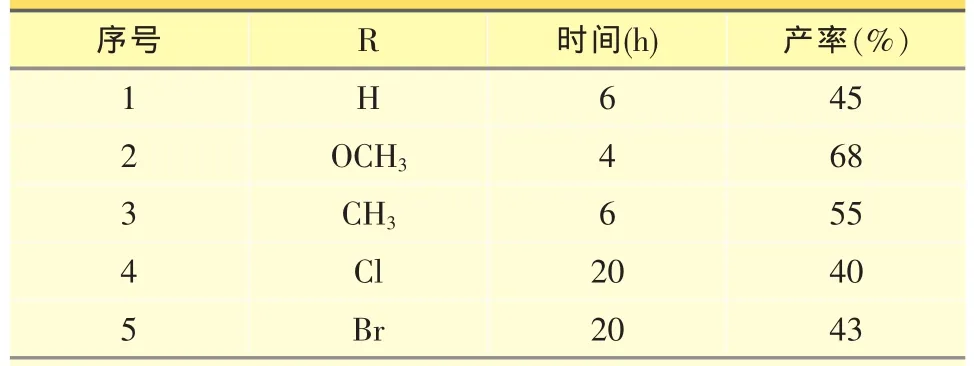
表2 不同底物与氯乙酸叔丁酯的反应结果
1 仪器和材料
1.1 仪器与试剂
1H-NMR在 300MHz的 Bruker核磁共振仪上测得。THF、甲苯用 Na-二苯甲酮在氮气氛下回流直至变为深蓝色,在使用前新蒸出来;二氯甲烷以五氧化二磷回流干燥,在使用前新蒸出来。
1.2 相转移催化体系的一般制备
向反应容器中投入碾碎的 KOH粉末约 0.4 g和催化剂约 0.1 g,加入溶剂后剧烈搅拌 20~30 min即得KOH-溶剂固—液相转移催化体系。
2 典型的 Darzens反应过程
以化合物2的合成为例:在反应管里,分别制备相转移催化体系后用注射器注入氯乙酸叔丁酯0.5 mL(约5 mmol),反应0.5 h后加入对甲氧基苯甲醛(0.4 mL),12℃下搅拌反应 4 h。薄层色谱检测反应完全后,用 CH2Cl2/H2O 洗涤,分出有机相,用无水硫酸钠干燥,蒸去有机溶剂,粗产品用制备板层析纯化得到产物(0.578g,收率70%)。1HNMR(CDCl3)δ:7.27-7.09(2H,d,J=8.7 Hz,Ar-H),6.79-6.73(d,2H,J=8.7 Hz,Ar-H),4.09-4.08(3 H,s, 甲氧基氢),3.71(1H,d,J=4.5 Hz, 环氧环上氢),3.61-3.59(1H,d,J=4.5 Hz,环氧环上氢),1.147(9H,s, 叔丁基氢)。
3 讨 论
[1] 潘 江,许建和,叶 勤.地尔硫手性中间体合成进展[J].生物加工过程,2009,3(7):1672-8.
[2] Lygo B,Wainwright PG.Phase-transfer catalyzed asymmetric epoxidation of enones using N-anthracenylmethyl-substituted cinchona alkaloids[J].Tetrahedron,1999,55(20):6289-300.
[3] Mamaghani M,Tabatabaeian K,Ghanadzadeh A,et al.An efficient enzymatic method for the separation of stereoisomeric cis and trans-glycidic esters synthesised via Darzens condensation reactions[J].Tetrahedron Lett,2003,44(25):4775-7.
[4] Arai S,Tsuge H,Oku M,et al.Catalytic asymmetric epoxidation of enones under phase-transfer catalyzed conditions[J].Tetrahedron,2002,58(8):1623-30.
[5] Seki M,Furutani T,Imashiro R,et al.A novel synthesis of a key intermediate for diltiazem[J].Tetrahedron Lett,2001,42(46):8201-5.
[6] Matsumae H,Furui M,Shibatani T.Lipase-catalyzed asymmetric hydrolysis of 3-phenylglycidic acid ester,the key intermediate in the synthesis of diltiazem hydrochloride[J].J Ferment Bioeng,1993,75(2):93-8.
[7] Schwartz A,Madan PB,Mohacsi E,et al.Enantioselective synthesis of calcium channel blockers of the diltiazem group[J].J Org Chem,1992,57(3):851-6.
[8] Arai S,Shioiri T.Catalytic asymmetric Darzens condensation under phase-transfer-catalyzed conditions[J].Tetrahedron Lett,1998,39(15):2145-8.
[9] Arai S,Shioiri T.Asymmetric Darzens reaction utilizing chloromethly phenyl sulfone under phase-transfer catalyzed conditions[J].Tetrahedron,2002,58(7):1407-13.

