利用传感器探究物质的溶解性
符益婷 金惠文
利用传感器探究物质的溶解性
符益婷 金惠文
(常州市田家炳实验中学分校江苏常州213003)
初中化学《溶液》一章理论性较强,概念比较抽象,学生在学习时有困难,所以要借助实验帮助学生理解。但其中与物质溶解性相关的实验较难设计;即使是实际教学中使用的实验,有的现象也很不明显。为此,笔者设计了三个相关实验来解决初中教学遇到的实际问题。
一、探究不溶性的物质在水中是否完全不溶
实验目的
不同的物质在水中的溶解性是不同的。不溶性物质是否完全不溶?本实验借助导电率传感器来探究这个问题。
实验设计
1.设计思路
若碳酸钙能溶解少量在水中,溶解的碳酸钙能电离出Ca2+和CO32-,离子浓度变大,则测量出的溶液的导电率应比蒸馏水的大,可说明碳酸钙并不是完全不溶于水的。
2.实验仪器与药品
导电率传感器、数据采集器、计算机、离心机、离心试管,碳酸钙粉末、蒸馏水。
实验过程
1.测量蒸馏水的导电率。
向一烧杯中加入45 mL蒸馏水,测出水的导电率。
2.测量溶液的导电率。
将碳酸钙的粉末分散到蒸馏水中,充分搅拌,测出溶液的导电率。
实验结果

_______样品_______ ______蒸馏水碳酸钙溶液导电率(μs/cm)4 18
同温度下,碳酸钙饱和溶液的导电率比蒸馏水大,说明在溶液中存在Ca2+和CO32-,从而证明碳酸钙并不是完全不溶于水的。
实验说明
初中学生在学习物质的不溶性时,因为没有相应的实验,学生没有直观感受,容易形成“不溶物就是完全不溶解”的错觉。这给高中学习“溶解平衡”时带来干扰。但初中学生已经知道如果溶液中存在自由移动的离子,溶液就能导电;并且还知道单位体积里的离子数目增多,溶液的导电性就能增强。因此可以借助导电率传感器来帮助使学生形成正确的概念。(实验使用的是美国威尼尔公司生产的导电率传感器,因为它能快速测量溶液中的离子浓度,因此可以探究电解质溶解性的相关问题。)
二、判断溶液是否饱和
实验目的
我们往往不能从外显现象上来判断某溶液是否饱和,借助导电率传感器则可以很直观的解决这个问题。
实验设计
1.设计思路
判断溶液饱和与否,在初中一般的方法是:一定温度下,向溶液中加入适量的该溶质,若不再溶解的为该溶质的饱和溶液,继续溶解的为该溶质的不饱和溶液,在接近饱和的溶液里继续加溶质,溶质是否发生溶解较难观察,对于氢氧化钙这样的微溶物更是如此。所以可以借助导电率传感器检测溶液的导电率是否发生变化,达到检测溶质是否溶解的目的。若溶质没有溶解,溶液中离子浓度不变,溶液导电率的随时间不发生变化,若溶质继续溶解,溶液中离子浓度变大,溶液的导电率随时间逐渐变大。
2.实验仪器与药品
导电率传感器、数据采集器、计算机、电磁搅拌机、烧杯,氢氧化钙固体、蒸馏水。
实验过程
1.配制氢氧化钙的不饱和溶液。
2.用导电率传感器判断溶液是否饱和。
向盛有氢氧化钙溶液的小烧杯中,逐渐加入适量的氢氧化钙固体,置于电磁搅拌机上边搅拌边放入已校准过的导电率传感器,每隔1秒采集一个数据,测溶液的导电率,绘制该溶液导电率与时间变化的曲线图。
实验结果
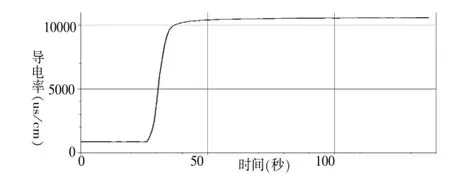
从图像上观察得出,氢氧化钙溶液的导电率随时间不断变大,说明溶液中离子浓度在变大,溶质在继续溶解,此时的氢氧化钙溶液还没有饱和;变大到一定程度又趋于平缓,溶质不再溶解,此时的溶液已经饱和。
实验说明
饱和溶液与不饱和溶液概念的理解和判断,是初中化学学习的难点。教师应借助实验,帮助学生理解和判断饱和溶液和不饱和溶液。但不管是演示还是学生实验,实验现象都不易观察,因为凭肉眼无法观察出溶质是否有少量的溶解。借助导电率传感器,通过溶液导电率的变化情况,判断溶质是否溶解,能明显的观察到实验现象,帮助学生理解概念。
三、探究一定量水中氢氧化钙溶解度随温度的变化情况
实验目的
氢氧化钙溶解度跟温度呈反比。我们可以利用导电率传感器和温度传感器绘制导电率随时间变化的曲线图,通过清楚的现象得到这个结论。
实验设计
1.设计思路
氢氧化钙是微溶性物质,虽然温度改变,氢氧化钙在水中的溶解度也发生改变,但因为变化量很小,凭肉眼很难判断。借助导电率传感器和温度传感器检测不同温度时溶液导电率的变化情况,便可达到检测目的。温度升高,氢氧化钙的溶解度减小,溶液中离子浓度减小,溶液的导电率减小。
2.实验仪器与药品
温度传感器、导电率传感器、数据采集器、计算机、电磁搅拌机、烧杯,氢氧化钙固体、蒸馏水。
实验过程
1.配制氢氧化钙的饱和溶液。
2.检测该溶液的导电率随温度升高的变化情况。
将盛有悬浊液的小烧杯,置于电磁搅拌机上,搅拌加热。放入导电率传感器,同时放入温度传感器,每隔1秒采集一组数据,测溶液的导电率和温度,并绘出导电率随时间变化的曲线图。
实验结果
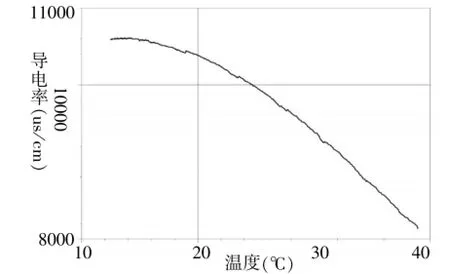
从图像的趋势看,温度升高,氢氧化钙饱和溶液的导电率变小,说明溶液中离子浓度变小,溶解的氢氧化钙变少。因此导电率随温度的变化情况,能定性反映溶解性随温度的变化情况。
实验说明
导电率本身还受到其他因素的影响,例如温度。但温度升高,因为溶液的离子粘度降低,离子运动速度加快,在水溶液中离子水化作用减弱等原因,导电能力增强,导电率是变大的。因此虽然溶液导电率受很多因素影响,但导电率随温度的变化趋势仍旧可定性的反映出溶解度随温度变化的趋势。
1008-0546(2011)04-0080-02
G633.8
B
10.3969/j.issn.1008-0546.2011.04.040
——饱和溶液与不饱和溶液

