对氨基苯甲酸修饰玻碳电极方波伏安检测铜离子
王嘉博, 杨国程, 王 璐, 赵振波, 李东风
(长春工业大学化学与生命科学学院,吉林长春 130012)
0 引 言
化学修饰电极是当前电化学、电分析化学方面十分活跃的研究领域。通过化学、物理化学或者电化学的方法对电极表面进行分子剪裁、修饰,可以按意图给电极预定结构和功能。目前,常用电化学氧化或者电化学还原的方法进行化学修饰,修饰分子与电极表面多以共价键形式相连,所制得的共价化学修饰电极结构稳定、长效[1]。由于重金属离子对环境生态及人类健康都有着至关重要的影响,因此,寻找简便、快捷、高效的重金属离子检测方法具有十分重要的意义,而具有预定功能的化学修饰电极在这方面显示出了强大的吸引力[2-4]。
文中将对氨基苯甲酸(4-aminobenzoic acid,4-ABA)通过电化学氧化方法共价修饰到玻碳电极(G lassy Carbon Electrode,GCE)上,考查了该修饰电极对铜离子的传感效应。
1 实验部分
1.1 试剂与仪器
K3Fe(CN)6,KCl,4-ABA,Cu(NO3)2均为分析纯;
电化学工作站(CS 350),武汉科斯特仪器有限公司;
单道固定量程移液器(Genex),Finland Genex;
超声波清洗器(KQ-100E),昆山市超声波仪器有限公司;
超纯水机(WP-UP-II-20),四川沃特尔水处理设备有限公司。
1.2 方法
1.2.1 共价化学修饰电极的制备
在使用GCE做实验之前,需要先清洁其表面:取适量α-A l2O3(1μm)抛光粉铺在抛光绒布上,用超纯水调成糊状,研磨GCE,然后用超声波清洗器清洗,再在 5 mmol/L Fe(CN)3-6(0.1 mol/L KCl作为支持电解质)溶液中进行循环伏安测试,磨到Fe(CN)3-6在GCE上氧化还原峰电位差值小于75mV方可使用。电极表面活性达到要求后,将GCE用超纯水冲洗,再超声清洗10 s,放入1 mmol/L 4-ABA溶液中(0.1 mo l/L KC l作为支持电解质)进行共价化学修饰,所得到的衍生结构如图1所示[5]。

图1 4-ABA在GCE上的修饰过程及衍生结构
1.2.2 方波溶出伏安检测Cu2+
将工作电极(GCE或4-ABA/GCE)、辅助电极(旋转铂丝电极)和参比电极(KCl饱和的Ag/AgCl电极)插入2m L 0.1m ol/L KCl溶液中(pH值接近7),首先测量空白溶液方波溶出伏安曲线,然后每次加4μL 50mmol/LCu(NO3)2水溶液,采用方波溶出伏安法进行检测Cu2+,具体的实验参数如下:清洗电位:0.4 V;清洗时间: 15 s;富集电位:-0.5 V;富集时间:15 s;静置时间:15 s;电位增量:0.004 V;初始电位:-0.5 V;终止电位:0.5 V;振幅:0.025 V。
2 结果与讨论
2.1 GCE修饰过程
4-ABA在GCE上的共价化学修饰过程及探针行为如图2所示。
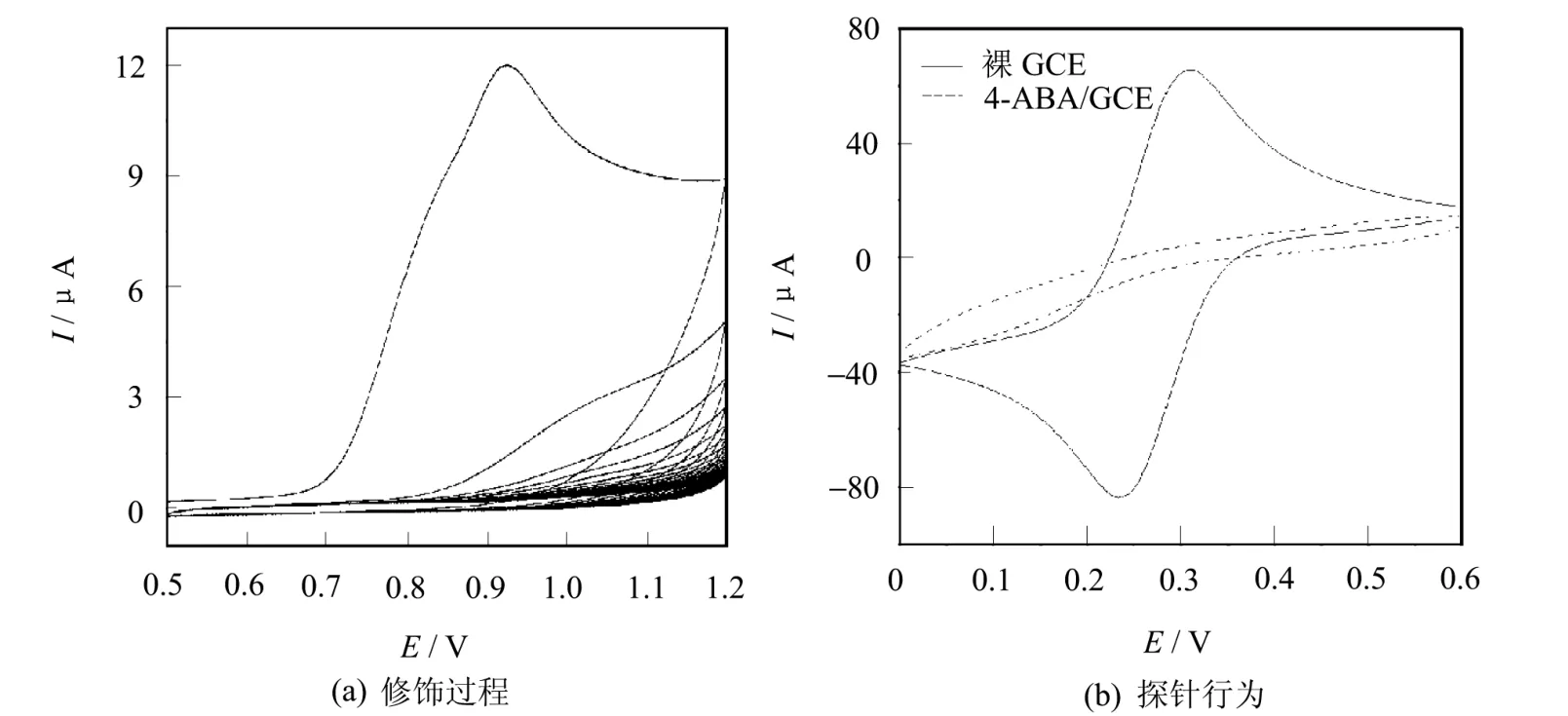
图2 4-ABA在GCE上的共价化学修饰过程及探针行为
GCE在4-ABA溶液中电氧化过程的循环伏安行为(见图2(a))。从图中可以看出,第一圈电位扫描时在~0.9 V处出现了一个不可逆的氧化峰,在随后的扫描中该氧化峰逐渐消失,这说明4-ABA共价键合到了GCE上。
考查了修饰前后电极在Fe(CN)3-6探针溶液中的循环伏安行为(见图2(b))。结果发现,在修饰前Fe(CN)3-6的氧化峰和还原峰出现,但修饰后却无峰出现,这也确定4-ABA键合到GCE上了,因为修饰后GCE表面的4-ABA外端为-COO-,使 GCE表面带负电荷,完全阻碍Fe(CN)3-6在GCE表面的氧化还原反应[5]。
2.2 溶出伏安检测Cu2+
GCE在 4-ABA修饰前后都被考查其对Cu2+的方波溶出伏安检测效果,结果如图3所示。

图3 Cu2+在裸GCE表面的溶出伏安曲线及校正曲线
从结果可以看出,裸GCE在溶出伏安检测Cu2+时,出现了两个溶出峰,分别在-0.012 V和0.188 V,底物浓度与溶出峰电流都成直线关系:
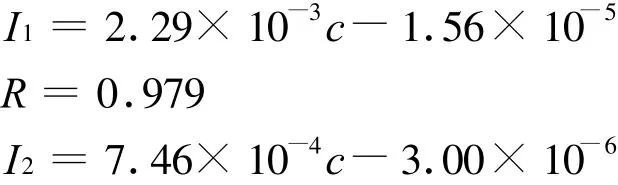
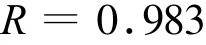
但是低电位的峰电流在Cu2+浓度相同时比高电位的要大。
Cu2+在4-ABA/GCE表面的溶出伏安曲线及校正曲线如图4所示。
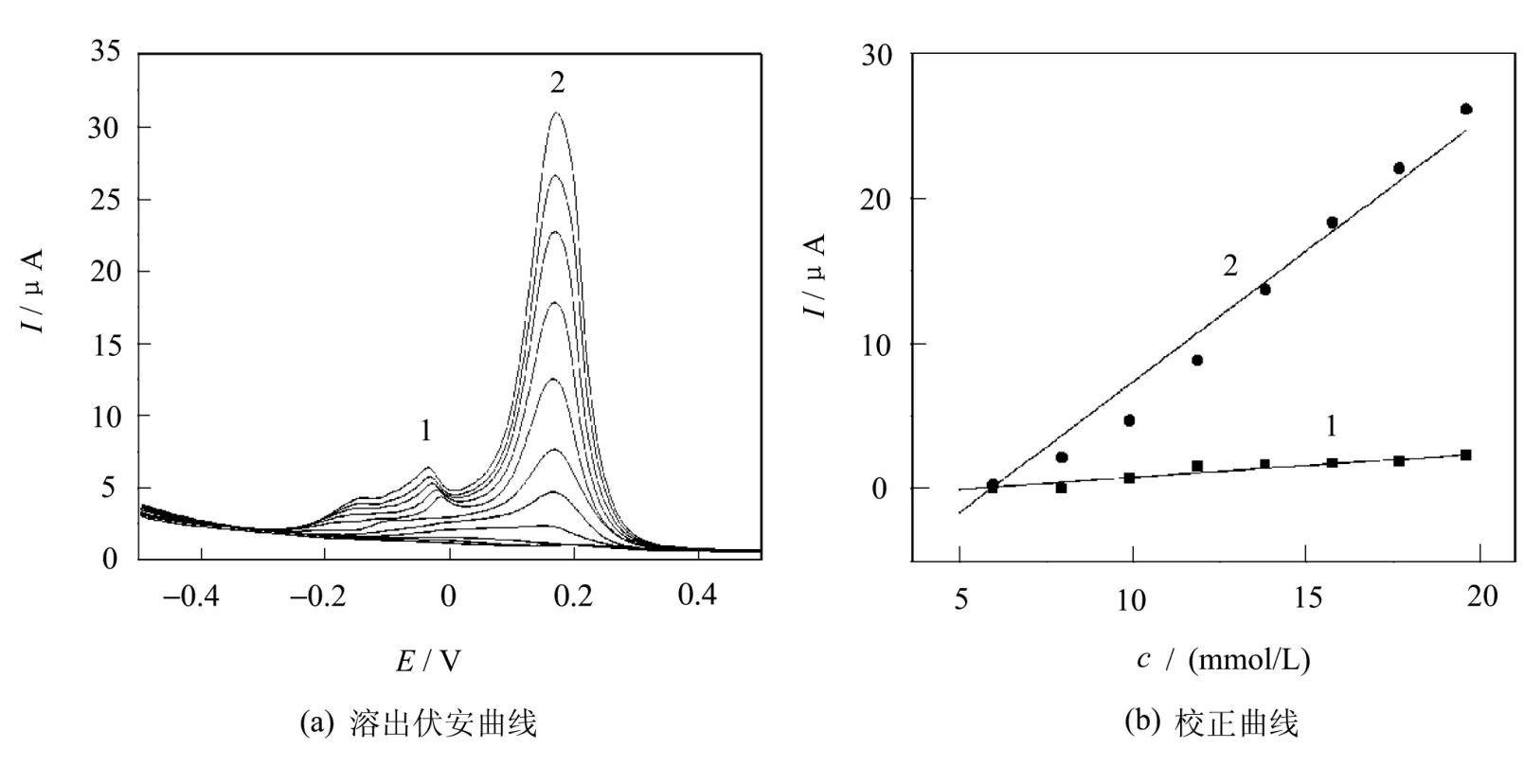
图4 Cu2+在4-ABA/GCE表面的溶出伏安曲线及校正曲线
用修饰后得到的4-ABA/GCE在同样的条件下方波溶出伏安检测Cu2+,方波溶出伏安曲线见图4(a)。可以看出,曲线也由两个溶出峰组成,底物浓度与溶出峰电流关系也成直线关系,见图4 (b)。
底物浓度与溶出峰电流直线关系的方程如下:

但是低电位的峰电流在Cu2+浓度相同时比高电位的要小很多,这一点与在裸GCE上的结果相反。
裸GCE和4-ABA/GCE对于Cu2+的溶出峰都有两个,说明在电沉积过程中都存在欠电位沉积和本体电沉积,分别对应于-0.012 V和0.188 V,但是浓度与峰电流关系不同,说明在两电位下沉积Cu2+的量不同。对于裸GCE来说,电极表面活性高,易于电沉积Cu2+,因而裸GCE对Cu2+的灵敏度也高,这一点从校正曲线的斜率就可以清楚地看出,而棱面碳的活性位点更多,欠电位沉积的量将会比本体电沉积的量要大。对于4-ABA/GCE,由于电极界面外端为-COO-,电极表面原有的活性被阻挡,活性位点降低,因而灵敏度变差,而羧基对Cu2+具有非常强的络合作用,特别容易形成多层膜,也就是特别容易发生本体电沉积[6-8]。
3 结 语
通过电化学氧化的方法将4-ABA共价修饰到GCE上,利用方波溶出伏安法研究了电极修饰前后对中性溶液中Cu2+的检测效果,结果显示,Cu2+在裸GCE和4-ABA/GCE表面上的溶出峰都有两个,即都存在欠电位沉积和本体电沉积行为,但是程度不同,GCE的欠电位沉积能力较本体电沉积要强,4-ABA/GCE则相反,这是由于裸GCE具有比4-ABA/GCE更好的表面活性引起的。
[1] 董绍俊,车广礼,谢远武.化学修饰电极[M].2版.北京:科学出版社,2003.
[2] Liu L X,Liu E.N itrogenated diamond-like carbon films for metal tracing[J].Surf.Coat.Technol.,2005,198(1/3):189-193.
[3] 刘颖,柳翱.电化学测定化学反应热力学函数变化值[J].长春工业大学学报:自然科学版,2009,30 (3):258-261.
[4] 林海波,伍振毅,黄卫民,等.工业废水电化学处理技术的进展及其发展方向[J].化工进展,2008,27 (2):223-230.
[5] Yang G C,Shen Y,W ang M K,et al.Copper hexacyanoferrate multilayer films on g lassy carbon electrode modified with 4-am inobenzoic acid in aqueous solution[J].Talanta,2006,68(3):741-747.
[6] A llen J B,Larry R F.Electrochem ical methods fundamentals and applications[M].2th ed.New York:John W iley&Sons,Inc.,2001.
[7] 张祖训,汪尔康.电化学原理与方法[M].北京:科学出版社,2000.
[8] 吴辉煌.电化学[M].北京:化学工业出版社,2004.

