热疗用阿霉素温敏纳米粒的制备及工艺优化Δ
樊秋平,梁嘉碧,杨海云,郭新铭,罗葆明,吴传斌
(1.中山大学药学院,广州市 510006;2.中山大学附属第五医院,珠海市 519000;3.中山大学附属第二医院,广州市 510120)
热疗用阿霉素温敏纳米粒的制备及工艺优化Δ
樊秋平1*,梁嘉碧2,杨海云3,郭新铭2,罗葆明3,吴传斌1#
(1.中山大学药学院,广州市 510006;2.中山大学附属第五医院,珠海市 519000;3.中山大学附属第二医院,广州市 510120)
目的:制备热疗用阿霉素温敏纳米粒,并对其制备工艺进行优化。方法:合成两亲性温敏嵌段共聚物P(NIPAM-co-DMAAM)-b-PCL,在水溶液中自组装形成温敏纳米粒。用滴注法制备载药温敏纳米粒,以包封率为评价指标,通过正交设计对温敏纳米粒制备工艺中温敏嵌段共聚物的浓度(A)、水相中阿霉素的浓度(B)、搅拌时间(C)等因素进行优化,对优化后工艺进行验证并在4℃下贮存90d考察其稳定性。结果:合成了两亲性温敏嵌段共聚物,其最低临界溶解温度(LCST)为40.3℃;最佳工艺为A0.15mg·mL-1、B 0.045mg·mL-1、C 1h,3批制剂的平均包封率为41.9%,平均粒径(155±2.7)nm;90d内制剂外观、粒径和包封率无明显变化。结论:成功制备了阿霉素温敏纳米粒,且其制备工艺可行,质量稳定。
阿霉素;温敏纳米粒;制备;正交设计;包封率;稳定性
热疗是将肿瘤区或全身加热至有效治疗温度范围并维持一定时间以杀灭肿瘤细胞的一种方法,作为肿瘤综合治疗的一个重要手段,在临床上被广泛用于实体肿瘤的治疗。热疗分为局部热疗和全身热疗[1],射频消融(RFA)属于局部热疗的一种方式,目前是肝癌非手术治疗的主要手段,但是RFA无论应用于“大肝癌”还是“小肝癌”都存在局部复发和转移的问题[2]。如果能通过化疗方法联合RFA进一步杀死残存的癌细胞,便可降低局部复发和转移问题。阿霉素(ADM)是临床常用的抗肿瘤药物,但其心脏、肾脏毒性大,治疗指数低,从临床应用的角度来看,应寻找一种更有效的制剂,以最大限度提高肿瘤组织内的药物浓度,最大限度地降低心脏和肾脏药物浓度(低毒性)[3]。聚N-异丙基丙烯酰胺(PNIPAM)类温敏药物载体由于其设计的多样性、最低临界溶解温度(LCST)的可调性,且具有被动靶向能力和定位释放等优点被广泛用于药物控释系统中[4]。鉴于上述临床需求和综合考虑,本研究制备了可以作为阿霉素载体的温敏纳米粒,为下一步开展阿霉素温敏纳米粒联合RFA治疗原发性肝癌研究奠定了基础。
1 仪器与试药
SP131320-33Q磁力搅拌热盘(美国Thermo公司);BS224S电子天平(德国赛多利斯公司);DZF-6050真空干燥箱(上海一恒科仪公司);400Mde核磁共振波谱仪(德国Bruker公司);UV-1800紫外分光光度计(日本岛津公司);HP1200高效液相色谱仪(美国安捷伦公司);LGJ-10C冷冻干燥机(长沙湘仪集团);5810R超低温高速离心机(德国Eppendorff公司);BS5510DTH超声波清洗器(上海生析超声仪器有限公司);Zetasizer Nano ZS90马尔文纳米粒度分析仪(英国马尔文公司)。
盐酸多柔比星(深圳万乐药业有限公司,批号:1004E1,纯度:>98%);N-异丙基丙烯酰胺(NIPAM,日本TCI公司,批号:44A8A,纯度:>98.0%);N,N-二甲基丙烯酰胺(DMAAM,美国Alfa Aesar公司,批号:J25S041,纯度:>99.5%);偶氮二异丁腈(AIBN)、β-巯基乙醇(2-ME)、辛酸亚锡、ε-己内酯、甲苯、无水乙醚等均为分析纯;阿霉素温敏纳米粒(中山大学附属第五医院研制)。
2 方法与结果
本试验先通过2个步骤合成了两亲性温敏嵌段共聚物P(NIPAM-co-DMAAM)-b-PCL,并对其结构和温敏特性进行表征。两亲性温敏嵌段共聚物在水中可自主装成纳米粒,再通过滴注法制备了载药纳米粒,用正交设计对温敏纳米粒的处方进行优化,并对纳米粒的粒径分布等进行表征。
2.1 两亲性温敏嵌段共聚物P(NIPAM-co-DMAAM)-b-PCL的合成和表征
2.1.1 温敏聚合物P(NIPAM-co-DMAAM)-OH的合成。参照文献[5]中的采用自由基聚合反应的方法。用AIBN为引发剂、2-ME为链增长剂进行反应。具体步骤如下:将一定量的NIPAM、DMAAM溶解在30mL的四氢呋喃中,加入适量的AIBN和2-ME,70℃条件下反应12h。整个反应过程在氩气保护下进行。用无水乙醚沉淀产物,沉淀物用少量的四氢呋喃(THF)复溶,再用无水乙醚沉淀,如此反复2次,所得产物在真空干燥箱(40℃)中干燥48h。
2.1.2 两亲性温敏嵌段共聚物P(NIPAM-co-DMAAM)-b-PCL的合成。参照文献[5]的方法,利用端基羟基轰击己内酯开环反应合成此嵌段共聚物。具体操作如下:取温敏聚合物P(NIPAM-co-DMAAM)-OH和一定量的ε-己内酯,在催化剂辛酸亚锡条件下,140℃反应24h,整个反应过程在氩气保护下进行。反应产物用过量乙醚沉淀,沉淀物用THF复溶后,再用乙醚沉淀,重复2次,所得产物在真空干燥箱(40℃)中干燥48h。
2.1.3 温敏嵌段共聚物的结构表征。用核磁共振波谱仪对上述 合 成 的 聚 合 物 P(NIPAM-co-DMAAM)-OH、P(NIPAM-co-DMAAM)-b-PCL进行结构特征的鉴定,其核磁共振(1H-NMR)图谱详见图1。
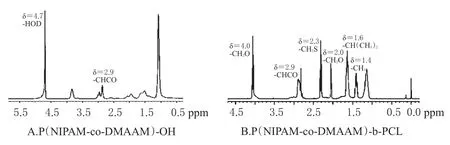
图1 1H-NMR图谱Fig1 1H-NMR spectra
图1A中由于用重水作溶剂,-OH上的活泼氢被交换,其质子峰消失,而在δ=4.7ppm处出现与HOD相应的单峰,表明端基羟基被连接上。图1B中,δ=4.7ppm的峰消失,而在1~4ppm之间,出现众多的多重峰,进行峰归属为聚合物中饱和烃基—CH3、—CH2—、—CHCO的峰,表明ε-己内酯开环而引入了大量的饱和烃基。结构表征表明成功合成了温敏两亲嵌段共聚物P(NIPAM-co-DMAAM)-b-PCL。
2.1.4 温敏嵌段共聚物的LCST的测定。PNIPAM类温敏共聚物水溶液随着温度的变化会出现相转变,此转变温度成为最低临界溶解温度,即LCST。当温度低于LCST时,聚合物分子呈现溶解特性;当环境温度升至其LCST以上时,聚合物呈现出疏水特性发生皱缩,导致聚合物溶液由透明变成浑浊。文献[6]中常用浊度法、以LCST为指标来测量两亲温敏嵌段共聚物的温敏特性,具体方法如下:制备适量浓度为0.1mg·mL-1的P(NIPAM-co-DMAAM)-b-PCL水溶液,将其置于恒温(30~50℃)水浴中,温度每升高1℃平衡10min,用紫外可见分光光度计在500nm波长处测其透光率(T),透光率为50%时的温度为其LCST。测定结果详见图2。
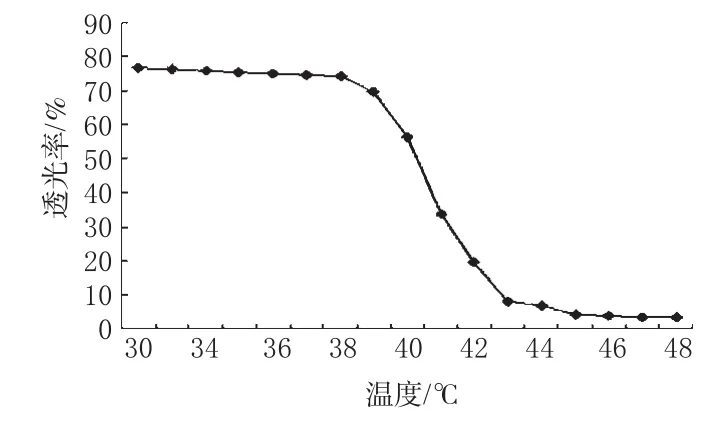
图2 温敏嵌段共聚物的温度-透光率曲线Fig2 Curve of temperature-transmittancy of thermosensitive block copolymer
从图2上可以看出,当环境温度从30℃升至39℃期间,聚合物溶液的透光率几乎无变化;当温度在40~41℃时,聚合物溶液的透光率急剧下降。因此,得到聚合物的LCST在40~41℃之间,约为40.3℃。
2.2 阿霉素温敏纳米粒的制备
用滴注法制备阿霉素温敏纳米粒。方法如下:取一定量温敏嵌段共聚物分散至5mL THF中,超声直至完全溶解后,滴加至100mL含药(阿霉素)溶液中。边滴加边搅拌,搅拌一定时间后即得阿霉素温敏纳米粒的混悬液。将混悬液转移至透析袋中(Mw:3500),用蒸馏水透析2d(换液6次,每次1000mL),除去未包封的药物和THF,透析完后冷冻干燥,即得载药微粒粉末,密封后于4℃冰箱中存放。
2.3 含量测定方法
2.3.1 色谱条件。色谱柱:Agilent Zorbax ODS-C18(150mm×4.6mm,5μm);流动相:5mol·L-1H3PO4水溶液-乙腈-甲醇-异丙醇(65%∶15%∶10%∶10%);选用荧光检测器,检测波长:激发波长505nm,发射波长550nm;柱温:室温;进样量:20μL。2.3.2标准曲线的制备。标准液的制备方法:按照“2.2”项下的制备方法,制备空白纳米粒混悬液,离心(12000r·min-1)30min后取上清液,用离心后的溶液作溶剂,精密制备一系列浓度的阿霉素标准溶液,浓度分别为0.05、0.1、0.2、0.5、1、2、5、10μg·mL-1,进样测定其峰面积(Y),以相应的Y对其溶液浓度(X,μg·mL-1)进行线性回归,求得标准曲线方程:Y=0.0011X+0.0227(R2=0.9996),结果表明阿霉素检测浓度线性范围为0.05~10μg·mL-1。
2.3.3 回收率试验。按照“2.3.2”项下标准曲线的制备方法制备高、中、低(10、1、0.05μg·mL-1)3个浓度的阿霉素样品,每个浓度5个样品。与随行标准曲线同法测定,每个样品分析测定1次,测定结果用随行标准曲线的回归方程计算样品的浓度,并以测定值平均值与制备的理论浓度值比较,即为回收率,结果平均回收率为98.4%(RSD=1.92%)。
2.3.4 精密度试验。分别制备高、中、低(10、1、0.05μg·mL-1)3个浓度的阿霉素标准液,于同日内测量,每种浓度连续进样5次,计算批内精密度;连续测量5d,每日进样测量1次,计算批间精密度。结果批内RSD小于1.02%,批间RSD小于1.97%。
2.4 包封率测定
采用高速离心法测定阿霉素纳米粒的包封率:取一定量的阿霉素温敏纳米粒混悬液,离心(12000r·min-1)30min,取上清液,上清液中的药物即为未包封药物。按照“2.3.1”项下条件进样测定,按照以下公式计算包封率:

2.5 阿霉素温敏纳米粒制备工艺的优化
根据预试验结果,对影响包封率的3种主要因素:温敏嵌段共聚物(以下简称共聚物)的浓度(A,mg·mL-1)、水相中阿霉素的浓度(B,mg·mL-1)、搅拌时间(C,h)进行正交设计,每个因素3个水平,采用正交表L9(34),以包封率为评价指标来进行工艺优化。因素水平见表1,工艺优化的正交设计结果见表2,方差分析见表3。
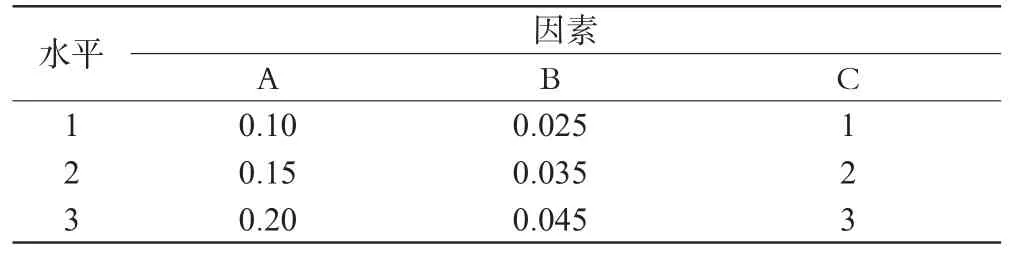
表1 因素水平表Tab1 Factors and levels
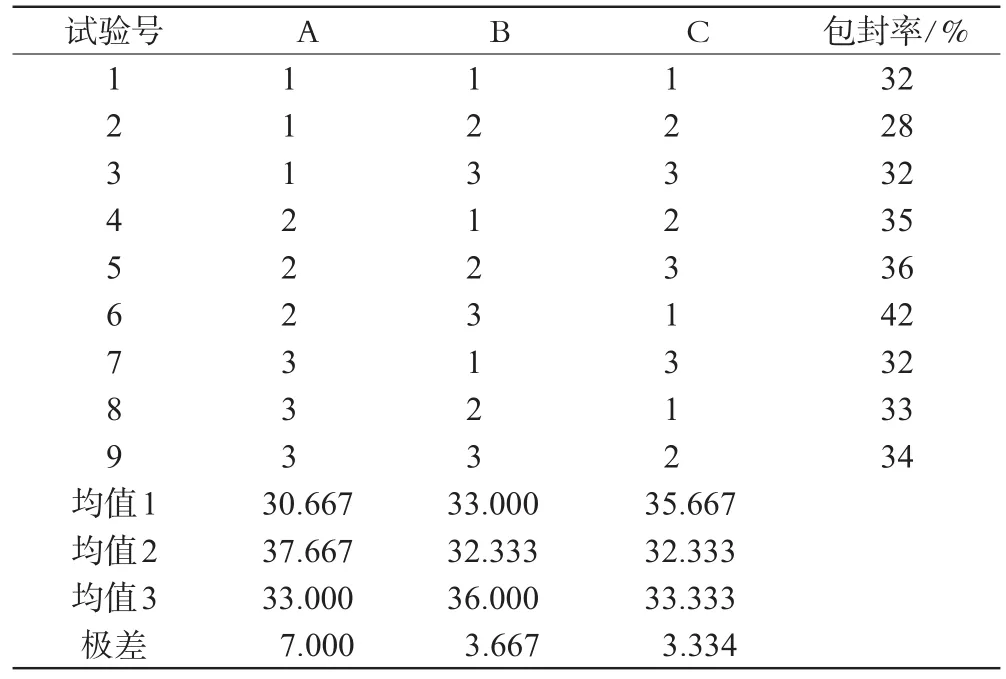
表2 正交试验结果Tab2 Result of orthogonal experiments
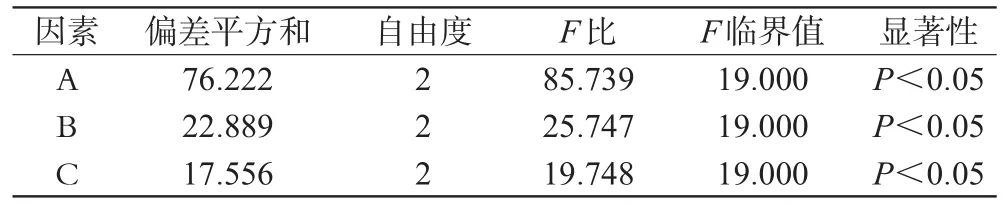
表3 方差分析Tab3 Analysis of variance
对包封率进行方差分析可以看出,3种因素A、B、C均有显著性差异,再结合直观分析,确定最佳制备工艺为A2B3C1,即共聚物浓度为0.15mg·mL-1,水相中阿霉素浓度为0.045mg·mL-1,搅拌时间为1h。
2.6 工艺验证
按“2.2”项下方法及选定的工艺条件制备温敏纳米粒3批,测定其包封率,结果分别为40.8%、43.2%、41.6%,平均包封率为41.9%。
2.7 阿霉素温敏纳米粒的粒径和稳定性
2.7.1 载药纳米粒粒径测定。取阿霉素温敏纳米粒混悬液适量,用纳米粒度分析仪测定其粒径,结果粒径分布较窄,粒径均匀,平均粒径为(155±2.7)nm,详见图3。

图3 阿霉素温敏纳米粒的粒径分布图Fig3 Particle size distribution ofAdriamycin nanoparticles
2.7.2 阿霉素温敏纳米粒稳定性观察。将制备的样品于4℃冰箱中保存3个月(90d),取出考察其外观、粒径和包封率的变化。结果,4℃储存条件下,阿霉素温敏纳米粒外观仍呈现均一、透明的分散体系,粒径和包封率也变化不大,由此看出阿霉素温敏纳米粒具有良好稳定性,详见表4。
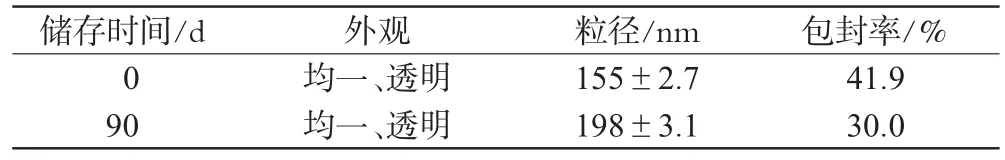
表4 样品稳定性结果Tab4 Stability of samples
3 讨论
PNIPAM是一类被广泛研究的温敏材料,其聚合物相变温度约32℃,当与其他亲水或疏水单体共聚合时可得到具有不同LCST的高分子:NIPAM与亲水性单体(DMAAM、HEMA等)共聚可以提高LCST[7]。在本研究中,为了得到LCST高于人体生理温度(37℃)的温敏共聚物,让NIPAM与一定比例的DMAAM共聚,最终通过调节比例使共聚物的LCST提高到40.3℃。通过加入不同比例的DMAAM,可以得到不同LCST的温敏共聚物,与参考文献[7]中的结论相符。
纳米粒的制备方法主要有透析法、溶剂蒸发法和滴注法等。本文采用的是滴注法,该方法简单易行,且所制备的纳米粒粒径均匀,粒径分布为(155±2.7)nm,平均包封率为41.9%,室温放置比较稳定。
国内、外对纳米粒中药物包封率的测定大多采用葡聚糖凝胶过滤法和超速离心法[8,9],前者较费时且效果不好,因此,本研究采用超速离心法测定纳米粒的包封率。考虑到高速离心过程中可能导致纳米粒中药物泄露和空白囊材的干扰等,在制备标准曲线时,用离心过的空白囊材溶液作溶剂来制备标准溶液,并对此法的回收率进行考察,多次测量后平均回收率为98.4%,RSD为1.92%。方法学结果表明此方法比较稳定,可以用来测定阿霉素温敏纳米粒的包封率。
恶性肿瘤的综合治疗已成为大势所趋,如联合化疗和热疗,二者联合具有协同效应。本研究合成的温敏纳米粒的LCST为40.3℃,而在人正常体温下(37℃),由于环境温度低于其LCST,药物被包裹在载体中,当局部通过热疗加热使温度高于其LCST(40.3℃)时,可使局部(加热部位)药物释放增加,而不引起药物在其他部位的释放。热疗联合药物化疗理论上可以增加恶性肿瘤治愈率,降低全身的毒副作用,但是有关其联合RFA时药物控释特性和相关动物体内实验还有待进一步研究。
综上所述,成功制备了阿霉素温敏纳米粒,且其制备工艺可行,质量稳定。
[1] 王化宁,包国强,赖大年.肿瘤热疗的临床应用及研究进展[J].现代肿瘤医学,2006,14(2):231.
[2] 柯 山,孙文兵.射频消融治疗肝癌的历史、现状与展望[J].中国临床医生,2010,38(10):725.
[3] 张阳德,席 浩,翟登高,等.半乳糖化磁性白蛋白阿霉素纳米粒与阿霉素对大鼠的毒性比较[J].中华实验外科杂志,2004,21(10):1189.
[4] Bikram M,West JL.Thermo-responsive systerms for controlled drug delivery[J].Expert Opin Drug Deliv,2008,5(10):1077.
[5] Choi C,Chae SY,Nah J-W.Thermosensitive poly(N-isopropylacryl-amide)-b-poly(3-caprolactone) nanoparticles for efficient drug delivery system[J].Polymer,2006,47:4571.
[6] Shingjiang Jessie Lue,Jing-Jung Hsu,Ta-Chin Wei.Drug permeation modeling through the thermo-sensitive membranes of poly(N-isopropylacrylamide) brushes grafted onto micro-porous films[J].Journal of Membrane Science,2008,321(2):146.
[7] 刘文博,王国明,蔡 晴.N-异丙基丙烯酰胺类共聚物温敏性研究[J].高分子报,2008,12(12):1214.
[8] Mehnert W,Mader K.Solid lipid nanoparticles:production,characterization and applications[J].Adv Drug Deliv Rev,2001,47(2-3):165.
[9] 官金岩,胡连栋,刘 洋,等.维甲酸固体脂质纳米粒中主药的含量及包封率测定[J].中国药房,2008,19(16):1252.
Preparation of Adriamycin Thermosensitive Nanoparticles for Hyperthermia Therapy and Optimization of Preparation Technology
FAN Qiu-ping,WU Chuan-bin
(School of Pharmacy,Sun Yat-sen University,Guangzhou 510006,China)
LIANG Jia-bi,GUO Xin-ming
(The Fifth Affiliated Hospital of Sun Yat-sen University,Zhuhai 519000,China)
YANG Hai-yun,LUO Bao-ming
(The Second Affiliated Hospital of Sun Yat-sen University,Guangzhou 510120,China)
OBJECTIVE:To prepare Adriamycin thermosensitive nanoparticles for hyperthermia therapy,and to optimize the preparation technology of it.METHODS:Amphiphilic block copolymer poly(N-isopropyl-acrylamide-co-N,N-dimethylacrylamide)-b-poly(ε-caprolactone)was synthesized.Owing to their amphiphilic characteristics,the block copolymer formed self-assembled thermosensitive nanoparticles in aqueous milieus.Nanoparticles were prepared using solvent injection method.The preparation technology of nanoparticles was optimized by orthogonal experiments using encapsulation efficiency as index with the concentration of thermosensitive polymer(A),the concentration of adriamycin in water phase(B)and stirring time(C)as factors.Optimized formula was validated and the stability of nanoparticles stored at 4℃ for 90days was investigated.RESULTS:The amphiphilic block copolymer was synthesized.And its lower critical solution temperature(LCST)was around 40.3℃.Optimal formula was as follows:A of 0.15mg·mL-1,B of 0.045mg·mL-1,C of 1h.The average encapsulation efficiency were 41.9%and the mean diameters of nanoparticles were(155±2.7)nm.The appearance,particle size and encapsulation efficiency of nanoparticles had no significant change within 90days.CONCLUSION:Adriamycin thermosensitive nanoparticles have been prepared successfully,and preparation technology is feasible and stable in quality.
Adriamycin;Thermosensitive nanoparticles;Preparation;Orthogonal experiment;Encapsulation efficiency;Stability
R943;R979.1
A
1001-0408(2011)17-1580-04
Δ国家自然科学基金资助项目(30872996);广东省科技计划项目(2009B030801081)
*硕士研究生。研究方向:药物新剂型和新技术。E-mail:fqpby2004@163.com
#通讯作者:教授,博士研究生导师。研究方向:缓、控释靶向制剂。E-mail:cbwu2000@yahoo.com
2011-01-04
2011-02-17)

