生物活性炭对焦化废水中萘的吸附降解
李文兵,王光华,郭 胜,蒋丽娟,杨书琴,朱亦男,张玉佳
(1.武汉科技大学煤转化与新型炭材料湖北省重点实验室,湖北武汉,430081;2.武汉科技大学化学工程与技术学院,湖北武汉,430081)
经生化处理后的焦化废水中虽去除了大部分有毒物质,但仍含有大量难以降解的芳烃类有机物[1],用常规的物理、化学方法处理这些有机物难以达到废水回用标准[2-3]。萘是焦化废水生化处理后最难降解的有机物之一[4]。微生物降解除萘是一种绿色无污染治理技术,采用微生物固定化技术可以提高萘去除效果[5],其中活性炭是一种去除水中污染物有效的固定化载体[6]。生物活性炭(Biological Activated Carbon,BAC)技术是以活性炭为载体,负载活性微生物,通过活性炭的物理吸附与表面附着微生物群落来实现生物降解去除污染的一项技术[7-9]。目前,BAC作为一种绿色水处理技术在微污染水体净化、工业废水处理和深度净化等领域愈来愈引起人们的关注[10-11]。
本研究以焦化废水生化处理后二沉池水中含量较高的萘为目标物,研究BAC系统对萘的吸附特征和生物学吸附降解动力学,以期为实际焦化废水的循环回用提供理论依据。
1 实验
1.1 实验材料
焦化废水取样于某焦化厂二沉池出水,CODCr为200 mg/L,色度900倍。生物样品取样于某焦化公司焦油车间土壤。实验用活性炭指标:比表面积1 000~1 200 m2/g,碘值为1 108 mg/g,粒径3.5~5.5 mm,堆积密度0.4~0.5 g/m L,苯酚值为80.9 mg/g。
1.2 培养基
无机盐培养基组成:NH4NO31.00 g,Na2HPO 1.00 g,KH2PO41.00 g,M gSO4·7H2O 0.02 g,CaCl20.05 g,微量元素1 m L,蒸馏水1 L,调pH值为7.0。
微量元素液组成:M nSO4·H2O 1.69 g,CoCl2·6H2O 0.24 g,H3BO31.16 g,Na2MoO4·2H2O 0.024 g,FeSO4·7H2O 2.78 g,ZnSO4·7H2O 1.15 g,CuSO4·5H2O 0.38 g,蒸馏水1 L。
LB培养基组成:酵母浸膏5 g,蛋白胨10 g,NaCl 10 g,蒸馏水1 L。固体培养基按2.0%加入琼脂。
1.3 实验方法
1.3.1 菌株的分离与筛选
将体积分数为1%的土壤接入200 m L的浓度为500 mg/L含萘无机盐液体培养基中,在30℃、150 r/m in条件下摇床培养3 d,按1%的体积分数转接入新的萘无机盐液体培养基中,按上述条件振荡培养3 d,按上述方法重复3次,将所得菌液稀释涂布于固体培养基上,置于30℃生化培养箱中培养3~4 d,在平板上挑取不同形态特征的菌落,重新转接入200 m L的浓度为200 m g/L含萘无机盐液体培养基中,培养验证其对萘的降解能力,待培养液明显浑浊后,重复3次分离纯化,最后将具有萘降解性能的菌种植入LB固体培养基中,保存于冰箱中备用。选取具有最高萘降解率的菌株NPA-5,对其进行革兰氏染色、显微观察和生理生化试验[12-13]。
1.3.2 BAC制备
将活性炭用5%盐酸浸泡24 h,以去除粉尘和可溶于酸的表面物质,用去离子水淋洗至中性,于120℃下干燥5 h,将活化后的活性炭置于干燥器中备用。采用生物挂膜法[14]将NPA-5负载于活性炭上,得生物活性炭(BAC)。
1.3.3 吸附实验
在一系列150 mL碘量瓶中分别加入0.1~1.0 g活性炭和100 m L的浓度为200 mg/L的含萘焦化废水溶液,在150 r/min、30℃条件下振荡5 h后取样,过滤离心,测定溶液中萘的浓度。活性炭对萘的吸附量为式中:V为溶液体积,L;Co和Ce分别为吸附前和吸附平衡时萘浓度,mg/L;m为活性炭质量,g。
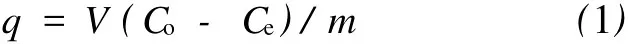
1.3.4 生物降解实验
在250 m L锥形瓶中加入0.2 g的生物活性炭和200 mL的浓度为200 mg/L的含萘焦化废水溶液,于30℃、150 r/min条件下振荡培养4 d,每隔12 h取样测溶液的萘含量。
1.4 分析方法
用Agilent 6890气相色谱仪测定萘含量,配置FID检测器。色谱条件:HP-5(30 m×0.32 mm×0.25μm),柱温150℃,汽化室温度200℃,检测器温度220℃。载气N2流量1 mL/min,H2流量20 m L/min,空气流量100 mL/min,进样量lμL。用正己烷分别按5、50、100、200 mg/L 4种不同浓度配置萘标样,每个浓度至少取样3次,测定样品的峰面积(取平均值),根据萘的浓度值和峰面积绘制标准曲线,其方程为
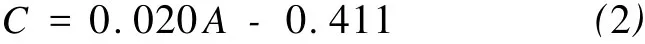
式中:C为萘浓度;A为峰面积;相关系数为0.999。
2 结果与讨论
2.1 萘降解菌的鉴定
平板观察NPA-5,其细菌特征呈乳白色,圆形(1~1.5 mm),边缘整齐,不透明,光滑,湿润(图1(a))。电子显微镜下该菌为无芽孢杆菌,细胞较小(0.5~1.0μm×1.5~5.0μm)(图1(b))。革兰氏染色为阴性。

图1 NPA-5的菌落形态特征Fig.1 The colonialmorphology characteristic of NPA-5
NPA-5生理生化特征试验结果如表1所示。

表1 NPA-5生理生化特征试验结果Table 1 Physiological and biochem ical characteristics of strain NPA-5
从表1结果可以判定NPA-5为铜绿假单胞菌(Pseudomonasaeruginosa)[12-13]。
2.2 活性炭对萘的等温吸附
图2为303 K时活性炭对萘的等温吸附线。由图2可见,活性炭对萘的平衡吸附量随萘的浓度增大而增大,对萘表现出较好的吸附性能。该等温吸附线符合IUPAC分类中的I型等温线,在低分压区,平衡吸附量随萘的浓度升高而增大,当萘的浓度升高至一定值时,平衡吸附量几乎不随萘的浓度升高而改变。
运用图2中描述的降解吸附数据,采用Langmuir和Freundlich等温吸附模型拟合有式中:qe为平衡吸附量,mg/g;qm为吸附容量,mg/g;Ka为Langmuir常数;Kf为Freundlich容量常数;Ce为吸附平衡时萘的浓度,mg/L;n为Freundlich强度常数。
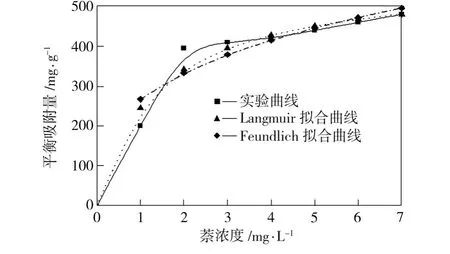
图2 活性炭对萘的等温吸附线(303 K)Fig.2 Adsorption isotherms of naphthalene on activated carbon
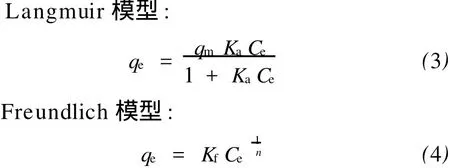
由等温吸附模型可得活性炭吸附萘的等温吸附方程

上述结果表明,活性炭吸附剂对萘的吸附符合Langm uir和Freundlich等温吸附模型(R2均在0.98以上)。这主要是因为萘的分子量较低,在溶液中扩散速率较快[15-16],分子间相互作用力较弱,在低萘浓度区,吸附会优先发生在吸附势高的微孔中,即微孔填充过程[16];当吸附剂表面微孔被吸附质占据后,萘分子会继续在吸附剂的中大孔表面发生吸附,但由于萘分子间分子作用力较弱,故该过程主要以单分子层吸附为主,这与Langmuir和Freundlich等温模型的基本假设一致。此外,Freundlich等温模型比Langmuir等温模型拟合程度高,这与文献[16]报道一致。
2.3 BAC对萘的生物吸附动力学
BAC和NPA-5对萘的吸附降解实验结果如图3所示。从图3中可看出,在较短的培养时间内,BAC主要发挥等温吸附作用[17],微生物降解作用未得到充分发挥;随着培养时间的延长,BAC和NPA-5对萘的降解能力逐渐接近。96 h后,BAC处理过的废水中萘残余浓度为1.4 mg/L,萘的去除率达99.3%;NPA-5处理过的废水中萘残余浓度为1.6 mg/L,萘的去除率达99.2%。
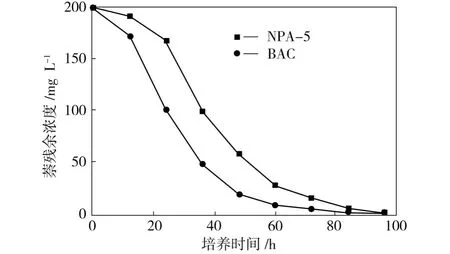
图3 BAC和NPA-5对萘的吸附降解Fig.3 The process of biodegradation of naphthalene
图3中生物活性炭对萘的吸附降解结果表明,BAC对萘的降解反应遵循一级反应动力学模型,该模型中反应速率常数为拟合直线的斜率,其动力学模型为

式中:C、C0分别为t时刻和初始时刻的萘浓度,mg/L;k为萘生物降解一阶反应速率常数,h-1;t为培养时间,h。
BAC对萘的降解动力学曲线如图4所示。其中反应速率常数是培养时间为96 h后的结果,数值为0.057 27 h-1,相关系数R2=0.978 3。该曲线表明生物活性炭对萘降解的动力学模型与一级反应动力学模型吻合,萘可以作为唯一碳源用于菌株NPA-5生长而消耗降解萘。
生物活性炭对萘的降解一级动力学方程为
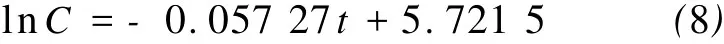
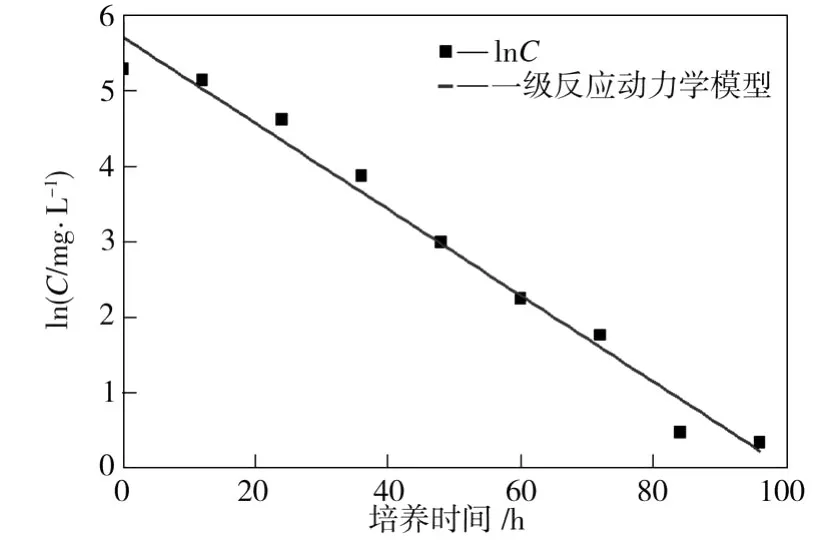
图4 BAC对萘的降解动力学曲线Fig.4 The kinetic curve of biodegradation of naphthalene with BAC
3 结论
(1)活性炭对萘的等温吸附符合Langm uir和Freundlich等温吸附模型,Freundlich模型比Langmuir模型拟合程度高。
(2)NPA-5作为一株高效降解萘的微生物,其降解率可达99.2%。
(3)负载菌株NPA-5的生物活性炭(BAC)以萘为唯一碳源生长并降解萘,96 h内降解率达99.3%。
(4)BAC对萘的降解符合lnC=-0.057 27t+5.721 5一级动力学模型。
[1] Ania CO,Cabal B,Pevida C,et al.Effectsof activated carbon p roperties on the adso rp tion of naphthalene from aqueous solutions[J].App lied Surface Science,2007,253:5 741-5 746.
[2] Jiang W,Zhang W,Li B,et al.Combined fenton oxidation and biological activated carbon process for recycling of coking plant effluent[J].Journal of Hazardous Materials,2011(2):37.
[3] Rivas F J.Polycylic aromatic hydrocarbons so rbed on soils,a short review of chemical oxidation based treatments[J].Journal of Hazardous Materials,2006,38(B1):234-251.
[4] Santos EC,Rodrigo J S,Jacques Bento FM,et al.Anthracene biodegradation and surface activity by an iron-stimulatedPseudomonassp.[J].Bioresource and Technology,2008,99:2 644-2 649.
[5] Mano S,Karegoudar T B.Degradation of naphthalene by cellsofPseudomonassp.Strain NGK 1 immobilized in alginate,agar and polyacrylamide[J].Appl Microbiol Biotechnol,1998,49:785-792.
[6] Anbia M,Moradi S E.Adsorption of naphthalenederived compounds from water by chemically oxidized nanoporous carbon[J].Chemical Engineering Journal,2009,148:452-458.
[7] Lin C,Tsai T,Liu J,et al.Enhanced biodegradatiob of petrochemical wastewater using ozonation and BAC advanced treatment system[J].Water Research,2001,35(3):699-704.
[8] Liang C H,Chiang PC,Chang E E.Modeling the behavio rs of adsorption and biodegradation in biological activated carbon filters[J].Water Researchm,2007,41(15):3 241-3 250.
[9] 吴伟,张龙,刘伟京,等.PACT工艺系统中的吸附和生物降解性能研究[J].环境科学研究,2010,23(8):1 062-1 067.
[10] Augulyte L,Kliaugaite D,Racys V,et al.Multivariate analysis of a biologically activated carbon(BAC)system and its efficiency for removing PAHs and aliphatic hydrocarbons from wastewater polluted with petroleum products[J].Journal of Hazardous Materials,2009,170:103-110.
[11] Gerrity D,Gamage S,Holady JC,et al.Pilot-scale evaluation of ozone and biological activated carbon for trace organic contaminant mitigation and disinfection[J].Water Research,2011,45:2 155-2 165.
[12] 东秀珠,蔡妙英.常见细菌系统鉴定手册[M].北京:科学出版社,2001:364-398.
[13] 张纪忠.微生物分类学[M].上海:复旦大学出版社,1990:95-97.
[14] 郭盛,王光华,李文兵,等.生物活性炭深度处理焦化废水的研究[J].洁净煤技术,2010,16(3):100-103.
[15] Cabal B,Ania C O,Parra J B,et al.Kinetics of naphthalene adsorption on an activated carbon:Comparison between aqueous and organic media[J].Chemosphere,2009,76:433-438.
[16] Ania C O,Cabal B,Parra J B,et al.Naphthalene adsorption on activated carbons using solvents of different polarity[J].Adsorption,2008,14:343-355.
[17] Walker GM,Weatherley L R.A simplified predictive model for biologically activated carbon fixed beds[J].Process Biochemistry,1997,32:327-335.

