溶剂热法制备Ag/TiO2纳米材料及其光催化性能
许平昌 柳 阳 魏建红,2,* 熊 锐 潘春旭 石 兢
(1武汉大学物理科学与技术学院,人工微结构教育部重点实验室,武汉 430072; 2低维材料与技术教育部重点实验室(湘潭大学),湖南湘潭 411105)
溶剂热法制备Ag/TiO2纳米材料及其光催化性能
许平昌1柳 阳1魏建红1,2,*熊 锐1潘春旭1石 兢1
(1武汉大学物理科学与技术学院,人工微结构教育部重点实验室,武汉 430072;2低维材料与技术教育部重点实验室(湘潭大学),湖南湘潭 411105)
以乙醇为溶剂,钛酸四丁酯为前驱体,用溶剂热法制备了Ag表面修饰的负载型纳米二氧化钛光催化剂.利用X射线衍射(XRD)、N2吸附-脱附(BET)、透射电子显微镜(TEM)、X射线光电子能谱(XPS)、紫外-可见(UVVis)光谱等技术对其进行了系统的表征,以亚甲基蓝(MB)溶液的脱色降解为模型反应,考察了不同Ag含量样品的光催化性能.结果表明:用溶剂热法制备的样品中TiO2皆为锐钛矿相,金属Ag颗粒沉积在TiO2表面,粒径为2 nm左右,比表面积较溶胶凝胶法制备的样品大大增加,最高可达151.44 m2·g-1;UV-Vis光谱和光催化实验表明:Ag修饰使TiO2对光的吸收能力大大增强,吸收带边红移至可见光区,亚甲基蓝在该复合材料上的光催化降解反应遵循一级反应动力学模型;溶剂热法制备样品的光催化性能明显好于溶胶凝胶法制备的样品,在紫外光和可见光下,Ag摩尔分数为5%的样品表现出最佳的光催化活性.
二氧化钛;银修饰;溶剂热法;溶胶凝胶法;亚甲基蓝;光催化
纳米TiO2光催化在环境治理领域中有广泛的应用前景,进一步提高TiO2的光催化活性是其应用的关键.现有研究结果表明,高活性的光催化剂往往具有较大的比表面积和高结晶度,而比表面积、结晶度等与制备方法密切相关.溶剂热法是一种新颖的低温合成单相TiO2的方法,不仅可以避免传统制备方法中出现的纳米粉末团聚、比表面积减小和晶相转变等问题,而且可以通过改变溶剂、pH值、反应时间和温度等参数控制晶体的结构和形貌,引起了研究者们广泛的兴趣[1-4].
TiO2由于带隙较宽(Eg=3.2 eV),仅能吸收波长小于380 nm的紫外光,加上光生电子和空穴容易复合,光量子效率低,阻碍了TiO2光催化材料的实际应用[5-7].研究表明,通过非金属元素掺杂[8-9]、金属修饰[10-17]、半导体复合[18]、有机物改性[19-20]等方法能不同程度地拓展吸收光谱,提高TiO2的光量子效率,进而提高TiO2的光催化性能.其中,Ag掺杂修饰TiO2纳米光催化剂的研究引起人们的广泛重视,如Binitha等[21]用溶胶凝胶法制得Ag掺杂的TiO2光催化剂,尤先锋等[22]通过用溶胶凝胶和水热协同法制备了不同Ag含量的负载型Ag-TiO2,都使得TiO2光催化性能得到了不同程度提高.但迄今为止,用溶剂热法制备Ag掺杂修饰TiO2纳米光催化剂的研究还少见报道.
本文采用溶剂热法制备了不同Ag含量负载型的纳米Ag/TiO2光催化剂,利用XRD、BET、TEM、XPS、UV-Vis等手段对样品进行表征,以MB溶液的脱色降解为模型反应,考查紫外和可见光下不同银负载量对其光催化性能的影响,并与用溶胶凝胶法制备的Ag/TiO2光催化剂进行比较.
1 实验部分
1.1 主要仪器与试剂
D8-ADVANCE X射线衍射仪(XRD)(德国BRUKERAXS公司);JW-BK静态氮吸附仪(BET)(北京精微高博科学技术有限公司);XSAM800多功能电子能谱仪(XPS)(英国Kratos Ltd.公司);CARY5000紫外-可见-近红外(UV-Vis-NIR)光谱仪(美国VARIAN公司);JEM-2010(HT)透射电子显微镜(TEM)(日本电子公司).
钛酸四丁酯(国药集团化学试剂有限公司,化学纯,>98.0%);AgNO3(国药集团化学试剂有限公司,分析纯,>99.8%);乙醇(国药集团化学试剂有限公司,化学纯,>99.7%);P-25样品从德国Degassor公司购买,所有试剂使用时未经进一步纯化.
1.2 Ag/TiO2光催化剂的制备
将一定量的AgNO3加入24 mL无水乙醇中,磁力搅拌至AgNO3完全溶解,将5 mL钛酸四丁酯逐滴加入溶液中,磁力搅拌10 min得到淡黄色溶液.在磁力搅拌下,将1 mL蒸馏水缓慢滴加入此溶液中,搅拌20 min后,将反应物移至反应釜中,用真空干燥箱加热,以3℃·min-1速率升温至180℃,保温6 h,而后自然冷却至室温,将所得产物用蒸馏水清洗,重复超声分散-离心分离四次,80℃下烘干即可得到Ag/TiO2催化剂.改变AgNO3的用量,分别制备了Ag摩尔分数为1%、3%、5%、10%、15%的Ag/ TiO2光催化剂,随着Ag含量的增加,样品颜色产生明显变化,分别为粉红色、深红色、红褐色、黑褐色、黑色.用同样方法制备了纯的TiO2,以考察Ag掺杂对TiO2结构及性质的影响.
作为比较我们用溶胶凝胶法制备了Ag摩尔分数为5%的Ag/TiO2,记为SG-TiO2.具体实验步骤如下:将定量的AgNO3溶于24 mL无水乙醇中,再将3 mL二乙醇胺和5 mL钛酸四丁酯先后加入此溶液,磁力搅拌10 min后,将1 mL蒸馏水缓慢滴加入此溶液中,搅拌30 min后,室温下静置24 h得湿凝胶,将湿凝胶放入真空干燥箱中,100℃下保温2 h,得到干凝胶,再将干凝胶放入马弗炉中,以5℃· min-1速率升温至520℃保温6 h,自然冷却至室温,研磨产物即得SG-TiO2粉末.
1.3 光催化性能的测试
以125 W高压汞灯为紫外光源,分别在紫外光和可见光(加滤波片)下,用MB溶液的脱色降解来表征Ag/TiO2的光催化活性.将0.3 g催化剂加到50 mL浓度为10-4mol·L-1的MB溶液中,置于自建的密闭光反应器里,磁力搅拌20 min,确保吸附平衡后打开光源进行光催化反应,每隔20 min取样1.7 mL,将所得样品离心分离去除催化剂,取上层清液测试.用UV-Vis测定MB在664 nm处的吸光度,评价在Ag/TiO2复合材料上的光催化降解活性.
2 结果与讨论
2.1 样品的XRD分析
图1为SG-TiO2和不同Ag负载量的Ag/TiO2样品的XRD图谱.各样品的XRD图谱与锐钛矿结构的TiO2的标准图(JCDPS卡片21-1272)完全吻合.由图1可以看出,溶胶凝胶法制备的SG-TiO2样品的各衍射峰强度都比溶剂热法制备的样品小,说明其晶化程度较低.含Ag 1%和3%的样品未发现有Ag的特征衍射峰,可能是由于Ag的含量太低.在SG-TiO2和Ag含量为5%、10%、15%的样品中有面心立方Ag的特征衍射峰出现在2θ为38.20°、44.40°、64.60°和77.60°处,分别对应于(111)、(200)、(220)和(311)晶面,且38.20°处的衍射峰与锐钛矿型TiO2在37.80°的衍射峰部分重叠.
表1列出了TiO2的晶型、粒径(d)以及比表面积.粒径利用(1)式的Scherrer公式计算得到:
d=Kλ/(βcosθ) (1)式中Scherrer常数K=0.89;入射线波长λ=0.15418 nm;β为衍射峰半高宽;θ为掠射角.由表1可知, SG-TiO2样品平均粒径为86.1 nm,而经过溶剂热处理后的TiO2粒径均在20 nm左右,与商业P-25粒径大小相当.比较图1中的XRD谱可知,Ag衍射峰的强度随负载量的增加而增加,而TiO2衍射峰的强度及半峰宽基本不变,说明Ag并没有进入TiO2晶格,而是以单质Ag的形式存在,Ag修饰对TiO2的晶型和大小并没有太大影响.
2.2 比表面积分析
比表面积是催化剂性能优劣的一个重要指标.由表1中可以看到,溶剂热法制备的的TiO2比表面积约是P-25的两倍,经过Ag修饰的TiO2比表面积都保持在100 m2·g-1以上,其中5%Ag/TiO2样品的比表面积最大,SBET=151.44 m2·g-1,而与其相应的SG-TiO2样品比表面积只有73.25 m2·g-1,说明溶剂热法制备大大提高了样品的比表面积,这有利于TiO2光催化性能的提高.

图1 不同Ag含量x Ag/TiO2,TiO2和SG-TiO2样品的XRD图谱Fig.1 XRD patterns of x Ag/TiO2,TiO2(pure solvothermal TiO2)and SG-TiO2(sol-gel 5%Ag/TiO2)x:molar fraction of Ag
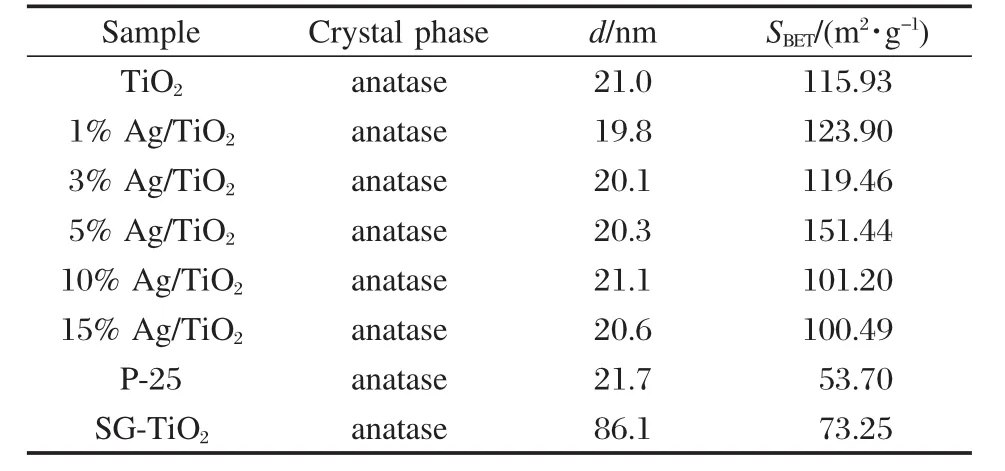
表1 样品的晶相、TiO2平均粒径(d)和比表面积(SBET)Table 1 Crystal phase,average TiO2particle size(d) and specific surface area(SBET)of the samples
2.3 样品的XPS结果
催化剂的表面状态会影响其光催化性能,采用XPS测试对5%Ag/TiO2样品表面各元素的化学形态进行了分析.图2为样品表面Ti 2p、O 1s和Ag 3d的高分辨扫描XPS图谱及分峰拟合谱.

测得的Ti 2p由位于458.7 eV的主峰和464.5 eV的伴峰组成,两峰峰形都呈比较标准的对称形状,分别对应于Ti 2p3/2和Ti 2p1/2的结合能,两峰电子结合能相差5.8 eV,是Ti4+存在的重要判据[23].经过分峰拟合后,发现有少量Ti3+(结合能为457.8 eV)存在,表面Ti3+能抑制电子-空穴对的复合[24],有利于光催化反应的进行.在Ag 3d的XPS谱中Ag 3d5/2峰的结合能为 367.8 eV,Ag 3d3/2峰的结合能为373.8 eV,Ag 3d5/2与Ag 3d3/2的结合能相差6.0 eV,这是金属态Ag的特征[25],即Ag主要以金属态的形式存在,这与XRD结果一致.
如图所示,O 1s的XPS谱为不对称的宽峰,说明样品中的氧物种不是单一的,经过分峰拟合后发现样品中氧主要以晶格氧(O—Ti,530.0 eV)存在,同时还存在表面羟基氧(O—H,531.2 eV),这与文献报道[26-28]的O 1s的结合能数值基本一致.表面羟基氧是光催化中氧化有机物的重要中间体,能够迅速捕获光生空穴,氧化吸附在表面的有机分子,抑制光生电子和空穴的复合[27].
2.4 样品的TEM表征
图3为不同样品的透射电镜图片,可以看到TiO2颗粒均匀且分散,粒径分布较窄,皆在20 nm左右,与XRD结果一致.a图中未发现银颗粒的存在,可能是由于Ag的含量太少;在b图和c图中可以看到少量Ag颗粒附着在TiO2上,大小为2 nm左右;d图和e图中有密集的Ag颗粒沉积在TiO2晶粒上.
图3f为溶胶凝胶法制备的SG-TiO2样品,TiO2粒径主要分布在50-100 nm之间,相对于溶剂热法制备的样品,颗粒大且不均匀.附着在TiO2表面的Ag颗粒大小为8-10 nm,而溶剂热法制备的样品中Ag颗粒仅为2 nm,说明溶剂热法不仅影响了TiO2晶体的大小和分散性,而且有利于形成很小的Ag颗粒.
2.5 UV-Vis光谱
图4为P-25和不同Ag含量Ag/TiO2的UVVis光谱.可以发现,负载Ag使TiO2的吸收带边发生了明显红移,随着Ag负载量的增加,样品对光的吸收不断增加.样品在可见光区500 nm处出现了一个新的的吸收峰,这可能是由纳米Ag颗粒等离子共振吸收(SPR)引起的,相对于文献中报道的纯纳米Ag颗粒的吸收峰(350-450 nm)产生了明显的宽化和红移[29].刘云等[30]也报道了同样的现象,并认为是由于TiO2对红外区的入射光具有较强的散射能力引起的.
2.6 光催化性能测试

图3 Ag/TiO2和SG-TiO2的TEM照片Fig.3 TEM images of Ag/TiO2and SG-TiO2(a)1%Ag/TiO2;(b)3%Ag/TiO2;(c)5%Ag/TiO2;(d)10%Ag/TiO2;(e)15%Ag/TiO2;(f)SG-TiO2
图5为P-25和制备的光催化剂样品在紫外光照射下降解亚甲基蓝的实验结果.发现对不同的样品,ln(C0/C)与降解时间都有较好的线性关系.说明光催化降解亚甲基蓝的反应均为一级反应,其反应模型可表示为ln(C0/C)=kt,其中k为一级反应速率常数,t为反应时间,C0和C分别代表反应时间为0和t时溶液的浓度.由图5和表2可知,在紫外光照射下,无催化剂时,亚甲基蓝基本不发生光降解;溶剂热法制备的纯TiO2光催化活性低于P-25,当催化剂表面负载1%的Ag后,比表面积增大至123.90 m2· g-1,光催化活性提高至接近P-25.由于Ag与TiO2具有不同的费米能级,Ag与TiO2在接触面形成肖特基势垒,TiO2在紫外光的激发下,价带中的电子跃迁至导带,产生电子-空穴对,电子会迅速地移向TiO2表面的Ag颗粒,Ag成了一个电子富集中心,从而降低了电子-空穴对的复合几率,提高了TiO2光催化性能[31].随Ag含量的增加,光催化活性得到进一步提高,当Ag负载量为5%时,比表面积达到最大值,样品表现出最佳的光催化性能.当Ag负载量超过5%时,光催化性能开始下降.这是由于过多的Ag颗粒附着在TiO2晶体表面,不仅影响TiO2对紫外光的吸收,降低电子-空穴对的产量,而且会导致催化剂表面的光生空穴复合几率增加,降低光量子效率[32].在紫外光照下,活性大小顺序为5%Ag/ TiO2>3%Ag/TiO2>SG-TiO2>10%Ag/TiO2>P-25>1% Ag/TiO2>TiO2>15%Ag/TiO2.

图4 P-25和Ag/TiO2的UV-Vis光谱Fig.4 UV-Vis spectra of P-25 and Ag/TiO2

图5 紫外光下不同样品的降解MB动力学曲线Fig.5 Degradation kinetics of MB over different samples under UV light

表2 紫外光和可见光下MB降解的动力学参数Table 2 Kinetics parameters of degradation of MB under UV light and visible light irradiation
图6为各样品在可见光照射下降解亚甲基蓝的实验结果,可以看出P-25和TiO2基本没有可见光活性,不同浓度的Ag负载都使TiO2具有了一定的可见光催化活性,活性大小顺序为5%Ag/TiO2>10% Ag/TiO2>3%Ag/TiO2>SG-TiO2>15%Ag/TiO2>1%Ag/ TiO2.表2详细列出了各样品在在紫外和可见光下的降解常数K和直线拟合相关系数R.
在可见光照射下,染料吸收可见光后被激发并向TiO2的导带注入电子,电子与TiO2表面吸附的O2结合生成活性氧物种,进而降解染料分子[22].在纯TiO2的降解MB反应体系中,由于被激发的电子很快又与亚甲基蓝正离子(MB+)结合,所以在可见光下纯TiO2对亚甲基蓝基本无降解效果.当TiO2表面附着Ag颗粒后,由于肖特基势垒的作用,注入TiO2导带的电子很快向Ag颗粒富集,并和吸附在Ag表面的氧分子发生反应生成活性氧物种,进而进攻溶液中的亚甲基蓝并将其降解,即Ag颗粒抑制了染料激发电子和MB+的复合,从而使TiO2具有一定的可见光催化活性.

图6 可见光下不同样品的降解MB动力学曲线Fig.6 Degradation kinetics of MB over different samples under visible light
催化剂的光催化活性主要取决于其晶体结构、晶化度、晶粒尺寸和比表面积等因素[33].虽然溶剂凝胶法制备的SG-TiO2样品中Ag负载量也为5%,但其光催化活性明显低于溶剂热法制备的5%Ag/ TiO2样品.由于溶剂热法制备的样品晶粒小、比表面积大、晶化程度高,所以具备更高的催化活性.另外,对于负载型Ag/TiO2光催化剂,减小Ag颗粒的大小,也有利于TiO2催化活性提高[31],Ag/TiO2样品中的Ag颗粒仅为2 nm,也是其具有更高催化活性的重要原因.
3 结 论
以乙醇为溶剂,用溶剂热法制备了负载型Ag/ TiO2光催化剂.表面Ag修饰提高了TiO2的比表面积,使其吸收带边扩展至可见光范围.Ag颗粒能有效地抑制电子和空穴的复合,使TiO2的光催化性能大大提高,在紫外光和可见光下,Ag摩尔分数为5%的样品表现出最佳的光催化活性.通过与溶胶凝胶法制备的Ag/TiO2比较研究发现,溶剂热法制备的样品尺寸小、比表面积大、结晶度高,负载Ag颗粒更小,因而表现出更高的光催化活性.
1 Lee,S.H.;Kang,M.;Cho,S.M.;Han,G.Y.;Kim,B.W.;Yoon, K.J.;Chung,C.H.J.Photochem.Photobiol.A,2001,146:121
2 Kim,C.S.;Moon,B.K.;Park,J.H.;Chung,S.T.;Son,S.M. J.Cryst.Growth,2003,254:405
3 Wu,J.J.;Lü,X.J.;Zhang,L.L.;Huang,F.Q.;Xu,F.F.Eur.J. Inorg.Chem.,2009:2789
4 Kolenko,Y.V.;Burukhin,A.A.;Churagulov,B.R.;Oleynikov,N. N.Mater.Lett.,2003,57:1124
5 Fujishima,A.;Rao,T.N.;Tryk,D.A.J.Photochem.Photobiol.CPhotochem.Rev.,2000,1:1
6 Yamashita,H.;Harada,M.;Misaka,J.;Takeuchi,M.;Ikeue,K.; Anpo,M.J.Photochem.Photobiol.A-Chem.,2002,148:257
7 Chen,X.B.;Mao,S.S.Chem.Rev.,2007,107:2891
8 Im,J.S.;Yun,S.M.;Lee,Y.S.J.Colloid Interface Sci.,2009, 336:183
9 Yu,A.M.;Wu,G.J.;Yan,J.J.;Zheng,C.M.;Zhang,F.X.;Yang, Y.L.;Guan,N.J.Chin.J.Catal.,2009,30(2):137 [于爱敏,武光军,严晶晶,郑春明,章福祥,杨雅莉,关乃佳.催化学报, 2009,30(2):137]
10 Zhao,Q.H.;Quan,X.J.;Tan,H.Q.;Sang,X.M.Chin.J.Catal., 2008,29(3):269 [赵清华,全学军,谭怀琴,桑雪梅.催化学报, 2008,29(3):269]
11 Siemon,U.;Bahnemann,D.;Testa,J.J.;Rodriguez,D.;Litter,M. I.;Bruno,N.J.Photochem.Photobiol.A-Chem.,2002,148:247
12 Navio,J.A.;Testa,J.J.;Djedjeian,P.;Padron,J.R.;Rodriguez, D.;Litter,M.I.Appl.Catal.A,1999,178:191
13 Pal,B.;Ikeda,S.;Kominami,H.;Kera,Y.;Ohtani,B.J.Catal., 2003,217:152
14 Kryukova,G.N.;Zenkovets,G.A.;Shutilov,A.A.;Wilde,M.; Gunther,K.;Fassler,D.;Richter,K.Appl.Catal.B,2007,71:169
15 Xia,X.H.;Gao,Y.;Wang,Z.;Jia,Z.J.J.Phys.Chem.Solids, 2008,69:2888
16 Silva,A.M.T.;Silva,C.G.;Drazic,G.;Faria,J.L.Catal.Today, 2009,144:13
17 Su,B.T.;Sun,J.X.;Hu,C.L.;Zhang,X.H.;Fei,P.;Lei,Z.Q. Acta Phys.-Chim.Sin.,2009,25(8):1561 [苏碧桃,孙佳星,胡常林,张小红,费 鹏,雷自强.物理化学学报,2009,25(8): 1561]
18 Cheng,G.;Zhou,X.D.;Li,Y.;Tong,P.R.;Wang,L.M.Chin.J. Catal,2007,28(10):885 [程 刚,周孝德,李 艳,仝攀瑞,王理明.催化学报,2007,28(10):885]
19 Kandiel,T.A.;Dillert,R.;Bahnemann,D.W.Photochem. Photobiol.Sci.,2009,8:683
20 Jiang,D.;Xu,Y.;Hou,B.;Wu,D.;Sun,Y.H.Acta Chim.Sin., 2007,65(14):1289 [姜 东,徐 耀,侯 博,吴 东,孙予罕.化学学报,2007,65(14):1289]
21 Binitha,N.N.;Yaakob,Z.;Reshmi,M.R.;Sugunan,S.;Ambili,V. K.;Zetty,A.A.Catal.Today,2009,147S:S76
22 You,X.F.;Chen,F.;Zhang,J.L.;Huang,J.Z.;Zhang,L.Z.Chin. J.Catal.,2006,27(3):270 [尤先锋,陈 锋,张金龙,黄家桢,张利中.催化学报,2006,27(3):270]
23 Mei,F.;Liu,C.;Zhang,L.;Ren,F.;Zhou,L.;Zhao,W.K.;Fang, Y.L.J.Cryst.Growth,2006,292:87
24 Li,F.B.;Li,X.Z.;Hou,M.F.Appl.Catal.B,2004,48:185
25 Zhang,H.J.;Chen,G.H.Environ.Sci.Technol.,2009,43:2905
26 Kuo,Y.L.;Chen,H.W.;Ku,Y.Thin Solid Films,2007,515: 3461
27 Wei,F.Y.;Ni,L.S.Chin.J.Catal.,2007,28(10):905 [魏凤玉,倪良锁.催化学报,2007,28(10):905]
28 Arabatzis,I.M.;Stergiopoulos,T.;Bernard,M.C.;Labou,D.; Neophytides,S.G.;Falaras,P.Appl.Catal.B,2003,42:187
29 Wiley,B.;Sun,Y.;Mayers,B.;Xia,Y.Chem.Eur.J.,2005,11: 454
30 Liu,Y.;Liu,C.Y.;Zhang,Z.Y.Acta Chim.Sin.,2000,58(4):397 [刘 云,刘春艳,张志颖.化学学报,2000,58(4):397]
31 Shan,Z.C.;Wu,J.J.;Xu,F.F.;Huang,F.Q.;Ding,H.M.J.Phys. Chem.C,2008,112:15423
32 You,X.F.;Chen,F.;Zhang,J.L.;Anpo,M.Catal.Lett.,2005, 102:247
33 Xiao,Y.;Dang,L.Q.;An,L.Z.;Bai,S.Y.;Lei,Z.B.Chin.J. Catal.,2008,29(1):31 [肖 义,党利琴,安丽珍,白士英,雷志斌.催化学报,2008,29(1):31]
March 8,2010;Revised:April 19,2010;Published on Web:June 18,2010.
Solvothermal Preparation of Ag/TiO2Nanoparticles and Their Photocatalytic Activity
XU Ping-Chang1LIU Yang1WEI Jian-Hong1,2,*XIONG Rui1PAN Chun-Xu1SHI Jing1
(1Key Laboratory of Artificial Micro-and Nano-Structures,Ministry of Education,School of Physics Science and Technology, Wuhan University,Wuhan 430072,P.R.China;2Key Laboratory of Low Dimensional Materials and Application Technology (Xiangtan University),Ministry of Education,Xiangtan 411105,Hunan Province,P.R.China)
Visible-light photoactive Ag/TiO2catalysts were successfully prepared by a solvothermal method.The samples were characterized by X-ray diffraction(XRD),N2adsorption-desorption isotherm(BET),transmission electron microscopy(TEM),X-ray photoelectron spectroscopy(XPS),and UV-visible(UV-Vis)spectroscopy.The photodegradation of methylene blue(MB)solution was used to evaluate the photocatalytic activity of the catalyst under UV and visible light irradiation(λ>400 nm).XRD results showed that the TiO2was in the pure anatase phase.Ag nanoparticles were loaded onto the TiO2nanoparticle surface and this had little influence on the crystal phase and the particle size of TiO2.The specific surface area of the samples was far higher than that for the samples prepared by the sol-gel method and the sample with Ag molar fraction of 5%had the highest value of 151.44 m2·g-1.The absorption spectrum of the Ag-modified TiO2increased greatly and the adsorption edge was extended into the visible region.The photodegradation of MB solution followed a pseudo-first-order kinetic expression.The photocatalytic activities of the Ag/TiO2composites prepared by the solvothermal method were remarkably higher than those prepared by the sol-gel method.Under UV or visible light irradiation,the optimal photoactivity was obtained for the sample with a Ag molar fraction of 5%.
Titania;Silver-modified;Solvothermal method;Sol-gel method;Methylene blue; Photocatalysis
[Article] www.whxb.pku.edu.cn
*Corresponding author.Email:jhwei@whu.edu.cn;Tel:+86-10-68754613.
The project was supported by the National Key Basic Research Program of China(973)(2009CB939704),National Natural Science Foundation of China(10974148)and the Open Project Program of Low Dimensional Materials and Application Technology(Xiangtan University),Ministry of Education of China(DWKF0806).
国家重点基础研究发展规划项目(973)(2009CB939704),国家自然科学基金(10974148)和低维材料与技术教育部重点实验室(湘潭大学)开放基金(DWKF0806)资助
O643

