环己醇硝酸氧化法制备己二酸的实验改良研究
冯欣 彭彩云 方渡 吴科
环己醇硝酸氧化法制备己二酸的实验改良研究
冯欣 彭彩云 方渡 吴科
本文对由环己醇制备己二酸的传统实验方法进行了改良,用 79%硝酸替代高锰酸钾作氧化剂,以硝酸、环己醇 8:1的摩尔投料比,在 80℃水浴下搅拌氧化 30m in,使制备操作时间由 5 h缩短至 2 h,己二酸产率由 30%提高至 87.67%,避免了高锰酸钾法中大量废渣后处理的麻烦,在一定程度上减小了制备实验对环境的污染,符合绿色化学设计的要求。
环己醇;己二酸;改良;摩尔投料比;绿色化学
1 实验目的
己二酸作为重要的合成原料,在工业和科研中都有很大的实用价值。由环己醇氧化制备己二酸则是国内高等院校本科学生常设的有机化学实验项目。然而,各院校实施的实验方案却不尽相同,通常采用传统的碱性高锰酸钾氧化剂氧化环己醇的方法来制备己二酸:
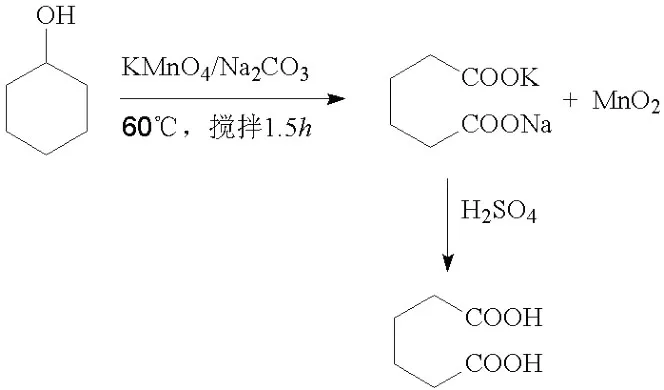
根据电子得失法配平的氧化反应方程式为 (1):

该实验方法有其不尽合理之处:其一,氧化反应要求高锰酸钾固体分批小量地加入,必须控制反应温度在 50℃以下。但在此温度下反应很慢,随着高锰酸钾加入量的增多和氧化剂的沉积,反应会迅速加快,瞬间温度骤升,常导致反应物冲出反应器。若要有效的避免“冲料”,需通过缓慢延时的方法少量多次加入高锰酸钾以控制反应温度。因此,单元实验时间需要 4~5 h[1],不便于学生在一个单元时间内完成实验。
其二,由于环己醇与高锰酸钾水溶液的互不相溶性,导致该实验过程为非均相反应过程,反应产率也不理想 (平均产率约 10%~15%)。学生的实验结果很不稳定 (有的学生甚至拿不到预期的产品),更为严重的是该实验方案产生大量二氧化锰沉淀,废渣的后处理较麻烦,后期搅拌因粘度太大抑制了氧化反应的充分进行,产品的吸附损失难以避免,没有反应完全的 KM nO4原料对产品的滤液还会产生色泽干扰,大量M nO2固体滤渣的废弃也会造成对环境的污染和资源的浪费。
为了提高反应收率,曾采用添加相转移催化剂 (三乙基苄基氯化铵,TEBAC)的改进方案,但催化效率依然不太高(平均产率约 25%~30%)。
诞生于上世纪 90年代的绿色化学,其目标是研究和寻找能充分利用的无毒害原材料和试剂,最大程度地节约能源,在化学反应和化学制备的各个环节都实现净化和无污染的途径。它的最大特点是从化学过程的源头就采用一切防止污染的科学手段,从而实现过程和终端的零排放和零污染。绿色化学主张在通过化学转换获取新物质的过程中充分利用每个原子,即“原子经济性”。此过程既能充分利用资源,又能从源头防止污染[2-4]。
在有机化学实验课教学中,可从原料或试剂的选择、实验方法、产率、原子利用率这四种因素进行创新和改良,把绿色化学原理和理念引入实验教学中。对传统实验进行科学的改进,在保证教学效果的前提下,尽可能减少有毒有害物质的使用和产生。[5]
2 实验原理
根据电子得失法配平的氧化反应方程式为 (2),环己醇、浓硝酸和己二酸的相关物理常数列举如下:
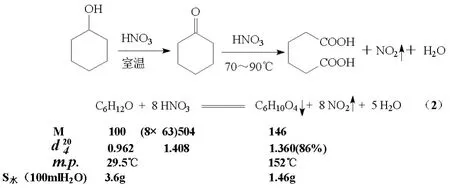
3 仪器设备
集热式恒温磁力搅拌器一台,水循环真空泵一台,X4型显微熔点测定仪一台,磁力搅拌子一枚,24#100m l三口烧瓶一个,24#球形冷凝管一支,24#40m l恒压滴液漏斗一个,100 m l和 10m l量筒各一个,24#弯颈导气管一个,500m l烧杯 1个,24#空心塞 2个,冷凝用橡胶管 2根,导气用乳胶管 (1M)一根,短颈玻璃漏斗一个,砂芯抽滤漏斗一个。
4 试剂与药品
78%(W/V)硝酸 A.R 24m l,79%(W/V)硝酸 A.R 40 m l,环己醇 A.R 5.3m l。
5 实验步骤
在 100m l(或 250m l)干燥的三口烧瓶中加入 Vm l硝酸和磁力搅拌子一枚,将烧瓶固定在集热式恒温磁力搅拌器平台上,在烧瓶中口安装回流冷凝管和橡胶冷凝水管 (开启小量冷凝水),在冷凝管上口连接一个弯颈导气管,导气管口连接一根约 1米长的乳胶管,在乳胶管的另一端再连接一个短颈玻璃漏斗,在 500m l烧杯中盛入约 1/2的冷水,将其置于实验台桌面,并将连有乳胶管的玻璃漏斗浸于桌面烧杯的水中,调节桌面烧杯的位置,使玻璃漏斗底口半浸于烧杯的水面)。
将搅拌器控温棒插入搅拌器内壁,并将搅拌器温控器调节至“0℃,搅拌器控速旋钮调节至最低档。开启搅拌器电源开关,使烧瓶内搅拌子缓缓旋转,以形成液面涡流为宜。
在 40m l(或 125m l)恒压滴液漏斗中加入 5.3m l环己醇(约 0.05mo l。注意:量取硝酸的量筒不能同时量取环己醇!),在称量过环己醇的 10m l量筒中再加入 1~2m l冷水,封闭振摇洗涤量筒后一并转入恒压滴液漏斗,将恒压滴液漏斗小心振摇均匀后插入三口烧瓶的侧口,用空心塞塞紧滴液漏斗上口,将另一烧瓶侧口用 24#空心塞塞紧。
开启实验室通风抽气设备,小心开启恒压滴液漏斗的旋钮,以 6~10滴/m in的速度缓慢向反应烧瓶中滴加环己醇(速度过快,会因反应放热过于猛烈而使反应液冲出,即冲料!)。约 20~25m in内将环己醇滴完。此时反应烧瓶中棕色二氧化氮气体逐渐增多并充满整个回流冷凝管内壁和导气系统。
环己醇滴加完毕后,在维持搅拌下,将搅拌温控器调节至指定加热的温度,当搅拌器温度达到指定温度后,继续搅拌 30m in。其间,棕色气体由浓转淡逐渐减少。
反应结束后,关闭搅拌器电源开关,移开气体吸收烧杯,关闭冷凝水,按序拆除导气吸收装置和回流装置。将反应烧瓶脱离水浴稍冷,即可看到反应液浑浊并出现白色沉淀,再将烧瓶置冰水中冷却 20m in以上,抽滤,用母液洗涤烧瓶和滤饼数次,得白色己二酸粗品,将粗品置 85℃烘箱鼓风干燥20m in,称重 (W 1),粗产品约 5.5~7 g,产率约 75%~96%。
也可将粗品重结晶精制:将已称重粗品转入 100m l锥形瓶中,加入适量冷水 (4m l水 /g粗品),将锥形瓶置于酒精灯(或电炉)上振摇加热溶解 3~5m in,待溶液透明后 (可趁热抽滤一次,此时,布氏漏斗、砂芯抽滤漏斗和另一个转移用盛液锥形烧瓶均需在 85℃烘箱中预热),将盛有透明热熔液的锥形瓶放于桌面静置 20m in,此时若有晶体部分析出,可将锥形瓶转置于冰水中深度冷却 20m in以上。用砂芯抽滤漏斗再次抽滤、干燥,称重 (W2),测熔点,产品约 4.5~6.4 g,熔点 150℃~153℃(温度未校正)。第二次计算产率。产率约 60%~88%。
产率计算公式:
己二酸产率%=W/7.30×100%
6 实验记录
实验数据记录见表 1、表 2。

表 1 6:1(摩尔投料比)硝酸在不同温度下的氧化反应产率
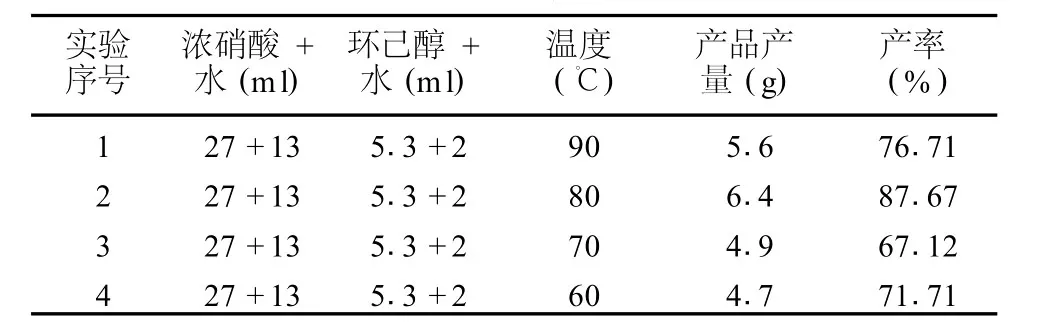
表 2 8:1(摩尔投料比)硝酸在不同温度下的氧化反应产率
7 实验结论
7.1 我们在确立环己醇用量为 5.3m l,(0.05mo l)、氧化反应时间为 30m in的前提下,选择了不同硝酸用量下温度对氧化反应产率的影响。78%(W/V)硝酸 24 m l的用量 (16 m l浓硝酸 +8m l水)是参照国内近期研究文献而选择的,由于硝酸氧化剂投料量与环己醇原料投料量的实际摩尔比不足6:1,即使在较高温度下 (90℃)反应产率也没有超过 70%。79%(W/V)硝酸 40m l的用量 (27m l浓硝酸 +13 m l水 )是我们通过氧化还原电子得失配平相应氧化反应方程式而确立的,按照环己醇与硝酸的氧化反应方程式,硝酸氧化剂投料量与环己醇原料投料量的理论摩尔比应为 8:1。国内近期研究文献用低于理论摩尔比的硝酸氧化环己醇肯定难以得不到理想的实验结果。我们用足量的浓硝酸 (79%硝酸 40 m l)考察了不同温度下的氧化反应产率,其产率与反应温度呈现正态分布状况。对比表一和表二可以看出,相同温度下8:1投料的反应产率都明显高于 6:1投料方式。我们认为,以硝酸氧化环己醇为己二酸的研究,应在硝酸与环己醇摩尔投料比 8:1的基础上展开。
7.2 经过在 60℃、70℃、80℃、90℃四个温度区段下的平行实验我们得出此反应的最适反应温度为 80℃。80℃以上,硝酸氧化环己醇的产率不再呈现上升趋势。在该温度下其产率是否随反应时间延长而提高还有待进一步的研究。
7.3 此反应的反应时间仅需 90 m in,即便考虑到实验的前期准备 (如综合实验装置的搭建与浓硝酸的配制等)和每名同学的实际操作能力,也完全可以保证学生在一个单元实验时间(3~4 h)内完成本实验并获得满意的实验结果。
7.4 建议在 40m l79%(W/V)硝酸浓度和 80℃的温度下开设本实验,产率可达 80%以上。
[1] 李继忠,石向林.用高锰酸钾氧化环己醇制备己二酸方法的改进延安大学学报(自然科学版),1997,16(4):89-90.
[2] 王春.化学新课程教学中实施绿色化学教育的策略探讨.教改实践与探索,2009(7):7-8.
[3] 方渡,等.药物合成-反应与设计吉林科学技术出社,2005.
[4] 潘一,等.绿色化学的研究现状及进展.化学工业与工程技术,2005,26(5):26-29.
[5] 毕坤鹏,尹韶青,唐娜.高校化学教学中绿色化学教育的实践与探索.中国科教创新导刊,2009(13):42-43.
In this paper,p reparation of ad ip ic acid from cyclohexano l the traditional 1experim en tal m ethod has been imp roved,w ith 79%nitric acid substitu tion of po tassium perm anganate as oxidan t,to nitric acid,cyc lohexano l8:1mo lar feed ratio,under stirring at80℃water bath Oxidation of30m inutes,so p repare to sho rten operating tim e from 5 h to 2 h,adip ic acid p roduction rate from 30%to 87.67%of the po tassium perm anganatem ethod to avoid post-p rocessing large quantitiesofwaste residue of troub le,to a certain extent,reduced the p reparation of experim ent on the environment po llution,in line w ith the design requirem ents of green chem istry.
Cyc lohexano l;A dip ic acid;Im p rovem en t;M o lar feed ratio;Green chem istry
410208长沙,湖南中医药大学
从绿色化学的角度出发,设计了用硝酸氧化剂氧化环己醇制备己二酸的改良实验方案,即将产生废渣沉淀、后处理麻烦的高锰酸钾碱性氧化法转变为仅产生二氧化氮气体、后处理简便的硝酸酸性氧化法,此法的优越性在于,酸型产品析出速度快,后处理简捷,整个制备操作的实验时间可由原来的 4~5 h缩短至 1~2 h,在硝酸摩尔用量充分的前提下,产率远远高于传统氧化法。实验研究证明:当硝酸、环己醇摩尔投料比为 8:1时,在 80℃水浴中搅拌反应 30m in,其产率可达 87.67%(高锰酸钾法的最高产率在 30%以下)。

