富勒醇C84(OH)x的合成及Gd-DTPA掺杂体系纵向弛豫时间的测量
何 睿,陈亮文,黄志坚
(杭州师范大学 生物医药与健康研究中心,浙江 杭州 310012)
医学影像领域应用最广泛的磁共振成像(MRI)造影剂一般都是顺磁性物质,尤其是含钆(Gd)的小分子螯合物[1](如:Gd-DTPA,钆的二乙三胺五乙酸螯合物),主要用于改善MRI图像质量.近年来,随着纳米材料科学尤其是富勒烯化学的发展,顺磁性金属富勒烯类MRI造影剂纳入研究人员的视野,并逐步成为新型MRI造影剂的研发新热点.如Shinohara等人的研究表明金属富勒醇Gd@C82(OH)40纵向弛豫率(R1)最高达到Gd-DTPA的20倍[2].
金属富勒烯类造影剂具有远高于Gd-DTPA类螯合物R1值的原因之一在于:其碳笼外接大量亲水性官能团(如-OH),可吸引众多水分子环绕并团聚形成纳米颗粒,从而减慢了体系旋转运动,即其旋转相关时间(τR)增加进而导致R1值的提高[3].然而,即便采用备受青睐、产率最高的电弧放电法合成金属富勒烯,其产率也只有1/105~1/106,且目前文献报道其最高产量仅达到毫克量级.此外,其还需采用费时费力的高效液相色谱法(HPLC)进行分离纯化.这些弱点大大局限了金属富勒烯作为MRI造影剂的应用研究.
空心富勒烯的合成产率比金属富勒烯的高1 000倍以上[4],相对于金属富勒烯其来源更容易,且二者水溶性衍生物具备相似的团聚性质,因而该研究组另辟蹊径,尝试利用空心富勒烯改造传统MRI造影剂以提高其R1值.该文利用电弧法合成碳炱中碳笼及分子量大小比较接近Gd@C82的副产物C84,制备新型富勒醇,并调查将其掺杂于Gd-DTPA溶液后体系增强水质子纵向弛豫速率的能力.
1 实验部分
1.1 试剂与分析仪器
所用试剂β-环糊精、四丁基氢氧化铵(TBAH)、双氧水(H2O2)、甲苯、氢氧化钠(NaOH)均为分析纯,Gd-DTPA为临床使用的商品名Magnevist的医用药品.质谱表征在BIFLEX Ⅲ型激光解吸附飞行时间质谱仪(MALDI-TOF MS)上完成,以337 nm N2分子激光解吸样品,以反射方式收集负离子模式信号.红外测量在Nicolet magna-IR750型红外光谱仪上完成,KBr压片,波长范围4 000~400 cm-1.元素分析在Flash EA1112型元素分析仪上完成.
1.2 HPLC分离纯化C84
实验所需的富勒烯C84来源于自制的电弧法合成Gd@C82的碳炱提取物[5].采用20 mm×250 mm 5PBB制备型色谱柱在LC-908-C60型HPLC上分离纯化C84.以甲苯作流动相,流速为15 ml/min,每次注入碳炱提取物的甲苯浓溶液体积为30 ml,检测波长335 nm,收集49~58 min流出液,浓缩待用.
1.3 C84(OH)x的合成
富勒醇C84(OH)x的合成按下述方法进行[2,6-7]:将100 ml含20 mg C84的甲苯溶液与50%NaOH溶液混合加入250 ml烧杯中(C84与NaOH的质量比为1∶50),加入0.5 ml 40%的TBAH作催化剂,再加几滴H2O2,充分接触空气,磁力搅拌24 h,烧杯壁及底部产生大量棕色附着物,加入适量去离子水继续搅拌24 h,分液,水相去除溶剂,残余物以甲醇洗涤,得粗产品,重溶于去离子水,滤膜过滤,利用葡聚糖凝胶(Sephadex G-25)层析法继续纯化,pH为7的去离子水作流动相,收集pH为6~7的色带,冷冻干燥,得纯产品.
1.4 纵向弛豫时间测量
样品准备:以pH为7的去离子水将Gd-DTPA和C84(OH)x分别配成1.0 mmol/L的母液,再混合二者,配置Gd-DTPA浓度固定为0.1 mmol/L而C84(OH)x浓度依次为0,0.05,0.1,0.15,0.2,0.25和0.3 mmol/L的一系列样品.进行对照实验时,将上述Gd-DTPA溶液中掺杂C84(OH)x体系改换为掺杂β-环糊精体系的一系列同浓度样品.所有样品各取0.5 ml分别转移到直径5 mm的核磁试管,待测.
MRI实验:在4.7 T动物成像仪(Bruker Biospeec 47/30)上进行.为测量每个样品的水质子纵向弛豫时间(T1),一系列充入样品的核磁试管捆扎成束,采用反转恢复自旋回波成像序列扫描,序列参数为:重复时间10 s,回波时间13.5 ms,成像面积3.5 cm×3.5 cm,片厚1.0 mm,数据矩阵64×64,在0.05~15 s之间选择一系列合适的TI值.采集的MRI原始数据利用Bruker扫描仪上自带的图像处理与分析软件PARAVISION进行处理,采用感兴趣区(ROI)分析方法,所有样品的ROI区域选择为面积相同的圆形,并分别记录相应信号的平均强度.将ROI信号的平均强度随TI值的变化通过三参数单指数函数拟合从而获得所有待测样品的T1.拟合过程中个别远远偏离所拟合直线的数据点将被剔除再重新拟合,拟合的每组数据其数据点间的相关系数(r)均大于0.99.
2 结果与讨论
2.1 分离与合成
碳炱提取物进行HPLC分离后收集的49~58 min流出组分(色谱图示于图1),经MALDI-TOF MS鉴定为C84.为避免混入Gd@C82,该组分可经5PBB柱进行二次分离,选取窄于该峰位置的时间范围进行收集,最终获得纯净的C84.结合色谱和质谱结果判断实验制备的C84纯度高于99.0%.电弧法制备Gd@C82的碳炱中含有多种空心富勒烯(最丰富的为C60,C70,C84等)和多种含Gd的金属富勒烯(Gd@C82,Gd2@C80,Gd@C80等).采用高温高压溶剂提取法可选择性从碳炱中有效提取出Gd@C82.同时,该提取物中仍含C60,C70,C84等副产物,利用HPLC可将上述空心及金属富勒烯相互分离并纯化.
标题化合物水溶液的MALDI-TOF MS表征图谱示于图2,其中质荷比(m/z)为1 008处离子峰归属于C84碎片.这与文献报道的结果是一致的.一般认为,富勒烯水溶性衍生物笼外所键联的亲水性官能团在MALDI-TOF MS实验过程中因激光解吸附作用而从碳笼上被剥离,从而导致质谱中出现富勒烯碎片的离子峰而不会出现母体分子的分子离子峰[7-9].由于C84本身并不溶于水相,上述谱图中出现的m/z为1 008的离子峰,应归属于该化合物分子在质谱实验过程中外接官能团从碳笼上被剥离而得到的富勒烯C84碎片的离子峰.由此可判断该化合物为富勒烯C84的水溶性衍生物.

图1 碳炱提取物经5PBB柱HPC分离后的色谱图Fig. 1 HPLC chromatogram for C84 separated by 5PBB columns

图2 富勒醇C84(OH)x水溶液的激光解吸附负离子模式飞行时间质谱图Fig. 2 A negative-ion MALDI-TOF mass spectrum of C84(OH)x
标题化合物固体粉末的红外吸收图谱示于图3,图中虚线为便于观察峰位置而添加.其中3 430 cm-1附近较宽的峰属于O—H的伸缩振动.1 630 cm-1处附近的峰属于C=C伸缩振动,由于反应中未引入除C84外其它含碳的物质,这一振动峰应归属于富勒烯碳笼.1 390 cm-1和1 115 cm-1处附近的吸收峰分别属于O—H的弯曲振动和C—O的伸缩振动,这意味着该化合物中存在羟基官能团.红外表征结果进一步证实标题化合物是富勒烯C84的羟基衍生物.
笔者发现C84与NaOH的反应若能顺利进行,氧化剂的存在是必不可少的.当反应物在惰性气体氛围下长时间搅拌,溶液几乎不变色,意味着反应几乎没发生.当反应物暴露在空气中搅拌8 h后溶液明显褪色,说明空气中O2参与了反应.当暴露在空气中同时又加入H2O2后0.5 h内溶液就完全褪色,说明H2O2更能促进此反应的进行,此即笔者对TBAH相转移催化法合成富勒醇的改进.笔者推测该反应机理应涉及到氧化过程,由于C84碳笼上具有反应活性的C=C双键数目众多,一个C84分子可能同时受到多个氧化剂分子攻击,得到多环氧化中间体C84(O)x/2,随后接受H2O/OH-的进攻,环氧水解,最终生成C84(OH)x.
综合以上反应机理以及谱学表征可以判断所合成化合物是C84多羟基化的水溶性衍生物,其分子表达式C84(OH)x中x值经元素分析确定为24.
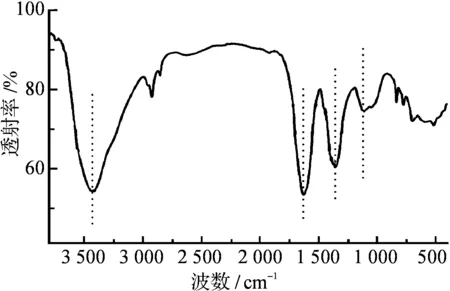
图3 C84(OH)x固体粉末的红外吸收光谱图Fig. 3 An FT-IR spectrum of C84(OH)x
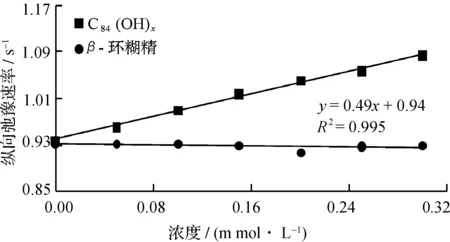
图4 Gd-DTPA掺杂体系水质子纵向弛豫速率(1/T1)随C84(OH)x/β-环糊精的浓度变化趋势图Fig. 4 Proton relaxation rate (1/T1) of water in doped Gd-DTPA solution as functions of C84(OH)x/β-cyclodextrin concentrations
2.2 MRI实验
Gd-DTPA溶液中掺杂富勒醇C84(OH)x及β-环糊精体系水质子T1测量的实验结果示于图4.由图4可知Gd-DTPA掺杂富勒醇C84(OH)x体系的纵向弛豫速率(1/T1)伴随体系中C84(OH)x的浓度增加而升高.显然,Gd-DTPA掺杂富勒醇能进一步缩短体系弛豫时间,即体系的R1值将伴随体系中掺杂富勒醇而升高;但是,掺杂β-环糊精体系的1/T1却不依赖β-环糊精浓度的改变而变化,也即掺杂β-环糊精后体系的R1值不变.C84(OH)x及β-环糊精二者分子量相近,且均为多羟基化合物,但Gd-DTPA溶液中分别掺杂二者后造成体系R1值变化互不相同.其原因在于:β-环糊精作为糖类化合物,在水溶液中不产生聚集体,仅以单分子形式存在,无法积聚体系中的Gd-DTPA,也就无法改变体系的R1值.然而,C84(OH)x具备纳米材料的特性,即众多的球形富勒醇分子间可通过非共价键作用方式团聚成纳米颗粒,当其掺杂于Gd-DTPA后,组成纳米颗粒的富勒醇碳笼表面大量存在的羟基官能团可通过氢键与Gd-DTPA形成相互作用,同时,该纳米颗粒亦可通过物理吸附及包裹大量Gd-DTPA于其表面和内部空隙之中,由此形成Gd-DTPA掺杂的顺磁性纳米颗粒可使体系τR值增加而导致R1值提升.
3 结 论
通过改进的相转移催化剂作用下碱性反应法成功合成新型富勒醇C84(OH)x,并利用MS、IR和元素分析确认其结构.通过MRI实验测量水质子纵向弛豫时间表明,新合成的C84(OH)x掺杂到Gd-DTPA中能够提高体系的R1值.上述实验现象归咎于顺磁性的Gd-DTPA与C84(OH)x纳米颗粒间存在相互作用,实现了利用碳纳米材料对传统MRI造影剂的改造,这为探寻新型高弛豫率MRI造影剂提供了一条全新的研究思路.
[1] Toth E, Helm L, Merbach A E. Relaxivity of MRI contrast agents[J]. Top Curr Chem,2002,221:61-100.
[2] Mikawa M, Kato H, Okumura M,etal. Paramagnetic water-soluble metallofullerenes having the highest relaxivity for MRI contrast agents[J]. Bioconjug Chem,2001,12(4):510-514.
[3] Kato H, Kanazawa Y, Okumura M,etal. Lanthanoid endohedral metallofullerenols for MRI contrast agents[J]. J Am Chem Soc,2003,125(14):4391-4397.
[4] Wilson L J. Medical applications of fullerenes and metallofullerenes[J]. Interface,1999,8(4):24-28.
[5] 何睿.金属富勒烯衍生物的合成、表征及作为磁共振成像造影剂的应用研究[D].武汉:中国科学院武汉物理与数学研究所,2008.
[6] Tang Jun, Xing Gengmei, Yuan Hui,etal. Tuning electronic properties of metallic atom in bondage to a nanospace[J]. J Phys Chem B,2005,109(18):8779-8785.
[7] Xing Gengmei, Zhang Jun, Zhao Yuliang,etal. Influences of structural properties on stability of fullerenols[J]. J Phys Chem B,2004,108(31):11473-11479.
[8] Sun Dayong, Huang Houjin, Yang Shihe,etal. Synthesis and characterization of a water-soluble endohedral metallofullerol[J]. Chemistry of Materials,1999,11(4):1003-1006.
[9] Shu Chunying, Gan Lihua, Wang Chunru,etal. Synthesis and characterization of a new water-soluble endohedral metallofullerene for MRI contrast agents[J]. Carbon,2006,44(3):496-500.

