酶解大蒜渣制备果葡糖浆*
黄菁,张宁,张永韬,黄雪松
(暨南大学食品科学与工程系,广东广州,510632)
酶解大蒜渣制备果葡糖浆*
黄菁,张宁,张永韬,黄雪松
(暨南大学食品科学与工程系,广东广州,510632)
采用2种商品蔗糖酶水解大蒜渣制备果葡糖浆,经过单因素试验以及正交试验确定了Sigma公司的蔗糖酶水解率较高。其最适酶解条件:pH值为4.8,温度为45℃,底物浓度为8mg/mL,加酶量为210 U/mL,酶解时间为12 h。在此酶解条件下,蔗糖酶的水解率达到80%,经离子色谱-积分脉冲安培检测法分析,酶解产物以果糖和葡萄糖为主。
蔗糖酶,大蒜渣,果葡糖浆
果葡糖浆是以果糖与葡萄糖为主要组分的健康型糖源,其中果糖含量较高。果葡糖浆的生产主要是以玉米淀粉通过淀粉酶,葡萄糖糖异构酶两步法生产[16],该方法纯化工艺复杂,果糖含量不高。果聚糖在无机酸或酶的作用下可水解成为果葡糖浆,因此通过水解一些含果聚糖的天然原料如菊粉制备果葡糖浆成为了一条新的途径。其中,通过酸法水解天然果聚糖原料制备果葡糖浆,果糖不稳定、风味差、色泽深,已逐渐被淘汰。而酶法水解则条件温和,产量高,副产物少,逐渐成为研究的热点[16]。
大蒜(Allium sativum)营养丰富,其中75%以上的干物质由碳水化合物组成,主要是大蒜果聚糖[1]。其果聚糖的果糖与葡萄糖比例约为15∶1,是制备果葡糖浆的理想原料。本文采用商品蔗糖酶制剂降解大蒜渣制备果葡糖浆,拟为生产质高,价廉的果葡糖浆开发新原料。
1 材料与方法
1.1 材料与设备
市售大蒜;蔗糖酶,Sigma和裕立宝生物公司;Na2HPO4、柠檬酸、NaOH、酒石酸钾钠、浓 H2SO4、苯酚、Na2SO3(均为分析纯),天津市福晨化工厂;3,5-二硝基水杨酸,化学纯,国药集团化学试剂厂;葡萄糖、果糖、木糖、阿拉伯糖、半乳糖、鼠李糖,均为Sigma色谱纯;蔗果三糖、蔗果四糖、蔗果五糖,均为WAKO(日本)色谱纯。
HH-4恒温水浴锅、SHA-B水浴恒温振荡器,江苏金坛市宏华仪器厂;KDC-1044低速离心机,科大创新股份有限公司中佳分公司;721分光光度计,上海精密科学仪器有限公司;DHG-9145A型电热恒温鼓风干燥箱,上海一恒科学仪器有限公司;DIONEX-2500离子色谱仪,配有GP50四元梯度泵,AS50自动进样器,美国戴安。
1.2 实验方法
1.2.1 大蒜渣预处理
将市售大蒜捣碎,用蒸馏水提取大蒜渣中的多糖,固液比 =1∶2,95℃下煮沸 40 min[3],再保温 1 h,纱布过滤,经3 500 r/min离心20 min,上清液即为大蒜果聚糖液[3]。分别测定其中总糖和还原糖的含量。
1.2.2 蔗糖酶水解大蒜多糖
2种蔗糖酶分别用Na2HPO4-柠檬酸缓冲液进行适当的稀释,加入至大蒜果聚糖液中,调至pH为5.0,温度保持在50℃,酶解12 h,得出样品,分别测其总糖含量和还原糖含量,计算酶解得率。2种蔗糖酶均用酶活浓度、底物浓度、温度、pH值以及时间为单因素试验,再对较高提取率的酶选出4种差异因素做4因素3水平的正交试验,测定最终蔗糖酶的水解率。
1.2.3 蔗糖酶酶活的测定
用pH值为4.6的乙酸钠-醋酸缓冲液对2种蔗糖酶进行适当的稀释,取1mL酶液加入4mL蔗糖液(浓度为0.05mol/L),40℃准确反应10min,加入1mL 1mol/L的NaOH摇匀,终止酶促反应[2]。测定反应液中的还原糖含量,计算酶活。得出初始Sigma蔗糖酶的酶活为1 320 U/mL,裕立宝蔗糖酶的酶活为1 500 U/mL。
1.2.4 水解液中总糖的测定
苯酚-硫酸法[4]。
1.2.5 水解液中还原糖的测定
3,5-二硝基水杨酸法[5]。
1.2.6 色谱条件
1.2.6.1 单糖检测的色谱条件
分析柱:CarboPac PA-10(4 mm ×250 mm),保护柱:CarboPac PA-10G(4 mm×50 mm);流动相:3%250 mmol NaOH;体积流量:0.20mL/min;进样体积:25μL;柱温:30℃;检测器:ED50A安培检测器(金工作电极,Ag-AgCl参比电极,钛对电极)。单糖标准品混合液的色谱图如图1。

图1 单糖标准品混合液的色谱图
1.2.6.2 低聚果糖检测的色谱条件
分析柱:CarboPac PA-100(4 mm×250 mm),保护柱:CarboPac PA-100G(4 mm×50 mm);体积流量:0.20mL/min;进样体积:25μL;柱温:30℃;检测器:ED50A安培检测器(金工作电极,Ag-AgCl参比电极,钛对电极)。流动相的比例如表1,低聚果糖标准品混合液的色谱图如图2。

图2 低聚果糖标准品混合液的色谱图(混合液由1mg/mL的蔗果三糖、蔗果四糖、蔗果五糖以1∶1∶1的体积比混合而成)

表1 流动相的比例设置
1.2.7 蔗糖酶水解率的计算

式中:m1为水解后还原糖的含量(mg);m0为水解前还原糖的含量(mg);m为样品液中总糖的含量(mg)。
2 结果与讨论
2.1 蔗糖酶水解条件
2.1.1 温度对蔗糖酶水解率的影响
分别在 35、40、45、50、55、60℃下,pH 值为 5.0,酶解12 h,水解率如图3所示。

图3 温度对水解率的影响
由图3可以看出,当温度由35℃升至45℃时,2种蔗糖酶的水解率都升高,50℃时,蔗糖酶的水解率达到最高,这是因为随着温度的升高,反应速率加快[15]。但由50℃升至60℃时,水解率骤降,这可能是由于温度过高,导致蔗糖酶本身的热稳定性下降[6],从而使得蔗糖酶的活性发生变化,导致水解率降低。因此,实验用2种酶的最适温度都在45~50℃。
2.1.2 pH值对蔗糖酶水解率的影响
分别研究 pH 值 3.0、4.0、4.4、5.0、6.0、7.0 下,温度为50℃,水解12 h的水解结果(如图4)。
由图4可知,当pH值由3升至5时,随着pH值的增加,2种蔗糖酶的水解率小幅度的升高,但当pH值由5升至6时,Sigma蔗糖酶的水解率稍微降低,但裕立宝蔗糖酶水解率继续升高,这是因为酶的活性中心对pH值敏感[6],不同酶具有不同的最适pH值。当pH值由6升至7时,添加Sigma蔗糖酶的样品水解率骤降,添加裕立宝蔗糖酶的样品水解率也明显下降。因此,sigma蔗糖酶和裕立宝蔗糖酶最适pH值范围均为4.0~6.0。

图4 pH对水解率的影响
2.1.3 加酶量对蔗糖酶水解率的影响
Sigma 蔗糖酶分别以 35、70、140、175、210 U/mL五种酶量,裕立宝蔗糖酶分别以 1.6、8、40、50、80U/mL加酶量,加入到底物浓度为12mg/mL的大蒜果聚糖液中,pH值为5.0、50℃下水解12 h,结果如图5和图6。

图5 Sigma蔗糖酶的加酶量对水解率的影响
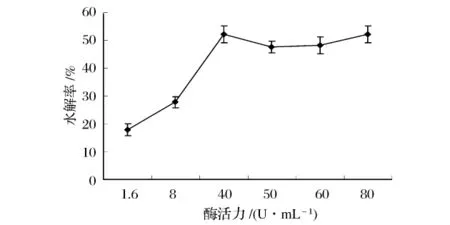
图6 裕立宝蔗糖酶的加酶量对水解率的影响
由图5和图6可以看出,在反应初期,随着加酶量的增加,2种蔗糖酶的水解率逐渐增加,这是因为随着酶活量的增加,水解体系中的反应速率增加,提高了水解率。当Sigma蔗糖酶加酶量达到175 U/mL后,蔗糖酶的水解率增加不显著,基本呈水平线。裕立宝蔗糖酶加酶量达到40 U/mL时,蔗糖酶的水解率较大,再增加加酶量时,水解率趋于平稳,这是因为后期水解速率减慢,水解率逐渐达到最大,因而趋于稳定[10]。因此,从水解率和经济方面考虑,分别选择175 U/mL、40U/mL的加酶量比较适合。
2.1.4 底物浓度对蔗糖酶水解率的影响
研究不同底物浓度 2、4、8、10、12mg/mL 的大蒜果聚糖液中,pH值为5.0时、50℃下水解12h,得结果如图7所示。

图7 底物浓度对转化率的影响
由图7可知,当底物浓度由2mg/mL升至8mg/mL时,随着底物浓度的增加,Sigma蔗糖酶的水解率呈上升趋势,这表明底物浓度对Sigma蔗糖酶水解率的影响十分明显[10];当底物浓度达到8mg/mL时,增加底物浓度,蔗糖酶水解率增加缓慢甚至不再增加。而裕立宝蔗糖酶的水解率也呈上升趋势,但变化不显著,这表明底物浓度对裕立宝蔗糖酶水解率的影响不显著[14]。一般当底物浓度达到10mg/mL时,酶解率达到最高,若果聚糖浓度太高,对蔗糖酶的水解率有一定的抑制作用,甚至向蔗糖酶转移方向发展[10]。
2.1.5 时间对蔗糖酶水解率的影响
底物浓度为12mg/mL,50℃、pH值为5.0时研究不同水解时间 2、4、6、12、18、24 h 的水解率,结果如图8所示。

图8 时间对转化率的影响
由图8可知,对于Sigma蔗糖酶,2~18 h时,随着时间的增加,蔗糖酶的水解率呈上升趋势,18~24 h时,单位时间内水解率没有显著提高。对于裕立宝蔗糖酶,2~12 h时,水解率显著提高,12~24 h时,蔗糖酶水解率不再增加。随着时间的延长,并不能显著提高酶解率,原因可能是高浓度的果糖对蔗糖酶具有抑制作用[14]。因此从经济和能耗的角度考虑,酶解时间选择12 h。
2.2 酶解条件的优化
在单因素的试验基础上,可以看出Sigma蔗糖酶的水解率较高。选择温度(A)、pH(B)、加酶量(C)、底物浓度(D)作为考察因素,每个因素选择3个水平做正交试验,因素水平见表2。正交试验结果见表3。

表2 Sigma蔗糖酶水解因素水平表
由表3的实验数据可知,实验号为5的正交试验得出的水解率最高。按极差大小决定的因素主次顺序为温度>pH>底物浓度>加酶量。水解温度和pH值为主要影响因素。结合极差与方差分析,得出最佳水解率的条件是:A2B3C2D1。即温度为45℃,pH为4.8,加酶量为210 U/mL,底物浓度为8mg/mL,水解率达到80%。

表3 sigma蔗糖酶正交试验结果
2.3 酶解产物的成分分析
正交试验结果显示,Sigma蔗糖酶的水解率达到80%。取最终样品根据色谱条件进行样品检测。样品中单糖结果如图9,样品中低聚糖结果如图10所示。

图9 样品中单糖的色谱图

图10 样品中低聚糖的色谱图
由图10可以看出,样品中果聚糖含量较少,酶解比较彻底,产物主要由大量的单糖组成;由图9可以看出,样品中单糖是由大量的果糖和少许的葡萄糖组成,其中以果糖为主,而鼠李糖、阿拉伯糖、半乳糖以及木糖含量很少;通过含量的计算,得出其中果糖含量约占样品成分的85%,葡萄糖含量约占9%,低聚糖及少量木糖等约占6%,因此样品中的成分以果糖为主,葡萄糖为辅;得出的含量结果与正交试验结果相一致,因此最终样品为果葡糖浆。
3 结论
采用2种蔗糖酶对大蒜渣进行水解,Sigma粉状蔗糖酶的水解率略高于裕立宝的液态蔗糖酶。结果显示,最适酶解条件是:pH值为4.8,温度为45℃,加酶量为210 U/mL,底物浓度为8mg/mL,最终水解率可以达到80%。经离子色谱-积分脉冲安培检测法的鉴定,酶解产物为果葡糖浆,组成成分以果糖为主,葡萄糖为辅。
[1]许春萱,魏金凤,魏红光.大蒜精油提取后废弃蒜渣综合利用的研究[J].环境科学与技术,2001(6):42-44.
[2]邓林.酵母蔗糖酶酶学性质的研究[J].四川食品与发酵,2007,44(3):41-42.
[3]陈雄. 从制备大蒜精油废弃物中提取大蒜多糖的研究[J].食品工业科技,2007,28(1):117-119.
[4]索朗桑姆.大蒜多糖的提取分离及含量测定分析[J].西藏科技,2004(4):22-26.
[5]陈毓荃.生物化学实验方法和技术[M].北京:科学出版社,2002:98-100.
[6]曾鸣,李翔.固定菊粉酶酶解菊芋提取液制备果糖的研究[J].食品研究与开发,2 000,21(2):10-13.
[7]Nakamura T,Ogata Y,Sgutara A,et al.Continuous production of fructose syrups from inulin by immobilized inulinase from Aspergillus niger utant 817 [J].J Ferment Bioengineer,1995,80(2):164-169.
[8]Yun J W,Kim D H,Kim B W,et al.Production of inulooligasaccharides from inulin by immobilized endoinuliase from Pseudomonas sp.[J].J Ferment Bioengineer,1997,84(4):369-371.
[9]Abasaeed A E,Asif M,Fakeeha A H.Zeolite–catalyzed hydrolysis of inulin to fructose in a fluidized bed reactor[J].Bioprocess Engineering,1999(20):343-348.
[10]彭英云.Aspergillus ficuum SK004产外切菊粉酶及其酶解菊粉制备高果糖浆的研究[D].江南大学食品学院,2005.
[12]赵国群,李秀敏,张桂.菊粉的固体酸水解[J].食品工业科技,2007,28(9):160-162.
[13]魏文铃.酶解菊粉法生产高果糖浆[J].厦门大学学报,1990(5):19-21.
[14]汪伦记,董英,邹风等.Kluyveromyces marxianus菊粉外切酶的制备及其水解菊粉的研究[J].食品与发酵工业,2009,35(11):18-23.
[15]彭英云.菊粉的制备及壳聚糖柔性固定化菊粉酶酶解菊粉的研究[D].江南大学食品学院,2007.
[16]王建华,刘艳艳,姚斌,等.一步法制备高果糖浆工程及产酶菌体营养价值研究[J].食品与发酵工业,1999,26(2):1-4.
[17]Kochhar A,Gupta A K,Kaur N.Purification and immobilization of inulinase from Aspergillus candidus for producing fructose[J].J Sci Food Agric,1999,79:549-554.
[18]Kochhar A,KaurN,Gupta A K.Inulinase from Aspergillus versicolor A potent enzyme for producing fructose from inulin[J].J Sci Ind Res,1997,56:721-726.
[19]Uhm T B,Jeon D Y,Byun SM,et al.Purification and properities of β-fructofuranosidase from Aspergillus niger[J].Biochim Biophys Acta,1987,362(1):119-126.
High Fructose Syrup Production by Invertase Hydrolysis on Garlic Dregs
Huang Jing,Zhang Ning,Zhang Yong-tao,Huang Xue-song
(Department of Food Science and Engineering,Jinan University,Guangzhou 510632,China)
Two sucrases were used for high fructose syrup production by hydrolyzing garlic dreg at optimal condition obtained from single-factor and orthogonal experiments.It was found that the high fructose syrup yield of 80%was achieved at pH 4.8,45 ℃,substrate concentration 8mg/mL,and enzyme concentration of 210 U/mL substrate after hydrolyzing for 12h.The hydrolysis products mainly consisted of fructose and glucose determined by ion chromatography-integrated pulsed aperometric detection.
invertase,garlic dregs,high fructose syrup
硕士研究生(张宁副教授为通讯作者)。
*国家高技术研究发展计划专项经费(2007AA10Z300)
2010-07-06,改回日期:2010-09-15

