Co-Mo系耐硫变换催化剂的硫化研究
余 新 吴林锋 张雄兵 李小定
(华烁科技股份有限公司,湖北武汉 430074)
Co-Mo系耐硫变换催化剂的硫化研究
余 新 吴林锋 张雄兵 李小定
(华烁科技股份有限公司,湖北武汉 430074)
介绍了钴钼耐硫变换催化剂的基本组成、硫化原理和硫化剂的选择;详细阐述了耐硫变换催化剂的硫化方法及其在工业上的应用。
Co-Mo;耐硫变换;催化剂;硫化
0 引 言
Co-Mo系变换催化剂与其它常用的催化剂相比具有变换活性高,不存在硫中毒的问题,因此近几十年来这类催化剂在合成氨、甲醇、制氢和城市煤气工业中得到了广泛应用,其使用技术就得到更多的研究与讨论。而大量试验结果表明,此类催化剂的活性相为硫化态,也即催化剂在使用前必须进行硫化处理,使活性组分的氧化态转化为硫化态。所以,此类催化剂的硫化技术是它应用的关键步骤之一,它直接影响着催化剂的变换活性和稳定性[1]。
1 钴钼系耐硫变换催化剂的基本组成
目前耐硫变换催化剂大多采用 Co、Mo金属元素作为活性组分,并以氧化态分散在多孔的载体上。国内外已开发成功的钴-钼系耐硫变换催化剂,按其性能可分为两类:一类为适用于高压和高汽气比条件下的中温耐硫变换催化剂;另一类为适用于低压的低温耐硫变换催化剂,我们也常称之为宽温耐硫变换催化剂[2]。
2 硫化原理
大量实验结果表明,催化剂的活性相为硫化态,也即催化剂在使用前必须进行硫化处理,在硫化剂和氢气存在下使活性组分的氧化态转化为硫化态。硫化反应为:

而目前应用最广的硫化方法都是基于华烁科技股份有限公司(原湖北省化学研究院)开发的高效快速硫化法对催化剂进行硫化。
3 硫化剂的选择
在催化剂的硫化过程中,无论采用何种硫化方法,最基本的硫化剂就是 H2S。因此,只要在硫化条件下容易提供H2S的物质都可用作硫化剂。目前行业界采用和推广的硫化剂一般选用的是CS2或者是湖北省化学研究院开发的ESS-1型固体硫化剂,也有一部分厂家使用高硫煤产生的高浓度H2S直接硫化,同时也有少数厂家采用有机硫或硫泡沫来进行硫化。
3.1 CS2硫化剂
CS2为有机溶剂,其沸点 47℃,闪点 105℃,在200℃左右就能与H2容易发生氢解反应生成H2S:
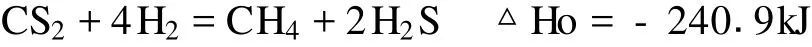
1989年湖北省化学研究院研究出一种钴-钼系一氧化碳变换催化剂的硫化新方法,采用 H2S或CS2在250~450℃(较佳温度400~450℃)进行硫化,比传统的硫化处理的活性提高了10%左右[3]。紧接着1991年湖北省化学研究院进一步研究出了用CS2硫化钴钼变换催化剂的方法,此方法是对前一种方法的改进和完善。催化剂用CS2进行硫化,使 H2S在200~300℃下,更好在230~270℃穿透(即出口 H2S浓度 >10g/m3(标)),并保持 1~6h,更好为 3~4h,再在300~400℃下,更好在370~400℃进行高温强硫化,并保持1~6h,更好为2~3h,该硫化方法使得催化活性又进一步提高10%左右[4]。
因为CS2的价格不高,它的氢解效率也比较高,氢解所需的温度也相对其它硫化剂比较低,储硫率也比较高,因此这种硫化方法在工业应用中得到广泛的推广与应用,而目前全国行业界应用最多的也是利用二硫化碳来硫化变换催化剂。
3.2 固体硫化剂
因为CS2的沸点、闪点低,是一种易燃易爆且有毒性的有机溶剂,在运输、灌装、使用过程中稍不小心就有着火、爆炸的危险。所以湖北省化学研究院吴大天等人就研发出了一种ESS型固体硫化剂,是用混碾法将活性单质硫、催化剂、含硫化合物及一定量的助剂附在固体颗粒上而成。主要反应原理为:

该固体硫化剂具有贮存、装卸、运输简单安全,不燃,不爆,无毒,出硫量高等优点。
半水煤气提供H2,当加热后的半水煤气经过固体硫化剂床层时,便产生了H2S。此类硫化剂在江西东乡化肥厂和江苏恒盛化肥有限公司氮肥厂等多家中小型化肥企业中得到广泛的应用,效果也比较显著[5-7]。
3.3 高硫煤硫化剂
煤的含硫量大于3%的煤称为高硫煤。就因为高硫煤本身含有一定含量的硫,所以它自身就具有硫化作用的能力,因此湖北省化学研究院早在90年代初就开发出了一种全低变一氧化碳耐硫变换催化剂的硫化方法,是以高硫煤或高硫煤加固体硫化剂的高硫煤气升温硫化。该方法适用于全低变和中串低变流程中Co-Mo系耐硫变换催化剂的硫化及工业应用、经该方法处理后的催化剂达到和了经过其他硫化剂(如CS2)和高温快速硫化法硫化处理后催化剂的活性及其它各项技术指标,同时可避免甲烷化副反应,减少了催化剂粉化所造成的工艺故障[8]。
3.4 硫泡沫和有机硫硫化剂
硫泡沫硫化剂实际上是向煤中添加硫或/和含硫的盐类或金属硫化物而制得的一种硫化剂。在1989年湖北省化学研究院与湖北恩施市化肥厂合作开发出了这种硫泡沫硫化剂及其应用。该硫化剂就是系硫或含硫的铵盐类化合物 ((NH4)S、NH4HS、(NH4)2SO4等一种或多种)或金属硫化物(FeS、Sb2S3、CaS等一种或多种)。其使用是当催化剂床层热点温度达200℃后,将硫或/和含硫铵盐或金属硫化物与煤按重量比0.001 5~0.02∶1的配比,搅拌均匀,添入合成氨厂的固定层煤气发生炉内,控制炉内温度900~1 100℃,使产生合成氨原料气的同时产生H2S,从而对耐硫变换催化剂进行硫化处理[9]。
有机硫化剂实际上就是有机多硫化物,这类有机多硫化物如:乙醇硫(EM)、正丁硫醇(NBM)、二甲基二硫化物 (DMDS)、二甲基硫化物(DMS)等在一定的条件下进行氢解能放出H2S气体,从而对一氧化碳变换催化剂进行硫化。其氢解反应式为:
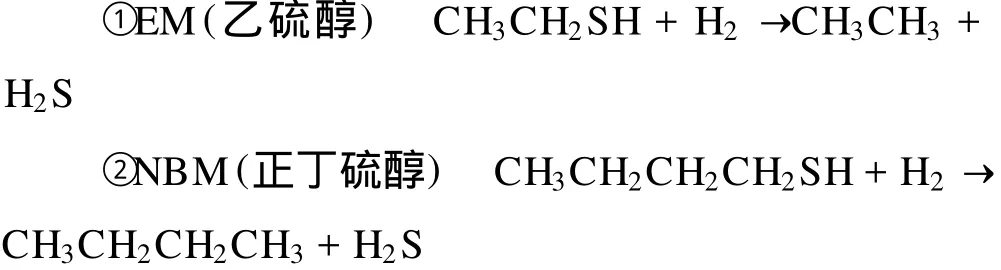

以上反应均属放热反应,平衡常数随温度升高而下降,但在催化剂的使用温度范围内都很大,即它们的转化很完全,不受化学平衡限制,而均受动力学控制。有机硫化剂在工业上的应用一般不是很广泛,但主要都是应用在高压变换催化的硫化上[10-11]。
4 硫化方法
工业上对一氧化碳耐硫变换催化剂进行硫化使用的硫化方法大体上分为两大类:一类是自然硫化和强制硫化,另一类是放空硫化和循环硫化。而循环硫化法又分为:半循环硫化法和全循环硫化法。
4.1 自然硫化与强制硫化
自然硫化是指直接用变换工艺气中的H2S对催化剂进行硫化处理,因为大部分的变换气中都会含有硫化氢成分,只是含量的不同。通过大量的自然硫化实践,认为当进低变的原料气中的 H2S含量>0.1g/m3(标),才能保证硫化后低变催化剂的较好活性和较短的硫化时间[12]。
自然硫化一便用于中变串低变工艺中,特点是操作简单,节约费用,硫化温度平稳,硫化条件容易控制,中变的变换工艺与低变的硫化工艺可以同时进行,但低变的催化剂硫化时间比较长,对进低变的工艺气中 H2S含量要求高,因为硫化时 H2S浓度对硫化后催化剂活性的影响比较大:
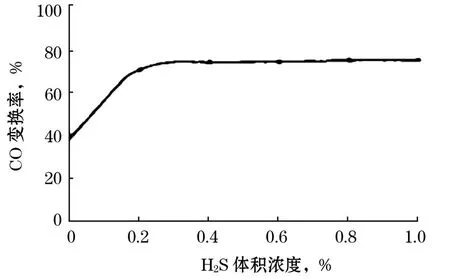
图1 H2S浓度对催化剂活性的影响
由图1可知,H2S浓度过低(≤0.2%)时,催化剂的活性较差,而H2S浓度较高时对催化剂的活性影响不大,由于一定量的催化剂的总吸硫量是一定的,因此催化剂达到一定硫化度所需的硫化时间与硫化时工艺气中的H2S浓度成反比例关系。所以自然硫化的应用就因为工艺气中H2S的含量而受到很大的限制。
与自然硫化相对应的就是强制硫化,强制硫化是指将变换工艺气在配入高含量的H2S或其他硫化剂(如DMDS或CS2)后对催化剂进行硫化处理。其硫化特点是有利于提高催化剂硫化效率和硫化度,从而提高催化剂的变换活性,另外该方法还缩短催化剂的硫化时间,节省工业装置的开车时间,因此工业上绝大多数工业装置优先使用,但此种硫化方法易造成催化剂床层温度超温。
在自然硫化与强制硫化中有人提出问题,究竟是用湿气硫化好还是干气硫化好。而大量的实践表明在催化剂硫化过程中,使用干气硫化与湿气硫化对催化剂的活性的确有很大的影响。在CO变换过程中,气体中有大量水蒸气存在,催化剂中的活性组分MoS2与水蒸气有一个水解反应平衡关系。化学反应式为:

可以看出大量水汽的存在会使得本身硫化好的活性组分部分水解而失去催化活性。实验表明当硫化过程中湿气的汽气比R(汽/气)增大到0.15时,硫化后催化剂的催化活性要比干气硫化的低~25%(见图2)[11]。
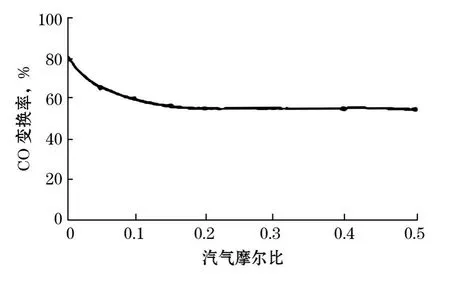
图2 汽气比对催化剂活性的影响
因此实际工业应用上尽量都用干气硫化就是防止工艺气中水蒸汽对硫化造成不利影响。
4.2 放空硫化
放空硫化工艺的具体操作(如图3)是:由造气工段经压缩机送来的半水煤气经电加热器加热进入装有耐硫变换催化剂的变换炉,当变换炉的床层温度升到180~200℃时,向进入变换炉前的半水煤气中加入CS2进行硫化反应,反应后的尾气直接放空,排入大气。
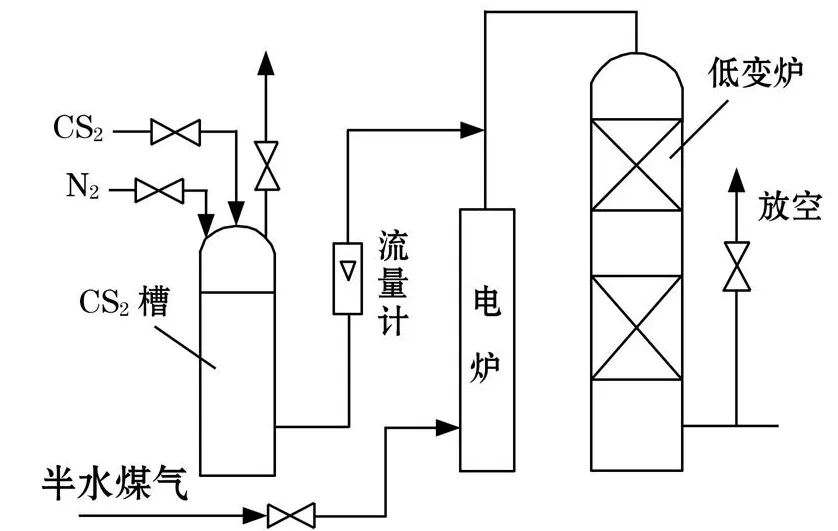
图3 放空硫化流程简图
该方法的优点是:流程简单,对中低低流程而言,不影响中变催化剂的升温也不影响中变系统向后续合成系统送气升温。缺点是:煤气量浪费大,H2S,CS2污染环境,硫化成本高,CS2用量多,煤气中O2波动时会造成床层温度的波动,不易控制,且轴向温差较大。
4.3 循环硫化
4.3.1 部分循环硫化法
此硫化方法在全低变工艺中常用,在部分中低低变中也使用,与放空硫化相比较,最大的不同点就是将反应后的尾气部分放空,其流程见图4。
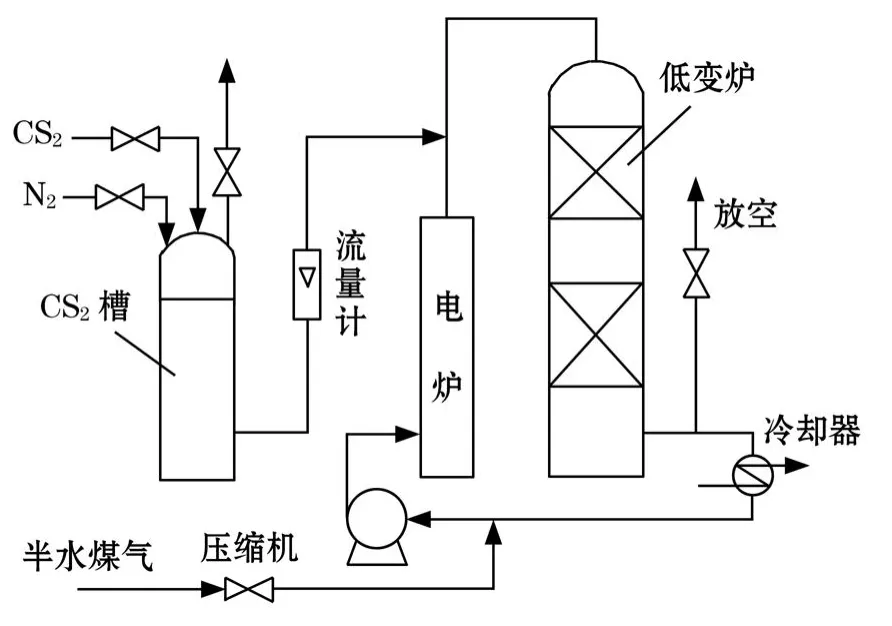
图4 部分循环硫化流程简图
前面的升温硫化过程与放空硫化基本相同。反应后的尾气主要含有未反应完的 H2S、CS2、少量的CH4、部分H2O和大量的半水煤气,也有含量较低的H2,几乎不含O2。尾气经冷凝器后再进入压缩机入口,再送至变换炉进行反应。为了保证一定的H2含量,部分尾气任然放空,并补充新鲜的半水煤气,剩下的大部分气体循环使用。
该硫化方法的优点在于半水煤气和CS2的用量消耗较少,半水煤气和CS2的用量分别降低了~50%和~30%。同时氧含量很低,炉温比较稳定,床层温差缩小了,容易操作,硫化成本低。其不足之处在于对于中低低变换流程,中低变催化剂若要同时升温,必须设置独立的硫化所需的送气和冷凝设备;若采取不同时升温则可不增加设备,但开车时间较长。
4.3.2 全循环硫化法
全循环硫化法与半循环硫化法过程也基本相同,最大的不同点就是采用全循环硫化法时反应后的尾气全部不放空而经过冷凝器气水分离后再进入循环系统进行硫化处理。
全循环硫化时,由于尾气中的CS2、H2S、H2等反复进出硫化系统,随着催化剂硫化物的形成,未反应完的H2S的浓度不断累积增加(因为过程中要不断定量补加CS2),而H2的浓度将逐渐下降。由硫化反应原理可知,H2的主要作用是产生 H2S,来用于MoO3和CoO的硫化反应,而部分的 H2参与MoO2和CoO的还原反应。所以,H2的浓度偏低不利于催化剂的硫化,而偏高容易将催化剂都直接还原成金属Mo、Co,硫化效果就达不到,还有可能催生副反应。那么H2的含量多高比较合适,有的文章提出>25%[13],也有从硫化中分析出 H2的含量~20%[14]。为了保证硫化效果,当CS2的加入量一定时,H2过高过低都是不利的,一般含氢量控制在20%~30%较合理。而在实际硫化操作中,前期床层需要硫穿透,CS2的加入量较大,氢含量也相应要高一些;后期 H2S循环利用,氢含量可以低一些,循环硫化就正好符合此要求。
全循环硫化过程中副产物的不凝气较低,主要就是甲烷,而生成的H2O被冷却分离了,为了整个气量的平衡,所以还需要相应地补充少量的新鲜半水煤气。全循环硫化气量大,几乎接近无O2进行硫化,所以催化剂床层温度稳定,轴向温差也可缩小40~80℃,各点温度较接近,硫化效果好,几乎无污染,硫化成本也大幅下降,故此种方法是一种值得广泛推广的硫化方法。
5 结 语
随着合成氨、城市煤气、合成甲醇工业的飞速发展,国内外对耐硫变换催化剂的研究越来越活跃,一氧化碳耐硫变换催化剂的硫化过程对催化剂的活性及稳定性又有至关重要的影响,所以了解和掌握耐硫变换催化剂的硫化方法和相关事宜也是相当重要的。本文主要对钴钼耐硫变换催化剂的基本组成、硫化原理和硫化剂的选择进行了简单的介绍;详细阐述了耐硫变换催化剂的几种硫化方法及其在工业上的运用,希望对耐硫变换催化剂的工业应用有一定的参考意义。
[1] 春国成,侯琳.Co-Mo系耐硫变换催化剂硫化的探讨.化学工业与工程技术,2007,28(4).
[2] 丛玉梅,孙鸿.钴钼耐硫变换催化剂应用技术探讨.化肥设计,2008,46(4).
[3] 湖北省化学研究院.钴-钼系一氧化碳变换催化剂的硫化法.中国专利,89100315.0.
[4] 湖北省化学研究院.用二硫化碳硫化钴钼变换催化剂的方法.中国专利,91102838.2.
[5] 李建新,吴大天.一种新型的用于Co-Mo系催化剂的固体硫化剂(ESS-1).湖北化工,1995,(1).
[6] 吴大天.ESS—1型固体硫化剂及其工业应用.小氮肥设计技术,2000,21(1).
[7] 余荣华.固体硫化剂的应用.化工设计通讯,2001,24(3).
[8] 李小定,陈劲松.钴-钼系耐硫一氧化碳低变催化剂的硫化方法.中国专利,90102615.8.
[9] 王先厚,李小定.耐硫一氧化碳变换催化剂的硫化及其应用.中国专利,89102614.
[10] 任志鹏,张谦温.非金属加氢催化剂的预硫化技术进展.北京石油化工学院学报,2009,(1).
[11] 高建国,谭永放.耐硫变换催化剂硫化技术探讨.大氮肥,2001,25(4).
[12] 张大同.耐硫低变催化剂的自然硫化.陕西化工,1990,(5).
[13] 华南平.EB-1球形耐硫变换催化剂的硫化.化工设计通讯,1989,15(4).
[14] 李永吉.粗煤气耐硫变换催化剂的使用和维护.大氮肥,1993,(3).
Study on the sulfurization of Co-Mosulfur-resistant shift catalysts
YU Xin,WU Lin-feng,ZHANG Xiong-bing,LI Xiao-ding
(Hua Shuo Technology Co.,Ltd.Wuhan,Hubei430074,China)
This article introduces the basic composition of the Co-Mo sulfur resistant shift catalyst,the sulfurization principle and the choice of curing agent.The sulfurization method of the sulfur-resistant shift catalyst and the application in industry are elaboratied.
Co-Mo;sulfur resistant shift;catalyst;sulfurization
TQ113.24+7
A
1003-6490(2010)03-0001-04
2010-08-05
余 新(1985.5-),男,湖北省化学研究院硕士在读(三年级)。联系电话:13554351964

