盐酸吡格列酮片含量测定方法学的研究
庄文斌 曾晨笛 杨爱群 肖文豪 陈吉生
盐酸吡格列酮是目前最新的噻唑烷二酮类药物,近年来,随着越来越多人对盐酸吡格列酮的研究,其制剂开发、含量测定方法学也逐渐有报道,但由于中国药典2005版和2010版,均无收录盐酸吡格列酮,查阅文献,关于盐酸吡格列酮片含量测定方法,采用流动相的有机相大多数为乙腈,由于乙腈价格昂贵、对人体的毒性较大[1]。为有效控制其质量标准,本文通过方法学摸索,开发出简单、快速、经济、低毒及灵敏度高的测定盐酸吡格列酮片含量的方法,为进一步开发盐酸吡格列酮新的制剂提供质量控制参考。
1 仪器与试剂
仪器:Waters高效液相色谱系统(沃特Water科技上海有限公司):1525泵,2487可变波长紫外检测器,Breeze色谱工作站。盐酸吡格列酮对照品(中国药品生物制品检定所,批号:100634-200401);盐酸吡格列酮片(15 mg/片,日本武田药品工业株式会社,分装批号:070401;081101;090101);试剂:甲醇为色谱纯;乙醇、氨水均为分析纯。
2 方法与结果
2.1 色谱条件的摸索和确定 参考文献所记载的盐酸吡格列酮的测定方法[2],通过对流动相品种、流动相配比、流速、最大检测波长、pH值等进行摸索,根据峰形、峰面积等指标确定的色谱条件为:色谱柱:Symmetry C18柱(4.6 mm×150 mm);流动相:甲醇:水(80:20),用新配置的氨试液将pH值调至7.0;流速:1.0 ml/min;紫外检测波长:224 nm;柱温:室温;进样量20 l。色谱图见图1。
2.2 方法学的验证
2.2.1 标准曲线的制备 精密称取相当于10 mg的盐酸吡格列酮对照品,置100 ml容量瓶中,加乙醇溶解并定容,摇匀,配成浓度为0.1 mg/ml的溶液。分别精密量取该溶液10 ml、8 ml、6 ml、5 ml、3 ml、1 ml,各置 10 ml容量瓶中,用乙醇定容,摇匀。按“2.1”项的色谱条件,分别进样三次测定。测得各浓度对应的峰面积,以盐酸吡格列酮的峰面积(A)对浓度(c)进行线性回归,结果表明,盐酸吡格列酮在10~100μg/ml浓度范围内与峰面积线性关系良好。回归方程为:A=5e+7c+42096;R2=0.9995。

图1 盐酸吡格列酮色谱图
2.2.2 稳定性试验 参考中华人民共和国药典稳定性实验的指导原则[3]精密称取约相当于5 mg的盐酸吡格列酮对照品,置100 ml容量瓶中,加乙醇溶解并定容,摇匀,配成浓度为0.05 mg/ml的溶液。在本实验条件下分别在室温放置不同时间(0、1、2、4、6、24 h),按“2.1”项的色谱条件,分别进样三次测定,测得各时间点对应的盐酸吡格列酮峰面积,计算RSD=0.96%,表明盐酸吡格列酮的乙醇溶液在24 h内基本稳定。
2.2.3 精密度的考察 精密称取约相当于5 mg的盐酸吡格列酮,置100 ml容量瓶中,加乙醇溶解并定容,摇匀,配成浓度为0.05 mg/ml的溶液。在“2.1”项的色谱条件下连续进样6次测定,其峰面积的RSD=0.36%(n=6)。
2.2.4 灵敏度-最低检测限的考察 按照“2.1”项的色谱条件,取溶解盐酸吡格列酮的乙醇溶液,进样20 l三次,作为空白溶液色谱图,根据样品出峰时间,取样品出峰附近的一段基线来计算燥声,测得基线噪音为1957,再配制浓度约为0.01 mg/ml盐酸吡格列酮样品溶液。分别精密量取该溶液8 ml、6 ml、5 ml、3 ml、1 ml,各置 10 ml容量瓶中,用乙醇定容,按“2.1”项的色谱条件,分别进样三次测定,记录出峰处信号值,见图12,在上述色谱条件下,以S/N=3计算得盐酸吡格列酮的最低检测限为0.08μg。
2.2.5 回收率试验 取已知含量的盐酸吡格列酮片20片,精密称定,研成细粉并混匀后,分别精密称取约相当于盐酸吡格列酮4、5、6 mg,各置200 ml量瓶中,精密加入盐酸吡格列酮对照品5 mg,加溶剂溶解并定容,摇匀,作为回收率测定用溶液,按“2.1”项的色谱条件,分别进样三次测定,记录峰面积。由公式:回收率=(测得量-样品中含量)/标准品加入量,计算出回收率。
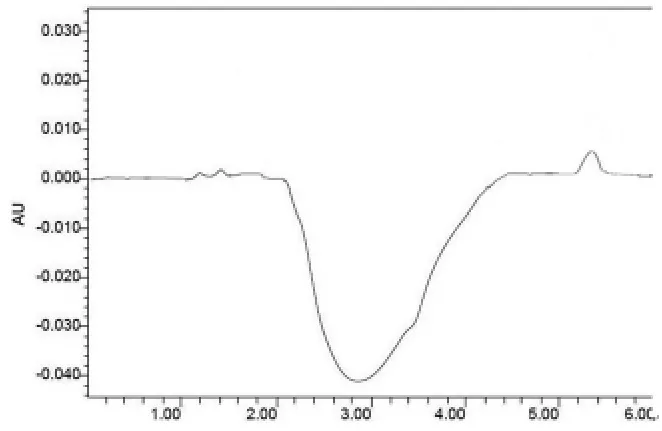
图2 盐酸吡格列酮在最低检测限浓度下的出峰情况
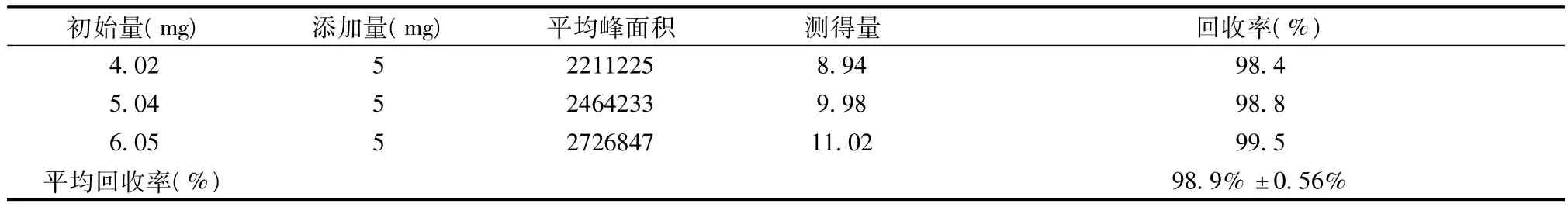
表1 盐酸吡格列酮的回收率
2.3 样品测定 取盐酸吡格列酮片20片,精密称定,研成细粉取细粉适量(相当于盐酸吡格列酮5 mg),精密称定,置100 ml量瓶中,用乙醇溶解,超声5 min使溶解,加乙醇稀释至刻度,摇匀,用0.45 μm微孔滤膜过滤,制成每1 ml中约含盐酸吡格列酮0.05 mg的溶液。按“2.1”项的色谱条件,测定本品三批,分别进样三次测定,记录峰面积,再根据标准曲线计算含量,结果如下:

表2 3个批次的盐酸吡格列酮片的含量
3 讨论
3.1 采用HPLC法测定盐酸吡格列酮片的含量,最首要的是选择合适的色谱条件和测定方法,作为HPLC的流动相,如果选择粘度较高的溶剂,会在分析时产生很高的压力,导致柱子的损坏加快。在有机溶剂与水混合的时候,根据混合比例的不同,所产生的粘度(=压力)的比例也会不同。在实验中发现,当甲醇与水的比例为50:50时,会产生很高的柱压,通过调节比例得出,甲醇与水的比例往两级增大,柱压会下降。在洗脱能力上,乙腈比甲醇的洗脱能力强[4],因此使用甲醇代替乙腈时,需要增大甲醇的比例,每次将甲醇的比例增加5%,再选择哪个比例可以到分离要求,试验结果显示,当甲醇:水=80:20时,盐酸吡格列酮片峰形及出峰时间合适,因此确定流动相的比例为甲醇:水=80:20,验证结果表明,该流动相适合用于盐酸吡格列酮片的含量测定。
3.2 应用HPLC法进行分析测定时,常常采用离子抑制法即向含水流动相中加入弱酸、弱碱或者缓冲溶液等改性剂,以使流动相的pH值控制一定数值,抑制溶质的离子化,减少谱带拖尾、改善峰形,以提高分离的选择性[5]。
3.3 通过验证实验确认,本文所用的盐酸吡格列酮含量测定方法学各项目均达到要求,且本测定方法简便,片剂不需提取分离,直接溶解过滤即可直接进样,测定时间短,只需8 min即可完成测定,流动相简单、毒性低、价格便宜,方法准确、重现性好、精密度高,具有较好的推广应用价值。
[1]钱伯章.全球乙腈生产紧缺.合成纤维,2009,06:53.
[2]朱鹏祥,钱南萍,魏润新,等.盐酸吡格列酮片的HPLC含量测定方法.江苏药学与临床研究,2004,12(6):15-16.
[3]国家药典委员会.中华人民共和国药典2005年版第二部.化学工业出版社,2005,附录:172.
[4]高效液相(HPLC)流动相乙腈与甲醇的区别,生物信息网,实验室安全专栏,http://www.biowww.com.cn/shiyan/safe/1970.html.
[5]宋永康,郭嘉,潘葳.影响测定反相高效液相色谱流动相pH值的因素.现代科学仪器,2005,1:95-97.

