聚吡咯纳米纤维修饰电极电容法脱盐实验
张玉洁,王 越,徐世昌,王纪孝,王世昌
(1. 天津大学化工学院化学工程国家重点实验室,天津 300072;2. 天津大学天津市膜科学与海水淡化技术重点实验室,天津 300072)
电容法脱盐技术(capacitive deionization,CDI)是近年来发展起来的一种新型溶液去离子方法,其利用具有大的比表面积和大的比容量的一对电极组成流通型电容器组件,并通过交替进行的电容器充电和放电操作实现溶液的脱盐和排浓.与已有的脱盐技术相比,CDI技术具有如下优点[1]:①利用低压直流电源供电,过程操作便捷可控且能耗低;②电极通过互换极性或加载负载的方式再生,无需消耗化学药品,也不产生环境污染;③电极再生过程释放的电能可被回收利用或储存;④电容法脱盐过程的产水回收率高.基于以上优点,CDI技术有望在苦咸水淡化、饮用水的深度净化及软化、高压锅炉及半导体用高纯水制备、电镀废水中重金属的回收利用等领域得到广泛应用[2].
电容法脱盐装置的核心构件是电极单元组件,其主要由电极、集电极和隔板组成,其中电极的材料性能对电容法脱盐过程的影响最大.目前,普遍使用的电极材料有碳材料、金属氧化物材料和导电聚合物材料3种,表1给出了这3种材料的主要性能参数[3-5].
从中可以看出:碳材料以双电层电容为主要储能机理,其比表面积最大,但比容量和比能量都最低,多用作电极复合材料之一或集电极材料.金属氧化物材料的比表面积虽然小于碳材料,但其表面会因发生氧化还原反应而产生法拉第拟电容,且其所具有的法拉第拟电容在数量级上也远大于其所具有的双电层电容,因此金属氧化物材料的比容量和比能量都高于碳材料.然而由于其制造成本较高,该类材料的电极多用于军事、航天及国防等特殊领域.导电聚合物(如聚吡咯、聚苯胺等)纳米材料具有菜花状、纤维状及片状等多种形貌,故其比表面积变化范围较大.导电聚合物电极材料表面与金属氧化物相同,也会因发生氧化还原反应而产生法拉第拟电容.因此导电聚合物材料的比容量与金属氧化物接近,但其比能量较金属氧化物材料和碳材料都高,加之其材料成本较低,故导电聚合物材料成为近年来最受关注和最具发展前景的电极材料之一.
有研究报道表明,聚吡咯纳米纤维电极的比容量在1.0,mol/L KCl溶液、0.5,A/g的电流密度条件下可达305,F/g,对应能量密度可达34.3,kW/g[6],这说明聚吡咯纳米纤维具有较高的比容量和比能量.但由于其比表面积较小,材料的机械性能也较差,因此,将其与其他比表面积较大的电极材料(如活性炭、碳纤维、碳纳米管等)复合,最大程度发挥各自材料的性能优势,成为近年来研究的热点.已有的研究表明:经聚吡咯修饰的碳纤维电极和碳纳米管电极的比容量均可增加 2倍以上,电极的能量密度、循环寿命及机械性能都得到改善和提高[7-10].
笔者以聚吡咯纳米纤维修饰石墨电极(简称PPy/G电极)为研究对象,进行电容法脱盐实验研究,重点考察了 CDI单元施加的工作电压、原料液(NaCl溶液)浓度和电极极间距离等操作条件对PPy/G电极的吸附量的影响规律.文中采用电极吸附量(即原料液中NaCl的质量在吸附过程的变化值与电极工作面积的比值)和电极再生率(即原料液在脱附过程的最终浓度与其在吸附过程的初始浓度的比值)来衡量PPy/G电极的脱盐效果.
1 实验条件和装置
常用电容电极材料的分类和主要性能如表 1所示.
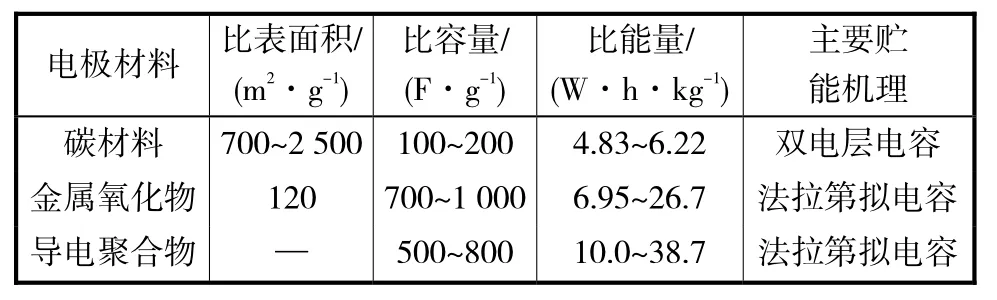
表1 常用电容电极材料的分类和主要性能Tab.1 Sorts and main performances of capacitor electrode materials
实验中采用热压法(150,℃、50,MPa),将石墨和酚醛树脂以 9∶1的比例混合制备石墨基材[11],所制备的石墨片基体的几何尺寸为直径 30,mm、厚度2,mm.将石墨片分别用 1000#和 2000#砂纸打磨处理,浸泡在无水乙醇中待用.
在三电极体系中,采用恒电位法制备 PPy/G电极,其中三电极体系为:处理过的石墨片为工作电极和辅助电极,饱和甘汞电极(SCE)为参比电极.电极的具体制备条件为:聚合电位为 0.85,V,聚合时间为150,s,反应体系为0.19,mol/L吡咯、0.10,mol/L LiClO4和 pH值为 5.91磷酸缓冲液组成的电解液[12].反应前,向反应体系中通入氮气 20,min以除去溶液中的溶解氧气.制备得到的 PPy/G电极在 1.0,mol/L HClO4溶液中浸泡24,h,然后在-0.2 V还原电压作用下,在去离子水中还原 1,000~2,000,s,电极对应的还原程度约为80%;之后将被还原的PPy/G电极浸泡在去离子水中待用.在进行电极电容法脱盐实验之前,再对电极进行循环伏安扫描预处理,以提高电极的稳定性.图1为PPy/G电极表面的扫描电镜图,可以看出在实验条件下可得到直径均匀的聚吡咯纳米纤维,其直径范围在 50~100,nm,电极的 BET比表面积为0.015,m2/g,电极的有效利用面积为13.9 cm2.
以实验制备的PPy/G电极为正极、石墨片为负极组成电容器单元,以一定浓度的 NaCl溶液为原料液进行电极电容法脱盐实验,其工艺流程如图 2所示.图 2中使用电磁搅拌器以保证容器内溶液浓度的均匀性,采用电导率仪及其数据采集系统在线记录溶液的瞬时电导率值,采用电源管理系统控制电容法脱盐过程中工作电压、吸附时间、脱附时间及循环次数等操作条件.实验中电极的再生过程是通过倒换电极极性的方式来实现的.

图1 PPy/G电极的SEMFig.1 SEM image of PPy/G electrode
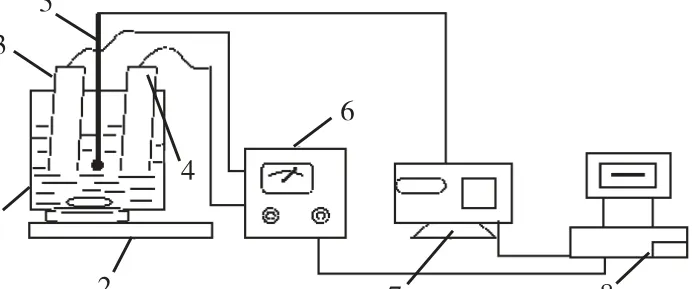
图2 PPy/G电极的电容法脱盐实验流程Fig.2 Flow chart of CDI cell experiments for PPy/G electrode
2 实验结果与分析讨论
2.1 工作电压对PPy/G电极电容法脱盐效果的影响
本实验以 20,mL、0.05% NaCl溶液为原料液体系,在电极极间距离为 10,mm、吸附时间为 600,s、脱附时间为 300,s的条件下,考察了工作电压分别为0.8,V、1.0,V、1.2,V、1.4,V 和 1.6,V 时,PPy/G 电极的电容法脱盐过程中溶液相对电导率(即溶液瞬时电导率相对于溶液初始电导率的变化值)的变化规律(见图3).从图3中可以看出:不同工作电压时,溶液相对电导率均呈近“V”型变化曲线;在电极吸附过程,随着工作电压的增加,相同时刻对应的溶液相对电导率绝对值逐渐增大,且在吸附过程结束时(V形曲线拐点附近)分别达到最大,但不同工作电压所对应的电极最大吸附量不完全相同.经计算可知,工作电压为 0.8,V时电极的吸附量最低,仅为 68.57,mg/m2;工作电压为 1.4,V和 1.6,V时,电极的吸附量最大,为228.6,mg/m2.这是因为随着工作电压的增加,离子在溶液中的迁移速度增加,从而使得电极的吸附量也增大.图中,工作电压为 1.4,V和 1.6,V时的电极吸附量基本相同,这可能是因为电压由 1.4,V增大到1.6,V时,电极表面的聚吡咯发生氧化降解或溶液发生电解反应,从而使得电极吸附量不再增加.
在电极脱附过程,当工作电压由 0.8,V增加到1.6,V时,所对应的电极再生率依次为 100.40%、100.13%、100%、99.87%和 100%.电极的再生率接近或略高于 100%,这说明在实验条件下 PPy/G电极均可得到很好的再生.实验结果中工作电压为0.8,V和1.0,V时电极的再生率均大于100%,这可能是因为在脱附过程中环境温度升高使得溶液的电导率增大所致.从上述分析可知:PPy/G电极在工作电压为1.4,V、吸附时间大于 480,s时,溶液的电导率不再发生变化,说明此时电极的吸附量已达到或接近饱和.在吸附时间为 180,s时,电极的吸附量为最大值的62.05%,电极的再生率在脱附时间为120,s时可达到 98.79%.因此,为提高工作效率,后面的脱盐实验中工作电压设定为 1.4,V,吸附时间和脱附时间分别设定为180,s和120,s.
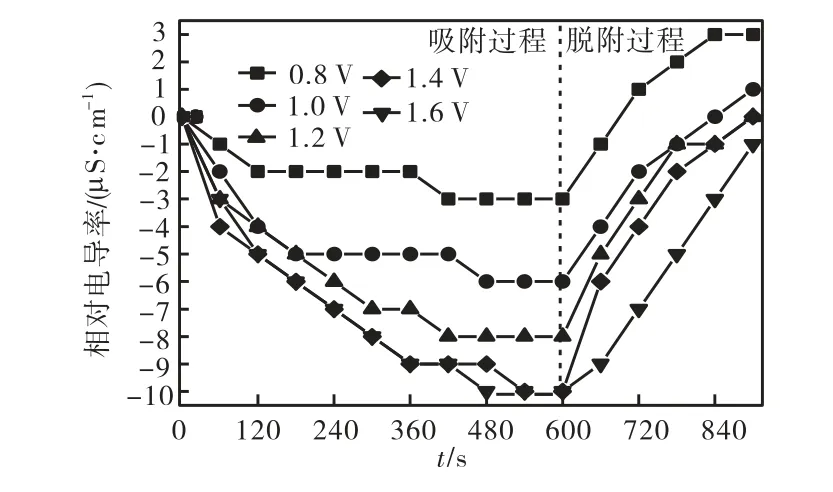
图3 不同工作电压时溶液相对电导率随时间的变化曲线Fig.3 Relative conductivity curves of solution at different Fig.3 working voltages
2.2 原料液浓度对PPy/G电极电容法脱盐效果的影响
图4 给出了工作电压为1.4,V,吸附时间为 180,s,脱附时间120,s,电极极间距离为10,mm,原料液质量分数分别为0.01%、0.05%和 0.1%的条件下,溶液相对电导率随时间的变化规律.从图中4可以看出,在电极吸附过程中,相同时刻的溶液相对电导率绝对值随着原料液初始浓度的增加而增大;在吸附过程结束时,0.1%原料液所对应的电极吸附量最大,为548.6,mg/m2,分别是 0.01%和 0.05%原料液时电极吸附量的4倍和1.33倍.说明在实验浓度范围内,原料液质量分数的增加有利于电极吸附速率及吸附量的提高.其可从以下两方面解释:①溶液浓度的增加,使得电极与溶液界面间分散层的厚度减小,界面电容值增大,增加了电极的吸附能力[13];②由于聚吡咯具有电化学控制的离子交换能力,而其电化学控制的离子交换量随着溶液浓度的增加也会相应增大[14].从电极的脱附曲线看:在上述实验条件下PPy/G电极均能够得到较好的再生,原料液质量分数分别为0.01%、0.05%、0.1%时,对应的电极再生率分别为83.33%、94.44%、95.83%.
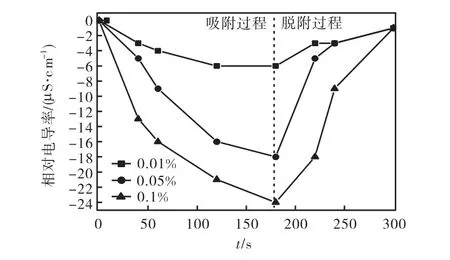
图4 不同原料液浓度条件下NaCl溶液相对电导率随时间的变化曲线Fig.4 Relative conductivity curves of NaCl solution at different NaCl concentrations
2.3 电极极间距离对PPy/G电极电容法脱盐效果的影响
图5给出了 PPy/G电极极间距离分别为28,mm、35,mm 和 48,mm,当 NaCl溶液质量分数为0.05%时,溶液相对电导率随时间的变化规律.从图 5中可以看出:在电极吸附过程,随着电极极间距离的增大、溶液相对电导率绝对值的减少,电极吸附量也相应降低.经计算可知:当极间距离为 28,mm 时PPy/G 电极的吸附量为 160.0,mg/m2,分别为极间距离35,mm和48,mm时电极吸附量的1.17倍和1.75倍.这说明极间距离与电极吸附量之间呈反比关系.在上述 3种实验条件下,电极的再生率均达到100%,这说明电极极间距离对其再生率的影响较小.

图5 不同极间距离时溶液相对电导率随时间的变化曲线Fig.5 Relative conductivity curves of solution at different ig.5草 electrode distances with time
2.4 PPy/G电极电容法脱盐稳定性测试
电极的稳定性是影响电极电容法脱盐过程操作成本的重要因素之一.图6给出了在NaCl溶液质量分数为 0.05%、电极极间距离为 10,mm 时,PPy/G电极在 10次循环吸附/脱附实验中溶液电导率随时间的变化曲线.从中可知:对每一个吸附/脱附过程而言,溶液的电导率曲线均呈“V”型的变化规律,且在第 10次吸附/脱附过程中电极的吸附量较第 1次降低了约 10%,电极的再生率均在 99%以上,初步显示出 PPy/G电极具有良好的循环吸附/脱附能力和实用化潜力.
3 结 语
电容法脱盐技术具有节能、环境友好等优点,是近年来最受重视的新型脱盐技术之一.以电化学法制备的PPy/G电极为研究对象,并将其用于NaCl溶液的电容法脱盐实验研究.实验结果表明:随着工作电压的增大,电极的吸附量也增大,电极工作电压为1.4,V时,PPy/G电极吸附量达到最大,为 228.6 mg/m2;电极吸附量随原料液浓度的增大而增加,溶液质量分数为 0.1%时所对应的电极吸附量最大,为548.6,mg/m2;电极吸附量随电极极间距离的增加而减小.实验结果为以 PPy/G电极为核心的 CDI装置设计和组件开发提供了依据.
[1] Xu Pei,Drewes Jorg˙ E,Heil Dean,et al.Treatment of brackish produced water using carbon aerogel-based capacitive deionization technology[J]. Water Research,2008,42:2605-2617.
[2] 尹广军,陈福明. 电容去离子研究进展[J]. 水处理技术,2003,29(2):63-66.Yin Guangjun,Chen Fuming. Progress incapacitive deionization[J]. Technoiogy of Water Treatment,2003,29(2):63-66(in Chinese).
[3] 夏 熙,刘洪涛. 一种正在迅速发展的贮能装置:超电容器[J]. 电池工业,2004,9(3):115-121.Xia Xi,Liu Hongtao. A rapidly developing energy storage device-super-capacitor[J]. Chinese Battery Industry,2004,9(3):115-121(in Chinese).
[4] Peng Chuang,Zhang Shengwen,Jewell Daniel,et al.Carbon nanotube and conducting polymer composites for supercapacitors[J]. Progress in Natural Science,2008,18:777-788.
[5] 肖 超,唐 斌,吴孟强,等. 超级电容器电极材料的研究进展[J]. 绝缘材料,2007,40(1):44-47.Xiao Chao,Tang Bin,Wu Mengqiang,et al. Rresearch progress of supercapacitor electrode materials[J]. Insulating Materials,2007,40(1):44-47(in Chinese).
[6] Wu Quanfu,He Kuanxin,Mi Hongyu,et al. Electrochemical capacitance of polypyrrole nanowire prepared by using cetyltrimethylammonium bromide(CTAB)as soft template[J]. Materials Chemistry and Physical,2007,101:367-371.
[7] Jurewicz K,Delpeux S,Bertagna V,et al. Supercapacitors from nanotubes/polypyrrole composites[J]. Chemical Physics Letters,2001,347:36-40.
[8] Kim Jong-Huy,Sharma Ashok K,Lee Yong-Sung. Synthesis of polypyrrole and carbon nano-fiber composite for the electrode of electrochemical capacitors[J]. Materials Letters,2006,60:1697-1701.
[9] Wang Jie,Xu Youlong,Chen Xi,et al. Capacitance properties of single wall carbon nanotube/polypyrrole composite films[J]. Composites Science and Technology,2007,67:2981-2985.
[10] Hughes Mark,Chen George Z,Shaffer Milo S P,et al.Electrochemical capacitance of a nanoporous composite of carbon nanotubes and polypyrrole[J]. Chemistry of Materials,2002,14:1610-1613.
[11] 赵若冬,刘宗浩,王宇新. 聚合物膜燃料电池 NG/PF复合双电极板研究[J]. 电源技术,2006,130(12):986-988.Zhao Ruodong,Liu Zonghao,Wang Yuxin. Study on the NG/PF composite bipolar plates applied for PEMFC[J].Chinese Journal of Power Sources,2006,130(12):986-988(in Chinese).
[12] 张玉洁. 聚吡咯纳米纤维修饰电极用于电容法脱盐实验研究[D]. 天津:天津大学化工学院,2008.Zhang Yujie. An Experimental Study on Polypyrrole Nanowire Modified Electrode Used in Capacitive Deionization[D]. Tianjin:School of Chemical Engineering and Technology,Tianjin University,2008(in Chinese).
[13] 李 荻. 电化学原理[M]. 北京:北京航空航天大学出版社,1999.Li Di. Electrochemical Principle[M]. Beijing:Beijing University of Aeronautics and Astronautics Publishing House,1999(in Chinese).
[14] 蔡本慧. 聚吡咯膜离子交换性能及电化学净水研究[D].大连:大连理工大学环境与生命学院,2008.Cai Benhui. Polypyrrole Films Ion Exchange Property and Electrochemical Water Purification[D]. Dalian:School of Environmental and Biological Science and Technology,Dalian University of Technology,2008(in Chinese).

