可见光活性TiO2的制备与表征
赵 丹,鄂 磊,雅 菁,赵 巍,徐明霞
(1. 天津城市建设学院,天津 300384;2. 天津大学,天津 300072)
TiO2作为一种环保、高效的光催化剂,可以广泛用于净化空气、废水处理、抗菌和表面自清洁材料等方面[1].一般认为,锐钛矿型TiO2的光催化活性要高于其他晶型,而无定型态TiO2不具有光催化活性[2].锐钛矿型 TiO2经常被用作光催化剂,但锐钛矿型TiO2的光吸收范围窄,只有波长小于380 nm的紫外光才能使其激发,其吸收光量大约只占太阳光谱的4%,限制了 TiO2的实际应用性.因此要提高TiO2的实用性,就必须扩宽其光吸收范围.目前已有报道:采用低温氢等离子体对 TiO2薄膜或粉体进行处理,或将 TiO2在 NH3或 N2气氛下进行热处理,形成非金属元素 N 掺杂,均可使其具有可见光活性[3-5].但无论采用上述任何一种方法对 TiO2光催化剂进行处理,都会导致生产成本升高.笔者介绍了一种简单的制备方法——以 TiOSO4和氨水为原料,通过化学沉淀法制备具有可见光活性的纳米TiO2光催化剂.
1 实验部分
1.1 纳米TiO2光催化剂的制备及表征测试
将工业级 TiOSO4配制成 1 mol/L的溶液,然后再将 TiOSO4溶液和 6 mol/L的氨水同时滴加到去离子水中,搅拌并保持反应液温度为 40 ℃.控制TiOSO4溶液和氨水的滴加速度,使反应液的pH值保持在7左右.滴加结束后继续保温搅拌0.5 h,使反应完全.反应结束后,将 TiO2水合物反复抽滤、洗涤以去除杂质.然后将洗净后的TiO2前驱体在80 ℃下烘干、球磨,再在不同温度下分别热处理 1 h,即可得到纳米TiO2光催化剂.
采用德国 LEO-1530VP扫描电子显微镜(SEM)观察 TiO2粉体的表面形貌.用 CHEMBET-3000进行粉体的比表面积测定.通过XRD分析了TiO2粉体组成及晶相,仪器为BDX3300(北京大学仪器厂).TiO2光催化剂的吸收特性由美国生产的 Agilent8453紫外可见分光光度计测定.光催化剂的表面化学态由 PHI-1600型 XPS测定.氧空位测试由EMX-6/1型电子顺磁共振仪(ESR)检测.
1.2 光催化实验
实验中采用 11 W 节能灯为光源,光照距离为10 cm.将 60 mL 甲基橙溶液(10 mg/L,pH=3)倒入光催化反应器中.准确称量0.5 g TiO2光催化剂放入甲基橙溶液中,将甲基橙溶液与粉体搅拌均匀.打开节能灯,开始计时,每 4 h测一次甲基橙溶液的吸光度(测量时将粉体从甲基橙溶液中分离出来),直到甲基橙完全脱色.甲基橙溶液浓度的计算公式为

式中:Ct为光催化 t小时甲基橙的浓度,mg/L;C0为甲基橙的原始浓度,mg/L;At为光催化 t小时甲基橙的吸光度;A0为甲基橙的原始吸光度.
2 结果与讨论
2.1 扫描电镜(SEM)和比表面积(BET)分析
图1和表1分别是经不同温度热处理1 h后的TiO2粉体光催化剂的SEM和BET测试结果.

图1 不同温度热处理后TiO2粉体的SEM照片
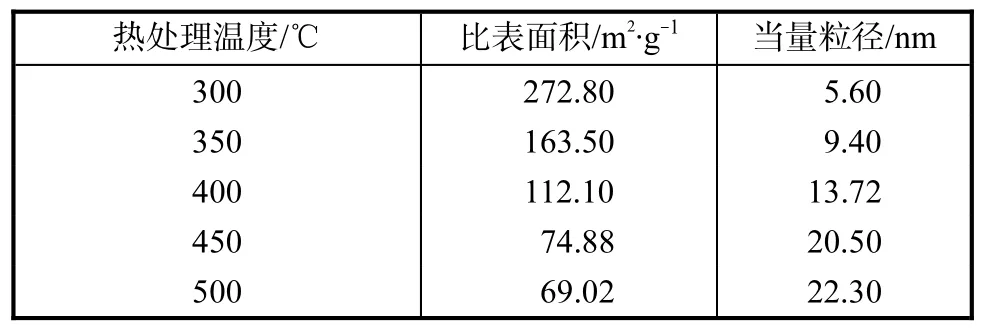
表1 TiO2粉体BET结果和当量粒径
由图1可以发现,经低温(如 300 ℃)热处理的TiO2粉体颗粒呈类球形,且表面粗糙,具有大的比表面积(见表1),颗粒尺寸约为 40~50 nm.当热处理温度升高到400 ℃时,TiO2粉体颗粒表面的粗糙度减小,可以明显看到颗粒的轮廓.当热处理温度升高到500 ℃时,TiO2粉体颗粒表面的粗糙度进一步减小,可以更加明显看到颗粒的轮廓,且颗粒尺寸约为20~40 nm,这与表1中的当量粒径结果相近.
2.2 X射线衍射(XRD)分析
图2为不同温度下热处理 1 h的 TiO2粉体的XRD 衍射图.从图2可以发现:300 ℃温度下经 1 h热处理的 TiO2粉体的衍射峰强比较弱,这表明粉体是由大量无定型态和少量锐钛矿相组成的.随着热处理温度的升高,锐钛矿相的含量不断增加.当热处理温度为 500 ℃时,TiO2粉体的晶型发育完整,为锐钛矿相.
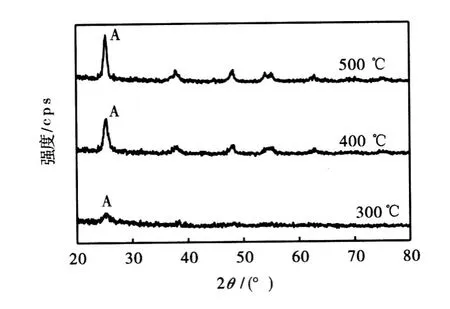
图2 TiO2粉体的XRD分析
2.3 粉体的UV-vis
经不同温度热处理的 TiO2粉体具有较强的可见光吸收特性.图3是 TiO2粉体的可见光吸收特性随煅烧温度的变化.
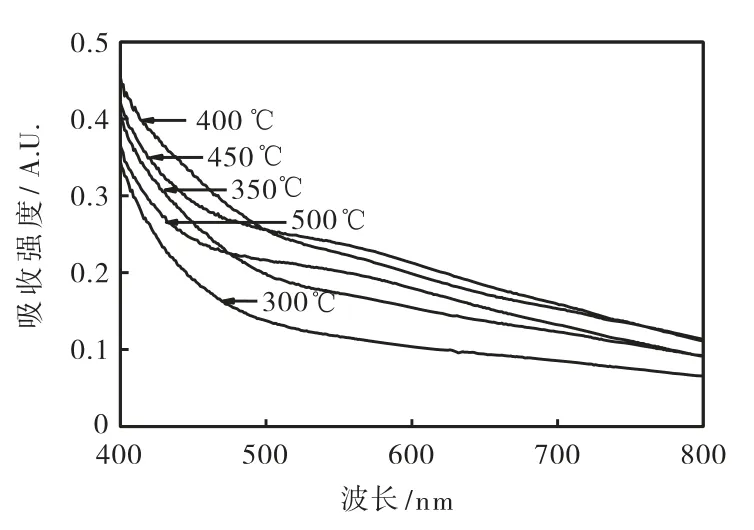
图3 TiO2粉体在可见光区的吸收曲线
从图3可以发现:TiO2粉体的可见区吸收强度与热处理温度密切相关.400 ℃时粉体的光吸收强度最大,T·Ihara等人[6]认为这是由氧空位的生成和氮掺杂引起的,因为光吸收强度是由生成氧空位的数量及氮占据氧空位的数量决定的.在煅烧温度为 300 ℃时,由于热处理温度比较低,使得大部分 TiO2以无定型态存在,只有少量的TiO2晶化成锐钛矿相.一般认为氧空位优先在结构较弱的晶界上生成.由于经较低温度下热处理的 TiO2颗粒的晶界较少,在晶界上生成的氧空位少,从而使在氧空位上掺杂的氮的数量较少,导致经 300 ℃热处理的 TiO2颗粒,在可见光区吸收强度较弱.随着热处理温度的升高,TiO2颗粒的晶化比例增大,晶界的数量增加,从而在晶界上生成的氧空位的数量增多,导致氧空位上掺杂的氮的数量增加,所以 TiO2粉体的光吸收强度也随温度增加而增强.当温度达到 400 ℃时,TiO2粉体的光吸收强度也达到最大值.当温度进一步升高时,由于在晶界上形成的氧空位是不稳定的,极易在高温下发生再氧化,而失去原本已形成的氧空位,造成氧空位和氮掺杂数量的减少,所以在高于 400 ℃热处理的 TiO2粉体的光吸收强度变弱.笔者分别通过ESR和XPS测试验证了氧空位和氮元素的存在.
图4为 ESR 测试结果,图中显示 g=2.003 7有一强信号,此信号表明氧空位的存在[7],而 XPS结果(见图5)表明:Eb=400.3 eV处的峰为N2的化学吸附引起的,也可以归因于 Ti—N键的结合能[5],因此,这种 N以分子形式占据了晶界上的氧空位,这是引起TiO2粉体的吸收光红移的主要因素.因此,这种 TiO2粉体是一种Ti—O—N系光催化剂.
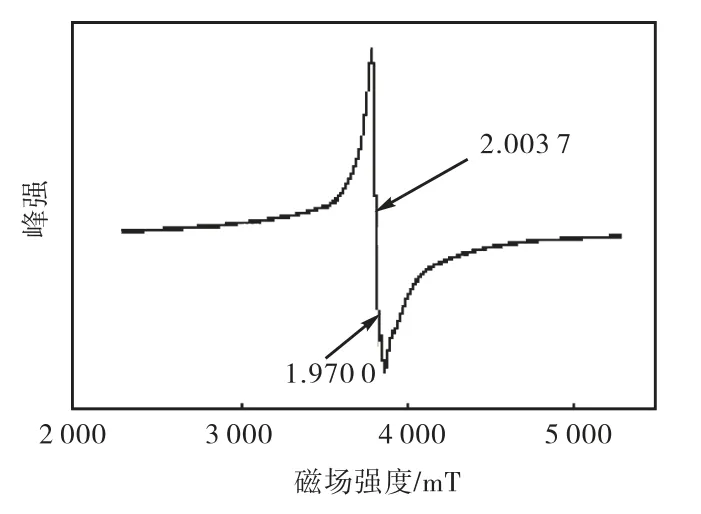
图4 TiO2粉体的ESR谱图
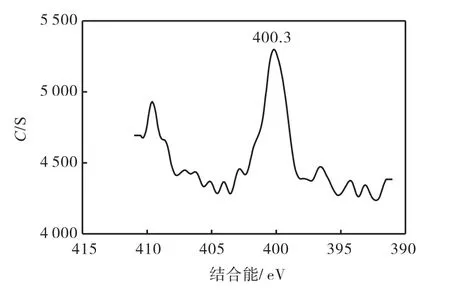
图5 TiO2粉体中N1s的XPS谱图
2.4 TiO2粉体的可见光活性研究
TiO2粉体在可见光下的光催化活性如图6所示.从图6可以发现,经不同温度热处理1 h的TiO2粉体对甲基橙溶液均有较好的光催化降解作用.但经 300 ℃热处理的 TiO2粉体在光催化反应前期表现出最好的光催化活性,而在光催化反应后期,光催化活性减弱,低于400 ℃热处理的TiO2粉体的活性.这是因为 TiO2光催化剂的活性取决于诸多因素,例如,比表面积、晶型结构、对可见光的吸收强度等.其中比表面积决定了有机物分子与 TiO2颗粒的接触面积和光照射面积等因素.对于TiO2粉体而言,比表面积的大小对 TiO2光催化活性的影响极大,是不可忽视的.另外,一般认为锐钛矿相 TiO2的光催化活性高于无定型和金红石型 TiO2的活性;对可见光的吸收越强,越有利于TiO2光催化剂对光子的吸收.光催化初期,比表面积对 TiO2光催化活性的影响占主导作用,而随着光催化反应的进行,晶型结构和对可见光吸收强度对TiO2光催化活性的影响逐渐起到了主导作用.

图6 TiO2粉体在可见光下的光催化活性
经 300 ℃热处理的粉体的比表面积最大,BET=272.80 m2/g(见表1).当粉体与甲基橙溶液混合时,甲基橙分子被快速吸附在 TiO2粉体颗粒的表面,使游离在体系中的甲基橙分子减少,表现为甲基橙溶液浓度的降低.所以在光催化反应初期,经 300 ℃热处理的粉体的光催化活性最好.
但是TiO2粉体的可见光活性还取决于TiO2粉体晶型结构和对可见光的吸收强度等因素.经 400 ℃热处理 1 h的 TiO2,其晶型为锐钛矿型(见图2)且粉体对 400~500 nm 的可见光的吸收最强(见图6),因此经 400 ℃热处理的 TiO2粉体在光催化进行大约6 h后表现出最好的光催化活性.当光催化反应进行到12 h时,甲基橙浓度几乎为0 mg/L,表明甲基橙溶液基本被光催化完全.
3 结 论
(1)以 TiOSO4为原料,氨水为沉淀剂,采用化学沉淀法制得了纳米 TiO2粉体.此粉体经煅烧后可吸收波长范围为400~600 nm的可见光.
(2)光催化实验结果表明,TiO2粉体在可见光下的光催化活性取决于其比表面积、可见光吸收强度和晶型结构的共同作用:光催化反应前期,经 300 ℃热处理的 TiO2粉体比表面积最大,能够更有效地吸附甲基橙分子并接受光照射,表现为光催化活性最好;光催化反应后期,经 400 ℃热处理后的 TiO2粉体显示出最好的光催化活性,其原因在于此粉体晶型结构为锐钛矿相,对可见光的吸收最强,能够有效利用可见光.
[1] FUJISHIMA A,HONDA K. Electrochemical photolysis of water at a semiconductor electrode[J]. Nature,1972,238:37-38.
[2] ANDERSSON M,ÖSTERLUND L,LJUNGSTRÖM S,et al. Preparation of nanosize anatase and rutile TiO2by hydrothermal treatment of microemulsions and their activity for photocatalytic wet oxidation of phenol[J]. J Phys Chem B,2002,106:10 674-10 679.
[3] ASAHI R,MORIKAWA T,OHWAKI T,et al. Visiblelight photocatalysis in nitrogen-doped titanium oxide[J].Science,2001,293:269-271.
[4] ANPO M,KISHIQUCHI S,ICHIHASHI Y,et al. The design and development of second-generation titanium oxide photocatalysts able to operate under visible light irradiation by applying a metal ion-implantation method[J]. Research on Chemical Intermediates,2001,27(4/5):459-467.
[5] 杨松旺,高 濂. 简单有效掺氮氧化钛纳米晶的制备及其可见光催化性能[J]. 无机材料学报,2005,20(4):785-788.
[6] IHARA T,MIYOSHI M,IRIYAMA Y,et al. Visiblelight-active titanium oxide photocatalyst realized by an oxygen-deficient structure and by nitrogen doping[J].Applied Catalysis B:Environmental,2003,42:403-409.
[7] IHARA T,MIYOSHI M,ANDO M,et al. Preparation of a visible-light-active TiO2photocatalyst by RF plasma treatment[J]. Journal of Materials Science,2001,36(17):4 201-4 207.

