带鱼下脚料水解螯合物制备及其生物特性研究
陈国章,谢 超
(1.浙江兴业集团有限公司,浙江舟山 316100;2.浙江海洋学院食品与药学学院、医学院,浙江舟山 316004)
带鱼加工过程中会产生许多下脚料,其重量约占原料鱼的40%~50%。下脚料中含有丰富的营养成分,有些组分甚至还有一定的功能特性,因而是一类重要的生物资源。长期以来,为了更有效地利用下脚料资源,研究人员进行了广泛而深入的研究。早在1940年,人们就开始研究酶降解鱼肉蛋白[1]。KRISTINSSON和RASCO[2]指出鱼蛋白酶解产物具有很多特性,并阐明了很多海洋生物酶解蛋白的生物及其功能特性。KRISTINSSON和RASCO[3]利用由4种商业酶研究了大西洋鲑鱼的酶解进程。LIASET等[4]以鳕鱼碎肉为原料,利用混合酶研究了鱼骨的酶解过程。JRON等[5]利用一系列超滤膜从酶解鳕鱼蛋白中分离出多种物质,并研究了具有转化酶抑制活性的血管紧缩素Ⅰ和其他抗氧化活性物质。邓尚贵等[6]通过复合酶手段制备得到HOP后,研究了对由环磷酰胺诱导的贫血的治疗功效。因此,为了提高带鱼下脚料利用程度,以带鱼下脚料为原料,经复合酶解途径研究亚铁螯合物的制备及其结构特点。这些螯合产物经无水乙醇分级沉淀后可得到不同成分,并对这些组分的功能特性进行了研究,将为带鱼的综合利用提供理论依据。
1 材料与方法
1.1 酶
木瓜蛋白酶(2×106IU/g)和风味酶(4×105IU/g)购于广西南宁庞博生物有限公司。最佳水解条件:pH 6.5,45℃,木瓜蛋白酶:风味酶=3:1,反应终止温度为90℃,反应时间为20 min。
1.2 原料
带鱼下脚料:由浙江兴业集团有限公司提供。原料随机分为2组(A,B)。A组原料经清洗、切碎后室温均质(3 000 r/min,30 s),贮藏于-18℃条件下备用。本组原料为未脱脂组(FM,含有4.20%的脂肪)。B组原料经清洗、切碎后,在室温条件下均质(3 000 r/min,30 s)后,用含 0.1%NaHCO3和 0.1%NaCl的溶液脱脂,再用去离子水洗涤至中性。处理后的B组原料贮藏于-18℃备用。B组原料为脱脂组(DM,含有0.60%的脂肪)。
1.3 水解产物的制备
取适量的A、B 2组原料,加入2倍体积的去离子水,调节pH为6.5。水解产物的制备参照邓尚贵等的复合酶法[7],复合酶活性比为1:1。水解结束后于90℃保持20 min以终止酶水解,冷却后过100目筛去除水解产物中的鱼骨,然后离心15 min(4,390×g)去除鱼油及未水解的鱼肉。超滤膜过滤去除分子量低于6 kDa的产物。收集水解产物于4℃条件下储存备用。
1.4 螯合修饰及组分分离
向一定的水解产物中添加1 mol/L FeCl2(1 mL),并设置不同温度和时间。沉淀A(螯合组分CA),螯合后离心15 min(4,390×g)获得。向离心后的滤出液加入无水酒精,使其浓度达到50%,静置15 min,离心15 min(4,390×g)获得沉淀B(螯合组分CB)。向滤出液中继续添加酒精使得其浓度达到80%,室温下静置15 min,产生悬浮物,分离此悬浮物即得到螯合组分CC;而螯合组分CD则沉积于容器底部,可去除溶液后直接获得。CA,CB,CC和CD于真空条件下(0.1 MPa)50℃干燥3 h后,置于硅胶干燥器保存。
1.5 分析方法
1.5.1 水解度的测定
DH=(h/ht)×100%=[(B-C)/(A-C)]×100%
式中,ht为蛋白质中的总肽键数;h为已水解的肽键数;A为原料中总氨基氮数;B为水解液的氨基氮数;C为原料游离的氨基氮数。其中,B、C由下列滴定法测得[8]:
取10 mL水解液置于100 mL容量瓶中,用去离子水定容至刻度。取20 mL稀释的溶液转移到200 mL烧杯中,加入60 mL去离子水,用0.05 mol/L NaOH溶液滴定至pH为8.2。然后加入10 mL中性甲醛,用0.05 mol/L NaOH滴定pH为9.2,所消耗氢氧化钠标准溶液的体积记为V1(mL),空白试验采用20 mL去离子水作为样品,加入甲醛后滴定至终点(pH 9.2)所消耗氢氧化钠标准溶液的体积记为V2(mL)。计算公式为:
B=[(V1-V2)×M×0.014/(m×20/100)]×100%
V1为样品加入甲醛后滴定至终点(pH 9.2)所消耗氢氧化钠标准溶液的体积;V2为空白试验加入甲醛后滴定至终点(pH 9.2)所消耗氢氧化钠标准溶液的体积;M为氢氧化钠标准溶液浓度(mol/L);0.014为氮的毫摩尔质量(g/mmol);M为测定用样品溶液相当于样品的质量(g)。
C也由上述方法测定完成,用10 mL非酶解样品替代。
1.5.2 螯合率的测定
1.5.2.1 游离铁含量的测定
精确称取0.497 g硫酸亚铁溶于100 mL水中,加入5 mL浓硫酸微热,溶解后即滴加2%高锰酸钾溶液,至最后1滴红色不褪色为止。用水定容至100 mL,摇匀,得标准贮备液。此液每mL含100 μg Fe3+。取铁标准贮备液10 mL于100 mL容量瓶中,加水至刻度,混匀,得标准工作液。此液每mL含Fe3+10 μg。精确吸取上述铁标准液 0.0、1.0、2.0、3.0、4.0、5.0 mL,分别置于 50 mL 容量瓶中,加入 1 mol/L 盐酸溶液 1 mL、10%盐酸羟铵1 mL、0.12%邻二氮菲1 mL,然后加入10%乙酸钠溶液5 mL,用水稀释至刻度,摇匀。以不加铁的空白液作对比,在510 nm波长处,用1 cm比色皿测光密度,绘制标准曲线。精确吸取滤液N mL(视含铁量而定)于50 mL容量瓶中,然后按标准曲线绘制操作,测定光密度,在标准曲线上查得相应的铁含量(μg)。
1.5.2.2 总铁含量的测定。
准确称取0.350 8 g硫酸亚铁铵,溶于25 mL 1∶1(体积比)硫酸溶液中,移入500 mL容量瓶,加水稀释至刻度。此溶液含铁0.1 mg/mL。准确移取标准贮备液10.00 mL置于100 mL容量瓶中,加水至标线摇匀。此溶液含铁 0.01 mg/mL。精密量取 0,1.0、2.0、3.0、4.0、5.0 mL 的铁标准液分别置于 510 mL 容量瓶中,加入pH 4.0的醋酸-醋酸钠缓冲液和pH 3.0的0.1%邻菲罗啉溶液,加入去离子水定容至刻度。在510 nm波长处测定吸光度,绘制标准曲线。精确吸取滤液N mL(视含铁量而定)于50 mL容量瓶中,然后按标准曲线绘制操作,测定光密度,在标准曲线上查得相应的铁含量(μg)。
1.5.2.3 螯合率的计算
CR=[(A-B)/A)]×100%
A(mg/g),样品中总 Fe2+含量,B(mg/g),样品中游离 Fe2+含量。
1.5.3 螯合组分红外光谱检测
取固体样品2 mg放入玛瑙研钵中,放入干燥的光谱纯KBr 200 mg,混合研磨均匀(在红外灯下进行),使其粒度在 2.5 μm 以下,压力约为 60 MPa,维持 3~5 min。CS,CA,CB,CC 和 CD 的结构由 IR-435 FTS-17SC 红外光谱仪(Bio-Red Co.Ltd.,USA)于 500~4 000 cm-1条件下测定。
1.5.4 抗氧化活性
抗氧化活性由硫代巴比妥酸法(TBA)测定。亚油酸的氧化测定根据OSAWA和NAMIKI[10]的方法并经少许改进:将0.2 mL亚油酸的样品加入30 mL试管中,然后加入10 mL 99.5%乙醇和10 mL 50 mol/L磷酸盐缓冲液(pH 7.0)。取样品(50 μg)加入到此混合溶液中,然后用蒸馏水定容至25 mL。将其放入到培养箱中在40℃培养7 d。TBA溶液根据OHKAWA等[9]的方法配制。该溶液含有0.8 mL水分、0.2 mL 8.1%SDS 和 1.5 mL 20%的醋酸,然后用 10 mol/L 的 NaOH 和 1.5 mL 0.8%TBA 调 pH 至 3.5。将 50 μL 的氧化性的亚油酸溶液加入到混合液中,并在5℃培养1 h,然后在100℃,加热1 h。生成的红色素采用波长535 nm测定其吸光度。结果表达为对亚油酸的氧化抑制率,采用α-生育酚作对照。抑制率的计算公式:
ROIR=[(A-B)/(A-C)]×100%
A为加50 μL去离子水,0.2 mL亚油酸的吸光值;B 为加50 μg样品,0.2 mL亚油酸的吸光值;C为加50 μL α-生育酚,0.2 mL 亚油酸的吸光值。
1.5.5 抗菌活性
抗菌能力测定方法:牛津杯双层平板法[11]。在无菌平皿中倒入10 mL加热融化的2%琼脂,待其充分冷却凝固后,放入已灭菌的牛津杯数个,并按一定次序排放整齐。将分装于大试管中的15 mL固体检测培养基融化后冷却至50℃左右,加入108个/mL指示菌液1 mL,迅速混合均匀,倒入平皿。冷却后,用无菌镊子取出牛津杯,作为螯合组分活性检测平板。用0.1 mL吸管吸取100~200 μL待测样品,以无菌操作加入到检测平板圆孔内,37℃培养15 h,观察并测定抑菌圈直径(mm)。
2 结果与讨论
2.1 原料脂肪含量对水解的影响
由图1和图2得出,FM的水解曲线可以分为两部分,第一部分为快速阶段(1~9 h),大量肽键遭到破坏;第二阶段反应速度明显减慢(9~20 h),仅有少量肽键遭到破坏。FM的水解曲线从第3 h开始就明显高于DM的曲线。但由于脂肪得到去除,DM的水解曲线中水解度和水解时间呈现一个典型的线性关系。这是因为DM中一些可溶性蛋白和脂肪被去除的缘故。
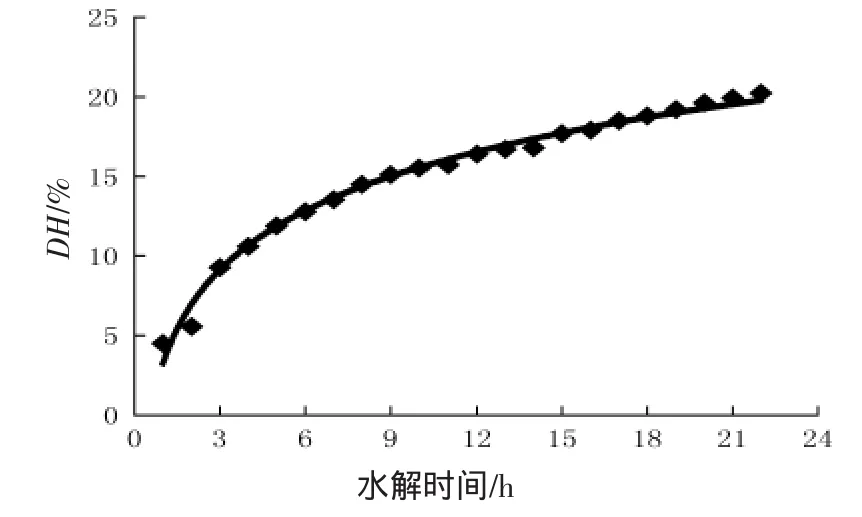
图1 水解时间与DH关系曲线(未脱脂)Fig.1 The relation of hydrolyzed time on DH(fatty)
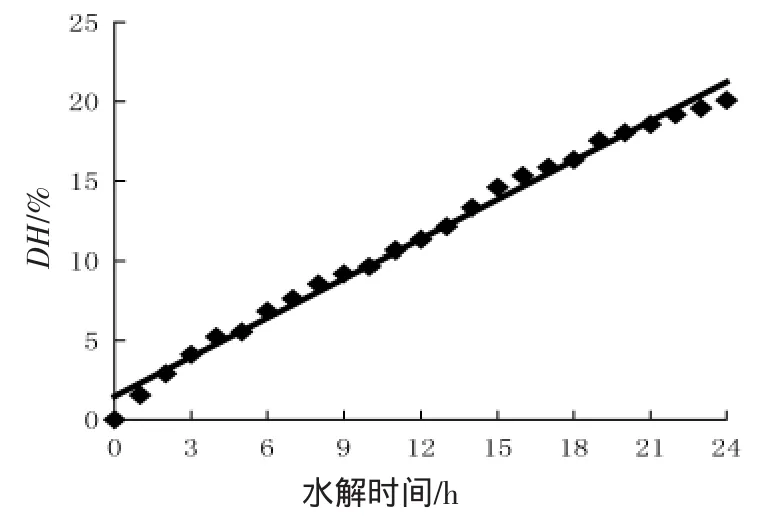
图2 水解时间与DH关系曲线(脱脂)Fig.2 The relation of hydrolyzed time on DH(defatted)
2.2 螯合条件的选择
2.2.1 螯合所需要的 DH 的确定
由图3可知,FM和DM的水解度低于5%时有最高的螯合率。结果显示最佳水解度为5%,在此条件下水解产物可以为Fe2+提供足够的反应底物。
2.2.2 螯合 pH 的确定
如图4所示,FM和DM的螯合率迅速增加,同时pH从4.0增加到7.0,pH达到7.0后迅速降低。螯合率增加的原因是水解产物氨基和羧基的螯合能力随着pH从4.0增加到7.0而增强,而当pH达到7.0后螯合率降低是由于Fe2+与OH-更容易结合形成Fe(OH)2。因此螯合最佳pH为7.0。
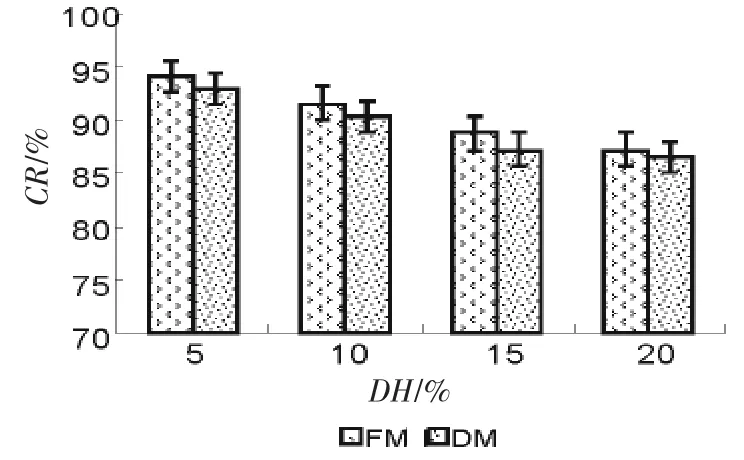
图3 不同原料种不同DH和CR的关系Fig.3 Effect of DH on chelating Fe2+
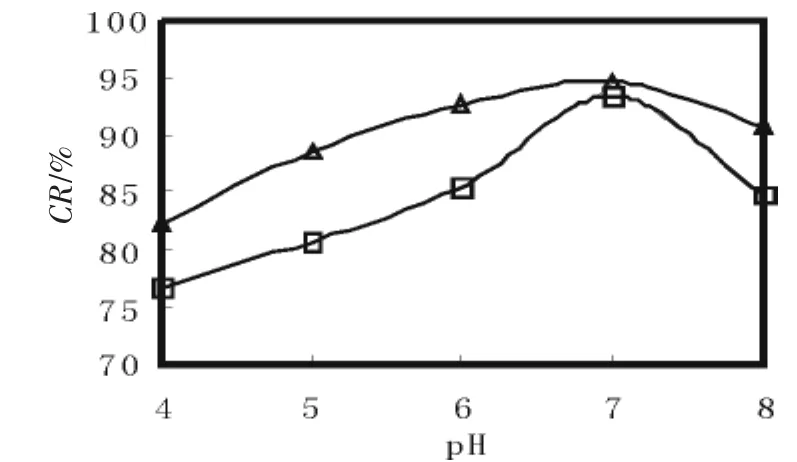
图4 pH对亚铁离子螯合率的影响(DH=5%)Fig.4 Effect of pH on chelating Fe2+(DH=5%)
2.2.3 螯合温度与螯合时间的确定
由图5和图6可知,随着温度由10℃增加到50℃,螯合时间由10 min增加到90 min,FM和DM中Fe2+的螯合率变化很小。这些结果表明温度和时间对螯合过程没有显著影响。所以建议10℃和15 min为螯合所需要的温度和时间条件。
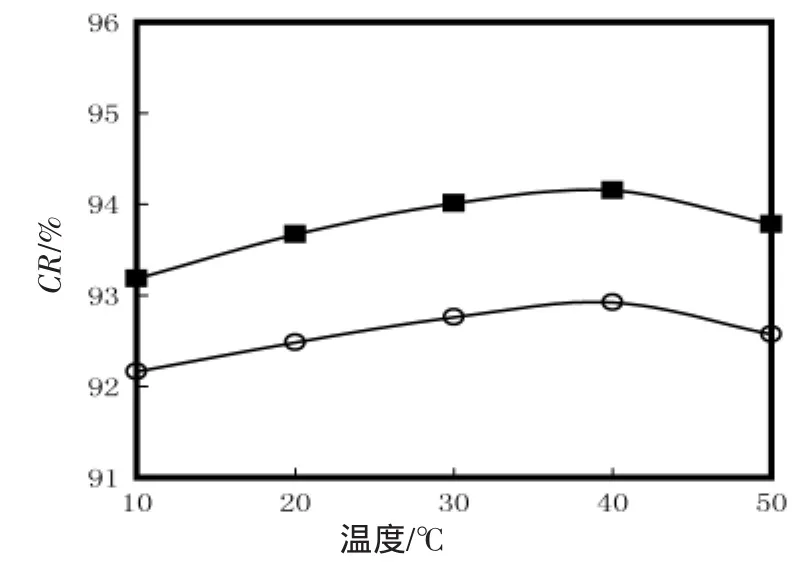
图5 温度对亚铁离子螯合率的影响Fig.5 Effect of temperature on chelating Fe2+
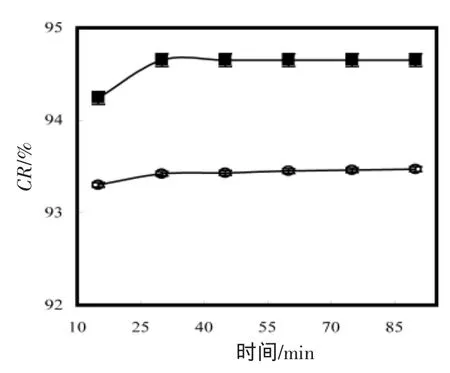
图6 时间对亚铁离子螯合率的影响Fig.6 Effect of time on chelating Fe2+
2.3 螯合物的结构分析
图7为蛋白质水解物样品(CS)、CA,CB,CC和CD的红外光谱图。同样品相比,CA,CB,CC和CD的NH4+的吸收光谱带(3 130~3 030 cm-1)消失,而 PtNH2的吸收光谱带(约为1 100 cm-1)得到明显显现,提示Fe2+与氨基已紧密结合。CA,CB,CC和CD有2个强烈的羧基吸收峰:羧基离子反对称振动(γascoo-)于1 650 cm-1附近,羧基离子的对称振动(γscoo-)于1 400 cm-1附近,且CA,CB,CC和 CD 的△υ(γascoo--γscoo-)分别为 235,250,250 和 250 cm-1,提示Fe2+与羧基是以单齿共价键的方式结合。CA,CB,CC和CD具有不同的溶解性可能是由于它们的铁含量不同因而溶解性差异明显。
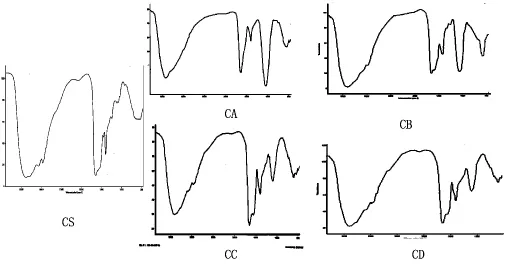
图7 CS、CA、CB、CC、CD 螯合样品的红外光谱分析Fig.7 IR spectra of CS,CA,CB,CC,CD peptides chelating Fe2+
2.4 螯合组分的抗氧化性
蛋白质、水解产物或者酶解物亚铁螯合组分具有其它一些功能性性质。在本文中,笔者研究了带鱼下脚料水解物4种酶解物亚铁螯合组分(CA,CB,CC和CD)的抗氧化活性,并同初始样品和a-生育酚进行了比较,如图8所示。CB的抗氧化活性最高,其抗氧化活性约为初始样品的1.3倍,为a-生育酚抗氧化活性的92%。CA和CB疏水性更强,原因是它们富含组氨酸,且它们的螯合环增强了组氨酸咪唑环的抗氧化能力。因此CA和CB可以用作天然抗氧化剂。同CA和CB相比,CC和CD具有较好的亲水性,在水环境中可溶。这些提示CC和CD可能主要由亲水氨基酸如天冬氨酸、谷氨酸、氨基乙酸、丙氨酸、苏氨酸和丝氨酸等组成,仅含有少量组氨酸[26]。所以CC和CD可以作为亲水性的天然抗氧化剂。
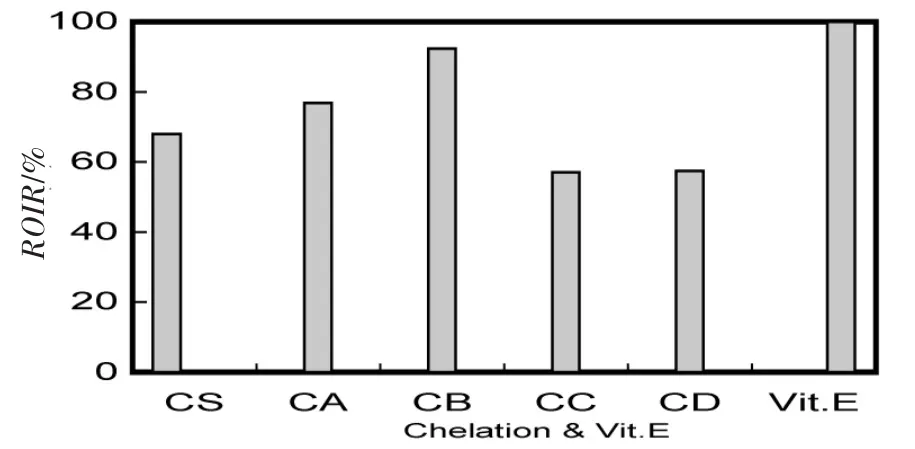
图8 螯合组分的抗氧化活性Fig.8 Antioxidative activities of peptides and peptides chelating Fe2+
2.5 螯合组分的抗菌活性
酶解物亚铁螯合组分和初试样品的抗菌活性见表1。CA对大肠杆菌、金黄色葡萄球菌、沙门氏菌和枯草芽胞杆菌无任何抗菌活性。而CB对大肠杆菌具有较弱的抗菌活性,CC对上述4种细菌也具有微弱抗菌活性。在所有4种螯合组分中,CD对4种细菌均有抗菌活性,抗菌活性最高。试验结果显示酶解物亚铁螯合组分具有一定的抗菌活性,这种活性取决于螯合组分的亲水性。所以在食品工业中,CD可以用作亲水性的天然抗菌剂。
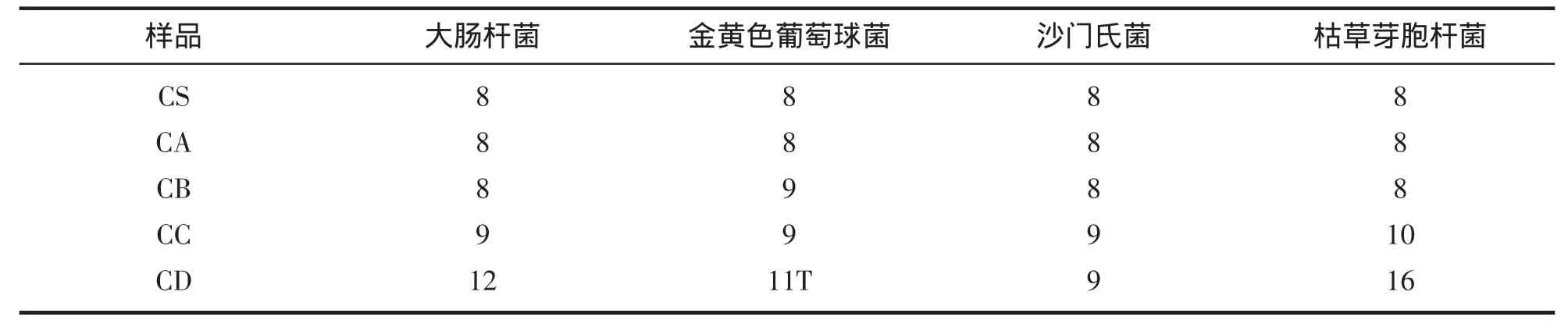
表1 酶解物亚铁螯合组分对大肠杆菌、金黄色葡萄球菌、沙门氏菌和枯草芽胞杆菌的抑菌圈直径Tab.1 The diameter of antibacterial against Escherichia coli,Staphylococcus aureus,Salmbnella typhi,Bacillus subtilis by peptides chelating Fe2+mm
3 结论
(1)酶解后通过分析发现水解时间和水解度的关系可以表达为DH=5.388 4 lnX+2.636 2(R2=0.992 3)(未脱脂),DH=0.815 7 X+1.086 4(R2=0.993 3()脱脂)。未脱脂原料的酶解物亚铁修饰制备条件为:水解度5%,pH 7.0,20℃,螯合时间15 min。通过无水乙醇沉淀可获得4种以未脱脂鱼肉为原料的螯合组分,即CA,CB,CC和CD。
(2)所有4种亚铁螯合组分都具有显著的抗氧化活性,可以用作亲水或疏水的天然抗氧化剂。在这4种螯合组分中,CB抗氧化活性最高,达到a-生育酚抗氧化活性的92%。同时,在这4种螯合组分中,CD对大肠杆菌、沙门氏菌、金黄色葡萄球菌和枯草芽胞杆菌的抗菌活性最强,可以作为天然抗菌剂。
[1]TARR H L A.Possibilities in developing fisheries by-products[A].Food Techol,1948,2:268-277.
[2]KRISTINSSON H G,RASCO B A.Fish protein hydrolysates:production,biochemical,and functional properties[J].CRC Crit Rev Food Sci Nutr,2000,40:43-81.
[3]KRISTINSSON H G,RASCO B A.Biochemical and functional properties of Atlantic salmon(Salmo salar)muscle proteins hydrolyzed with various alkaline proteases[J].Agric Food Chem,2000;48:657-666.
[4]LIASET B,LIED E,ESPE M.Enzymatic hydrolysis of by-products from the fish-filleting industry;chemical characterisation and nutritional evaluation[J].Sci Food Agric,2000,80:581-589.
[5]JEON Y J,BYUN H G,KIM S K.Improvement of functional properties of cod frame protein hydrolysates using ultrafiltration membranes[J].Process Biochemistry,1999,35:471-478.
[6]DENG S G,PENG Z Y,CHEN F,et al.Amino acids composition and anti-anaemia action of hydrolyzed offal protein from Harengula zunasi Bleeker[J].Food Chemistry,2004,87(1):97-102.
[7]DENG S G,PENG Z Y,CHEN F,et al.Hydrolysis dynamics model of protein from Harengula zunasi by compound enzymes[J].Zhanjiang Ocean University,2004,24(4):28-32.
[8]ZHAO H G,HUANG M R.Aquatic product inspection[M].1st ed.Tianjin:Tianjin Science and Technology Press,1987:165-166.
[9]OHKAWA H,OHISHI N,YAGI K.Assay for lipid peroxides in animal tissues by thiobarbituric acid reaction[J].Anal Biochem,1979,95:351-358.
[10]OSAWA T,NAMIKI M.A novel type of antioxidant isolated from leaf wax of eucalyptus leaves[J].Agric Biol Chem,1981,45:735-73.
[11]HE N,WANG C L,GU X B,et al.Study on the optimization of the activity of lactobacillin with well test[J].Tianjin Institute of Light Industry,1999,2:17-20.

