锂离子电池电解液LiTFSI/EMI-TFSI的性能
谭晓兰,尹鸽平,马玉林
(哈尔滨工业大学化工学院,黑龙江哈尔滨 150001)
离子液体[1-3]用作锂离子电池电解液备受关注[4-5]。离子液体的合成方法大体上有直接合成法和两步合成法[6]。
直接合成法通过酸碱中和反应或季铵化反应,一步合成离子液体,操作经济简便,没有副产物,产品易纯化。若直接合成法难以得到目标产物,就要使用两步合成法。首先通过季铵化反应制备出含目标阳离子的卤盐([阳离子]X型离子液体),然后用目标阴离子Y-置换出X-离子或加入Lewis酸MXY,得到目标产物。
本文作者通过直接合成法制备了离子液体二(三氟甲基磺酰)1-乙基-3-甲基咪唑(EMI-TFSI),研究了制备工艺及1 mol/L二(三氟甲基磺酰)锂(LiTFSI)/EMI-TFSI作为锂离子电池电解液的性能。
1 实验
1.1 离子液体的制备
称取一定量的溴化1-乙基-3-甲基咪唑(EM ImBr,杭州产,电池级)和 LiTFSI(美国产,电池级),分别用超纯水溶解后,混合搅拌(600 r/min),待静置分层后,用分液漏斗把油性离子液体相与水相分离,用超纯水洗涤油相4~5次,再在100℃下真空(-0.1 MPa)干燥10 h,得到澄清的油状离子液体 EMI-TFSI。将2 mmol LiTFSI溶于2 ml制备的EMITFSI中,得到 1 mol/L LiTFSI/EMI-TFSI。
1.2 电化学性能测试
采用电化学阻抗谱法,用DDS-11A电导率仪(上海产)测试EMI-TFSI和电解液1 mol/L LiTFSI/EMI-TFSI的电导率(σ)。体系为不锈钢|电解液|不锈钢,频率为1~105Hz,每个测量温度(15~85℃)下保持15 min。σ由式(1)计算。

式(1)中,R为电解液的电阻,S为不锈钢的表面积,L为不锈钢片的间距。
采用循环伏安和核磁共振(NM R)检测EMI-TFSI的纯度。循环伏安的研究电极为铂丝(日本产,99.99%),参比电极和辅助电极分别为银丝(美国产,99.99%)和银网(美国产,99.99%),扫描范围为-2.5~3.0 V(vs.Ag+/Ag),扫描速度为50 mV/s。以氘代氯仿(CDCl3,德国产,99.8%)为溶剂,采用Av300核磁共振仪(德国产)测定 EMI-TFSI的1HNMR谱图,测试温度为26℃,测试频率为 300 MHz。循环伏安测试在CHI604B电化学工作站(上海产)上进行。
以1 mol/L LiTFSI/EMI-TFSI为电解液,金属锂(成都产,99.9%)为对电极,LiCoO2(山西产,电池级)或Li4Ti5O12(哈尔滨产,电池级)为研究电极,分别组装成Li/LiCoO2、Li/Li4Ti5O12半电池。在1 mol/L LiTFSI/EMI-TFSI中分别加入5%双草酸硼酸锂(LiBOB,德国产,电池级),5%碳酸亚乙烯酯(VC,北京产,电池级),分别以1 mol/L LiTFSI/EMITFSI、1 mol/L LiTFSI/EM I-TFSI+5%LiBOB 以及 1 mol/L LiTFSI/EMI-TFSI+5%VC为电解液,石墨(哈尔滨产,电池级)为研究电极,组装Li/C半电池,进行循环性能测试。所有半电池循环性能测试均在BTS 5V3mA充放电测试仪(深圳产)上进行。Li/LiCoO2、Li/Li4Ti5O12半电池循环伏安扫描的电位范围分别为 2.7~4.5 V(vs.Li+/Li)和1.0~2.5 V(vs.Li+/Li),扫描速度均为0.2 mV/s。
2 结果与讨论
2.1 离子液体的产率
离子液体(EMI-TFSI)的产率(η)由式(2)计算。

式(2)中,m为实际制备的油状液体的质量;ME-T为EMI-TFSI的摩尔质量(391 g/mol),mE-Br为称取 EMImBr的质量;ME-Br为EMImBr的摩尔质量(191 g/mol)。表1为 η与n(EM ImBr)∶n(LiTFSI)、搅拌时间(t)的关系。

表1 η与n(EMImBr)∶n(LiTFSI)、搅拌时间(t)的关系Table 1 The relation among n(EMImBr)∶n(LiTFSI),stirring time(t)and the reaction yield(η)
从表1可知,η随着t的延长而增加,12 h后基本不再变化,并随EMImBr比例的提高而增加。EMImBr不能被水洗除掉,因此一定要比 LiTFSI少;Br-与 EMI-TFSI中的微量水反应生成HBr,会影响离子液体的性能。当n(EMImBr)∶n(LiTFSI)=9.95∶10.00、t为12 h时,η有最大值86.4%。
2.2 离子液体的纯度
1 mol/L LiTFSI/EMI-TFSI的循环伏安曲线见图1,图2为 1 mol/L LiTFSI/EMI-TFSI的1H-NM R谱图。

图1 1 mol/L LiTFSI/EM I-TFSI的循环伏安曲线Fig.1 CV curves of 1 mol/L LiTFSI/EMI-TFSI
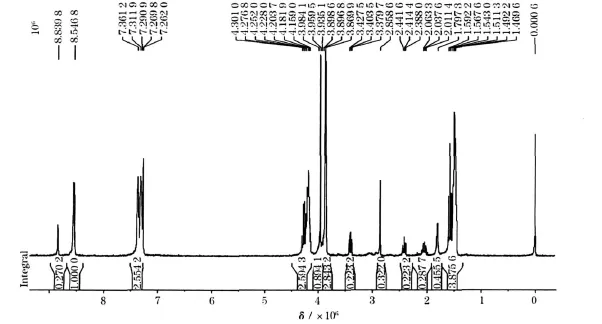
图2 离子液体EMI-TFSI的1H-NMR谱图Fig.2 1H-NM R spectrum of ionic liquid EMI-TFSI
从图1可知,1 mol/L LiTFSI/EMI-TFSI的氧化、还原电位分别为2.4 V和-1.9 V,电化学稳定窗口约4.3 V。由于Ag+/Ag与 Li+/Li的电位差约 3.2 V,该体系的还原电位相对于Li+/Li约 1.3 V,不能以石墨为负极材料。图 1中平台区的电流很小,说明此处几乎无电化学反应,与文献[7]的结果基本相同,可预计制备的离子液体纯度较高。
1H-NMR谱图(图2)的具体分析结果见表2,其中δ为化学位移,J为耦合常数。

表2 1H-NMR峰位移分析结果Table 2 Analyses results of1H-NMR peak shift
图2和表2的分析结果,与文献[8]中离子液体 EMITFSI的特征峰基本一致,说明制备的离子液体纯度较高。
2.3 电导率
EMI-TFSI和 1 mol/L LiTFSI/EMI-TFSI在不同温度下的电导率见图3。

图3 离子液体在不同温度下的电导率Fig.3 The conductivity of ionic liquid at different temperatures
在离子液体EM I-TFSI中,有EMI+、TFSI-两种离子导电,在电解液 1 mol/L LiTFSI/EM I-TFSI中,有 Li+、EMI+和TFSI-等3种离子导电。从图3可知,无论是否加入锂盐,离子液体的电导率均随着温度的升高而升高。这是因为随着温度升高,体系的黏度降低,离子的溶剂化、离子对的离解度及溶剂化离子的迁移速度都会增大。当温度为15~85℃时,EMI-TFSI的电导率为 6~33 mS/cm;加入锂盐后,溶剂化的Li+增多,增强了与溶剂分子之间的相互作用,使迁移阻力增加,移动速率降低,电导率下降为2~15 mS/cm。
2.4 电池测试
2.4.1 循环伏安测试
Li/LiCoO2、Li/Li4Ti5O12半电池前3次循环的循环伏安曲线见图4。

图4 Li/LiCoO2、Li/Li4Ti5O12半电池的循环伏安曲线Fig.4 CV curves of Li/LiCoO2and Li/Li4Ti5O12half cells
从图 4可知,两种体系在 1 mol/L LiTFSI/EMI-TFSI中的稳定性都比较好,首次循环后的曲线几乎重合。LiCoO2在1 mol/L LiTFSI/EMI-TFSI中的氧化、还原电位分别为4.3 V和3.6 V,氧化和还原都只有1个峰且电流值不很大。离子液体的黏度比商用电解液大,导致 Li4Ti5O12在1 mol/L LiTFSI/EMI-TFSI中的可逆性相对差些,氧化、还原电位分别为2.0 V和1.2 V。
2.4.2 倍率性能
Li/LiCoO2、Li/Li4Ti5O12半电池在不同倍率下的首次充放电曲线见图5。

图5 Li/LiCoO2、Li/Li4Ti5O12半电池的首次充放电曲线Fig.5 The initial charge-discharge curves of Li/LiCoO2and Li/Li4Ti5O12half cells
从图5a可知,3种倍率下LiCoO2充电平台的电位基本一致(4.0 V),1/8 C、1/4 C时放电平台的电位基本一致,但1/2 C时放电平台的电位明显负移。1/8 C、1/4 C和1/2 C时的首次放电比容量分别为 144.3 mAh/g、142.2 mAh/g和145.7 mAh/g,首次库仑效率分别为 96.1%、93.4%和91.6%,说明电解液 1 mol/L LiTFSI/EMI-TFSI对 LiCoO2的库仑效率影响不大。从图5b可知,3种倍率下Li4Ti5O12放电平台的电位基本一致(1.5 V),但逐渐变短,导致嵌锂量逐渐减少,1/4 C、1/2 C时充电平台的电位一致,均较1/8 C时正移,平台宽度也短些。充电比容量从1/8 C时的167.4 mAh/g下降到1/2 C时的141.1 mAh/g,可能是大电流使脱锂不完全造成的。1/8 C、1/4 C和1/2 C时的首次库仑效率分别为63.5%、69.0%和78.9%。
2.4.3 循环性能
Li/LiCoO2、Li/Li4Ti5O12半电池在不同倍率下的循环性能见图6。

图6 Li/LiCoO2、Li/Li4Ti5O12半电池的循环性能Fig.6 Cycle performance of Li/LiCoO2and Li/Li4Ti5O12half cells
从图6可知,LiCoO2在1 mol/L LiTFSI/EMI-TFSI电解液中比容量衰减明显,以 1/8 C、1/4 C和1/2 C充放电,20次循环分别衰减约25 mAh/g、30 mAh/g和 35 mAh/g,表明1 mol/L LiTFSI/EMI-TFSI与 LiCoO2的兼容性不好。Li4Ti5O12在 1 mol/L LiTFSI/EMI-TFSI中循环 20次,比容量没有衰减,且有微弱的上升趋势,以1/8 C充放电的比容量最高约为170 mAh/g,以1/2 C充放电的比容量相对较低,最高约为140 mAh/g,表明Li4Ti5O12与 1 mol/L LiTFSI/EMI-TFSI的兼容性优于 LiCoO2。
2.4.4 添加剂的影响
将成膜添加剂LiBOB、VC加到1 mol/L LiTFSI/EMITFSI中,并与不含添加剂的 1 mol/L LiTFSI/EMI-TFSI体系进行比较,结果见图7。

图7 石墨在不同电解液中的首次充放电曲线和循环性能Fig.7 The initial charge-discharge curves and cycle performance of graphite in different electrolytes
从图7a可知,在1 mol/L LiTFSI/EMI-TFSI和1 mol/L LiTFSI/EMI-TFSI+5%LiBOB中,首次放电平台都比较长,但没有充电平台,原因是与Li+共嵌,电解液发生了还原分解。在1 mol/L LiTFSI/EMI-TFSI+5%VC中,首次充放电性能较好,充放电平台电位几乎一致,均约为0.1 V,但首次库仑效率仅有71.0%。从图7b可知,石墨在1 mol/L LiTFSI/EMI-TFSI+5%VC的循环性能较好,比容量能稳定在约300 mAh/g,说明加入VC降低了EMI-TFSI的还原电位,即成膜效果较好。
3 结论
研究了离子液体EMI-TFSI的制备及电解液1 mol/L LiTFSI/EMI-TFSI在锂离子电池中的应用。EMI-TFSI的产率与搅拌时间、n(EMImBr)∶n(LiTFSI)有关。当n(EMImBr)∶n(LiTFSI)=9.95∶10.00、搅拌时间为 12 h 时,产率达到最大值86.4%;EMI-TFSI的电化学窗口达4.3 V,在室温下的电导率可达10 mS/cm,1 mol/L LiTFSI/EMITFSI的电导率为 3 mS/cm。LiCoO2在 1 mol/L LiTFSI/EMI-TFSI中循环,容量发生了明显的衰减,而Li4Ti5O12没有衰减,1/8 C时为170 mAh/g;石墨在1 mol/L LiTFSI/EMI-TFSI+5%VC中的循环性能较好,比容量可达约300 mAh/g,在20次循环内没有衰减。
[1]YANG Wen-zhong(杨文忠),ZHUANG Cheng(庄澄),WANG Jin-tang(王锦堂),et al.离子液体作为锂离子电池电解液[J].Battery Bimonthly(电池),2008,38(4):228-230.
[2]Toshinori S,Yosuke A,M anabu K,et al.Ionic liquid electrolyte systems based on bis(fluorosulfonyl)imide for lithium-ion batteries[J].J Power Sources,2009,189(1):802-805.
[3]Masashi I,Toshinori S,Manabu K,et al.Pure ionic liquid electrolytes compatible with a graphitized carbon negative electrode in rechargeable lithium-ion batteries[J].J Power Sources,2006,162(1):658-662.
[4]Diawa M,Chagnes A,Carré B,et al.Mixed ionic liquid as electrolyte for lithium batteries[J].J Power Sources,2005,146(1-2):682-684.
[5]ZHENG Hong-he(郑洪河),SHI Jing(石静),LIU Yun-wei(刘云伟),et al.室温离子液体电解质与锂离子电池碳负极材料的相容性[J].Chemistry(化学通报),2008,71(7):488-490.
[6]ZHANG Ying-feng(张英锋),LI Chang-jiang(李长江),BAO Fushan(包富山),et al.离子液体的分类、合成与应用[J].Chinese Journal of Chemistry Education(化学教育),2005,26(2):7-12.
[7]Garcia B,Lavallée S,Perron G,et al.Room temperature molten salts as lithium battery electrolyte[J].Electrochim Acta,2004,49(26):4 583-4 588.
[8]Bonhô te P,Dias A P,Papageorgiou N,et al.Hydrophobic,highly conductive ambient-temperature molten salts[J].Inorg Chem,1996,35(5):1 168-1 178.

