盐酸普罗帕酮的核磁共振谱分析
薛民杰/上海市计量测试技术研究院
0 引言
盐酸普罗帕酮(Propafenone Hydrochloride),化学名称为3-苯基-1-[2-[3-(丙胺基)-2-羟基丙氧基]-苯基-1-丙酮盐酸盐(图1),是一种抗心律失常药物,主要用于治疗快速室上性心律失常等症状。据文献报道,盐酸普罗帕酮通过相转移催化合成的方法进行制备[1,2],合成反应中会带入环氧酚类杂质[3]。随着相转移催化合成中催化剂种类的增多,有必要建立一个对该化合物结构鉴定分析方法。本文采用核磁共振1H-1H COSY、13C-1H HSQC和13C-1H HMBC等二维实验方法对盐酸普罗帕酮的氢谱与碳谱进行完全归属,这一结果可以作为盐酸普罗帕酮药物定性与纯度分析的科学依据。

图1 盐酸普罗帕酮分子结构示意图
1 实验部分
Varian NMR System 500 MHz(美国Varian公司),使用1H-19F/15N-31P 5mm带梯度双宽带正向探头,1HNMR和13CNMR的观测频率分别为499.77 MHz和125.68 MHz。1H和13C实验采用标准脉冲程序,二维实验应用梯度场来实现快速采样,所用脉冲序列为gCOSY[4]、gHSQC[5]和gHMBC[6]。实验溶剂为DMSO-d6,该溶剂用来锁场,内标化学位移定为2.50 ppm(1H)和39.60 ppm(13C)。实验温度为室温。
实验样品采用USP标准样品。
2 结果与讨论
2.1 盐酸普罗帕酮氢谱分析
为了解析盐酸普罗帕酮的结构,首先要解析出盐酸普罗帕酮的氢谱特征结构,盐酸普罗帕酮氢谱如图2所示,其中,a)为DMSO-d6溶剂,b)为DMSO-d6溶剂加少量D2O。由于δ9.00和δ5.95两组峰分别在D2O交换氢离子中消失,显示δ9.00、δ5.95和δ3.35这三组质子为活泼氢,根据氢谱特征化学位移,可以把δ9.00归属为盐酸质子,δ5.95归属为羟基氢,δ3.35归属为胺基氢。δ(7.02~7.55)区间内的4组峰积分面积与盐酸普罗帕酮中芳环上的氢原子数目相同,从化学位移的特征上来看,该4组峰应归属于盐酸普罗帕酮芳环氢原子,其他质子峰为烷烃链段上的峰。δ0.88的三重峰积分面积为3,鉴于盐酸普罗帕酮化学结构中只有一个-CH3,该三重峰归属为H-19。
2.2 盐酸普罗帕酮的1H-1H COSY谱图分析
图3为盐酸普罗帕酮1H-1H COSY谱。由图3可知,δ0.88峰和δ1.64多重峰相关,后者与δ2.74三重峰相关,可知三者成为A3B2C2自旋系统[7],由δ1.64和δ2.74的氢谱峰积分面积和相关峰相互关系,该两组峰归属为H-18和H-17。δ5.95处-OH峰与δ4.28多重峰相关,并且该相互关系为-OH唯一相关峰,故后者归属为手性氢原子H-15。
2.3 盐酸普罗帕酮的13C-1H HSQC与13C-1H HMBC谱图分析

图2 盐酸普罗帕酮1H谱,a)DMSO-d6溶剂,b)DMSO-d6+D2O溶剂
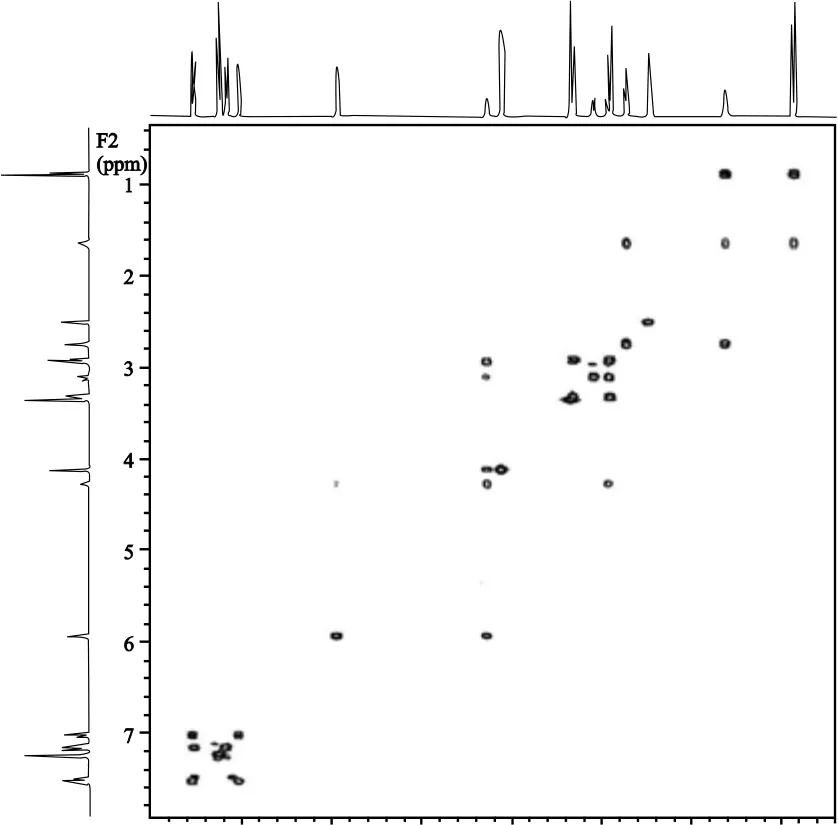
图3 盐酸普罗帕酮1H-1H COSY谱
图4、图5、图6和图7为盐酸普罗帕酮13C、13C DEPT、13C-1H HSQC与13C-1H HMBC谱。 为了解析异核二维谱图,首先要对13C谱中特征峰进行判别。比较图4和图5,可知δ128.01、δ141.29、δ157.07和 δ201.07为 季 碳 峰, 相对应的碳原子为季碳原子,其中δ201.07为羰基 C-7。由图6可知,F2维上δ0.88、δ1.64、δ2.74和δ4.28的1H峰分别与F1维上δ10.97、δ18.71、δ48.79和δ64.79的13C峰形成相关关系,因此这4条13C峰可以归属为C-19、C-18、C-17和C-15。
由图3可知,手性H-15(δ4.28)分别与δ4.13和δ3.021H-1H相关,13C-1H HMBC实验(图7)证实,1Hδ4.13与13Cδ157.07存在多键相关信号,而1Hδ3.02与低场13C峰没有相关峰出现,故可以将δ4.13和δ3.02归属为H-14和H-16。图6显示,这两组1H分别与δ70.38和δ49.72两条13C峰有相关信号,δ70.38和δ49.72归属为 C-14和C-16。

图4 盐酸普罗帕酮13C谱
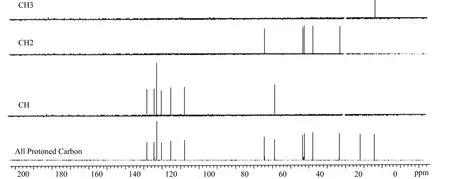
图5 盐酸普罗帕酮13C DEPT谱
图4中,高场区域δ44.46和δ29.63应属于烷烃链段13C峰,图7提示,13Cδ29.63峰与芳烃链段上的1Hδ7.26多重峰存在多键13C-1H相关,因此13Cδ29.63归属为C-5,13Cδ44.46归属为C-6,通过13C-1H HSQC实验(图6)可以通过13C-1H单键相关信号将1Hδ2.92(三重峰)和δ3.32(三重峰)分别归属为H-5和H-6。
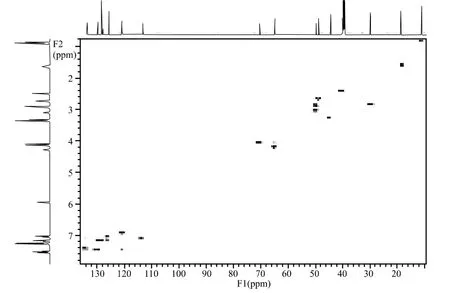
图6 盐酸普罗帕酮13C-1H HSQC谱
盐酸普罗帕酮的化学结构(图1)中,存在2个化学环境完全不同的芳环,导致1H谱和13C谱低场区域谱峰较多,并且峰形较为复杂,如不借助二维实验方法,归属谱峰难度较大。由图7可知,羰基碳(C-7)与1H谱芳环区域中δ7.52峰产生13C-1H多键相关,结合图6上的相关信号,1Hδ7.54(两重峰)和13Cδ129.62归属为H-9和C-9。采用同样的方法,通过13C-1H HMBC实验(图7)将多键相关信息联系起来,从H-9出发,依次得到芳环上碳原子与氢原子的化学位移归属,1Hδ7.51、δ7.17和δ7.04分别归属于H-10(三重峰)、H-12(两重峰)和 H-11(三重峰),13Cδ157.07、δ133.58、δ128.01、δ120.78和δ113.22分别归属于 C-13、C-10、C-8、C-12 和 C-11。

图7 盐酸普罗帕酮13C-1H HMBC谱
1H(图1)中低场芳环区域剩余1Hδ7.26(多重峰)归属于H-2和H-3,δ7.14(两重峰)归属于H-1。通过13C-1H HSQC实验(图6),可以将δ125.76归属于C-1。H-2和H-3四个氢原子在1H谱中产生交叠现象,主要是由化学环境相似导致,但在13C谱中,C-2和C-3为分开的两条13C峰,据文献报道[8],δ128.32和δ128.27分别归属于C-3和C-2。由图7可知,13Cδ141.29与H-2和H-3存在唯一多键相关信号,该季碳峰归属为C-4。
至此盐酸普罗帕酮的1H谱和13C谱得到了完全归属,以上结果列于表1和表2,从而为此类化合物的核磁共振谱的分析提供了参考。
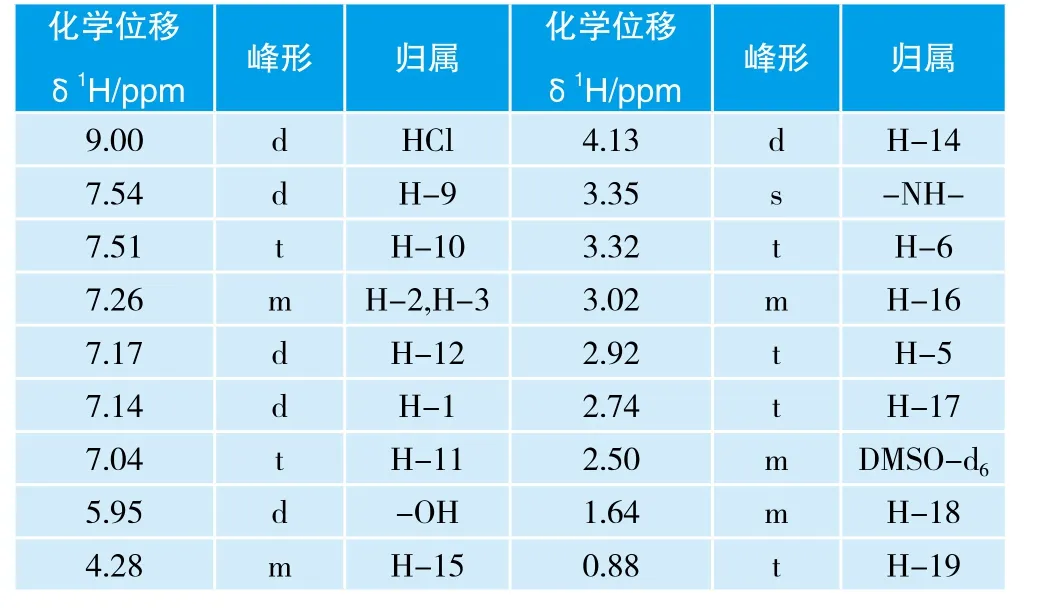
表1 盐酸普罗帕酮1H谱信息与数据
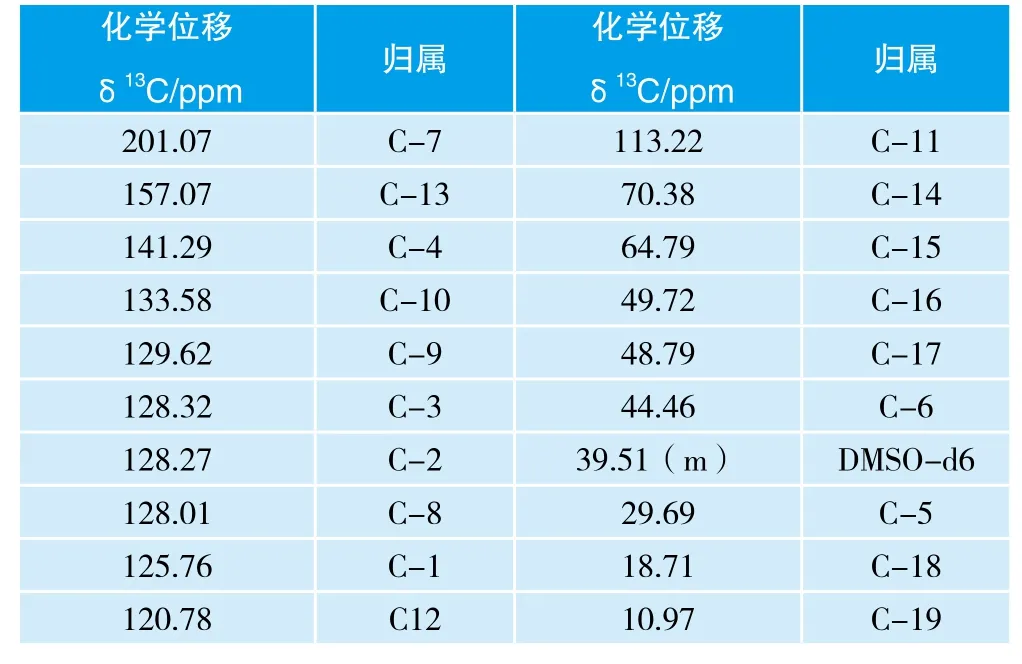
表2 盐酸普罗帕酮13C谱信息与数据
[1]王文洲,曹胜利,潘长敏.盐酸普罗帕酮的合成[J].中国医药工业杂志,1992,23(5).
[2]刘润涛,曹胜利,陈恒昌,刘振中.盐酸普罗帕酮的相转移催化合成[J].中国医药工业杂志,1994,25(6).
[3]邵泓,汪洁.盐酸普罗帕酮片及注射液的HPLC测定[J].中国医药工业杂志,2001,32(10).
[4]R.E.Hurd.Gradient-enhanced Spectroscopy[J].J Magn Reson, 1990,87,422.
[5]L.E.Kay, P.Keifer, T.Saarinen.Pure Absorption Gradient Enhanced Heteronuclear Single Quantum Correlation Spectroscopy with Improved Sensitivity[J].J Am Chem Soc, 1992, 114, 10663.
[6]W Willker, D Leibfritz, R Kerssebaum, et al.Gradient Selection in Inverse Heteronuclear Correlation Spectroscopy[J].Magn Reson Chem, 1993, 31, 287.
[7]M Balci.Basic1H- and13C-NMR Spectroscopy[M].US, ELSEVIER,2005.
[8]R M Silverstein, F X Webster, D J Kiemle.Spectrometric Identification of Organic Compounds[M].7th Edition, US, JOHN WILEY & SONS,INC, 2005.

