如何通过分子式直接推断分子的立体结构
周冬梅
(江苏省如皋市第一中学江苏如皋226500)
如何通过分子式直接推断分子的立体结构
周冬梅
(江苏省如皋市第一中学江苏如皋226500)
教材在介绍分子立体结构模型时先给出了分子的分子式和结构式后介绍了有关分子的立体结构,所以有些学生在学习这部分内容时常常会从结构式着手推分子立体结构,其实这只是一部分同学学习过程中的一个误区。应用价层电子对互斥理论推测ABn型分子的立体结构模型时,只要知道分子式就能确定分子的立体结构。学生在学习过程中只要清楚这样几个关系式就可以了。
一、VSEPR模型的确定
早在1940年,希吉维克和坡维尔在总结实验事实的基础上提出一种简单的理论模型,用以预测简单分子或离子的立体结构,这种理论模型经过吉例斯比和尼霍尔姆在20世纪50年代加以发展,定名为价层电子对互斥理论模型,简称为VSFPR模型。其理论依据是:分子中的价电子(包括σ键电子对和孤对电子对)由于相互排斥作用,而取向彼此远离以减小斥力,分子尽可能采取对称的空间构型。也就是说对于ABn型分子(A是中心原子,B是配位原子)要确定其分子立体结构,只要能确定其价层电子对就可以了,要确定价层电子对首先要清楚这样一个关系:
价层电子对=σ键电子对+孤对电子对
接下来我们需要解决的问题就是如何确定σ键电子对和孤对电子对。对于σ键电子对根据共价键的知识可知:共价单键都是σ键;共价双键中一个是σ键,另一个是π键;共价三键是由一个σ键和两个π键组成。也就是说,中心原子不管以什么键型与配位原子相连,中心原子每连接一个配位原子就有一个σ键。所以我们又可以得出这样一个关系:

我们还需要解决的另外一个问题就是如何确定中心原子上的孤对电子对,我们可以通过这样一个通式:
孤对电子对=(A的价电子数-∑B达稳定结构所需电子数×B原子数+/-离子电荷相应电荷数)/2
对于这个通式主要是对离子电荷的处理,正离子的电荷相当于中心原子失去电子,负离子就相当于中心原子得到电子。
例如:
SO42-孤对电子对=(6+2-4×2)/2=0
通过上面的三个关系式我们就能轻松解决ABn型分子中心原子A的价层电子对,就可以得到VSFPR模型。教科书只要求掌握价层电子对≤4的分子或离子的立体模型。我们可以概括如下:
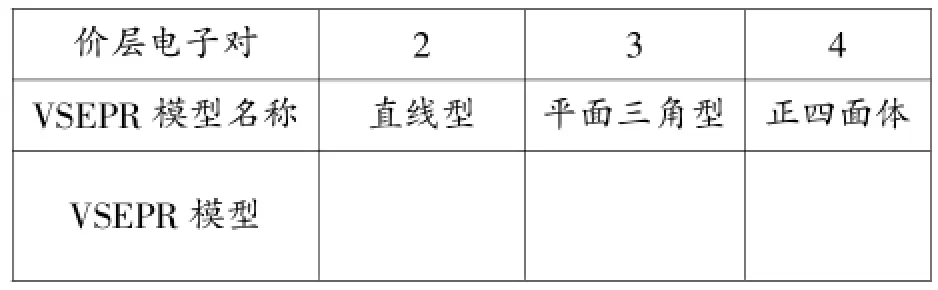
价层电子对2 3 4 VSFPR模型名称直线型平面三角型正四面体VSFPR模型
二、分子立体模型
通常所说的分子立体模型是指分子中的原子在空间的排布,不包括孤对电子。因为对ABn型分子而言,中心原子上价层电子对之间存在这样一种斥力关系:孤对电子-孤对电子>孤对电子-键合电子>键合电子-键合电子,使得分子或离子的立体模型偏离VSFPR理想模型而发生畸变。所以我们在得到VSFPR模型后,只要略去VSFPR模型中的孤对电子对,就得到分子或离子的立体模型。可以概括如下:
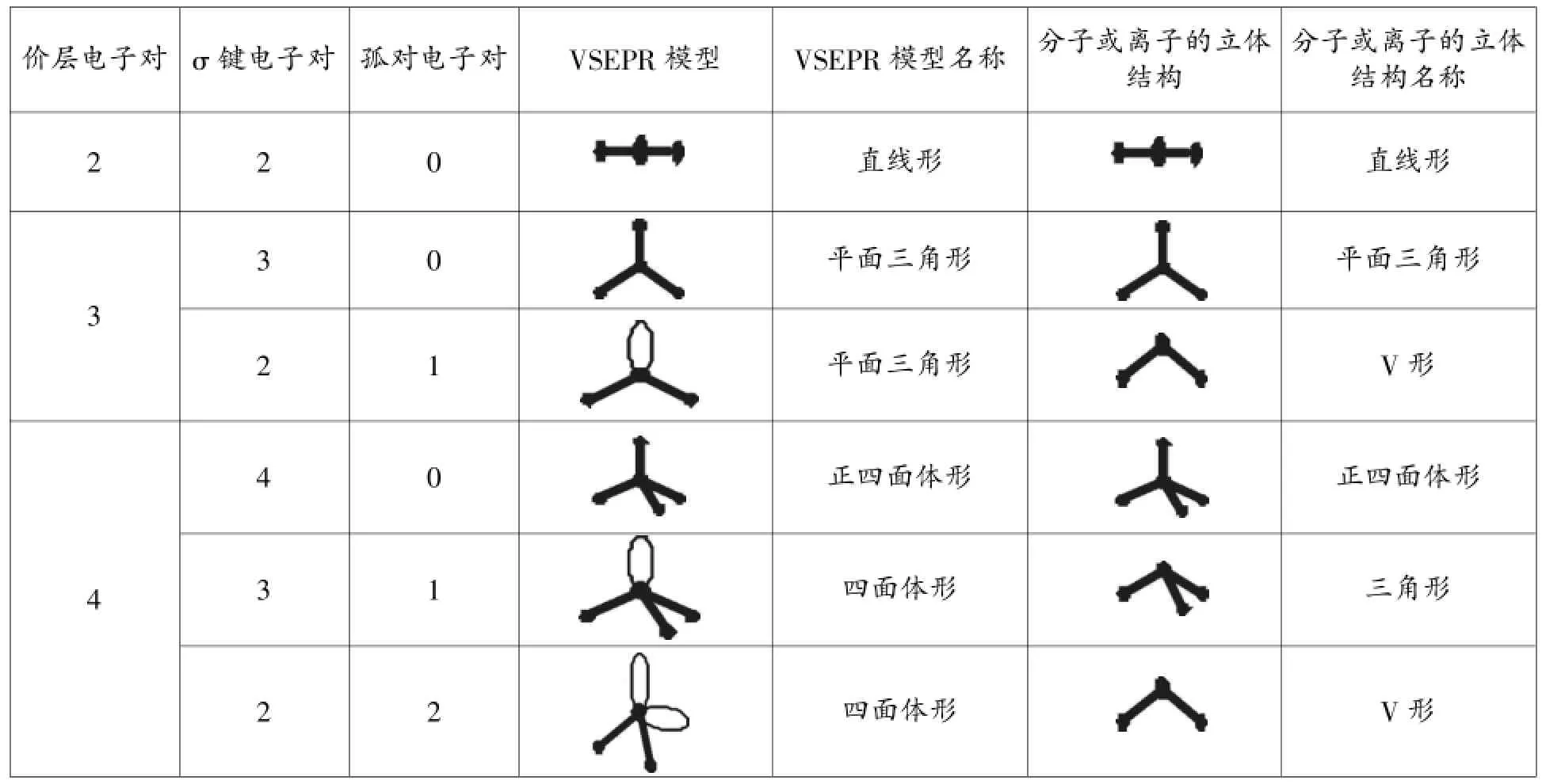
价层电子对σ键电子对孤对电子对VSFPR模型VSFPR模型名称分子或离子的立体结构直线形直线形2 2 0平面三角形平面三角形03 2平面三角形V形10 4正四面体形正四面体形4 3 12四面体形三角形四面体形V形3 2分子或离子的立体结构名称
根据上表,就可以轻松推测分子立体结构模型。
例如:NH4+中心原子N原子的σ键电子对为4,孤对电子对0,所以NH4+立体结构模型为正四面体型。
可见,应用价层电子对互斥理论推测ABn型分子的立体结构模型时,只要知道分子式就能确定分子的立体结构。
文章编号:1008-0546(2010)03-0078-01中图分类号:G632.46
文献标识码:B
doi:10.3969/j.issn.1008-0546.2010.03.034

