大黄酚-羟丙基-β-环糊精包合物的工艺优选及鉴定
郑晓霞, 张丹参, 黄红娜, 薛贵平
(河北北方学院药理教研室,河北张家口075029)
大黄酚(chrysophanol,Chry)是在大黄、虎杖、何首乌等蓼科植物中提取的一种蒽醌类化合物,具有抗菌、兴奋神经、抗癌、止咳、抗衰老等药理作用[1,2]。大黄酚属于脂溶性化合物,在水中溶解度极小,生物利用度不高,限制了大黄酚在临床中的应用。本实验旨在通过大黄酚-羟丙基-β-环糊精包合物(Chry-HP-β-CD)制备工艺的研究以及对包合物的鉴定,为探索中药单体有效成分的新剂型提供依据。
1 实验材料
1.1 仪器
Waters600高效液相色谱仪,美国waters公司;LabTech紫外分光光度计,北京莱博泰科仪器有限公司;XQM-0.4L变频行星式球磨机,南京科析实验仪器研究所;RE-52AA旋转蒸发器,上海亚荣生化仪器厂;85-2A数显恒温测速磁力搅拌器,金坛市金南仪器厂;JN-5200DT超声波清洗机,宁波江南仪器厂。
1.2 材料
大黄酚(chrysophanol,含量≥98%),南京泽朗医药科技有限公司;羟丙基-β-环糊精(hydroxypropyl-β-cyclodextrin,HP-β-CD),淄博千汇精细化工有限公司;大黄酚标准品(chrysophanol,批号:110796-200310),中国药品生物制品检定所;甲醇(methanol)为色谱纯,水为重蒸水,其他试剂为分析纯。
2 方法与结果
2.1 Chry-HP-β-CD含量测定方法的确定
2.1.1 色谱条件:选用Thermo BDS HYPERSIL C18(4.6 mm ×250 mm,5 μm)色谱柱;以甲醇-水(95∶5)为流动相;柱温为30℃;检测波长:254 nm;流速为 1.0 mL/min;进样量为 20 μL。
2.1.2 Chry对照品溶液的制备:精密称取Chry标准品1.13 mg,以甲醇为溶剂溶解后定容到10 mL,摇匀得113 μg/mLChry对照品溶液,备用。
2.1.3 Chry-HP-β-CD供试品溶液的制备:取Chry-HP-β-CD适量,置于10 mL的量瓶中,加入甲醇,超声20 min,并用甲醇稀释至刻度,摇匀,用0.45 μm的微孔滤膜过滤,取续滤液即得。
2.1.4 标准曲线的建立:精密吸取Chry对照品溶液2、10、20、100、200、400、1 000 μL 至 2 mL 量瓶中,加甲醇稀释至刻度,摇匀,使浓度成为0.113、0.565、1.13、5.65、11.3、22.6、56.5 μg/mL 的一系列对照品溶液,进样,测定。以质量浓度对峰面积做线性回归,得回归方程为:Y=44 504X+3 440.3,r=0.999 9,线性范围为 0.113 ~56.5 μg/mL。
2.1.5 回收率试验:精密称取同一批Chry-HP-β-CD样品9份,制成供试品溶液,取每份供试品溶液500 μL置于1 mL量瓶中,然后分别加入Chry对照品溶液(5.56 μg/mL)100、200、400 μL(每个平行 3份)后用甲醇稀释至刻度,按上述色谱条件测定供试品与混合样品的峰面积,分析含量,计算回收率,结果平均回收率为98.33%,RSD=1.54%。
2.2 Chry-HP-β-CD制备方法的选择
包合物常用的制备方法有搅拌法、研磨法、超声波法。分别采用3种方法制备包合物,以包合率为评价指标,选择最佳制备方法。
2.2.1 搅拌法:分别称取规定量的Chry与HP-β-CD置于烧杯中,加入50%乙醇使二者溶解,置于磁力加热搅拌器上,在30℃下,固定转速为800 r/min,搅拌2 h后,静置。将溶液真空旋转蒸发除去乙醇,用0.45 μm的微孔滤膜过滤以除去未被包合的大黄酚,将滤液进行真空干燥(30℃),即得Chry-HP-β-CD固体粉末。
2.2.2 研磨法:按搅拌法中的处方比称取Chry与HP-β-CD,加入适量50%乙醇溶解,倒入球磨罐中,在100 r/min的转速下,研磨2 h后,静置。将所得糊状物减压抽滤并用少量乙醇洗涤,真空干燥(30℃)后,得Chry-HP-β-CD固体粉末。
2.2.3 超声波法:按搅拌法中的处方比称取Chry与HP-β-CD于烧杯中,用50%乙醇溶解,置于超声波清洗机中,功率为300W,超声处理2 h后,静置。将溶液真空旋转蒸发除去乙醇,用0.45 μm的微孔滤膜过滤,将滤液进行真空干燥(30℃),即得Chry-HP-β-CD固体粉末。
2.2.4 样品分析:分别称取用搅拌法、研磨法和超声法制备的Chry-HP-β-CD适量置于10 mL量瓶中,加甲醇适量,超声20 min,再用甲醇稀释至刻度,摇匀。按上述色谱条件进行分析,根据外标法计算Chry的含量,代入下式计算包合率。
包合率=(包合物中Chry的含量/Chry的投入量)×100%
3种制备方法制得的包合物中,大黄酚包合率分别是搅拌法为(63.83±0.21)%,研磨法为51.38±1.29)%,超声法为(35.06±0.95)%。
结果表明,搅拌法所制备的Chry-HP-β-CD具有较高的包合率,因此选择搅拌法作为制备Chry-HP-β-CD的方法。
2.3 正交试验优化Chry-HP-β-CD制备工艺
根据相关文献报道[3-5],经过单因素考察可知,影响HP-β-CD包合物的形成的因素主要有药物与HP-β-CD的质量比、乙醇的浓度、包合时间、包合温度。以药物与HP-β-CD的包合率为评价标准,采用三水平L9(34)正交表安排实验,对 Chry-HP-β-CD的制备条件进行优选。因素水平见表1。

表1 因素水平表
按照正交设计的制备条件,采用搅拌法制备9种工艺的Chry-HP-β-CD,照2.1项下测定包合物的含量。
2.3.1 正交实验结果 按上述L9(34)表对其进行正交实验,实验结果以及方差分析分别见表2和表3。直观分析以及方差分析分析表明,影响包合物包合率大小的因素为A>B>D>C。通过方差分析可知,Chry与HP-β-CD的质量比有显著性统计学意义(P<0.05)。根据工艺实际情况,最佳制备工艺为:A3B3C2D1,即Chry与 HP-β-CD 的质量比为1∶60,乙醇的浓度为50%,包合时间为2 h,包合温度为30℃。
Chry在水中的溶解度很低,若将Chry的醇溶液滴入到HP-β-CD的水溶液中会有黄色固体析出。鉴于Chry与HP-β-CD在乙醇中均有较好的溶解度,本实验以50%乙醇作为溶剂,将二者都溶于其中。在包合过程中,疏水力是促进包合的主要推动力,所以包合一般在水中或稀醇中进行[6]。在进行包合时药物分子首先溶解在溶剂中,然后再与HP-β-CD形成包合物[7]。实验结果表明,使用50%乙醇作为溶剂,可以完全溶解Chry分子,又不会明显影响Chry-HP-β-CD的形成。延长包合时间可增加乙醇在搅拌过程中的挥发,乙醇挥发后有利于药物由有机层进入水层,进一步提高包合率,所以最佳包合时间定为2 h。由于Chry热稳定性差以及药物分子与HP-β-CD的结合通常是放热反应,所以升高温度不利于包合过程,因此通过正交试验确定包合温度为30℃。
2.3.2 验证试验:以最佳制备工艺平行制备3批样品,按照含量测定方法测定Chry的含量,3份Chry-HP-β-CD 包 合 率 分 别 为:64.65%、63.96%、63.72%,包合率平均值为:64.11%,RSD为0.75%,说明该工艺稳定可行。
2.4 包合物的定性验证
2.4.1 紫外分光光度法:采用紫外分光光度法,以吸收曲线与吸收峰的位置来判断包合物形成的情况。扫描范围:200~400 nm。扫描的溶液为:样品1:Chry标准品的甲醇溶液;样品2:Chry-HP-β-CD的水溶液;样品3:Chry-HP-β-CD的供试品溶液(按2.1.3项下制得);样品4:HP-β-CD的水溶液。取上述各少量样品进行紫外扫描,结果见图1。结果显示,Chry包合前后,紫外吸收峰变化很大,包合后Chry在254 nm的特征吸收峰消失,说明Chry经包合后进入了HP-β-CD分子腔内形成了稳定的包合物。Chry-HP-β-CD经甲醇提取后又重现包合前的吸收特征,说明包合物已经形成。

图1 Chry-HP-β-CD验证紫外扫描光谱图
2.4.2 薄层色谱法:取Chry标准品的甲醇溶液作为样品1;Chry-HP-β-CD的水溶液为样品2;Chry-HP-β-CD的供试品溶液为样品3(按2.1.3项下制得);HP-β-CD的水溶液为样品4。吸取上述4种溶液各2 μL,分别点于同一硅胶G薄层板上,以苯-乙酸乙酯(8∶2)为展开剂展开,取出,晾干,放置在254 nm紫外灯下观察。结果表明,样品1与样品3在同一位置显相同颜色的黄色斑点,而样品2与样品4无此斑点显示,说明Chry已被HP-β-CD包合,包合物已经形成。
2.5 相溶解度研究
精密称取HP-β-CD用蒸馏水配成质量分数为1、2、5、10、15、20%的系列溶液,分别吸取 5 mL 置具塞试管中,均加入过量的Chry固体粉末,超声10 min后置恒温振荡器(25℃)中,调整振荡频率为100 r/min,振荡48h。使溶解达到平衡后,静置,取上清液用0.45 μm的微孔滤膜过滤,滤液用高效液相法测定Chry的峰面积,用标准曲线计算Chry的浓度。
2.5.1 包合稳定常数的测定:以HP-β-CD的浓度(mmol/L)为横坐标,Chry的浓度(mmol/L)为纵坐标,绘制平衡相溶解度图。结果线性回归方程为:Y=3.599×10-4X+8.974×10-4(r=0.998 7),表明随着环糊精浓度的增加,药物的溶解度呈线性提高,因此可以判定相溶解度曲线为AL型,说明Chry与HP-β-CD形成1∶1摩尔比的包合物。包合常数由公式:Kc=斜率/[截距(1-斜率)]求得,Kc越大,表明该药物与环糊精的结合越稳定,越容易形成包合物。经计算Chry-HP-β-CD的Kc=401.19 L/mol,说明Chry可被HP-β-CD包合。
2.5.2 HP-β-CD对Chry的增溶作用:通过相溶解度的研究可知,随着HP-β-CD比例的增大,对Chry的增溶作用逐渐增强。经文献查阅[8],大黄酚在水中的固有溶解度为4.91×10-7mol/L(质量浓度0.125 mg/L),HP-β-CD对Chry的增溶作用见表4。当HP-β-CD的质量分数为20%时,可使Chry溶解度增大102.66倍,说明用HP-β-CD包合Chry后,可有效地提高其在水中的溶解度。
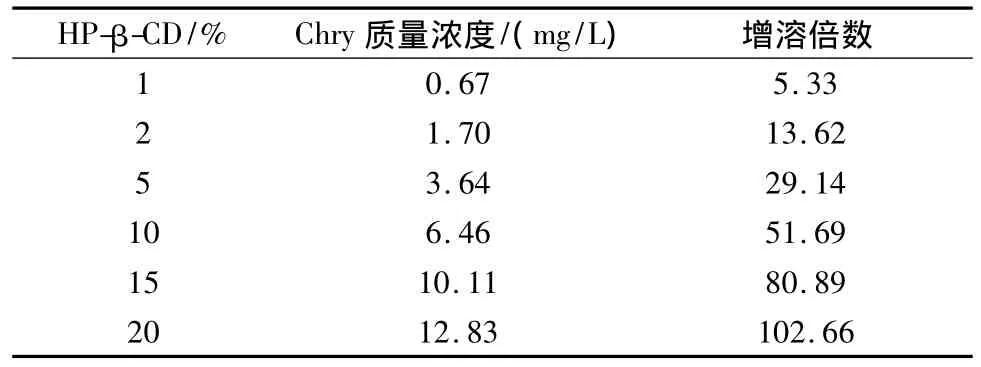
表4 HP-β-CD对Chry的增溶作用
3 讨论
大黄酚的药理作用涉及改善脂肪代谢、抗炎、利尿、缩短凝血时间、保肝利胆、促进学习记忆及抗衰老等多方面作用[9-11]。大黄酚是具有酚羟基的蒽醌类化合物,脂溶性极高,利于药物发挥作用,但其溶解度小没有适宜的剂型供临床应用。HP-β-CD为β-环糊精(β-cyclodextrin,β-CD)的羟丙基衍生物,是一种低毒、安全、有效的药物增溶剂[12],作为注射用辅料被《美国药典》收载。本研究利用包合技术,采用HP-β-CD为包合材料将大黄酚制成包合物,以提高其溶解度、拓展临床应用。
本研究证实搅拌法制备的Chry-HP-β-CD的药物包合率较高且具有操作简单、工艺条件易于控制的优点。采用正交试验对Chry-HP-β-CD的制备工艺进行了研究,在最佳制备条件下Chry-HP-β-CD包合率达到64.11%,工艺稳定可行。通用紫外光谱法、薄层色谱法与相溶解度法对Chry-HP-β-CD进行验证。研究表明,以HP-β-CD为包合材料,将大黄酚制成包合物后,起到了增加大黄酚溶解度的作用,为大黄酚新剂型的研究提供了依据。
[1]王开金,张颖君,杨崇仁.蓼属植物的化学成分与生物活性研究进展[J].天然产物研究与开发,2008,18:151-164.
[2]李玉芳,何玄华.何首乌现代研究进展[J].中成药,1997,19(5):37-38.
[3]廖正根,平其能,邹 红,等.丹皮酚-β-环糊精包合物的制备工艺研究[J].中草药,2005,36(6):842-846.
[4]张学农,阎雪莹,唐丽华,等.正交试验优化马蔺子素-羟丙基-β-环糊精包合物的制备工艺[J].中成药,2004,26(9):695-698.
[5]简 辉,高丽丽,孙婷婷,等.正交设计实验优化丹皮酚HP-β-CD包合物制备工艺[J].中国实验方剂学杂志,2008,14(12):37-40.
[6]韩 光,李景华,杨 蕾,等.超声法制备穿心莲内酯-β-环糊精包合物的研究[J].中国新药杂志,2008,17(7):582-585.
[7]刘培丽,杨琳琳,王永生,等.羟丙基-β-环糊精对冬凌草二萜类成分的包合作用[J].沈阳药科大学学报,2006,23(9):557-560.
[8]李向军,连 军,张 勇,等.β-环糊精对大黄酚的增溶效应[J].应用化学,1999,16(3):112-113.
[9]朱有光.中药大黄止血作用的研究进展[J].临床和实验医学杂志,2008,7(1):138-139.
[10]聂 克.大黄药理作用研究及思考[J].山东中医药大学学报,2009,33(3):239-240.
[11]张丹参,张 力,薛贵平,等.大黄酚的抗衰老作用[J].中国医院药学杂志,2005,25(1):15-17.
[12]陶 涛.羟丙基倍他环糊精的特性及其药剂学应用[J].中国医药工业杂志,2002,33(6):304-308.

