壳聚糖及其降解产物黏均分子质量的测定
寇晓亮,王 琛
(西安工程大学纺织与材料学院, 西安 710048)
壳聚糖是一种十分丰富的海洋资源,是一种很有发展前途的高分子材料,被科学家誉为第六生命要素。壳聚糖及其衍生物,由于其独特的性能,在纺织、印染、食品、化工、医药、农业等方面得到了广泛的应用。壳聚糖特有的分子结构,使其对许多类型的染料(活性染料、直接染料等)具有极高的吸附力,可用于提高织物上染率和印染废水处理等。壳聚糖的应用性能与分子质量密切相关,例如,不同分子质量的壳聚糖作为棉织物染色增深剂的作用效果是不同的,因此,测定壳聚糖的分子质量,对于壳聚糖的应用十分重要[1]。黏度法测定高聚物分子质量是一种常用方法。一定浓度壳聚糖溶液,它的黏度直接反映了壳聚糖的分子质量,在其他因素固定不变的情况下,壳聚糖相对分子质量越高,其溶液的黏度就越大,相对分子质量越低,黏度就越小。这就是黏度法测定壳聚糖分子质量的原理[2]。本文没有采用毒性很大的苯作为溶剂体系,采用CH3COOH-NaCl溶剂体系[3]测定壳聚糖及其降解物的分子质量。该方法原料处理简单,仪器易于清洗,实验数据重现性好。
1 实验部分
1.1 仪器与试剂
乌氏黏度计一支(0.5 ~0.6 mm); 恒温水槽一套(包括:电动搅拌器、继电器、温度计、调压器、加热器)秒表一块; 3#砂芯漏斗两个。
经乙酸溶解、沉淀提纯后的壳聚糖(脱乙酰度85%); 冰乙酸、氯化钠均为分析纯。
1.2 壳聚糖降解物的制备
采用降解体系为2% 的壳聚糖的4% 乙酸溶液,用搅拌器搅拌至呈均相状态,在超声波条件下滴加一定量的H2O2,超声波温度控制在40 ℃。降解持续180 min,用氢氧化钠将壳聚糖沉淀出来,用丙酮洗涤、再水洗,真空低温烘干。
1.3 测分子质量实验步骤
1.3.1 测定溶剂流出时间
将恒温水槽调至(250.1)℃,在黏度计(图1)B、C管上小心地接上医用橡皮管,用铁夹夹好黏度计,放入恒温水槽,使毛细管垂直于水面,使水面浸没a线上方的球。用移液管从A注入10 ml经砂芯漏斗过滤的溶剂(0.1 mol·L-1乙酸-0.2 mol·L-1氯化钠溶液)恒温10 min后,用夹子夹住C管橡皮管使其不通气,而将接在B管的橡皮管用洗耳球抽气,使溶剂吸至a线上方的球一半时停止抽气。先把洗耳球拔下,而后放开C管的夹子,空气进入D球,使毛细管内溶剂和A管下端的球分开。这时水平的注视液面下降,用秒表记下液面流经a线和b线的时间,此即为t0,重复三次以上,误差不超过0.2 s。取其平均值做t0。然后将溶剂倒出,黏度计烘干。
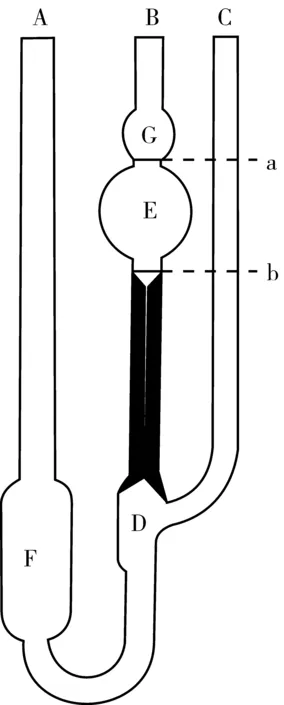
图1 乌氏黏度计
1.3.2 溶液流出时间的测定
精确称取一定量的壳聚糖或其降解物,用0.1 mol·L-1CH3COOH-0.2 mol·L-1NaCl溶剂配成一定浓度的溶液,此样品溶液的浓度为C0,此溶液经砂芯漏斗过滤,用移液管吸取10 mL溶液注入黏度计,黏度测定与溶剂相同。测定溶液流出时间为t1。然后再移入5 mL溶剂,这时黏度计内溶液的浓度为原来的2/3,将其混合均匀,并把溶液吸至a线上方的球一半,洗两次,再用同样方法测定t2。同样操作,再依次加入5 mL、10 mL、10 mL溶剂,这时黏度计内溶液
的浓度分别为原来的1/2、1/3、1/4,用同样方法测得t3、t4、t5[4-5]。
1.3.3 数据处理

2 结果处理与结论
2.1 结果处理
按实验步骤中公式计算出未降解的壳聚糖和降解180 min的壳聚糖的相关数据,结果如表1、表2和图2、图3所示。
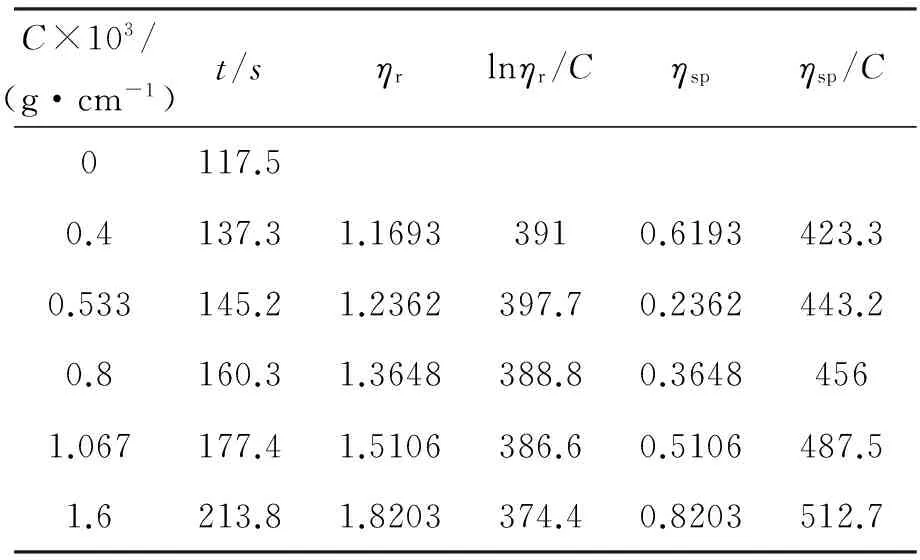
表1 未降解壳聚糖黏度测定数据表
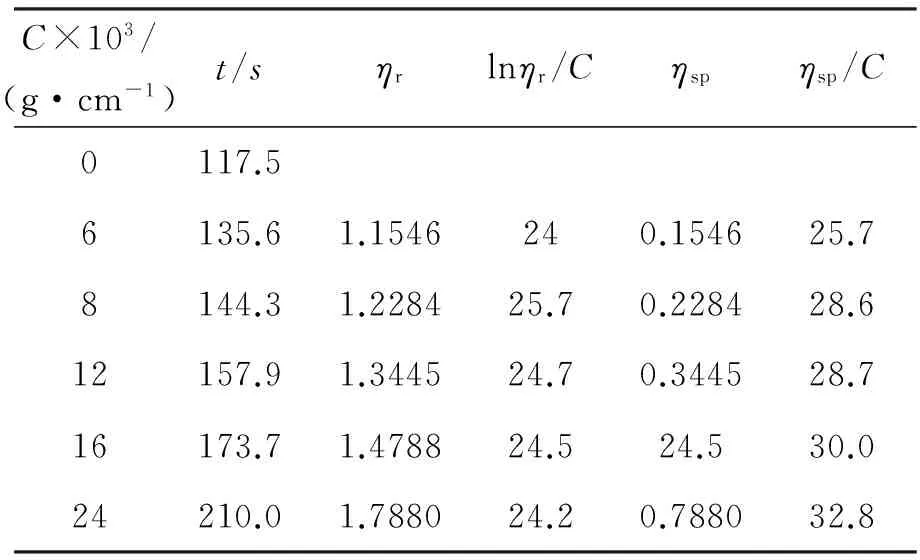
表2 降解180 min的壳聚糖黏度测定数据表

图2 未降解壳聚糖溶液lnηr/C-C及ηsp/C-C图
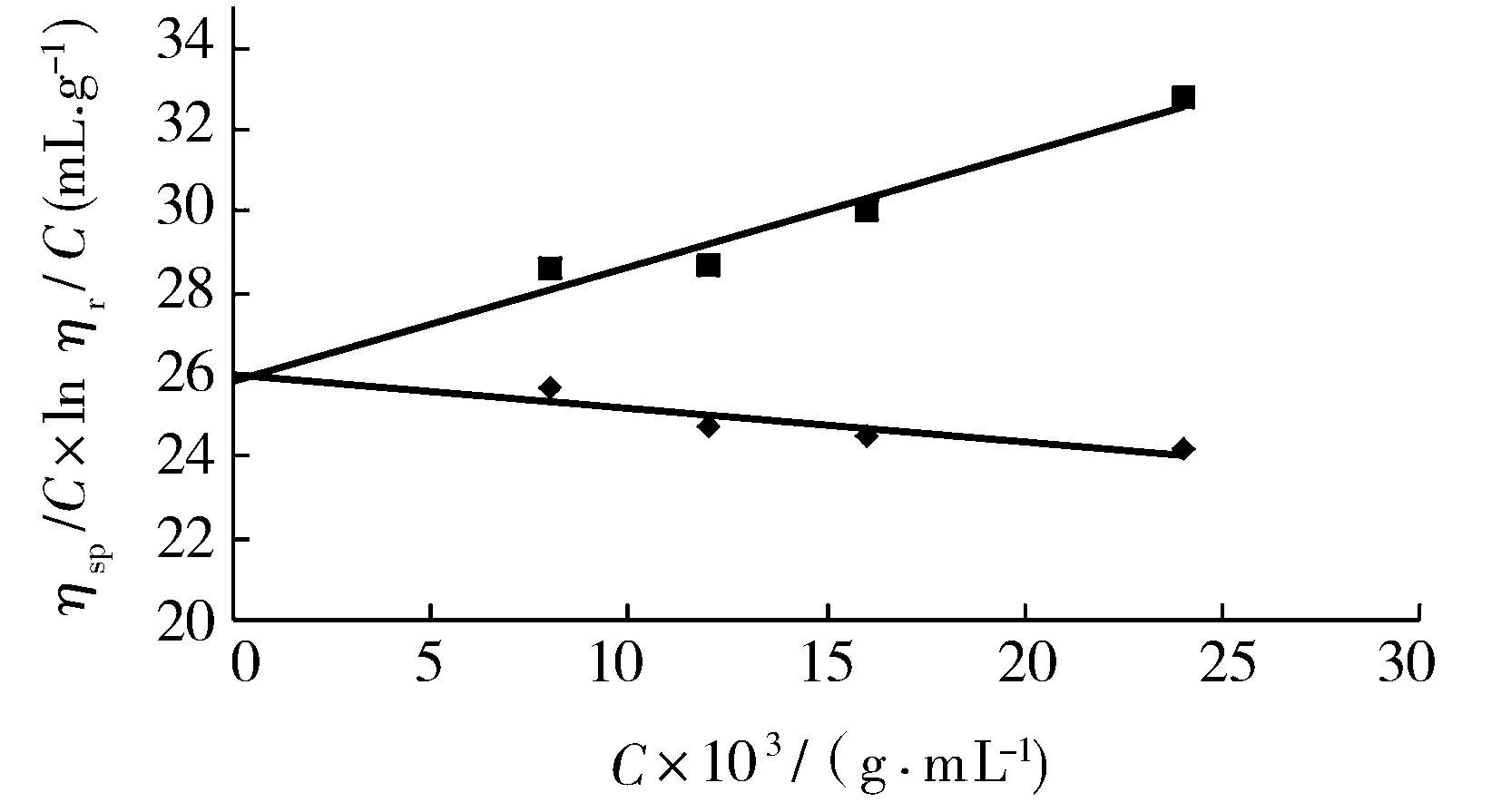
图3 降解180 min的壳聚糖溶液lnηr/C-C及ηsp/C-C图
2.2 结论
(1)由图2、图3可知,未降解壳聚糖[η]为407.6,然后按公式计算得出分子质量约为5.7×105。降解180 min的壳聚糖[η]为26.0,按公式计算得出分子质量约为2.9×104。
3 影响黏度法测定壳聚糖分子质量的因素
3.1 乌氏黏度计尺寸大小的影响
常用毛细管黏度计有乌氏、奥氏、品氏和逆流式等几种,测量分子质量一般选用乌氏黏度计。乌氏黏度计是高分子科学研究和高分子材料工业生产领域中使用最广泛的表征高聚物稀溶液性质和高聚物分子质量的仪器。有人在研究了流出时间对动能修正项影响的同时,也提出了合理的黏度计设计尺寸。一般认为毛细管半径对动能修正的影响最大,毛细管较细的黏度计可以大大降低动能修正项的影响,但黏度计的毛细管也不宜过分细小,否则不但测定时间过长,且毛细管洗涤困难,易于堵塞。一般市场上出售的乌氏黏度计,流出体积约4~5 mL,毛细管长度在10~14 cm,变化都不大,但毛细管直径可从0.2 mm到1.6 mm,变化范围较大。使用时应根据实际情况选择适当规格的黏度计。由于本实验开始使用直径为0.93 mm,测出溶剂的流出时间太短,改用毛细管直径较小的黏度计,直径在0.5~0.6 mm范围。
3.2 溶液浓度的选择与配制
随着溶液浓度的增加,壳聚糖分子链之间的距离逐渐缩短,因而分子间作用力增大.当溶液浓度超过一定限度时,高聚物溶液的lnηr/C或ηsp/C与C不成线性关系。通常选用ηr在1.2~2.0浓度范围。有时尽管浓度的配制相当准确,在其它实验条件合理的情况下,测出壳聚糖的相对分子质量仍然误差很大。这主要与所用乌氏黏度计的类型有关。常用的乌氏黏度计除了典型的一次只能测一种浓度的黏度计外,还有一种就是称为稀释型的乌氏黏度计,其最大的优点在于贮液球体积增大(约50 mL),便于在球内稀释被测液体,以便测试不同浓度液体的黏度。使用稀释型乌氏黏度计可大大省去常规乌氏黏度计每次测完一个浓度必须用待测液润洗的麻烦,且乌氏黏度计的洗涤和润洗也不像普通的玻璃仪器那样易于操作,稍有不慎就可使配制准确的一系列溶液的浓度改变,导致作图时引起较大误差。因此在实验中尽量使用稀释型乌氏黏度计,便于直接在贮液球内稀释被测液体,减少由于稀释溶液引起的浓度误差。
3.3 恒温槽控温精度的影响
测试温度对高聚物溶液黏度的测定特别敏感。有人作过温度对聚酯切片黏度测定影响的实验,实验结果表明,特性黏度值随温度升高而下降。一般而言,温度上升0.01 ℃黏度不受影响; 温度上升0.02 ℃,特性黏度下降0.004; 温度上升0.05 ℃,特性黏度下降0.011; 如温度上升0.08 ℃,特性黏度则下降至0.021,该值对高聚物相对分子质量的计算已产生明显的偏差。由此可见温度参数直接影响黏度的大小,故必需严格控制温度精度范围,测定结果才有可靠保证。作为高聚物的壳聚糖也是如此,温度对其溶液黏度测定影响很大。ISO12228规定黏度法测定相对分子质量的恒温槽的控温精度为±0.05 ℃,而学生实验中所用恒温槽的最小波动范围为±0.1 ℃,显然恒温槽的控温精度也在很大程度上影响实验的测定结果。
4 结语
虽然黏度法测定壳聚糖分子质量的方法并不复杂,但为保证测试结果的正确性,必须严格把握好实验各个环节,尽量避免误差。很多其他因素的影响也不可忽视,如壳聚糖样品的称量; 黏度计尤其是毛细管部分的清洗; 测定黏度时黏度计的垂直程度; 目视标线时的水平情况; 计时器按动速度以及外界的震动等等。总之,只有将实验各环节的误差减至最小,才能保证测量出的高聚物相对分子质量的可靠与可信度[6]。
[1]贺岚,白海红,艾有年. 黏度法测定壳聚糖分子量的一些体会[J]. 中国卫生检验杂志,2001,11(5):631-632.
[2]唐振兴, 石陆娥, 易喻. 壳聚糖及其降解物分子量的测定[J].化工技术与开发,2004,33(6):38-39.
[3]赵立明, 全哲山, 金海善,等. 壳聚糖黏均分子质量的测定[J].延边大学医学学报,2005,28(1):36-37.
[4]刘建平,赵玉斌. 高分子科学与材料工程实验[M]. 北京:化学工业出版社,2005:40-44.
[5]何平笙,杨海洋,朱平平,等. 高分子物理实验 [M]. 合肥:中国科学技术大学出版社,2002:95-101.
[6]王亚珍,林雨露,吴天奎. 黏度法测高聚物相对分子量实验成败探讨[J]. 江汉大学学报, 2004, 32(4): 59-60.

