液相串联质谱法测定食品级烟酰胺中烟酸含量

烟酰胺又名尼克酰胺、维生素PP、维生素B3,是B族维生素的一种,对人体有多种益处,其在食品中主要是作为抗氧化剂和营养强化剂使用,有助于延缓食品氧化过程,保持食品的新鲜度和口感,同时提高食品的营养价值。受烟酰胺生产工艺的影响,一般原料中都含有少量烟酸,其含量对烟酰胺的质量有着重要影响。由于烟酰胺与烟酸的结构相近,因此分离较为困难。现有的检测方法中,一般采用液相色谱法同时检测样品中的烟酰胺和烟酸,这种方法要求烟酰胺与烟酸的含量相近,互不产生干扰,并不适用于测定大量烟酰胺中烟酸的含量。本文采用了MAX混合型阴离子交换固相萃取柱,最终实现了烟酰胺与烟酸的分离,能准确测定出烟酰胺中烟酸的含量,为提高烟酰胺的质量提供了技术支持。
1. 材料与方法
1.1 仪器与试剂
赛默飞液相串联质谱仪,包括四元泵、在线真空脱气机、柱温箱、自动进样器、TSQ质谱检测器,美国赛默飞世尔科技公司;电子天平:感量为0.0001mg,德国赛多利斯;Milli-Q型纯水系统;MAX混合型阴离子交换固相萃取柱:1000mg/6mL,深圳逗点生物技术有限公司;烟酸标准品:纯度大于99.0%,德国Dr.E;甲醇:色谱纯,上海安谱实验科技股份有限公司;甲酸:分析纯,西陇科学股份有限公司。
1.2 溶液配制
烟酸标准储备溶液(1000mg/L):称取烟酸标准品10mg于10mL容量瓶中,用水溶解并稀释至刻度,于4℃冰箱中保存备用,使用时用水稀释至所需质量浓度。
1.3 仪器工作条件
色谱柱:赛默飞Thermo Hypersil ODS(C18)色谱柱(1.7μm,50mm*2.1mm),或具有同等柱效的色谱柱;柱温:35℃;进样体积:5uL;流速:0.2mL/min。流动相A为0.1%甲酸水溶液,流动相B为甲醇,等度洗脱,A:B=50:50。
正离子模式扫描;雾化气:氮气;雾化室温度:350℃;毛细管电压:3.5kV;MRM多反应监测模式检测;烟酸的离子对参数为124/106、124/80,定量离子参数为124/106。
1.4 实验步骤
1.4.1 样品预处理。取0.1g烟酰胺原料样品,加入10mL去离子水,制成烟酰胺水溶液。向MAX混合型阴离子交换固相萃取柱内加入3mL甲醇和3mL去离子水进行活化,将上述10mL烟酰胺水溶液加入至MAX混合型阴离子交换固相萃取柱中,自然流干。取3mL甲醇溶液洗脱MAX混合型阴离子交换固相萃取柱,弃去洗脱液。再向MAX混合型阴离子交换固相萃取柱中加入6mL含16%甲酸的甲醇溶液,对其进行洗脱,并收集洗脱后的甲醇溶液。向收集的甲醇溶液中加入去离子水,并定容至10mL。采用0.45μm滤膜过滤,液相串联质谱仪测定。
1.4.2 定量方法。取烟酸的系列混合标准工作溶液,按照仪器工作条件测定其标准曲线,进行样品分析,利用外标法进行定量,样品中烟酸的含量为X(mg/kg),按照公式(1)计算。
X=C*V/m (1)
公式中:X表示烟酸的含量,单位为mg/kg;C表示外标法曲线所得烟酸浓度,单位为mg/L;V表示定容的体积,单位为mL;m表示样品的称样量,单位为g。
2. 结果与讨论
2.1 固相萃取柱的选择
虽然烟酰胺与烟酸的定性离子对不一样,但烟酰胺会严重干扰烟酸的测定,可能XqnlI3yt/OZbiWEkeMCinoCqUhBT11FvTTC4ddobCj4=是因为在正模式的测定条件下,大量烟酰胺分子在离子源处与烟酸产生竞争离子化现象,严重降低了烟酸的响应值,使得烟酸不容易被检测到。因此,试验采用固相萃取柱实现烟酰胺与烟酸的分离。
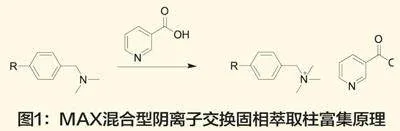
从烟酰胺与烟酸的化学结构式可以看出,两者的结构差异主要体现在酰胺键与羧基的差别。利用这个结构差异,试验选取MAX混合型阴离子交换固相萃取柱,利用其与烟酸羧基的强碱弱酸离子键作用来富集烟酸,从而实现烟酰胺与烟酸的分离。MAX混合型阴离子交换固相萃取柱的富集原理见图1。
2.2 流动相的选择
本试验对比了甲醇-0.1%甲酸水溶液、乙腈-0.1%甲酸水溶液、甲醇-水、乙腈-水四种不同的流动相混合溶液,结果表明,甲醇-0.1%甲酸水溶液作为流动相时,烟酸的响应值更高。这可能是因为在正模式监测下,添加0.1%甲酸有利于烟酸吡啶环上的氮原子结合氢原子,提高其响应值。同时,一般情况下,甲醇比乙腈更适合于正模式监测,因此,经过试验,采用甲醇-0.1%甲酸水溶液作为混合流动相。
本试验同时尝试了不同比例的甲醇-0.1%甲酸水溶液,最后确定流动相比例为,A:B=50:50。见表1。
2.3 色谱柱的选择
本试验选用反相色谱柱、正相色谱柱进行色谱柱条件选择,其型号分别为Thermo Hypersil ODS(C18)色谱柱、ZORBAX Rx-SIL色谱柱。结果表明,使用Thermo Hypersil ODS(C18)色谱柱时,烟酸出峰良好,并没有发现待测物质过早出峰的情况。
2.4 质谱条件的优化
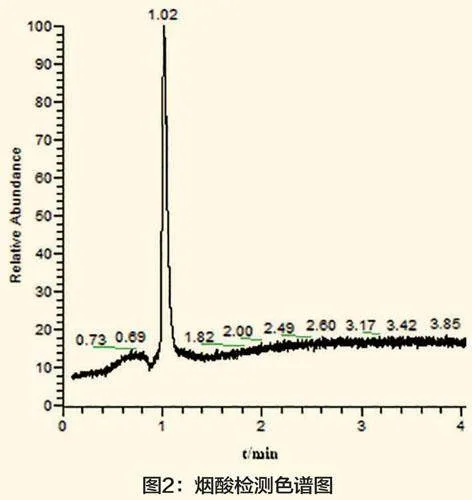
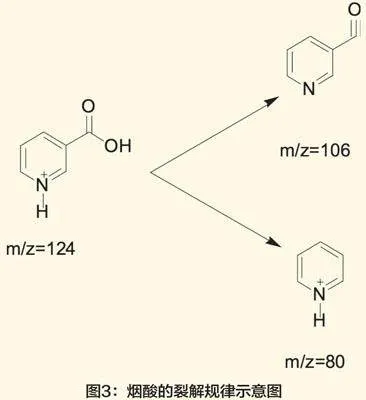
将一定浓度的标准溶液以注射式连续直接进样的方式进行一级质谱全扫描分析,通过优化雾化室温度、毛细管电压等参数,得到烟酸的准分子离子峰。结果表明,烟酸在正模式比负模式的响应值更高,因此选择m/z=[M+H]+作为准分子离子峰。然后选取准分子离子峰进行轰击,通过优化碰撞能量、质谱分辨率等参数,最大化地提高检测的灵敏度。通过分析二级质谱信息得出,烟酸的二级质谱碎片主要包括m/z=106、m/z=80。试验选取124/106、124/80作为监测离子,其中定量离子参数为124/106。烟酸检测色谱图见图2,烟酸的裂解规律见图3。
2.5 洗脱溶液的选择
MAX柱与烟酸的结合作用力为季铵离子与羧基的强碱弱酸离子键作用,要从MAX柱上洗脱烟酸,洗脱液的酸性一般要求比烟酸更强。烟酸的吡啶环是一个强吸电子基团,能够增强烟酸上羧基的酸性,因此,烟酸的酸性比较强。本试验分别尝试5%乙酸的甲醇溶液、10%乙酸的甲醇溶液、16%乙酸的甲醇溶液、5%甲酸的甲醇溶液、10%甲酸的甲醇溶液、16%甲酸的甲醇溶液等6个不同组合溶液洗脱MAX柱。结果表明,乙酸的甲醇溶液并不能有效洗脱烟酸,回收效率并不高。为了能够充分地洗脱MAX柱上富集的烟酸,本试验采用含有16%甲酸的甲醇溶液洗脱MAX柱。
2.6 标准曲线、检出限、回收率及精密度
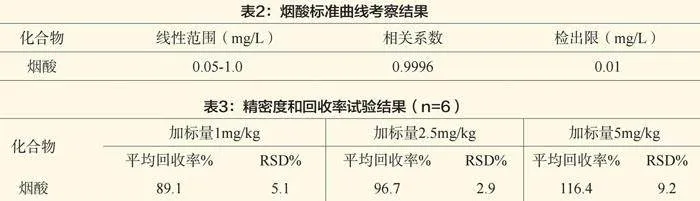
配制质量浓度分别为0.05、0.10、0.20、0.50、1.0mg/L的烟酸混合标准溶液,按仪器工作条件测定其标准曲线。结果表明,在0.05-1.0mg/L范围内线性关系良好,其相关系数r>0.9990。结果见表2。
称取空白烟酰胺样品1.0g,分成三组,分别添加0.1、0.25、0.50mg/L三个浓度烟酸,相当于含有1、2.5、5mg/kg烟酸。按照本方法进行添加回收率和精密度(n=6)实验,计算得到回收率为89.1%-116.4%,相对标准偏差为2.9%-9.2%。空白烟酰胺样品加标回收率试验结果表明,方法测定下限(10倍信噪比)可达1mg/kg。实验结果见表3。
本文建立了固相萃取-液相串联质谱法测定烟酰胺中烟酸含量的方法,其中的关键技术是根据烟酰胺与烟酸的结构,采用MAX混合型阴离子交换固相萃取柱实现烟酰胺与烟酸的分离,避免了两者之间的互相干扰。实验结果显示,该方法线性关系良好、检出限低,能够满足对食品级烟酰胺中烟酸的测定。
作者简介:黄锦波(1988-),男,汉族,广东茂名人,助理工程师,大学本科,研究方向为食品、化妆品与环境分析。

