核心素养理念下的初中化学教学设计

新课标背景下初中化学教学要围绕学科核心素养,注重培养学生的化学观念、科学思维、科学探究与实践能力、科学态度与责任感。在“金属资源的利用和保护”的教学中,教师需要精心设计教学内容和活动,引导学生从认识到实践,全面提升学生的素养水平,增强他们的社会责任意识。
一、教材分析
九年级化学教材中的“金属资源的利用和保护”一节涉及金属资源在日常生活和工业中的重要作用以及如何合理利用和保护这些资源,包括金属的种类及其相关应用、金属资源的开采与冶炼、金属资源的利用、金属资源的保护等内容。这一节通过对金属资源的合理开发、利用与保护的教育,旨在增强学生的环保意识和责任感,为可持续发展奠定基础。
二、设计理念
本设计以“技术融合创新”为核心思路,旨在探索信息技术在化学中的创新应用,尤其是在教学教研、课堂应用、学生评价和有效反馈等方面的突破。教师将信息技术融入课堂教学,能够打破传统教学模式,增强课堂的互动性和学生的参与度,激发学生的学习兴趣,同时利用信息技术对学生进行过程性评价,能全面、客观地反映学生的学习情况,帮助学生认识自我、调整学习策略;也可以通过信息技术及时、准确地收集和分析教与学的数据,进而优化教学过程。
三、教学目标
1.知道常见的金属如铁、铝、铜等矿物;了解从铁矿石中将铁还原出来的方法。
2.知道钢铁锈蚀的条件,了解防止金属锈蚀的简单方法。
3.通过废弃金属对环境的污染的学习,树立环保意识,回收、利用废旧金属等,认识到保护金属资源的重要性。
四、教学重难点
1.铁的冶炼实验中的相关问题(主要是酒精灯和一氧化碳的先后顺序)。
2.化学方程式中有关杂质问题的计算。
3.对铁的锈蚀防护的“活动与探究”的结论的辨析、归纳,从而得出铁生锈的条件以及防止锈蚀的方法。
五、教学过程
(一)课程导入
多媒体投放图片,发现金、银等主要以单质形式存在于自然界,其余金属大多以化合物的形式存在。
师追问:金、银为什么可以以单质的形式存在?
生:因为金、银的活动性非常弱,不易与其他物质反应。
学生回忆并齐背“金属活动性顺序”,通过多媒体设备播放金属活动性顺序表。
师:不同种类的金属在地壳中的含量并不相同,它们在地壳中呈现怎样的分布趋势呢?通过多媒体设备播放“金属元素在地壳中的含量”的柱状图。
师:我们来聊一聊自然界中金属的存在形式。我们通过前面两节课的学习,知道金属资源在自然界中其实是很丰富的,比如,自然界地壳中含量最高的几种元素:第一个是氧,然后就是硅,下一个就是金属元素铝。所以我们日常生活生产还有自然界的储量当中,金属占了很大一部分。并且绝大部分金属是以化合态形式存在,极少数以游离态形式存在。那么通过前面的学习,什么是化合态?什么是游离态?
生:游离态指的是元素以单质的形式存在,也称为零价态,化合态也叫做非零价态,需要与其他元素发生化学反应,从而以化合物的形态存在。
师:所谓化合态,即为非零价态,它可能是正价态,也可能是负价态,但金属元素通常情况下都显正价。
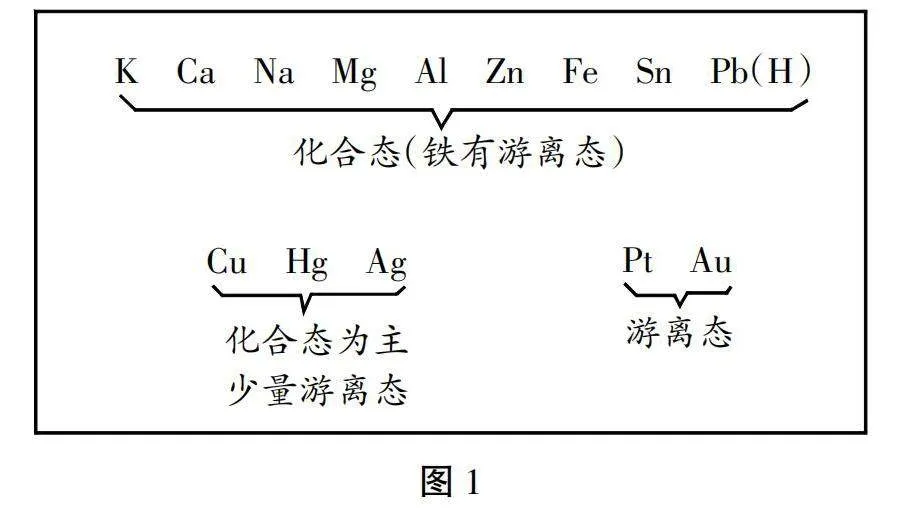
师:我们来看金属元素的活动性,钾、钙、钠、镁、铝、锌、铁、锡、铅、氢、铜、汞、银、铂、金,绝大部分都是以化合态形式存在,但我们看到铁有一个游离态,本质上地球中所产生的铁都是化合态,但有一些陨铁,也就是以陨石形式散落到地表上面的那个陨铁,属于单质形态,但也存在于自然环境当中,所以我们说铁有游离态,属于特殊例子(见图1)。
师:接下来看铜、汞、银,主要是以化合态为主,当然少量的也有游离态,如单质银;然后铂和金主要的存在形式就是单质形式,也就是游离态,如我们常见的单质金。
师:那我们看地壳中金属的含量,第一元素氧,然后就是硅,然后就是铝占比7.73%,铁占比为4.75%,占比都是比较高的。接下来是我们常见的矿石。矿石也就是工业上能用来提炼金属的矿物。第一个赤铁矿,其中主要成分就是Fe2O3。Fe2O3其实就是铁锈,呈红棕色,所以我们看到的赤铁矿也是呈红棕色;磁铁矿的主要成分为Fe3O4,能够被磁铁吸引,(但除了Fe3O4以外,单质铁也能够被磁铁吸引,这也就是其被称为磁铁矿的原因);菱铁矿的主要成分为FeCO3;铝铁矿的主要成分为Al2O3;黄铜矿的主要成分为CuFeS2;辉铜矿的主要成分为Cu2S。黄铜矿和辉铜矿中的铜我们可以看到是不一样的,CuFeS2里面的这个铁是+2价,铜也是+2价,铜最高价就是+2价,我们说亚铜就是比最高价又低一级的价态,比如,辉铜矿里的Cu2S,S是-2价,铜是+1价,所以这个铜称之为亚铜。
师:人类从自然界中提取量最大的金属还是铁,冶炼金属的选矿原则:矿石中金属含量高;冶炼过程污染小;冶炼途径简便。
(设计意图:利用信息技术创新教学方式,提高学生学习兴趣和参与度。大量的图片可以使学生更直观地看到各种金属的特性,以及在自然界中的呈现方式,能够最大限度地提高学生的积极性,参与到课堂活动中,用生活常识回答化学中的问题,将化学与生活联系起来。学生也可以更好地记忆和应用基础知识。)
(二)铁的冶炼
探究:实验室——用一氧化碳还原氧化铁
教师演示实验:一氧化碳还原氧化铁的实验。展示实验仪器装置图片,让学生回忆仪器名称及各类仪器的使用方法。
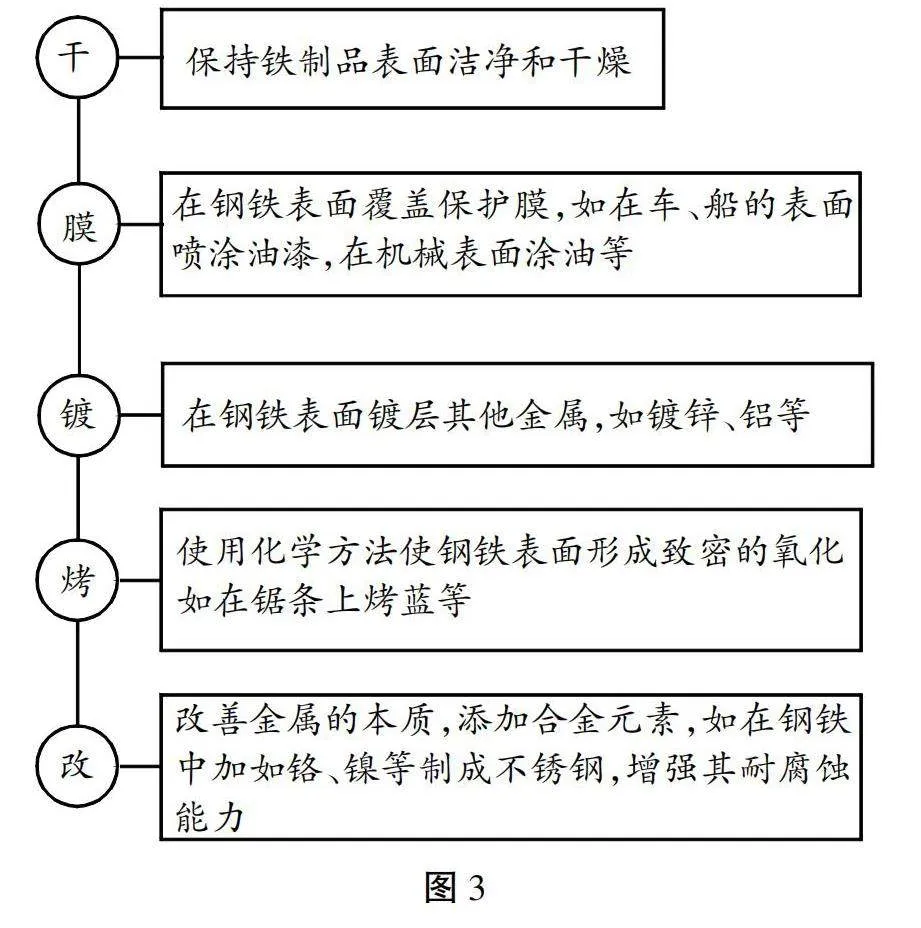
师:用一氧化碳还原氧化铁的实验原理:3CO+Fe2O3=2Fe+3CO2。再来看看实验装置(见图2),一氧化碳从左端进入,中间这个硬质玻璃管当中放入Fe2O3,下面使用酒精喷灯加热。看到酒精喷灯就要判断出它的环境就是高温。我们知道一氧化碳是不会和澄清石灰水发生反应的,但是如果生成二氧化碳的话,澄清石灰水就会变浑浊,换言之,这里的澄清石灰水就是用来检测有没有二氧化碳生成的,最后我们需要点燃酒精灯,因为我们知道CO是有毒的,因此需要通过引燃的方式处理尾气,避免污染空气。
师:接下来我们来看实验步骤。实验一定要按照顺序进行,否则一氧化碳可能会发生爆炸或者危险。第一步,检查装置的气密性,任何发生反应的装置都需要检查其气密性。第二步,装入药品并固定好装置。第三步,通入一氧化碳,排出空气,点燃尾部酒精灯。这里需要强调一下,任何可燃气体都存在爆炸性,因此需要先进行通风。第四步,点燃酒精喷灯。这里需要注意,先点燃尾部酒精灯,再点燃酒精喷灯,意味着一氧化碳和三氧化二铁开始发生反应,生成二氧化碳和铁。注意这个反应不属于置换反应,因为反应物没有单质。第五步,当红棕色粉末变成黑色时,熄灭酒精喷灯。当固体变成黑色时,表示反应已经完成,也就是Fe2O3完全变为Fe;最后继续通入一段时间CO气体,待装置冷却后,熄灭尾部酒精灯。这里为什么还要继续通入CO气体?
生:刚发生反应的单质铁处于高温状态,容易发生氧化反应生成Fe2O3,因此继续通入一段时间CO气体是为了保护单质铁不被氧化,并且玻璃管在冷却期间可能发生热胀冷缩,导致澄清石灰水倒吸,发生玻璃管破裂。
(设计意图:通过观看模拟实验,帮助学生直观地理解化学反应原理,提升学习效果。虚拟现实技术能够真实地模拟化学反应的过程和现象,让学生在虚拟环境中进行观察和实践,降低了实验的危险性,同时提高了学生对实验的理解深度。)
(三)金属的腐蚀与防护
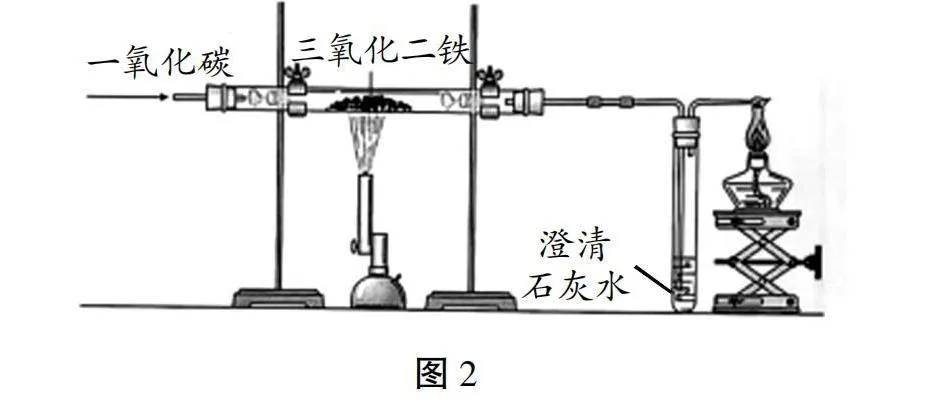
1.探究铁制品生锈的条件(见表1)
师:实验中使用煮沸后冷却的蒸馏水的目的是防止水中溶解氧的干扰;铁生锈是铁与空气中的氧气、水蒸气等发生复杂化学反应;温度高、在酸性或食盐溶液中腐蚀速度快,钢铁纯度越高,腐蚀速度越慢。
2.防止铁制品锈蚀的原理和方法
防锈原理:阻断铁锈蚀所必需的反应物的接触(水与空气)。
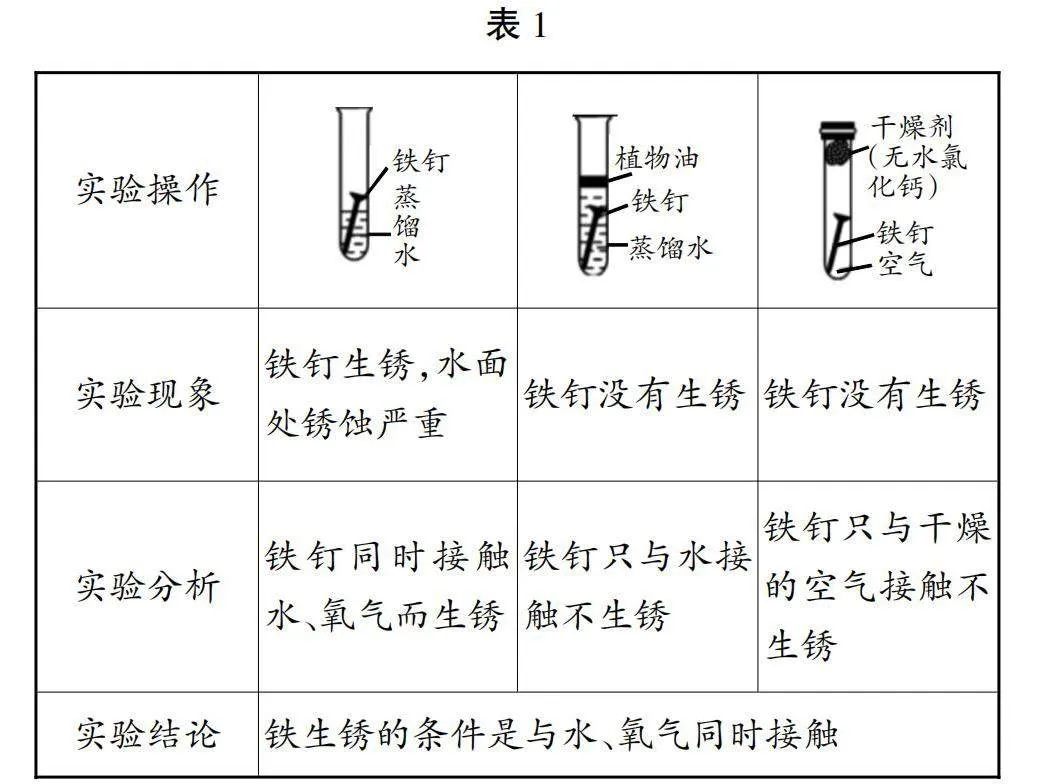
防锈方法(见图3):
除锈方法:物理方法——砂纸打磨;化学方法——酸洗。
铁生锈的利用:在月饼等包装袋中放入袋装铁粉作为干燥剂,吸收包装袋中的水分和氧气;利用铁生锈放热制成暖宝宝。
六、教学反思
金属资源的利用与保护包括地球上及我国的金属资源情况、铁的冶炼、有关化学方程式计算中的杂质问题计算以及金属资源的保护等,既有知识、技能方面的内容,又有环境意识和资源意识等情感领域的内容,与生活、生产联系密切。教师教学时需要注意从多方面对学生进行引导,一是引导学生从熟悉的生活现象中发现问题,通过寻找解决问题的方法,将课本中学到的知识与实际结合起来,体现化学的应用价值。二是发挥学生的主体作用,多设计学生的活动,通过对采集资料的处理和在实验探究活动的观察与分析,获得新的感悟,让他们亲自动手实验,然后总结。三是采用多媒体手段辅助教学后,学生能更加直观地观察到实验现象。按照课本上的方法讲解完以后,顺势引导学生考虑其他方法,然后自主评价,谈谈收获和看法。最后教师总评,激励学生学习的信心。
(作者单位:南京师范大学附属中学丁家庄初级中学)
编辑:温雪莲

