突出“宏微符”化学思维的课堂构建

化学是在原子、分子的基础上研究物质组成、结构、性质及其应用的基础科学。本文以粤教版九年级上册“质量守恒定律”为例,利用实验探究、归纳总结等多种方法引导学生理解“质量守恒定律”知识点,培养学生“宏微符”化学思维。
一、教材分析
“质量守恒定律”是粤教版九年级上册第四章第三节的内容,既是化学学科的重要知识点,也是中考高频考点。教材不是单纯从“质量守恒定律”定义讲解着手,而是设计实验探究,引导学生思考化学反应过程中反应物质量与生成物质量间的关系,提出猜想假设,并进行实验探究、交流讨论、得出结论等探究过程。学生可依据以往所学知识,设计化学实验方案,亲自参与到实验方案设计、实验现象观察、实验结果思考等过程中,从宏观、微观层面认知“质量守恒定律”知识,并熟练运用符号加以表达。
二、学情分析
初中生正处于化学学习的起步阶段,对化学现象并不敏感,仅能分辨化学变化以及物理变化,但对化学变化本质的理解程度不高,尤其是化学反应前后各物质的质量总和。初中生的思维正从形象思维转向逻辑思维,对化学现象的理解并不深入,只能掌握浅显的化学知识,但对质量守恒定律难以灵活运用。学生要想达到核心素养“宏微结合”的要求,应在发现问题—提出假设—设计实验方案—验证假设—总结规律—揭示本质这一探究过程中理解新知。在探究过程中,教师可以引导学生进行自主学习、小组合作学习等活动,实现学生“宏微符”化学思维的有效培养。
三、教学目标
1.通过实验探究理解“质量守恒定律”概念;总结化学反应前后各物质的质量关系;微观角度认识化学反应前后原子种类、质量、数目的变化情况。
2.观察实验探究现象,总结规律,探究本质;参与实验探究活动,锻炼学生的积极性以及动手操作能力;通过剖析化学典型题型,加强对“质量守恒定律”概念的理解,并灵活运用在习题解答中。
3.培养学生“宏微符”化学思维;锻炼学生问题解决能力;感受化学变化美;通过化学实验探究,树立透过实验现象认识事物本质的辩证唯物主义观点。
四、教学过程
(一)新课导入
准备多媒体课件(铜片加热过程、铁丝生锈过程、高锰酸钾加热过程)。
教师通过课件播放视频,并设问:视频中铜片加热、铁丝生锈、高锰酸钾加热发生了化学变化,这些物质在化学变化前后总质量有没有变化呢?又有哪些变化呢?
学生A:我认为化学反应前后总质量发生了变化,反应前的总质量大于反应后的总质量。
学生B:我有不同意见,我认为化学反应前的总质量小于反应后的总质量。
学生C:我认为化学反应前后的总质量是不变的。
(二)实验探究
准备若干锥形瓶、胶塞、注射器、天平、粉末状石灰石、稀盐酸。
教师:让我们看一下教材第111页的实验4-7和实验4-8。两个实验都是石灰石与稀盐酸的化学反应,但这两个化学实验的区别在哪里呢?
学生A:两个实验的区别在于锥形瓶内是否与大气相通。实验4-7是瓶内与大气相通,实验4-8不相通。
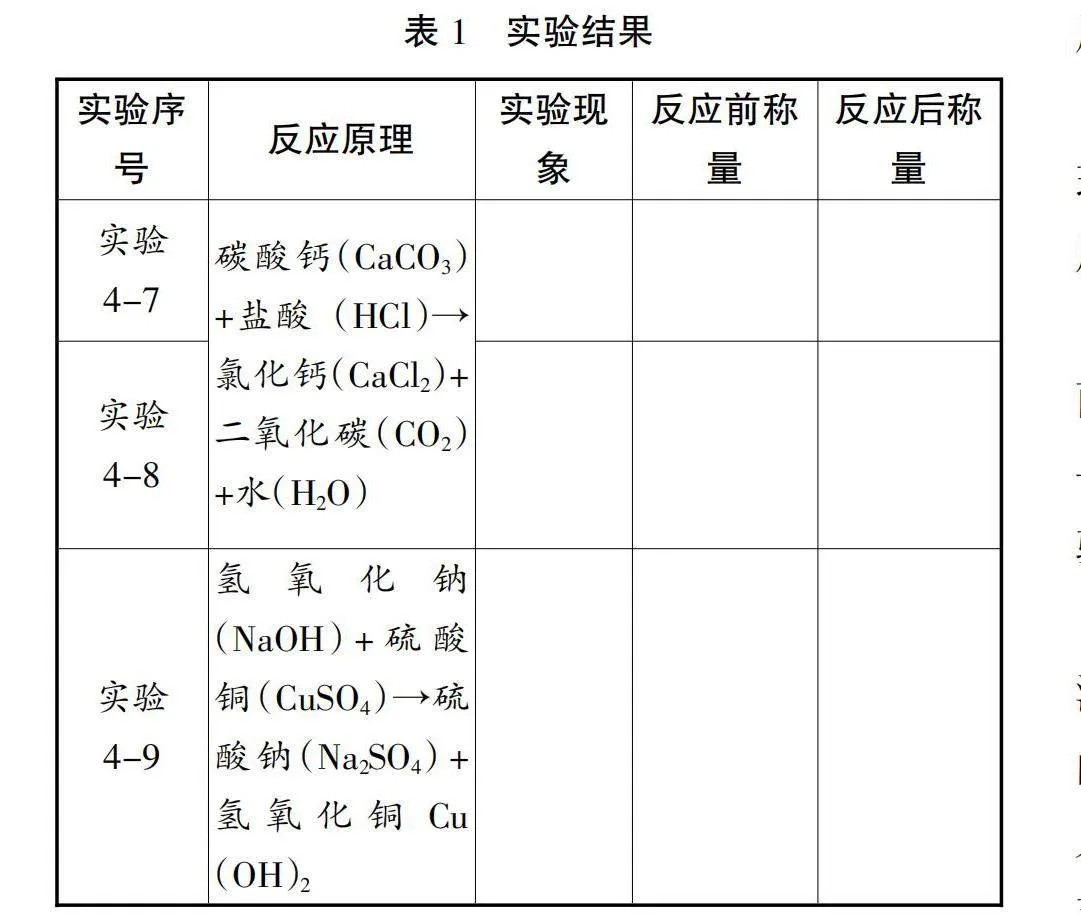
教师:很好,那我们分成小组,按照实验4-7、实验4-8的实验安排、操作步骤进行实验操作,观察实验现象,并填在表1中的相关位置。
小组活动:(1)将0.5 g石灰石粉末装入锥形瓶内,注射器吸入2 mL稀盐酸;(2)将注射器活塞推至1 mL刻度处,将1 mL稀盐酸注入锥形瓶内。记录实验现象。
教师:哪位同学来说一下实验反应原理与实验现象?
学生A:石灰石的主要成分是碳酸钙(CaCO3),化学本质是碳酸钙(CaCO3)与稀盐酸(HCL)发生化学反应。实验现象是有气泡产生。
教师:同学们,让我们写出化学反应方程式。
教师板书。
教师:化学反应前的反应物有石灰石、稀盐酸,化学反应后的生成物有氯化钙、二氧化碳、水,思考一下,化学反应前后物质的总质量是如何变化的?
(小组讨论、探究)
小组A:分别于化学反应前后进行称量,反应前,锥形瓶里的总质量包含0.5 g石灰石和2 mL稀盐酸;反应后,锥形瓶里包含水和氯化钙,但没有二氧化碳,因为锥形瓶与大气相通,二氧化碳逸出瓶外。化学反应前物质总质量高于化学反应后物质总质量,缺少了二氧化碳这部分的质量。
教师:这组同学总结得不错,这是实验4-7的实验结论,那实验4-8呢?
(小组按照实验4-7的操作步骤进行实验4-8,区别在于实验4-8锥形瓶不与大气相通)
教师:哪位同学说一下实验4-8的实验现象与原理?
学生A:实验4-8同样出现了实验4-7的气泡现象,但二氧化碳并未逸出,化学反应前后物质的总质量相等。
教师:实验4-7和实验4-8是同一个实验,但是两者化学反应前后物质的总质量并不相同。为了进一步验证我们提出的假设是否正确,再进行一个实验,看教材第111页实验4-9。
小组活动:(1)锥形瓶中装有5 mL的硫酸铜溶液,注射器吸入3 mL氢氧化钠溶液;检查实验装置的气密性和仪器的完好无损;(2)将注射器的针头插入胶塞中,并缓慢推压注射器活塞,直至达到1 mL刻度处。记录实验现象。
教师:哪组同学说一下实验4-9的实验现象与原理?
小组A:在实验4-9中,溶液颜色由初始的蓝色变为最终的浅绿色;实验生成了蓝色沉淀。化学反应前后物质的总质量相等。
教师:好的,同学们观察得很仔细,让我们写一下实验4-9的化学反应方程式。
教师板书。
教师:通过三个实验,我们可以得出什么结论?
学生A:在化学反应中,反应前各物质的总质量和反应后各生成物的总质量相等。
教师:这就是我们这节课学习的知识点——质量守恒定律。
教师:从宏观角度,我们知道物质是由元素组成的,那立足宏观角度理解实验4-8和实验4-9,总结特征,并加以阐述。
(小组讨论研究)
小组A:我们组认为从宏观角度阐述质量守恒定律主要体现在三个方面,第一是反应前后总物质的质量不变,从称量化学反应前后物质的总质量可知;第二是元素的种类不发生变化,从化学反应方程式前后元素种类情况可知;第三是元素的质量不发生变化,从化学反应方程式前后元素质量可知。
教师:你们还有其他的想法吗?
小组B:我们组认为化学反应前后的物质种类一定会发生变化。
教师:说得很好,我们从宏观角度理解了质量守恒定律,那同学们再思考一下,如何利用微观解释质量守恒定律?
(小组讨论研究,教师在巡视过程中给予相应的提示,宏观上物质是由元素组成的,那微观上物质是由什么构成的呢?以此引导小组学生讨论思考)
小组C:在微观上,物质是由原子以不同方式构成的。化学反应发生前后,原子的数目没有发生改变,原子的种类没有发生改变,原子的质量也没有发生改变。我们可以从碳酸钙与盐酸、氢氧化钠与硫酸铜的化学反应方程式得出结论。
教师:说得不错,还有没有其他的想法?
小组D:虽然原子种类、数量不变,但由原子构成的分子会发生变化,也就是分子的种类一定发生改变。
教师:总结得很好,我们分别从宏观角度和微观角度解释了质量守恒定律。接下来,同学们再思考一下化学分子的数目在化学反应前后发生变化了吗?可以从宏观角度和微观角度再次说明这两个实验吗?
(小组讨论研究)
小组A:我们小组认为分子数目在化学反应前后发生了变化。从石灰石与盐酸的反应方程式可以看出,反应前后的分子数目发生了变化;由碳酸钙、盐酸反应生成氯化钙、二氧化碳与水,分子数目不同。从宏观角度来看,化学变化的现象较为丰富,不仅有气体的释放,也有溶液酸碱性的变化。从微观角度来看,碳酸钙中的一个钙原子与盐酸中的两个氯原子结合,形成一个氯化钙分子;一个碳酸根与两个氢原子结合,形成二氧化碳和一个水分子。
小组B:我们小组认为化学分子数在化学反应前后不发生变化。从硫酸铜与氢氧化钠的反应方程式可以看出,硫酸铜和氢氧化钠的分子数为1∶2,尽管在反应中涉及不同分子的相互作用,但从整个反应方程式中的分子数来看并未发生改变。从宏观角度来说,化学反应生成了蓝色沉淀,溶液也由蓝色转变为绿色;从微观角度来说,铜离子(Cu2+)和氢氧根离子(OH-)的结合,形成不溶于水的氢氧化铜Cu(OH)2沉淀,同时生成硫酸钠(Na2SO4)溶液。
教师:我对化学反应前后分子数变化有着不同的见解,但两个化学反应也都合理,所以说,在化学反应前后分子数可能发生改变,也可能不发生改变。那同学们思考一下元素的化合价在化学反应前后发生变化了吗?
(小组讨论研究)
小组D:在石灰石与盐酸、硫酸铜与氢氧化钠两个化学反应中,各元素的化合价并没有发生变化。
教师:同学们,你们同意这种说法吗?
(大多数学生同意这种说法)
教师:同学们,我有着不同的看法。我认为化学反应前后各元素化合价可能会发生变化,而不是不发生变化的。让我们用下面的实验再来验证一下吧。
(准备镁条、陶土网、火柴、天平)
教师:先在托盘天平的一侧放置陶土网,并在陶土网上放置一段打磨过的镁条,称量记录;再点燃镁条,陶土网上化学反应生成的白色固体,冷却后称量记录。对比化学反应前后质量情况,用化学反应方程式表达,再从宏观、微观角度解释。
(各小组按照教师的实验步骤操作,分别记录了实验前后物质的质量值,并讨论)
小组A:2Mg+O2===2MgO。化学反应后物质的总质量大于化学反应前物质的总质量。出现这种情况的原因:燃烧产生的氧化镁的质量等于反应前镁条的质量加上参与反应的氧气的质量之和。从宏观角度来看,镁燃烧会释放光和热,但这些都不会影响生成白色固体的质量;从微观角度来看,镁吸收氧气中的氧元素生成氧化镁。
教师:你们对镁条燃烧前后物质总质量变化的微观、宏观解释也很好。但我表达的看法是化学反应前后元素化合价发生变化,这一点哪位同学能表达一下?
……
教师:大家都背过元素周期表,镁位于第三周期第二主族元素,最外层有两个价电子,所以在化学反应中,镁常常失去两个电子而呈现+2价;另外,镁单质的化合价为0价。氧单质的化合价为0价,一般情况下氧元素的化合价为-2价。所以我们再来看一下2Mg+O2===2MgO的化学反应方程表达式,化学反应前后的元素化合价有没有发生变化。
学生A:发生变化了,氧元素由反应前的0价变为反应后的-2价;镁元素由反应前的0价变为反应后的+2价。所以,在化学反应前后,元素化合价可能发生变化,也可能不发生变化。
教师:我们将这节课学习的关于质量守恒定律的内涵整理如图1所示,分别从宏观角度、微观角度加以总结。
出示板书:
(三)练习巩固
教师:我们学习了质量守恒定律,了解了质量守恒定律的“六个不变、两个一定变、两个可能变”,接下来我们看一下第113页的第一题。
★在化学反应前后,下列各项中,肯定不会改变的是_____;肯定会改变的是_____;可能改变,也可能不变的是_____。
A.分子的种类 B.原子的种类
C.分子的数目 D.物质的总质量
学生A:肯定不会改变的是物质的总质量和原子的种类;肯定会改变的是分子的种类;可能改变,也可能不改变的是分子的数目。
教师:这一题巩固质量守恒定律概念,考查大家对质量守恒定律的“六个不变、两个一定变、两个可能变”的掌握程度,牢记质量守恒定律对解答化学反应计算类习题有重要意义。
教师:我们再看一下第四题,正确答案是哪个?为什么?
★下列叙述完全符合质量守恒定律的是( )
A.水结成冰前后,质量保持不变
B.50 mL水和50 mL乙醇混合后总体积小于100 mL
C.在100 g过氧化氢溶液中,含有30 g过氧化氢和70 g水
D.1.2 g碳与3.2 g氧气恰好完全反应可生成4.4 g二氧化碳
学生A:我认为答案是C,过氧化氢溶液是由过氧化氢和水混合生成的。
学生B:我认为答案是D,因为D是化学反应,A、B、C都是物理变化。题干中的关键点在于“质量守恒定律”,其适用于化学反应,而不是物理变化,所以正确答案是D。
教师:这位同学说得很好,正确答案是D。在这个习题中,要区别化学反应还是物理变化,才能更好地判断各答案的正误。
教师:剩余的习题大家可以在课后完成,作为本节课的作业。
五、教学反思
在本节课中,教师要引导学生在实验探究中培养学生的“宏微符”化学思维,让学生分别从宏观角度、微观角度理解质量守恒定律,增强学生对符号的理解程度,从而让学生享受化学学习的快乐。在整个教学活动中,依然存在一定的不足之处,教材上的习题为基础型作业,缺乏拓展型作业、实践型作业的设计,未能涵盖各个层次的学生。
(作者单位:甘肃省天水市甘谷县六峰初级中学)
编辑:温雪莲

