2016至2020年杭州地区无偿献血人群HIV感染状况分析
励晓涛 董杰 凌霞 祝宏 吴丹霄

[摘要] 目的 了解杭州地区无偿献血人群HIV感染状况,为本地区降低HIV经输血传播风险,制定有效献血者招募及艾滋病防控策略提供数据支持。方法 采用酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)和病原体核酸检测技术(nucleic acid testing,NAT)对2016年1月至2020年12月杭州地区902 847例无偿献血者标本进行抗HIV-Ⅰ/Ⅱ抗体/抗原和HIV RNA检测。抗-HIV抗体/抗原或HIV RNA 反应性标本送杭州市疾病控制中心进一步采用Western blot法和NAT进行确认。结果 2016年1月至2020年12月杭州地区共检测HIV确证阳性103例,阳性检出率为0.01%,其中101例ELISA和NAT筛查均为阳性反应,2例ELISA筛查为阴性反应,NAT为阳性反应。103例感染者中,以男性(91.26%,94/103)、18~35岁(69.90%,72/103)、初次献血者(68.93%,71/103)为主。2016至2020年献血者HIV阳性率呈逐年下降趋势(χ2= 7.181,P=0.007)。男女献血者HIV陽性率各年的差异无统计学意义(χ2= 10.336,P=0.350;χ2= 0.653,P=0.957)。各年龄组献血者HIV阳性率各年的差异无统计学意义(χ2= 6.378,P=0.173;χ2=2.318,P=0.678;χ2= 5.284,P=0.259;χ2= 9.183,P=0.057)。结论 近5年HIV感染在杭州市无偿献血人群中呈低流行水平,但仍存在感染风险,应加强在低危人群中招募献血者并且应采用先进的检测技术,选择合适的检测策略,保证血液安全。
[关键词] 献血者; HIV感染; 酶联免疫吸附试验;核酸检测
[中图分类号] R446.6 [文献标识码] A [DOI] 10.3969/j.issn.1673-9701.2024.14.003
Analysis on HIV infection status of unpaid blood donors in Hangzhou from 2016 to 2020
LI Xiaotao1, 2, DONG Jie1, 2, LING Xia1, ZHU Hong1, 2,WU Danxiao1
1.Blood Center of Zhejiang Province, Hangzhou 310006, Zhejiang, China; 2.Zhejiang Provincial Key Laboratory of Blood Safety Research, Hangzhou 310006, Zhejiang, China
[Abstract] Objective To understand the status of HIV infection among unpaid blood donors in Hangzhou, and to provide data support for reducing the risk of HIV transmission through blood transfusion, and formulating effective blood donor recruitment and AIDS prevention and control strategies in Hangzhou. Methods Enzyme-linked immunosorbent assay (ELISA) and nucleic acid testing (NAT) were used to detect HIV-I/ Ⅱ antibody/antigen and HIV RNA from 902 847 unpaid blood donors in Hangzhou from January 2016 to December 2020. Anti-HIV antibody/antigen or HIV RNA reactive samples were sent to Hangzhou Center for Disease Control (CDC) for further confirmation by Western bloting and NAT. Results A total of 103 HIV positive cases were detected in Hangzhou area from January 2016 to December 2020, with a positive detection rate of 0.01%, 101 cases were positive for ELISA and NAT screening, 2 cases were negative for ELISA screening and positive for NAT. Among the 103 infected patients, males (91.26%, 94/103), 18–35 years old (69.90%, 72/103), and first-time blood donors (68.93%, 71/103) were the majority. The positive rate of HIV among blood donors decreased year by year from 2016 to 2020 (χ2= 7.181, P=0.007), but there was no significant difference in HIV positive rate between male and female blood donors (χ2= 10.336, P=0.350; χ2= 0.653, P=0.957). There was no significant difference in HIV positive rate among blood donors of different age groups (χ2= 6.378, P=0.173; χ2 = 2.318, P = 0.678; χ2= 5.284, P=0.259; χ2= 9.183, P=0.057). Conclusion In recent 5 years, HIV infection has been at a low epidemic level among unpaid blood donors in Hangzhou, but there is still an infection risk. It is necessary to strengthen the recruitment of blood donors from low-risk groups, adopt advanced detection technology and select appropriate detection strategies to ensure blood safety.
[Key words] Blood donors; HIV infection; Enzyme linked immunosorbent assay; Nucleic acid testing
近几年随着医疗技术水平的进步,血液及血液制品在临床疾病治疗领域比如外伤、分娩、血液病等得到广泛应用,挽救了患者的生命,但也导致一些血液传播疾病的感染风险[1]。由于现有医学技术限制,无法克服HIV检测的“窗口期”,导致血液安全受到影响,近几年出现经输血传播HIV的事件[2-3]。《血站技术操作规程》2015版要求自2016年3月1日起,血供血机构对献血者捐献的血液进行核酸检测,缩短检测的“窗口期”,降低输血传播疾病风险。尽管如此,到目前为止仍无法完全排除窗口期造成的感染[4]。因此,需加强献血者献血前的健康教育、筛查,从低危献血者中采集血液,保证血液的安全。
1 资料与方法
1.1 一般资料
对献血者进行献血前健康征询和一般检查,经献血者知情同意后采集2016年1月至2020年12月无偿献血者标本,并对其进行HIV抗体和HIV核酸检测。献血者同意可匿名用于血液安全相关的科学研究,并且同意血站向CDC报告艾滋病感染等检测阳性的结果和个人资料。
1.2 检测方法
1.2.1 抗HIV抗体/抗原筛查检测 酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)采用两个不同厂家的抗HIV抗体/抗原 ELISA试剂进行检测,分别为珠海丽珠有限公司和美国BIO-RAD公司产品,其中BIO-RAD公司采用第4代HIV检测试剂,联合检测P24抗原。所有试剂均为中国药品生物鉴定所批批检合格产品,并严格按照试剂说明书要求进行操作和判定。抗HIV抗体/抗原 ELISA试剂初次检测呈现反应性,采用原有试剂进行双孔复试。双孔中至少有1孔呈现反应者,判定该试剂抗HIV抗体/抗原检测有反应性。两种试剂中任意1种试剂呈现反应性,判定该标本抗HIV抗体/抗原检测呈现反应性。抗HIV抗体/抗原ELISA试剂初次检测呈现无反应性或双孔复试中两孔均为无反应性,即判定该试剂抗HIV抗体/抗原检测无反应性。两种试剂均呈现无反应性,判定该标本抗HIV抗体/抗原检测无反应性。
1.2.2 核酸检测 病原体核酸检测技术(nucleic acid testing,NAT)采用西班牙Grifols公司和美国Roche Molecular Systems公司的试剂及其配套的操作平台,严格按照试剂和仪器说明书进行操作和结果判定。单检和混样(分项目或混合项目)按照检测模式判定规则检测结果为无反应性的,报告核酸检测合格;检测结果为有反应性的,报告核酸检测不合格。
1.2.3 抗-HIV抗体/抗原或HIV RNA 初筛阳性的血液标本送杭州市CDC的HIV确证实验室采用 Western blot法和NAT确认(全国艾滋病检测技术规范 2020年修订版[5]),阳性者判定为HIV感染者。
1.3 统计学方法
采用SPSS 21.0 统计学软件对数据进行处理分析,计数资料用例数(百分率)[n(%)]表示,采用χ2 检验。P<0.05为差异有统计学意义。
2 结果
2.1 HIV阳性率比较
2016年1月至2020年12月共检测献血者血液标本902 847个,HIV确证阳性103例,HIV阳性率为0.01%。HIV阳性率呈逐年下降趋势,差异有统计学意义(χ2= 7.181,P=0.007)
2.2 HIV确认阳性标本ELISA和核酸检测结果分析
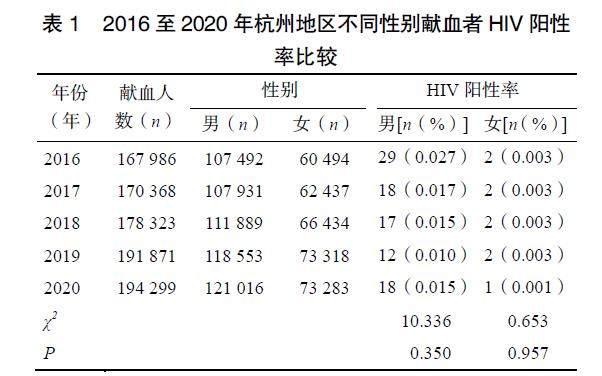
2016年1月至2020年12月杭州地区共检测出HIV确证阳性103例,其中101例ELISA和NAT筛查均为阳性反应,2例ELISA筛查为阴性反应。2016年1月至2020年12月男性无偿献血者566 881人,HIV感染者94例,女性无偿献血者35 966名,HIV感染者9例。男性和女性各年间HIV阳性率差异无统计学意义,见表1。
2.3 不同年龄组献血者HIV阳性率比较
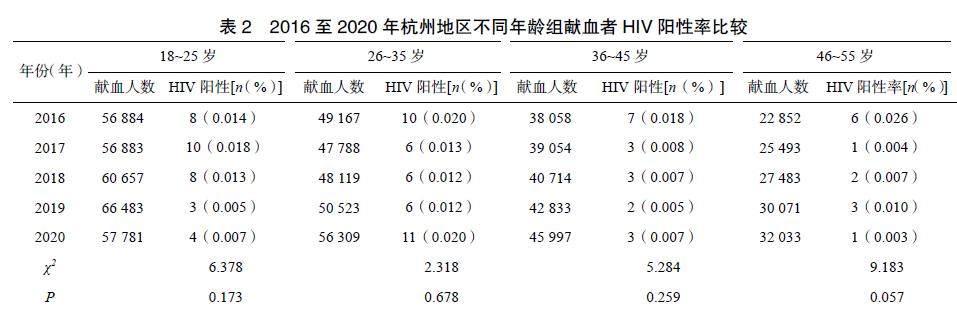
2016年1月至2020年12月杭州地区无偿献血者18~25岁、26~35岁、36~45岁、46~55岁各年龄组HIV感染者分别为33例、39例、18例、13例,各年龄组各年间HIV阳性率差异无统计学意义,见表2。
2.4 HIV阳性献血者人口学特征
103例HIV确认阳性的感染者中,男性占91.26%,18~35岁青年人占69.90%,本市占18.45%;大专及本科占33.01%,高校学生占12.62%;初次献血者占68.93;捐献全血占98.06%。
3 讨论
目前艾滋病已严重威胁我国公众的健康。截止2022年底,全国报告存活HIV感染者122.3万例,死亡4.18万例,新发10.78万例[6]。我国HIV感染者95%以上是通过性途径感染,这种传播途径可能在艾滋病从高危人群向普通人群传播发挥桥梁作用,这无疑给血液安全带来一定的压力[7]。全国各地无偿献血人群HIV阳性率存在一定的差异,2016至2020年杭州地区无偿献血者HIV感染状况呈低流行水平,阳性率为0.01%(11/10万)低于广州地区HIV阳性率29.6/10万,洛阳地区HIV阳性率22/10萬和唐山市HIV阳性率19.9/10万[8-11]。自2011年起浙江省采供血机构开展阻断经输血传播HIV项目,从血站、血站员工和献血者三个方面着力,献血者HIV感染快速上升的趋势被遏制,2016至2020年杭州地区HIV阳性率出现逐年下降趋势[12]。
随着2010年核酸检测试点工作的推进,浙江省血液中心检测模式从原来的2次ELISA法改为两次ELISA法和1次核酸检测。自开展核酸检测以来,发现血清学阴性核酸阳性的HIV感染者两例,1例Western blot法鉴定为HIV-1抗体阳性,1例为NAT阳性,核酸检测缩短了HIV窗口期。目前国外许多国家献血者HIV的筛查采用化学发光免疫分析(chemiluminescence immunoassay,CLIA)法和NAT,化学发光法比较ELISA具有较高的特异性和敏感度,但是由于化学发光试剂使用成本相对较高,限制了CLIA在血站献血者筛查方面的推广应用。因此目前开展NAT和ELISA共同检测可以有效的避免漏检并缩短窗口期,更能确保血液安全,降低经输血传播HIV残余风险[13-16]。
但是由于窗口期的存在,并不能完全依靠检测手段排除经输血感染HIV的风险。所以应采取一系列的措施从源头上阻断经输血传播HIV。第一,当地政府部门要加大防艾教育的力度,将艾滋病预防工作与无偿献血宣传活动结合起来[17]。2017年国务院下发的《中国遏制与防治艾滋病“十三五”行动计划》中指出通过发挥社会公众人物影响和互联网、微博、微信等新媒体作用和一系列专题讲座增强宣传效果,居民和易感染艾滋病重点和危险行为人群知晓艾滋病防治知识分别达到80%和90%以上,公民在献血前能够自我排除,保证从低危献血者中采集血液[18]。第二,应加强一线医务人员的培训,提升工作人员征询排查水平,拒绝潜在高危献血者献血。本研究发现103例HIV感染的人群中以男性、18~35岁青年人、初次献血者为主,这与既往研究的结果相一致[19-20]。所以在咨询时应该特别关注这类献血人群。第三,建立区域性献血者屏蔽监测系统,从源头上阻止高危行为献血者的异地献血,保证血液安全[21]。目前,HIV确认阳性献血者信息共享系统在华东地区建立,实现几个城市之间HIV确认阳性献血者的联合屏蔽[22]。继续推进与疾病预防控制中心的信息联网,共享HIV确证阳性人员信息,防止HIV感染者恶意献血。
随着新的输血技术的进一步发展,一些新的输血技术对于防止HIV通过输血感染发挥了重要的作用。自身输血技术,可以避免由于输注异体血液导致感染风险[23]。有研究表明,使用亚甲蓝光化学法处理血浆,可将人类免疫缺陷病毒灭活效果达到5logs以上[24]。目前仍在研究阶段未广泛用于临床的人工血液,可以缓解医疗系统用血紧张状况,避免HIV造成的输血传播。
利益冲突:所有作者均声明不存在利益冲突。
[参考文献]
[1] SEHGAL S, SHAIJI P S, BRAR R K , et al. Seroprevalence and trend of transfusion transmissible infection in blood donors in Andaman and Nicobar island-an institutional retrospective study [J]. J Clin Diagn Res, 2017, 11(4): 21–24.
[2] 刘嘉馨, 耿鸿武, 孙俊, 等. 中国输血行业发展报告(2017)[M].北京: 社会科学文献出版社, 2017: 383–397.
[3] CHEN S, LU X, BAI G, et al. Twenty-seven year surveillance of blood transfusion recipients infected with HIV-1 in Hebei Province, China[J]. PLoS One, 2018, 13(8): e0202265.
[4] 国家卫生健康委. 血站技术操作规程[EB/OL]. (2019-04- 28)[2024-03-06].http://www.nhc.gov.cn/yzygj/s7658/201905/bdd4f4ccd15c4201bfb6d9e7492d7fab.shtml.
[5] 中国疾病预防控制中心.全国艾滋病检测技术规范 (2020年修订版)[EB/OL]. (2020-04-27)[2024-03-06]. https://ncaids.chinacdc.cn/fzyw_10256/gzjz_10269/202005/W020200522484711502629.pdf.
[6] 汪俊杰, 杜凌遙, 唐红, 等. HIV感染的全程综合管理策略[J]. 中华临床感染病杂志, 2023, 16(2): 113–119.
[7] SHIL, LIUV, J WANGJX, et al. HIV prevalence and incidence estimates among blood donors in five regions in China[J]. Transfusion, 2020, 60(1): 117–125.
[8] 宋文倩, 张丽, 高勇, 等. 全国357家省、市两级采供血机构检测的献血人群HIV检出率调查[J]. 中国输血杂志, 2012, 25(12): 1244–1246.
[9] 黎世杰, 冯凡凡, 陈锦艳, 等. 2010-2015年广州地区无偿献血人群HIV感染现状分析[J]. 临床输血与检验, 2018, 20(5): 457–462.
[10] 陈善华, 朱丽莉, 吴宗泽, 等. 2011-2018 年洛阳地区无偿献血人群HIV感染情况[J]. 江苏预防医学, 2019, 30(4): 301–303.
[11] 趙婧, 徐微微, 周红艳. 2015—2019年唐山市无献血人群HIV感染状况及其特征分析[J]. 国际病毒学杂志, 2022, 1: 58–61.
[12] 孟忠华, 陈安心, 吕豪, 等. 浙江省采取综合措施阻断经输血传播HIV的探索[J]. 中国输血杂志, 2015, 28(8): 885–887.
[13] PRIYADARSINI J A, HEM C P, POONAM C, et al. Comparative evaluation of ADVIA Centaur? XP chemiluminescence system for screening of HBV, HCV, HIV and syphilis in Indian blood donors [J]. Transfusion Apheres Sci, 2022, 61(2): 103318.
[14] 王远芳, 李冬冬, 谢轶, 等. 人类免疫缺陷病毒实验室诊断策略的实施与质量控制[J]. 中华预防医学杂志, 2023 , 57(1): 1–7.
[15] Fiedler S A, Oberle D, Chudy M, et al. Effectiveness of blood donor screening by HIV, HCV, HBV-NAT assays, as well as HBsAg and anti-HBc immunoassays in Germany (2008-2015)[J]. Vox Sang, 2019, 114(5): 443–450.
[16] Ye X, Li T, Shao W, et al. Nearly half of ultrio plus NAT non-discriminated reactive blood donors were identified as occult HBV infection in South China[J]. BMC Infect Dis, 2019, 19(1): 574–578.
[17] 夏云峰. 个性化PITC策略对控制无偿献血人群HIV感染率的影响[J]. 中国当代医药, 2019, 26(25): 192–194.
[18] 何松芹, 冯岩. 2011–2018 年漯河地区无偿献血人群HIV感染状况分析[J]. 河南预防医学杂志, 2020, 31(12): 884–886.
[19] ZengPB, JI LiuJ, ZhangCH, et al. Current risk factors for HIV infection among blood donors in seven Chinese regions [J]. Transfusion, 2020, 60(2): 326–333.
[20] May S, Murray A, Sutlon M Y. HIV infection among women in the United States: 2000-2017[J]. AIDS Care, 2020, 32(4): 522–529.
[21] 王擁军, 周华平, 陈安心, 等. 构建献血者监测系统阻断输血传播HIV的策略[J]. 中国输血杂志, 2017, 30(7): 776–778.
[22] 孔长虹, 高瑜, 徐晔彪, 等. 华东地区HIV确认阳性献血者信息共享系统的建立[J]. 中国公共卫生, 2020, 36(9): 1365–1367.
[23] 王承琳, 张锡敏. 自体输血的临床应用发展现状[J]. 临床血液学杂志, 2019, 32(4): 319–321.
[24] 黄佳丽, 刘正婷, 陈尚良, 等. 亚甲蓝光病毒灭活血浆的研究进展[J]. 临床输血与检验, 2021, 23(2): 268–272.
(收稿日期:2023–07–01)
(修回日期:2024–03–06)

