多重技术在神经内镜下经鼻蝶垂体大腺瘤切除的应用
黄 进,孙 骏,计 巍,程 超,焦建同,黄维一,邵君飞
(南京医科大学附属无锡人民医院神经外科,江苏 无锡 214023)
随着神经影像、神经导航及神经内镜技术的不断发展和进步,内镜下经鼻蝶鞍区肿瘤的手术疗效得到显著提高,但对初始开展神经内镜下切除垂体大腺瘤的医疗单位,如何降低术后并发症(如脑脊液漏、颅内感染、颅内出血等),提高手术疗效一直困扰着手术医师[1-2]。本研究回顾性分析2019 年-2022 年43 例采用多重技术辅助神经内镜经鼻蝶切除垂体大腺瘤的临床资料,现报告如下。
1 对象与方法
1.1 临床资料 男20 例,女23 例;年龄24~71 岁,平均(33.2±2.4)岁;平均病程(11.2 ±1.5)个月。临床表现:头痛15 例,视力、视野改变12 例,月经紊乱3例,性功能减退4 例,肢端肥大4 例,Cushing 病临床表现2 例,无明显临床症状3 例。Knosp 分级:Ⅱ级24 例,Ⅲ级13 例,Ⅳ级6 例。病理分型:泌乳素(PRL)型9 例,生长激素(GH)型5 例,促肾上腺皮质激素(ACTH)型5 例,无功能型24例。病人均行头颅鞍区薄层CT、MRI 检查,包括T1、T2、Flair、T1增强、MRA及相应导航序列。
1.2 手术治疗
1.2.1 术前准备: 神经导航系统(StealthStation工作站)将术前影像融合进行术前评估,了解颅底骨质和蝶窦气化情况。本组病例蝶窦呈甲介型4例,鞍前型25 例,鞍型14 例。术前常规剪净鼻毛并清洗鼻腔,给予左氧氟沙星滴眼液和麻黄碱滴鼻液滴鼻,术前1d 根据病人内分泌指标给予氢化可的松静脉应用。
1.2.2 手术设备: Medtronic(S7.0)神经导航系统,德国Karl Storz 神经内镜及配套手术器械、视频采集系统,美敦力微型高速磨钻。
1.2.3 手术方法: 病人仰卧位,全麻成功后,头后仰10°~15°,偏向术者10°~20°,Mayfield 头托固定。头架连接导航参考架,注册成功后,安尔碘常规消毒面部和鼻腔,铺无菌巾,更换无菌参考架与探针,将气动臂固定于手术床后安装Storze 内镜,在0°内镜引导下,使用浸有盐酸羟甲唑啉(达芬霖)的棉片收缩鼻腔黏膜,同时予安尔碘反复清理鼻道,通过双侧鼻孔进入辨认下鼻甲、中鼻甲、上鼻甲,寻找并确认蝶窦开口与后鼻孔,做带蒂鼻中隔弧形黏膜瓣备用。根据病人蝶窦实际发育情况,导航辅助下磨除蝶窦前壁,蝶窦内分隔,显露并磨开鞍底,根据肿瘤大小开窗直径1~1.5cm,常规穿刺针穿刺鞍内,证实安全后,切开鞍底硬膜。根据海绵间窦出血情况决定是否应用流体明胶止血,在切开菲薄透明的垂体包膜后,即可明确假包膜界面,锐性切开假包膜沿假包膜界面仔细钝性分离腺瘤。沿假包膜按顺序切除肿瘤,首先切除背侧及两旁的肿瘤组织,再处理腹侧及鞍上的肿瘤,随着肿瘤切除,换用30°内镜探查术野,以便全切腺瘤,止血纱、明胶海绵填充术区止血,庆大霉素注射液冲洗鞍区。根据脑脊液漏情况进行个体化颅底修复:对术中无脑脊液漏或仅有低流量脑脊液漏病人,仅采用鞍底硬膜缝合、鼻外纱条支撑。术中有明显脑脊液漏者,采用自体脂肪、阔筋膜、鞍底硬膜缝合。而对于术中高流量脑脊液漏者,则应用自体脂肪、可吸收人工脑膜、自体阔筋膜、带蒂鼻中隔黏膜瓣分层修补,间断缝合硬膜术后填塞瘤腔,最后予纱条支撑填塞鼻腔(图1)。
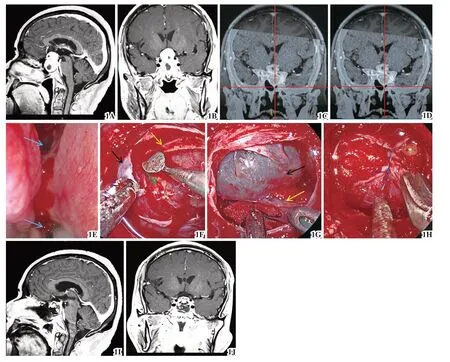
图1 神经内镜下经鼻蝶切除垂体大腺瘤1A、1B 术前T1增强MRI提示垂体大腺瘤,肿瘤超出左侧颈内动脉海绵窦段与床突上段的内侧连线,提示海绵窦受侵犯可能1C、1D 神经导航MRI/CT 影像融合指导下定位蝶窦分隔及鞍底暴露范围1E 镜下确认蝶筛隐窝及后鼻孔开口(箭头所示),并以此基准做鼻中隔带蒂黏膜瓣1F 根据术前影像及神经导航影像融合指导镜下充分开窗,创面止血充分,识别腺瘤周围的膜性结构,假包膜外分离技术可有效提高肿瘤的全切率(黑色箭头指示鞍底硬膜,黄色箭头指示垂体包膜,绿色箭头指示假包膜及肿瘤组织)1G 大部分切除肿瘤后鞍隔塌陷,在保护垂体功能的前提下,进一步切除鞍隔表面残余肿瘤(黄色箭头指示鞍隔表面残余肿瘤,黑色箭头指示受压的正常垂体)1H 切除肿瘤后根据脑脊液漏情况镜下行多重颅底修复:自体脂肪、可吸收人工脑膜、自体阔筋膜、带蒂鼻中隔黏膜瓣分层修补、间断缝合硬膜术后填塞瘤腔1I、1J 术后1d复查MRI提示肿瘤全切除,鞍内局部高信号为脂肪填塞、覆盖整个鞍隔
2 结 果
本研究43例病人进行手术治疗,术中均未发生损伤海绵窦、颈内动脉、误入颅前窝底、斜坡等严重并发症。术中观察到9例肿瘤真正侵入海绵窦,而其余34 例未侵入海绵窦。术中镜下观察到36 例病人未出现脑脊液漏,而7例病人出现脑脊液漏,根据脑脊液漏严重程度分为Ⅰ级4例,Ⅱ级2例,Ⅲ级1例。
在术中修补方面,根据脑脊液漏的情况进行个体化处理。对于36 例无脑脊液漏和4 例低流量脑脊液漏的病人,采用鞍底硬膜缝合、鼻外纱条支撑的方法进行修补。2例术中有明显脑脊液漏的病人,采用自体脂肪、阔筋膜、鞍底硬膜缝合的方式进行修补。1 例术中高流量脑脊液漏的病人,应用自体脂肪、可吸收人工脑膜、自体阔筋膜、带蒂鼻中隔黏膜瓣进行分层修补,并通过间断缝合硬膜术后填塞瘤腔,最后予纱条支撑填塞鼻腔。
术后43 例病人均未出现脑脊液鼻漏,9 例病人出现一过性尿崩,3例出现颅内感染,经对症治疗后均好转。对于特定类型的垂体腺瘤,如9例PRL型腺瘤,术后PRL 水平恢复至正常或以下;5 例GH 型垂体腺瘤术后GH及IGF-1水平均达到正常范围;5例ACTH型腺瘤术后相关激素水平也恢复正常。
术后48h 复查MRI提示肿瘤全切除39 例,次全切除4 例。术后3 个月、6 个月和1 年的复查中,39 例肿瘤全切除病例未见复发;4 例次全切除病例中,3例无明显进展,1例接受再次手术并恢复良好。
3 讨 论
神经内镜手术作为微侵袭神经外科的关键技术,具有显著优势。对于内镜下经蝶入路的手术方式,神经导航的应用尤为关键,其能够有效解决手术视野受限导致定位困难的问题,尤其在处理蝶窦气化不良时表现突出[3-4]。在应对常规垂体腺瘤手术时,若肿瘤大小适宜、位置居中、侵袭程度低且蝶窦分化良好,经验丰富的术者可凭借精湛技艺实现满意的肿瘤切除和手术效果,无需依赖神经导航。然而,为确保手术过程的安全与稳定,在条件允许的情况下,建议将神经导航作为备选工具,以应对可能出现的意外情况。
3.1 假包膜外分离 垂体大腺瘤在生长过程中通常会将海绵窦内侧壁向外侧推挤,而非真正侵入其内部。海绵窦受侵犯的影像学特征主要包括肿瘤包绕颈内动脉海绵窦段,海绵窦内侧部分信号被肿瘤替代,以及肿瘤超出颈内动脉海绵窦段与床突上段的连线等[5-7]。这些影像学特点有助于医者更准确地评估垂体大腺瘤的生长状态和侵袭程度。同时,垂体腺瘤假包膜是存在于肿瘤与正常垂体组织之间的一种特殊结构,其发现至今已有近90 年的历史[8]。尽管对其组织学来源和组成结构仍存在争议,但多数学者认为其是由肿瘤周围相邻细胞基底膜受压形成,主要成分包括成纤维细胞、胶原纤维以及受压的正常垂体细胞[8-10]。然而,在大型肿瘤中,假包膜可能因肿瘤发展过程中膨胀和拉长,或肿瘤细胞侵袭而变得不连续或被破坏。此外,从形态学角度来看,假性包膜并非总是完全覆盖整个肿瘤表面,有时仅部分覆盖。这一特点使得在手术过程中需要更加精细地操作,充分利用假包膜与肿瘤之间的解剖关系,实现更高的全切率。
笔者认为,对于Knosp Ⅲ级以下及部分Ⅲ级的垂体瘤,尽量做到假包膜外整块切除(En bloc 切除技术)。对于Knosp Ⅳ级形态不规则的巨大肿瘤,术中海绵窦出血、颈内动脉(ICA)损伤以及脑脊液漏风险极大,甚至术后局部血肿或填塞物过多导致的占位效应可能会引起脑神经麻痹或损伤。为避免此类并发症,需在术前进行准确的手术计划和影像学评估,术中导航和电生理监测等技术的应用可帮助确认ICA 及周围重要神经血管结构的走行[11]。手术过程中,广泛显露,肿瘤与其包膜之间的黏连应通过细致的钝性分离,镜下辨别肿瘤与正常结构,尽可能保持膜结构完整性[12]。早期控制静脉出血后,选择性离断周围韧带,逐步游离瘤体可减少手术对ICA 的损伤,如果预计术中ICA 损伤风险很高,则可在这些风险区域进行次全切除,并通过后续放疗来治疗残余肿瘤[13]。
3.2 个体化颅底修复 垂体大腺瘤切除过程中,由于假包膜破损、自身缺损以及与鞍隔紧密黏连,常无法整块切除肿瘤。不同手术医师的分离技巧差异,导致脑脊液漏成为术后常见的并发症。术中脑脊液漏是术后脑脊液漏的独立危险因素,多数术后脑脊液漏源于术中修补失败[14-15]。内镜下定位漏口是脑脊液漏修补术的关键步骤。术中脑脊液漏根据漏口大小可分为三级[16-18]:Ⅰ级为裂隙状或小孔状缺损,伴有少量脑脊液渗漏;Ⅱ级为硬膜缺损直径<5mm,伴有明显脑脊液漏;Ⅲ级为硬膜缺损直径>5mm,可见大量脑脊液漏,高流量脑脊液漏主要发生在扩大经鼻蝶入路手术中。
预防术中脑脊液漏和鞍底修补重建是减少术后脑脊液鼻漏的关键措施。随着颅底修复技术的不断发展,如带蒂鼻中隔黏膜瓣、Gasket-seal 技术、原位骨瓣回纳技术、鞍底缝合技术的进步,鞍底重建效果得到显著提升,术后脑脊液漏的发生率已明显降低[19-20]。然而,过度修补也可能引发一系列并发症,如鼻中隔穿孔、鼻腔出血、鼻腔干燥、嗅觉减退甚至丧失等,因此需要在术中精细操作,避免过度修补带来的附加损害。
颅底重建的理想状态在于将手术过程中产生的缺损恢复至其正常的解剖层次,即实现解剖结构的完整性与层次性的精准复原。在此过程中,最大程度地保留原有的解剖层次,不仅是重建的最佳标准,也是确保术后功能恢复与减少并发症的关键所在。因此,颅底重建的终极目标是通过精细的手术操作,使颅底结构恢复至其生理状态下的解剖层次,从而达到最佳的重建效果[21-22]。笔者认为在颅底修复过程中,脂肪组织的填塞修补极其重要,一般取大腿皮下脂肪和阔筋膜用于修补,完全覆盖于缺损处。本组病例术中出现明显脑脊液漏者,术者将脂肪覆盖整个鞍隔及周围结构,脂肪组织不仅作第一层修补材料,而且术中可呈沙漏状放置于硬膜内外,并置于蝶窦内作为阔筋膜的支撑。笔者认为:术中脂肪封堵硬膜破口时,不可过度填塞,以无脑脊液渗出及脂肪原位搏动良好作为修补良好的标志。此外,术中明胶海绵的少量应用仅为分隔鞍内及蝶窦,不应影响引流液从蝶窦流出,在此基础上,应用鼻中隔黏膜或带蒂黏膜瓣覆盖鞍底作用显著,但鼻中隔黏膜瓣的应用会影响病人鼻腔的舒适性,对术中无脑脊液漏或仅低流量脑脊液漏病人,可仅采用鞍底硬膜缝合、鼻外纱条支撑;术中有明显脑脊液漏者,采用自体脂肪、阔筋膜、鞍底硬膜缝合;而对于术中高流量脑脊液漏者,则应用多重颅底修复技术。术中个体化修复技术实时封堵漏口、覆盖鞍隔及周围结构,以及术中鼻腔良好的底部支撑,术后根据病情行腰椎穿刺持续引流,有效抗生素的应用,及细致的护理指导,不仅可提高脑脊液漏修补成功率,也可降低术后颅内感染发生率。
在现代垂体瘤诊疗的多学科诊疗(multidisciplinary treatment,MDT)模式下,多学科团队针对病人的神经症状、内分泌指标、全身情况、神经影像及个体需求进行全面评估,制定出规范的个体化诊疗方案。手术成功的关键取决于手术医师的经验,对垂体内分泌功能的认识是临床诊断、围手术期管理及术中保护垂体功能的核心,良好的手术疗效是改善病人预后及生活质量的前提,神经导航影像融合技术有助于手术医师评估肿瘤及其与周边结构的位置关系,尤其适合于对残留或复发肿瘤的再次手术。内镜下辨别腺瘤周围的膜性结构,在保护垂体功能的前提下,尽可能切除假包膜和腺瘤可有效提高肿瘤的全切除率,日渐成熟的个体化颅底修复技术可显著降低脑脊液鼻漏的发生率。

