基于文献挖掘的雷公藤制剂建立卵巢功能障碍动物模型分析
程齐,丁樱,,黄欣,徐闪闪(.河南中医药大学儿科医学院,河南 郑州 450046;.河南中医药大学第一附属医院儿童医院,河南 郑州 450000)
雷公藤(tripterygium wilfordii,TG)是祖国传统医药宝库中的一味治疗免疫性疾病疗效显著的中草药,随着现代工艺技术发展,已经从雷公藤药用部位提取出多种衍生物,如:雷公藤多苷、雷公藤甲素等[1-2],此外还从雷公藤落叶中提取出了新成分雷络酯[3]。雷公藤及其衍生制剂在临床使用中常出现卵巢功能障碍等生殖毒性,利用这一特点,在动物实验中常被用来制备卵巢功能损伤动物模型[4-5]。本研究检索相关数据库建库至今公开发表的有关应用雷公藤及衍生制剂建立卵巢功能障碍动物模型的实验研究文献,对其实验动物种类、给药剂量及周期等进行归纳分析,以期对未来研究雷公藤制剂建立卵巢功能障碍动物模型标准化提供参考。
1 资料与方法
1.1 数据来源
1.1.1数据库 计算机检索中文数据库(维普数据库、万方数据库、中国医学生物文献数据库、中国知网)和英文数据库(Embase、Cochrane library、PubMed、Springer、Web of Science)的相关文献。
1.1.2检索时间及时段 检索时间为2023年8月1日,检索时段设置为各数据库2000年1月1日至2023年7月31日。
1.1.3检索词 中文检索词为“雷公藤”“卵巢”和“动物模型”等;英文检索词为“tripterygium glycosides”“ovary”“animalmodel”等。
1.2 纳入与排除标准
1.2.1纳入标准 各数据库2000年1月1日至2023年7月31日研究雷公藤建立卵巢损伤的动物实验文献。
1.2.2排除标准①排除雷公藤对雌性生殖毒性研究进展综述类和会议类、雷公藤建立卵巢颗粒细胞损伤相关细胞实验类、雷公藤治疗卵巢癌症相关研究类文献;②排除同一作者毕业论文与期刊重复发表的文献;③排除无法获取造模方式、造模药物等详细内容的文献。
1.3 数据提取由两位检索者采用独立双盲方式对文献进行筛选,数据提取,并进行交叉检查。数据提取过程中如有任何疑问,请求第三位研究人员对存有异议的文献进行复审后三人共同讨论、决定。文献提取的数据内容主要包括:文献名称、实验动物的品类、初始年龄、初始体质量、模型类别、实验操作前动物的筛选标准、雷公藤制剂的品牌、给药方式、给药剂量、造模周期、模型成功的标志及最终检测指标。
1.4 统计学方法分析将 符合纳入标准的文献中实验动物名称、品类等按照《常用医药研究动物模型》[6]进行规范化,使用Excel 2021软件进行频数分析。
2 结果
2.1 文献筛选结果初次检索到中文文献768篇,英文文献134篇,英文文献翻译为中文,阅读全文后排除不符合纳入标准的文献,最终筛选符合纳入标准的中英文文献共计278篇,其中中文文献270篇、英文文献8篇。
2.2 发文量分析见图1。通过分析年均发文量可明确该领域研究热度的变化趋势。中英文文献2000—2005年(包含2005年全部发表文献,以下类推)总发文量2篇,2006—2010年发文量增至34篇,2011—2015年总发文量快速增加至75篇,2016—2020年发文量增至106篇,2021—2023年7月31日总发文量61篇。

图1 2000—2022年雷公藤制剂建立卵巢损伤模型发文情况Figure 1 The publication of articles related to establishment of ovarian injury model with tripterygium wilfordii preparation from 2000 to 2022
2.3 实验动物选择纳入的278篇雷公藤制剂建立卵巢损伤动物实验研究文献中,共涉及10种实验动物,使用频数排前5位的分别是SD大鼠(205次,73.74%),Wistar大鼠(22次,7.91%),昆明小鼠(21次,7.55%),BALB/c小鼠(8次,2.88%),C57BL/6小鼠(8次,2.88%),具体分布情况见图2。数据分析显示实验动物品类与造模方式之间并无直接关联。实验动物的初始年龄多在7~12周龄之间,见表1。其中在278篇纳入的中英文文献中,有192篇文献在开展正式实验前对实验动物进行了阴道脱落细胞检测动物动情周期的筛选,剩余86篇文献未对实验动物进行动情周期筛查。

表1 雷公藤制剂建立卵巢功能障碍动物模型文献实验动物频率≥1%的动物年龄分布Table 1 Age distribution of experimental animals with frequency≥1%

图2 雷公藤制剂建立卵巢功能障碍动物模型文献实验动物种类分布Figure 2 Species distribution of experimental animals in articles related to establishment of ovarian inyurymodel with tripterygium wilfordii preparation
2.4 模型类别见表2。将278篇有效文献中应用雷公藤制剂建立的卵巢损伤模型进行汇总统计发现,主要有3类,分别是卵巢早衰(premature ovarian failure,POF;96次,34.53%)、卵巢储备功能低下(diminished ovarian reserve,DOR;80次,28.78%)、早发性卵巢功能不全(premature ovarian insufficiency,POI;27次,9.71%)。

表2 雷公藤制剂建立卵巢功能障碍动物模型文献建立频率≥1%的模型类别Table 2 Model categorieswith frequency≥1%
2.5 造模方式将纳入的278篇文献中涉及的造模方法进行分类,共得到3种常应用的雷公藤衍生制剂:雷公藤多苷、雷公藤甲素、雷络酯。通过分析得出使用频次最高的是雷公藤多苷(应用次数254次,占91.37%),其次是雷公藤甲素(应用次数13次,占4.68%),雷络酯(应用次数2次,占0.72%)。造模途径以灌胃最为常用(275次,98.92%),胃饲占2例,腹腔注射仅占1例。表3~表5显示,使用雷公藤多苷的剂量在5~100mg·kg-1,雷公藤甲素剂量在25~400μg·kg-1,其中雷公藤多苷剂量选择以50、75、40 mg·kg-1最为常用,雷公藤甲素剂量以400μg·kg-1最为常用;造模周期最短14 d,最长可达6个月;造模方式常见的有6种情况,其中给药剂量50 mg·kg-1,每天1次,连续14 d这种方法使用频率最多。
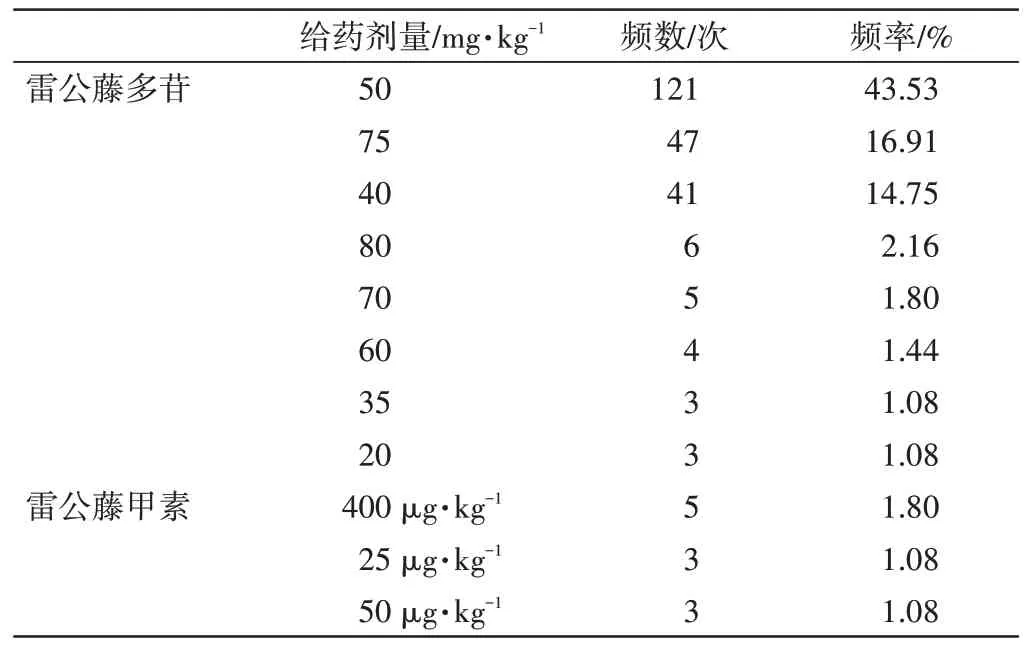
表3 雷公藤制剂造模≥1%的给药剂量分布Table 3 Dosage distribution of modeling frequency with tripterygium wilfordii preparation≥1%
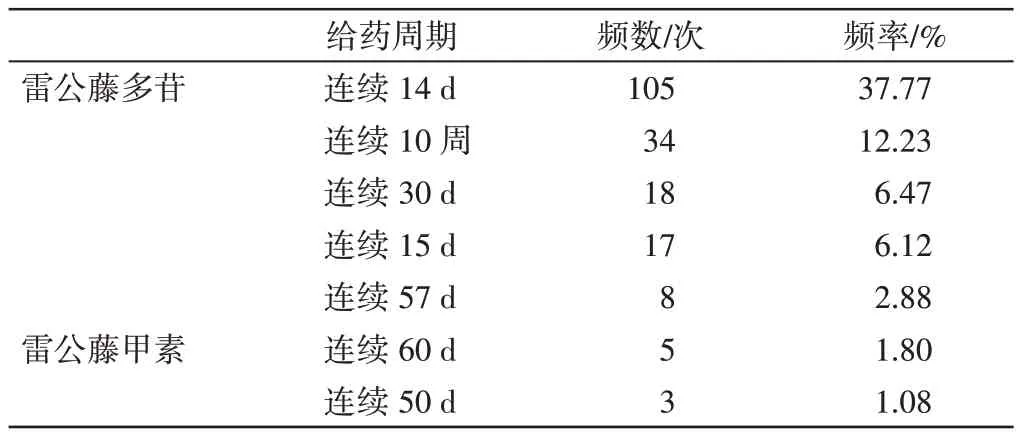
表4 雷公藤制剂造模≥1%的造模周期分布Table 4 Distribution of modeling cycle of modeling frequency with tripterygium wilfordii preparation≥1%
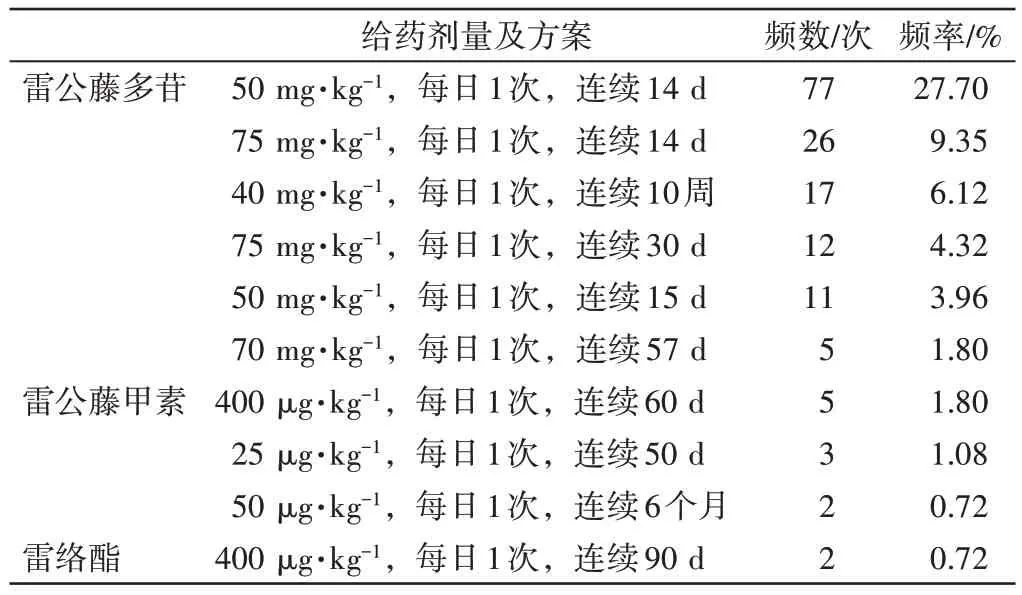
表5 雷公藤制剂常用的造模给药剂量及方案频数分布Table 5 Distribution of common dosage and frequency of tripterygium wilfordiipreparation
2.6 成模标准纳入文献中有97篇文献明确以动情周期紊乱(动情周期延长、停滞在某一时期或杂乱无章甚至周期不完整)作为成模标准,其中6篇文献以动情周期紊乱和血清性激素异常共同作为成模标准。剩余181篇文献中虽未明确说明造模成功的标志,但其中105篇文献对采用雷公藤制剂造模后的实验动物进行了阴道涂片,并根据阴道上皮细胞种类(是否角质化)、白细胞占比判断了实验动物所处的动情周期阶段。
2.7 检测频数纳入文献中的检测指标主要包括一般情况、动情周期、血清性激素水平、卵巢和(或)子宫指数、卵巢组织病理改变、卵泡计数等,累计频数885次,其中排前4位的分别是血清性激素(229次,25.87%)、动情周期(201次,22.71%)、卵巢组织病理形态(142次,16.05%)、卵巢和(或)子宫脏器指数(94次,10.62%),见图3。其中血清性激素主要检测的激素为:雌二醇(estradiol,E2)、促卵泡激素(folliclestimulating hormone,FSH)、促黄体生成素(luteinizing hormone,LH)、抗缪勒管激素(anti-müllerian hormone,AMH)、孕激素(progesterone,P)及抑制素B(inhibin B,INHB),见表6。其中E2、FSH、AMH等指标被作为评估卵巢损伤动物模型卵巢储备功能的重要指标[7-9]。血清性激素水平检测以酶联免疫吸附法(enzymelinked immunosorbent assay,ELISA;103次,51.24%)、放射免疫法(radioimmunoassay,RIA;68次,33.83%)两种方法为主。

表6 雷公藤制剂建立卵巢功能障碍动物模型文献血清性激素检测频率Table 6 Detection frequency of serum sex hormones

图3 雷公藤制剂建立卵巢功能障碍动物模型文献指标检测频率Figure 3 Detection frequency of index in articles related to establishment of ovarian injury model with tripterygium wilfordii prepartion
3 讨论
卵巢功能障碍是临床上常见的一种危害女性生殖健康的疾病,发病机制复杂且病情多变,常见于卵巢早衰(POF)、卵巢储备功能低下(DOR)等疾病,其临床症状多表现为经量减少、闭经或月经稀发同时伴随FSH升高、E2降低等内分泌异常等症状[10-12]。若病情不能得到及时有效的治疗,可能导致不孕,严重危害女性的身心健康。雷公藤制剂有抗炎、免疫抑制的作用[13-14],在临床使用中有生殖毒性反应,可使女性患者出现月经紊乱、闭经、卵巢功能下降等症状,被广泛运用于生殖损伤研究模型构建[15]。本研究通过数据分析发现雷公藤制剂通过抑制卵泡生长发育、干扰生殖内分泌、诱导卵巢细胞凋亡等[16-17]建立POF、DOR、POI(早发性卵巢功能不全)一系列卵巢损伤模型。
本研究文献挖掘结果显示,目前雷公藤制剂建立卵巢损伤动物模型选取的动物品系以SD雌性大鼠为主,主要的原因在于SD大鼠性情温和,便于实验操作,易于饲养且生理病理与人类具有较高的相似性[18],是复制卵巢功能障碍模型的理想动物。造模动物的年龄多选择7~12周龄,主要是由于7~12周龄大鼠(或小鼠)经过适应性喂养及雷公藤制剂灌胃实验操作后生长至3~6月龄,此阶段处于青年到中年阶段,相当于人类的20~40岁[19],适合生殖疾病方面的有关研究。
理想的动物模型是研究发病机制与新药研发的重要基础。数据分析发现目前建立卵巢损伤动物模型使用的雷公藤制剂以雷公藤多苷为主,雷公藤多苷造模以50、75、40 mg·kg-1三种剂量最为常用,周期在14 d至6个月不等。雷公藤多苷灌胃后,在动物体内累积一定浓度,通过抑制颗粒细胞增殖并促进其凋亡、抑制卵泡发育等机制使模型组大鼠(或小鼠)出现动情周期延长或紊乱,子宫和卵巢的湿质量减轻,卵泡及黄体数量减少,闭锁卵泡增多,FSH、LH升高,E2降低等症状[20-24],这一系列卵巢损伤的病理结果与人类一致,符合中西医临床病证结合卵巢损伤动物模型的要求,而且比环磷酰胺(cytoxan,CTX)成模更为理想[25]。研究[26-27]发现,雷公藤多苷75 mg·kg-1时大鼠动情周期紊乱发生率达100%,且剂量≥75 mg·kg-1时,卵巢中的各级卵泡(原始、初级、次级、窦卵泡以及总卵泡)数量均降低,闭锁卵泡数量增加。而雷公藤多苷40 mg·kg-1建立卵巢损伤模型时虽能引起E2和P水平降低,生长卵泡数、成熟卵泡数、黄体数减少,子宫及卵巢指数降低,内膜、肌层变薄,但FSH、LH、PRL、T水平变化一般不显著[28-29]。
此外,本研究发现采用雷公藤多苷低于40mg·kg-1时,实验周期一般较长,而长期应用雷公藤制剂可能导致卵巢以外的脏器毒副作用,这些毒副作用不仅降低模型的成功率,还会导致实验动物在造模过程中出现死亡;运用雷公藤多苷剂量超过70 mg·kg-1,造模天数长时,卵巢组织损伤重,会出现不易被药物逆转的纤维化增生[30];造模剂量高达100 mg·kg-1时,无论造模14 d还是28 d都会出现动物于造模给药实验结束前死亡,解剖死亡的大鼠发现肝脏呈现黑色样变[31]。
根据文献挖掘统计发现,研究者主要通过血清性激素、动情周期、卵巢组织病理形态、卵巢和(或)子宫脏器指数等指标检测,评价卵巢损伤模型成模情况。所统计文献中,以实验动物适应性喂养3~7 d,连续5~10 d行阴道脱落细胞学检测动情周期,挑选正常动情周期的实验动物为筛选标准开展正式实验,初步为建立卵巢损伤模型奠定了基础。后续指标检测以动情周期为检测模型复制是否成功的标准,且指标检测建议在实验开始前两周至实验结束每天都需对实验动物进行阴道细胞涂片观察动情周期。因卵巢功能衰退后,通过负反馈机制反馈至下丘脑,卵巢性腺轴调节功能下降,进而影响性激素水平[32]。因此,以血清性激素检测用来判断卵巢是否损伤。尽管POF、POI等疾病都存在卵巢损伤情况,但临床症状并不完全一致,尤其对血清性激素水平异常的定义,因此对于雷公藤制剂建立的卵巢损伤相关模型来说,血清性激素的检测评估模型的方法并不是典型,可进一步探讨相关问题。
综上所述,目前建立卵巢损伤动物模型应用的雷公藤多苷剂量种类较多,但缺少统一的制备动物模型剂量标准及评价标准。本文通过对雷公藤制剂建立卵巢损伤动物模型制备高频剂量及关键指标进行总结分析,可为提高动物模型的成模率及药效试验提供参考依据,并提出了合理建议,可为相关疾病研究提供基础。
4 展望
利用雷公藤诱导卵泡细胞凋亡,引起卵泡闭锁,抑制卵巢功能,导致生殖内分泌紊乱,出现因卵巢功能下降引起的高FSH闭经生殖毒性特点建立雌性卵巢损伤动物模型,不仅可以进行卵巢功能障碍疾病的诊断、治疗以及对其机制进行更深入的研究,另一方面也可以对雷公藤相关制剂的药理作用进行更深入的研究,探讨临床使用雷公藤及相关制剂的安全用药时间及剂量,关注使用雷公藤治疗后导致的卵巢损伤,可从根本上减少或者预防其导致的育龄期妇女卵巢功能低下的发生。

