药物基因检测对难治性精神分裂症患者治疗预后的影响
朱建南 林晓方 王从杰
精神分裂症的病因学和发病机制至今不明,临床上只有30%~60%患者对抗精神病药物有效,20%~30%的患者属于难治性精神分裂症,给社会和家庭带来负担。该病的治疗目前仍以药物为主,遗传因素的差异性是导致药物治疗出现巨大个体差异的因素之一,遗传因素的差异主要体现在药物转运蛋白、受体,药物代谢酶,药物靶点的遗传多态性,这些因素与药物效应和毒性的个体差异密切相关。因此,在患者使用药物之前,如果能够明确患者的药物相关基因类型,预先了解患者疗效敏感及不良反应少的药物,就可以有效促进临床医师制定更加科学的给药方案。近年来研究显示,将基因检测的精准医疗手段应用于精神分裂症治疗效果较好,但基本上只针对某个基因进行研究[1]。如能从药物作用靶点和药物代谢酶基因以及与药物不良反应相关基因多态性方面,检测不同患者所携带的等位基因和基因型对目前国内普遍使用的16种抗精神病药的应答率和代谢情况,以此针对不同患者筛选出疗效较好,应答、代谢正常及不良反应较少的抗精神病药,将大大提高难治性精神分裂症的治疗效果。本研究旨在探讨基因检测指导下应用抗精神病药对难治性精神分裂症临床预后的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取2020年1月—2022年6月江苏省淮安市第三人民医院门诊和住院的100例难治性精神分裂症患者。纳入标准:(1)符合《国际疾病分类诊断标准第10版》[2](International classification of diseases-10,ICD-10)有关精神障碍中精神分裂症的诊断标准。(2)确诊为难治性病例:符合《沈渔邨精神病学》[3]中有关难治性精神分裂症的概念,指按通常方法进行治疗而不能获得理想疗效的一群患者,包括过去5年内,至少使用过2种抗精神病药物足量(400~600 mg/d氯丙嗪等效剂量)、足疗程(4~6周)治疗均没有充分缓解[简明精神病评定量表(brief psychiatric rating scale,BPRS)总分≥45分,临床疗效总评量表(clinical global impression,CGI)≥4分,或者4项阳性症状中,至少2项≥4分]。(3)年龄16~60岁。(4)阳性阴性症状量表(positive and egative symptom scale,PANSS)评分总分≥60分。排除标准:(1)各种器质性精神障碍。(2)精神活性物质所致精神障碍。(3)对基因检测筛选出的抗精神病药过敏者。其中男性54例,女性46例;年龄16~59岁,平均(33.56±12.37)岁;病程5~41年,平均(31.26±9.37)年;PANSS评分61~85分,平均(69.13±5.47)分,社会功能评估量表(personal and social function assessment scales,PSP)评分21~42分,平均(34.84±4.03)分。本研究经江苏省淮安市第三人民医院药学伦理委员会批准(2019-001)。
1.2 方法
入组后记录患者的性别、年龄、婚姻、职业等人口统计学资料。刮取患者口腔黏膜上皮脱落细胞,送上海康黎医学检验所有限公司进行基因检测,根据基因检测结果选择或联合使用应答最佳、副作用最少的抗精神病药物治疗,并根据相应抗精神病药使用要求,滴定药物剂量至治疗剂量,一般在1~2周滴定至治疗量。
1.3 观察指标
PANSS量表共有30项,每个项目都有特定的操作定义和具体的评分标准,并按照精神病理水平分7级评分:1-无;2-很轻;3-轻度;4-中度;5-偏重;6-重度;7-极重,最后算所有项目的总分,评分为30~210分[4]。TESS量表严重度评定症状的严重水平,33项目,对应项目出现即得1分,0~8分可疑或较轻,>8~16分轻度,>16~24分中度,>24~33分重度[4]。CGI疗效指数分4级。(1)“无变化”,指症状毫无减轻或恶化。(2)“稍进步”,指症状略轻。(3)“进步”指症状有肯定进步或部分症状消失[4]。(4)“显进”指症状完全或基本消失。PSP包括工作和学习、个人关系和社会关系、自我照料、扰乱及攻击行为4个方面,每方面又分无、轻度、明显、显著、严重、非常严重6种严重程度,个人和社会功能从这4个方面6种严重程度累计打分,分值为1~100分[4]。威斯康星卡片分类测验全过程在计算机上进行,记录正确应答数、错误应答数、持续性应答数和持续性错误数的分数[4]。同时分别于治疗前、治疗后4、8、12、16周时进行血常规、心电图、脑电图、肝功能和肾功能等辅助检查。
1.4 统计学处理
采用SPSS 13.0统计学软件进行数据分析。计量资料以()表示,采用单因素重复测量方差分析和两两配对比较,每项比较前先进行球形对称检验,如不对称则采用Greenhouse-Geisser检验结果;计数资料以n(%)表示,采用2个相关样本非参数秩和检验。P<0.05为差异有统计学意义。
2 结果
2.1 基因检测推荐的首选治疗药物及联合用药情况
喹硫平:21例,阿立哌唑:19例,氯氮平:18例,氨磺必利:13例,利培酮:11例,帕利哌酮:9例,哌罗匹隆:4例,齐拉西酮:3例,奥氮平:2例。其中联合应用2种药物28例,均为基因检测推荐的首选治疗药物联用原治疗药物。
2.2 治疗前后临床疗效和社会功能比较
2.2.1 治疗前后PANSS和PSP评分比较
依据基因检测结果调整药物治疗4~16周PANSS评分均有降低,与治疗前比较,差异有统计学意义(P<0.001);PSP评分均上升,与治疗前比较,差异有统计学意义(P<0.001)。见表1。
表1 100例患者治疗前后PANSS和PSP评分比较(分,)

表1 100例患者治疗前后PANSS和PSP评分比较(分,)
注:治疗4、8、12、16周PANSS评分与治疗前比较,t=14.051、19.473、25.275、26.871,①P<0.001;治疗4、8、12、16周PSP评分与治疗前比较,t=8.696、12.439、17.395、19.782,①P<0.001。
时间PANSS评分PSP评分治疗前62.93±5.5530.14±4.26治疗4周59.62±6.29①35.94±8.30①治疗8周54.83±7.37①44.90±13.36①治疗12周49.34±7.93①54.13±15.38①治疗16周44.68±8.73①60.28±16.74①F值602.153257.585 P值<0.001<0.001
2.2.2 治疗后8~16周GGI与治疗后4周比较
治疗8~16周临床疗效均优于治疗4周,差异有统计学意义(P<0.001)。见表2。
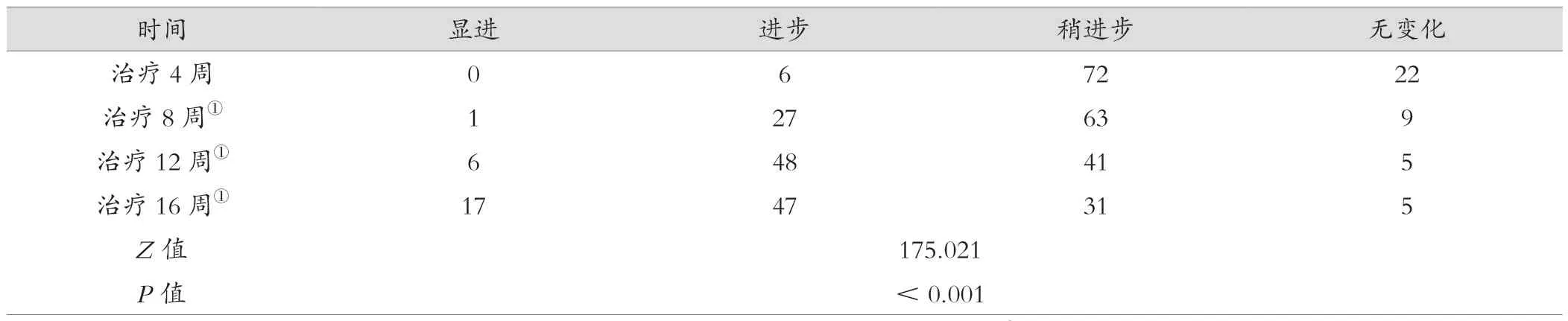
表2 100例患者治疗后8~16周GGI与治疗后4周比较(例)
2.3 治疗前后威斯康星卡片分类测验评分比较
治疗4~16周,正确应答数、持续应答数均有上升,错误应答数、持续错误数均下降,与治疗前比较,差异有统计学意义(P<0.001)。见表3。
表3 100例患者治疗前后威斯康星卡片分类测验评分比较(分,)
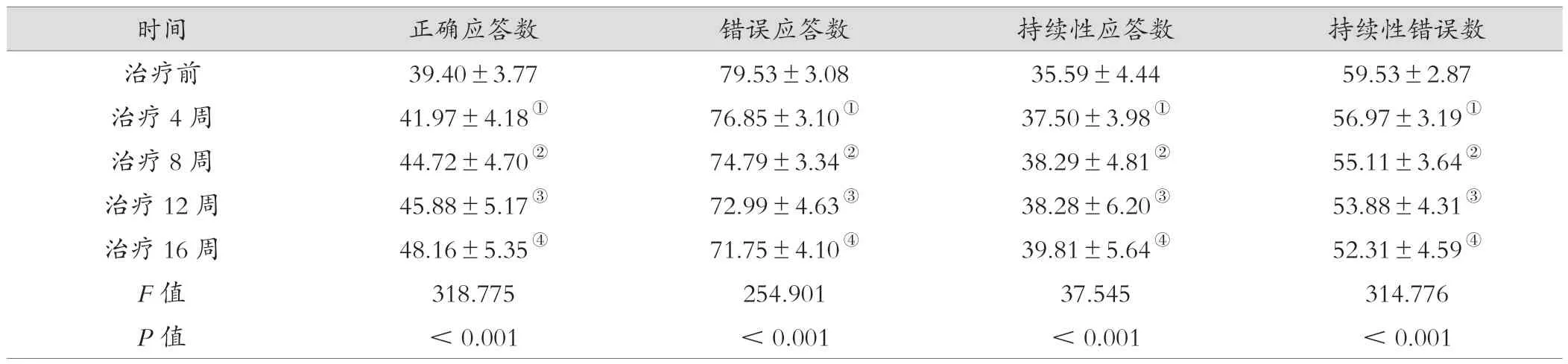
表3 100例患者治疗前后威斯康星卡片分类测验评分比较(分,)
注:治疗4周分别与治疗前比较,t=15.547、22.719、17.642、20.097,①P<0.001;治疗8周分别与治疗前比较,t=17.908、21.865、12.249、21.553,②P<0.001;治疗12周分别与治疗前比较,t=17.633、18.254、5.426、20.042,③P<0.001;治疗16周分别与治疗前比较,t=21.707、21.460、11.423、21.888,④P<0.001。
时间正确应答数错误应答数持续性应答数持续性错误数治疗前39.40±3.7779.53±3.0835.59±4.4459.53±2.87治疗4周41.97±4.18①76.85±3.10①37.50±3.98①56.97±3.19①治疗8周44.72±4.70②74.79±3.34②38.29±4.81②55.11±3.64②治疗12周45.88±5.17③72.99±4.63③38.28±6.20③53.88±4.31③治疗16周48.16±5.35④71.75±4.10④39.81±5.64④52.31±4.59④F值318.775254.90137.545314.776 P值<0.001<0.001<0.001<0.001
2.4 药物不良反应比较
治疗16周TESS评定与治疗4周比较,差异有统计学意义(P<0.01)。见表4。但治疗16周的血常规、心电图、脑电图、肝功能和肾功能异常检查与治疗前比较均差异无统计学意义(P>0.05)。

表4 100例患者治疗16周TESS与治疗4周比较(例)
3 讨论
精神分裂症是一种严重的慢性疾病,多种因素包括男性、阳性家族史、阴性症状为主、起病年龄早、未治期长、治疗依从性差等易导致患者发展成难治性,难治性精神分裂症具有病程长、治愈率低、疾病进展缓慢、复发率高等特点[5]。当前难治性精神分裂症的治疗主要以抗精神病药物为主,其镇静作用明显,毒副作用也十分突出,如肝、肾损伤与不良反应等,使患者服药依从性逐渐降低[6-7]。药物治疗存在很大的个体差异,遗传因素,即基因多态性是引起药物效应个体差异最为严重的因素之一[8]。抗精神病药疗效、不良反应、有效治疗剂量等与药物代谢、转运及靶基因多态性关联[9]。随着药物基因组学研究的深入,利用基因检测指导抗精神病药物的临床治疗成为一种新的手段,为难治性精神分裂症患者的治疗带来希望[10]。
许多抗精神病药物的临床效果不佳,与药物作用靶点不同和药物代谢差异易发生的不良反应有关,结合美国食品药品管理局(food and drug administration,FDA)公布的药物基因标记物注释,确定多巴胺受体D2(dopamine receptor D2,DRD2)、多巴胺受体D3(dopamine receptor D3,DRD3)、5-羟色胺受体1A(serotonin-1A receptors,5-HTR1A)、儿茶酚胺氧位甲基转移酶(catechol-O-methyltransferase,COMT)、G-蛋白信号转导调节子-4(regulator of G-Protein signaling,RGS-4)、锚蛋白重复和激酶域1基因(位于DRD2受体附近)(ankyrin repeat and kinase domain containing 1,ANKK1)以及ATP结合盒家族B运载体1基因(ATP-binding cassette sub-family bmember1,ABCB1)等方面检测入组患者所携带的基因型并对应了解16种抗精神病药的各自应答情况;药物代谢方面,主要从细胞色素P450同工酶1A2(cytchrome P450 protein-1A2,CYP1A2)、细胞色素P450同工酶3A4(cytchrome P450 protein-3A4,CYP3A4)、细胞色素P450同工酶(cytchrome P450 protein-2D6,CYP2D6),黑色皮质素受体-4(melanocortin-4 receptor,MC4R),5-羟色胺受体(serotonin-2c receptors,5-HTR2C)等方面检测入组患者所携带的等位基因和基因型,结合FDA公布的药物基因标记物注释及已有的文献研究结果,确定携带不同等位基因和基因型的患者对16种抗精神病药的代谢情况及不良反应情况[11]。
通过对患者进行基因检测,分析和权衡基因检测结果,确定使用药物代谢速率正常,应答率最佳,发生不良反应的风险较低的抗精神病药治疗。本研究中治疗后的PANSS、CGI、PSP及威斯康星卡片分类测验优于治疗前(P<0.001),与彭焱等[12]报道的结果相一致。众所周知,药物治疗效果的好坏与药物代谢和应答有关,在药物代谢相关途径中的细胞色素P450酶系(cytchrome P450 protein,CYP450)是最主要的药物代谢酶,CYP450的多种同工酶参与了精神科药物的代谢,在个体和种族间存在较大差异,基因多态性导致酶活性不同,通过基因检测,能避免选择参与代谢的超快代谢型酶的药物,从而保证血药浓度在治疗窗口内的药物优先使用,同时通过基因检测,能选出应答最佳的药物,故患者的阳性、阴性症状恢复快,临床疗效、社会功能、认知功能恢复就好[13]。
在所有精神分裂症患者中,不能完全遵照医嘱用药的比例为20%~60%,其中,药物不良反应是导致依从性较差的重要因素,治疗依从性差也会导致精神分裂难治[14-15]。PHILLIPS等[16]研究发现在引起不良反应的27种药物中近60%的药物是由至少1种呈多态性的药物代谢酶所代谢,且引起不良反应的为代谢酶活性下降及失活的慢代谢型患者,说明药物不良反应确实与药物代谢酶基因多态性有一定的关联。所以,在对精神分裂症患者治疗过程中开展药物基因检测,对于患者的精准化药物治疗具有重大的意义。本研究中,TESS评定与治疗4周时比较,主要考虑有些患者刚开始治疗时未服药物,结果显示治疗16周时TESS评定与治疗4周比较,差异有统计学意义(P<0.01)。但治疗16周的血常规、心电图、脑电图、肝功能和肾功能异常检查与治疗前比较,差异无统计学意义(P>0.05),这可能与TESS量表评定者的判定差别有关。不良反应情况与兰吴沅等[17]药物基因组学检测在难治性精神分裂症患者中的临床研究和刘吴斯博[18]在基于基因检测的精神分裂症个体化药物治疗的临床研究中不良反应发生率低相一致,主要是通过基因检测,避免选择代谢酶活性下降及失活的慢代谢型的药物,不会出现超高的血药浓度,从而降低了药物对躯体的损害程度。此文的研究结果为《中国精神分裂症防治指南》[19]中关于难治性精神分裂症患者精准治疗的后期标准制定提供了借鉴内容。
综上所述,难治性精神分裂症患者并非不可治,在治疗前能借助基因检测,选择药物正常代谢型、应答最佳、发生不良反应的风险较低的药物,能够使患者治疗更为个体化、精准化,能最大限度提高患者临床疗效和治疗依从性。

