宫腔镜子宫肌瘤电切术与腹腔镜子宫肌瘤剔除术治疗子宫肌瘤的临床对比
何金阁
(河南省长垣市妇幼保健院 长垣 453400)
子宫肌瘤早期可无自觉症状,为良性肿瘤,研究认为子宫肌瘤的发病原因可能与性激素、局部生长因子、正常肌层细胞突变等诸多因素相互作用有关,部分患者甚至终生未察觉患病,但随着肌瘤持续生长可诱发不规则出血、下腹疼痛或影响患者排便功能,严重者甚至影响妊娠,增加不孕不育风险[1]。为改善患者预后,临床主张早期规范化治疗,控制肌瘤生长[2]。腹腔镜是外科常用微创技术,腹腔镜子宫肌瘤剔除术仅需建立微小切口即可直观切除肌瘤组织,在起到治疗目的的同时可减轻患者身心痛苦,利于早期康复[3]。宫腔镜子宫肌瘤电切术同样为微创术式,术中无须建立切口,经阴道至宫颈口置入手术器械,可进一步减轻手术创伤,且电切术可彻底清除肌瘤及残留组织,可控制病情复发,利于改善患者预后[4]。本研究旨在对比腹腔镜子宫肌瘤剔除术和宫腔镜子宫肌瘤电切术在子宫肌瘤治疗方面的差异,进一步探索手术治疗子宫肌瘤的有效性和安全性。现报道如下:
1 资料与方法
1.1 一般资料 选取2020 年11 月至2021 年11月我院收治的60 例子宫肌瘤患者临床资料进行回顾性分析,根据手术方式不同,将所有患者分为观察组和对照组,各30 例。观察组肌瘤直径3.8~6.1 cm,平均直径(5.32±0.22)cm;年龄34~49 岁,平均年龄(38.72±1.72)岁;肌瘤数量:肌瘤多发17 例,肌瘤单发13 例;肿瘤病发位置:浆膜下肌瘤9 例,肌壁间肌瘤15 例,黏膜下肌瘤6 例;体质量指数19~24 kg/m2,平均(21.15±0.48)kg/m2。对照组肌瘤直径3.3~6.2 cm,平均直径(5.08±0.27)cm;年龄35~49岁,平均年龄(39.17±1.49)岁;肌瘤数量:肌瘤多发19 例,肌瘤单发11 例;肿瘤病发位置:浆膜下肌瘤10 例,肌壁间肌瘤13 例,黏膜下肌瘤7 例;体质量指数19~24 kg/m2,平均(21.43±0.52)kg/m2。两组年龄、肌瘤直径、肌瘤数量、肌瘤病发位置、体质量指数等一般资料比较,差异无统计学意义(P>0.05),存在可比性。本研究经医院医学伦理委员会审批通过[伦理编号:长保字(2021)15 号]。
1.2 入选标准 纳入标准:符合子宫肌瘤诊断标准[5];均为单发病灶;随访资料完整;术前未接受过相关治疗;无明显基础疾病,符合手术指征,无任何过敏史,无凝血功能障碍;患者及家属签署知情同意书,手术均由同一组医疗团队完成,术后观察时间均至少6个月。排除标准:存在长期疼痛史;合并卵巢、输卵管器质性病变;伴有宫腔粘连、阴道炎、盆腔炎;内分泌功能障碍;处于妊娠期或哺乳期。
1.3 治疗方法 观察组接受宫腔镜子宫肌瘤电切术:患者取截石位,先行硬膜外麻醉,清洁会阴及周围皮肤,采用扩宫器扩张宫颈,并持续注入膨宫液,之后置入宫腔镜。探查肌瘤位置、大小及数量并行电切割术,彻底切除肌瘤组织,对于蒂黏膜下肌瘤行表面切割,待瘤体缩小后取出,若无黏膜下肌瘤,则先切开肌瘤包膜,切碎瘤体后逐个取出。取出肌瘤后,行电凝止血,之后取生理盐水冲洗术腔,最后取出器械,术毕。两组术后均行镇痛、抗凝、抗感染等治疗。对照组接受腹腔镜子宫肌瘤剔除术:患者取膀胱截石位,常规消毒后行全身麻醉,将举宫器置入阴道内便于暴露肌瘤位置。行常规三孔法,于脐上缘2 cm处作一10 mm 切口,穿刺后建立人工气腹,之后置入10 mm Trocar 并放入腹腔镜,探查腹腔情况;于两侧下腹分别作切口并置入10 mm Trocar 作为副操作孔,置入把持钳和超声刀。观察肿瘤大小、特征等信息,提拉肌瘤并纵向切口瘤体,分离取出肌瘤组织,止血后取生理盐水连续冲洗术腔,确认无活动性出血后取出器械,排出二氧化碳,采用0 号可吸收线逐层缝合组织,置引流管,术毕。
1.4 观察指标 根据临床病例资料,分析两组手术一般情况及子宫肌层愈合情况、治疗前后卵巢储备功能、子宫内膜容受性和并发症发生率。(1)子宫肌层愈合:通过超声检查进行判定,若子宫肌层无线状回声且回声均匀,可判定为子宫肌层愈合。(2)卵巢储备功能情况:采集两组外周静脉血5 ml,采用离心机(北京迈创医疗器械销售有限公司,型号:MF 200),离心半径为10 cm,以3 500 r/min 离心10 min取血清,以酶联免疫吸附法检测雌二醇(Estradiol,E2)、血清抗苗勒管激素(AMH)、黄体生成素(Luteinizing Hormone,LH)、卵泡刺激素(Follicule-Stimulating Hormone,FSH)水平,试剂盒购自贝林医疗器械(北京)有限责任公司,上述操作均遵守实验室相关规定进行。(3)子宫内膜容受性:结合子宫超声检查测定子宫内膜厚度及血流搏动指数、阻力指数。(4)统计随访病例资料中两组并发症发生情况:如阴道出血、尿潴留、宫腔感染、腹腔粘连等。
1.5 统计学方法 将本研究获得的所有数据导入SPSS23.0 统计学软件中分析,计量资料以()表示料,采用t检验;计数资料以%表示,采用χ2检验,若期望值<5 用连续校正卡方检验。P<0.05 为差异有统计学意义。
2 结果
2.1 两组卵巢储备功能比较 术前、术后,两组患者AMH、E2、LH、FSH 水平比较,差异无统计学意义(P>0.05)。见表1。
表1 两组卵巢储备功能比较()
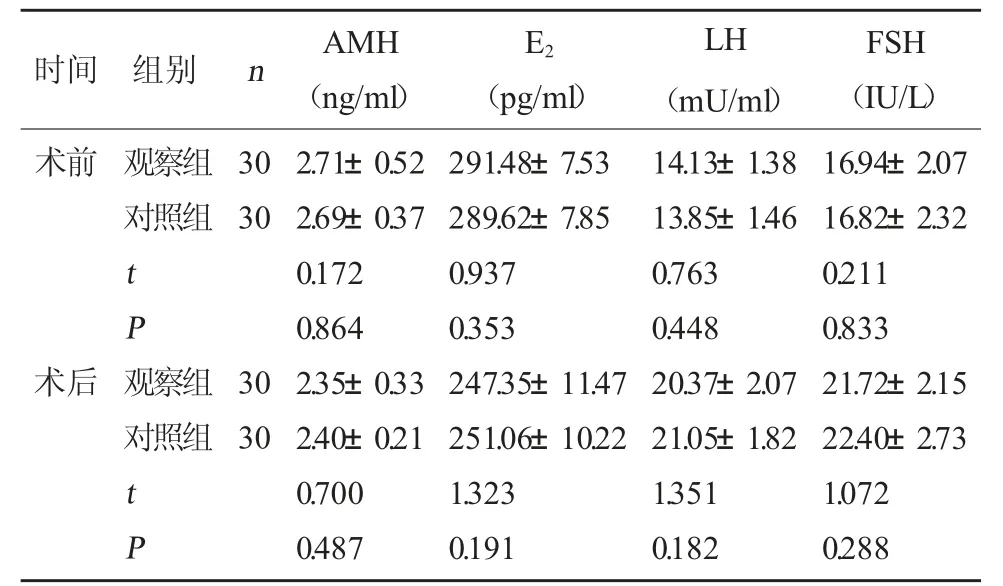
表1 两组卵巢储备功能比较()
2.2 两组子宫内膜容受性比较 术后,两组血流搏动指数、阻力指数及子宫内膜厚度均显著改善,且观察组子宫内膜容受性各指标改善幅度优于对照组(P<0.05)。见表2。
表2 两组子宫内膜容受性比较()
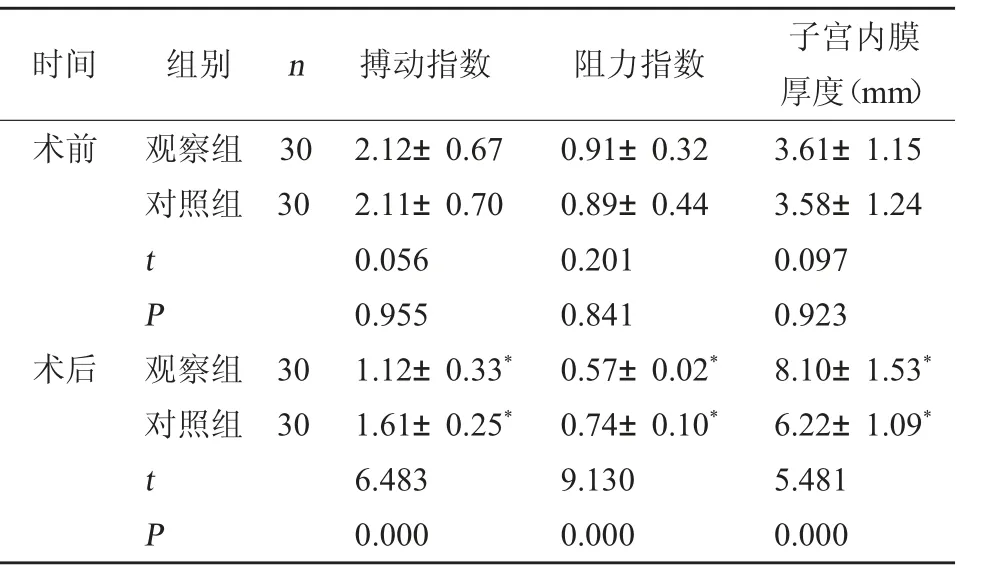
表2 两组子宫内膜容受性比较()
注:与同组术前相比,*P<0.05。
2.3 两组子宫肌层愈合、手术一般情况比较 观察组住院时间、术后排气时间、手术时间均短于对照组,术中出血量少于对照组,差异有统计学意义(P<0.05);术后1、3、6 个月,观察组子宫肌层愈合率均高于对照组,差异具有统计学意义(P<0.05)。见表3。
表3 两组子宫肌层愈合、手术一般情况比较()
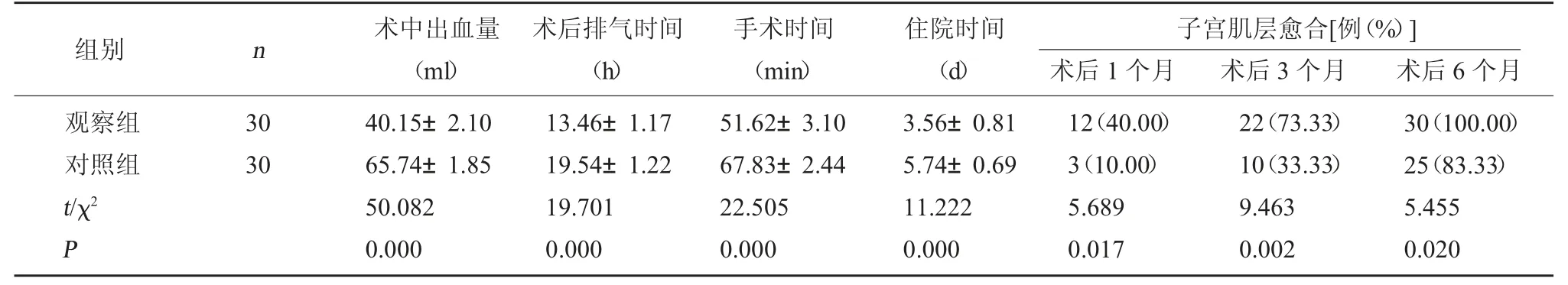
表3 两组子宫肌层愈合、手术一般情况比较()
2.4 两组并发症发生情况比较 观察组并发症发生率为13.33%,对照组并发症发生率为16.67%,两组间比较,差异无统计学意义(P>0.05)。见表4。
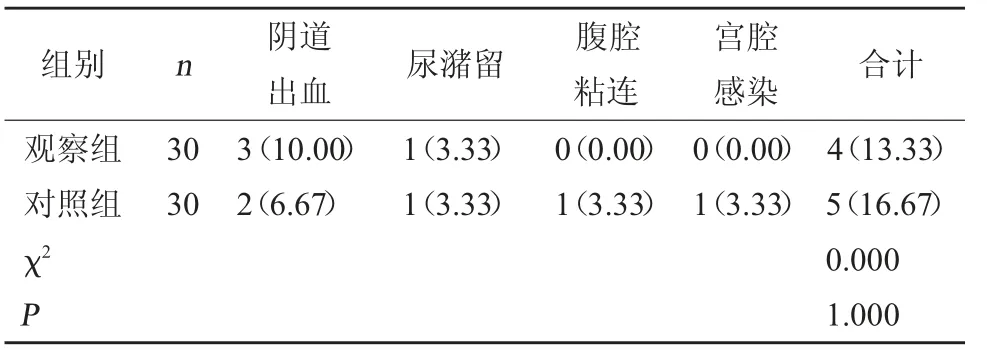
表4 两组并发症发生情况比较[例(%)]
3 讨论
子宫肌瘤为良性病变,现代临床研究显示,随着病情进展,子宫肌瘤可影响受精卵着床,导致不孕,甚至导致不良妊娠结局,或增加恶性病变风险,加重患者身心创伤,不利于患者预后[6~7]。因此,早期行手术切除治疗是改善患者预后的关键,且大多患者要求保留子宫的完整性,最大限度地减少手术对机体生理结构的破坏。
腹腔镜子宫肌瘤剔除术为当前应用广泛的微创术式,术中无须过度剥离组织即可切除肌瘤,减轻患者痛苦。腹腔镜手术中腹腔密闭性较好,利于减少腹腔脏器暴露[8~9]。此外,腹腔镜可放大局部区域,利于发现微小和隐匿病灶,避免病变组织残留[10]。但腹腔镜术中建立气腹易压迫腹腔脏器,一定程度影响脏器功能,且该术式需切开肌层,主要通过牵拉剥除和电凝切除肌瘤,对患者刺激大,还可能损伤子宫内膜,增加后期瘢痕子宫妊娠破裂风险,安全性有待进一步提升。腹腔镜手术要求手术医师一定要具备较高的技术,操作不当可能增加术中风险,尤其针对较大直径的肌瘤,若手术医师手法不熟练,可能导致肌瘤剥除耗时长、创面大,增加出血量,不利于患者术后恢复[11]。
宫腔镜手术较腹腔镜相比,更具微创性,利用人体既有的腔道作为手术入路,术中无须做切口或开腹,可进一步减轻手术创伤,对腹腔环境影响小,可有效减轻患者身心痛苦,基本不存在切口感染、子宫穿孔、腹腔粘连并发症,利于术后早期康复[12~13]。此外,宫腔镜子宫肌瘤电切相对锐利,在切割肌瘤组织的同时可直接进行电凝止血,减少术腔出血量,利于缩短术后康复时间;且宫腔镜手术可维持完整的浆膜层,保证局部组织血流灌注良好,从而保持良好的子宫内膜厚度、血液供应及形态等条件,保障子宫内膜受容性[14]。本研究结果显示,观察组术后排气时间、手术时间、住院时间均短于对照组,观察组术中出血量少于对照组,观察组术后1 个月、3 个月、6 个月的子宫肌层愈合率均高于对照组(P<0.05);术前,两组血流搏动指数、阻力指数及子宫内膜厚度比较,差异无统计学意义(P>0.05);术后,两组血流搏动指数、阻力指数及子宫内膜厚度均显著改善,且观察组子宫内膜容受性各指标改善幅度优于对照组(P<0.05)。
有研究显示,手术治疗子宫肌瘤易伤及卵巢,影响卵巢储备功能,进而对患者生育功能造成一定影响,增加不孕风险[15]。腹腔镜和宫腔镜手术仅伤及子宫浅层肌,对子宫卵巢动脉及卵巢供血动脉无明显影响,均可最大程度减轻卵巢损伤,保护卵巢供血,进而保护卵巢功能。本研究结果显示,术前、术后两组AMH、E2、LH、FSH 指标水平,卵巢储备功能比较,差异无统计学意义(P>0.05)。这表明两种手术治疗方式对子宫肌瘤患者卵巢功能均无明显影响。此外,两组并发症发生率比较,差异无统计学意义,表明这两种子宫肌瘤切除治疗术式均具有一定的安全性。综上所述,腹腔镜子宫肌瘤剔除术治疗子宫肌瘤,与宫腔镜子宫肌瘤电切术治疗均具有一定的安全性,并发症相对较少,且对患者卵巢储备功能无明显影响,但宫腔镜子宫肌瘤电切术更具微创性,术中出血量少,子宫肌层术后恢复更快,且保持良好的子宫内膜容受性。

