DEB-TACE治疗肝功能Child-Pugh评分8分肝细胞癌的疗效评价
卞帅 石奇 谢志江 周旭升 汪磊 朱敏 戴家应
原发性肝癌为全球范围常见癌症第6 位及癌症死亡因素第3 位,中国为肝癌发病大国,目前在我国较为常见的恶性肿瘤中,原发性肝癌位居第4 位,是第2 位肿瘤致死病因,且在原发性肝癌中肝细胞癌(hepatic cell carcinoma,HCC)占比为75%~85%,已成为严重影响我国居民健康的一种疾病[1]。肝切除术为肝癌患者的最佳治疗选择,特别是针对早期肝癌患者,由于肝癌前期临床表现不明显,大部分肝癌患者一经检查就已经到中、晚期,从而错失最佳治疗时间。目前对中晚期肝癌患者治疗主要采用的方式为经导管动脉化学栓塞(transcatheter arterial chemoembolization,TACE),根据化疗方式的不同分为2类,包括常规TACE(conventional-tace,cTACE)和药物洗脱微球TACE(drug eluting beads-TACE,DEBTACE)[2]。研究表明,与cTACE 相比,DEB-TACE 具有良好的治疗效果、更长生存期和至少相似的安全性,使患者获益更多[3]。CalliSpheres 载药微球作为国产新产品,在载药速度、载药量及缓释时间等方面表现了良好的优势[4]。然而,对于中晚期肝癌给予CalliSpheres载药微球进行治疗肝功能Child-Pugh 分级B 级8 分的安全性和治疗效果,近几年相关文献报道比较少。本研究旨在分析实施CalliSpheres 载药微球治疗中晚期肝癌患者经治疗后的安全性及近期疗效。
1 资料与方法
1.1 一般资料
选取2021 年11 月—2022 年11 月于安庆市立医院介入治疗科诊治的肝癌患者20 例,总胆红素32 ~51μmol/L,平均总胆红素(42.15±6.50)μmol/L;白蛋白 31 ~45 g/L,平均白蛋白(33.41±4.26)g/L;凝血酶原时间11 ~18 s,平均凝血酶原时间(14.37±2.19)s ;有腹腔积液20 例,无腹腔积液0 例;有肝性脑病5 例,无肝性脑病5 例。纳入标准:(1)所有研究对象都需符合《原发性肝癌中西医结合介入诊疗专家共识(试行第一版)》[5]中对肝癌的诊断标准,并且取下的病理组织经诊断为原发性肝细胞肝癌。(2)年龄18 ~80 岁,预计生存期≥3 个月。(3)肿瘤数目≤3 个、最大直径≤10 cm(单个>5 cm,或2 ~3 个、至少1 个>3 cm)。(4)肝功能Child-Pugh分级[6]B 级8 分,且经美国东部肿瘤协作组体能状况评分[7]≤2 分,见表1。(5)凝血功能处于正常、无出血倾向或可经治疗凝血功能异常改善者。(6)白细胞计数≥3.0×109/L,血小板计数≥50×109/L。(7)凝血酶原时间(prothrombin time,PT)国际标准化比值≤2.3或延长≤3 s。(8)血清肌酐小于正常上限的1.5 倍。排除标准:(1)弥漫性肝癌。(2)胆管细胞癌。(3)Ⅲ~Ⅳ级门静脉癌栓。(4)肿瘤的体积超过肝脏体积的2/3 者。(5)经治疗后无法改善凝血功能异常,有显著的出血迹象者。(6)未控制的感染,如败血症、胆系感染、肝脓肿等。(7)孕妇及哺乳期妇女。(8)无法进行CT/MRI 检查者。本研究经安庆市立医院伦理委员会的审查批准,患者知情并签署同意书。
表1 手术前后肝功能变化比较 (±s)
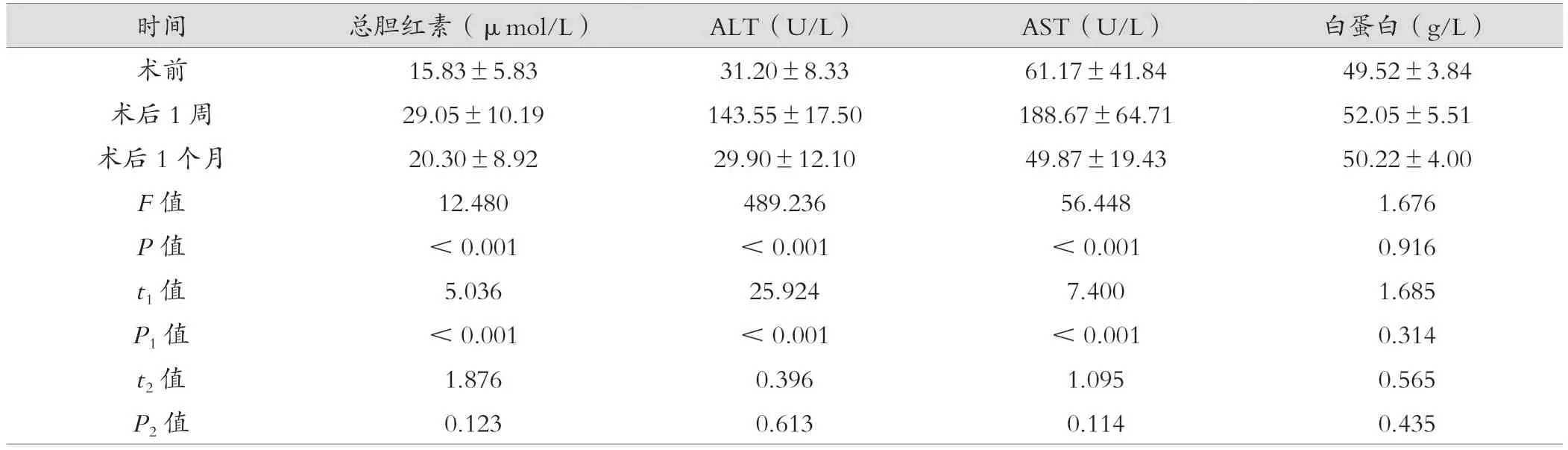
表1 手术前后肝功能变化比较 (±s)
注:t1,P1 值为术后1 周与术前比较;t2,P2 值为术后1 个月与术前比较。
时间总胆红素(μmol/L)ALT(U/L)AST(U/L)白蛋白(g/L)术前15.83±5.8331.20±8.3361.17±41.8449.52±3.84术后1 周29.05±10.19143.55±17.50188.67±64.7152.05±5.51术后1 个月20.30±8.9229.90±12.1049.87±19.4350.22±4.00 F 值12.480489.23656.4481.676 P 值<0.001<0.001<0.0010.916 t1 值5.03625.9247.4001.685 P1 值<0.001<0.001<0.0010.314 t2 值1.8760.3961.0950.565 P2 值0.1230.6130.1140.435
1.2 方法
1.2.1 栓塞材料
采用CalliSpheres 可载药微球(购自苏州恒瑞伽俐生生物医药科技公司,规格:1 g/7 mL,100 ~300 μm 或300 ~500 μm/瓶),化疗药物为吡柔比星(深圳万乐药业有限公司,国药准字H10930105,规格:10 mg)。
1.2.2 DEB-TACE
采用改良塞丁格技术(Seldinger technique,Seldinger)穿刺右股动脉,置入5F 动脉短鞘,将RH 导管插入右股动脉、肝动脉及其分支进行常规动脉造影,明确肿瘤供血动脉。通过微导管超选取肿瘤供血动脉。DEB-TACE选择合适粒径的载药微球,注射用水或5% 葡萄糖水溶解吡柔比星60 ~80 mg,药物浓度不低于20 mg/mL,选用1 瓶合适粒径(100 ~300 μm 或300 ~500 μm)载药微球加载吸附吡柔比星30 min。然后以1 ∶1.1 或1 ∶1.2的比例加入非离子型造影剂并混匀,静置5 min。以不超过1 mL/min 速率间断,且在肿瘤供血动脉中缓慢注入载药微球,注射时注意保持注射器内微球分布均匀,防止微球沉淀。根据肿瘤供血情况逐支超选、栓塞。观察对比剂流速,待达到栓塞终点(肿瘤供血动脉末梢血管接近停滞,即造影剂在血管内停滞4 ~6 个心动周期)时停滞注射。5 min 后再次进行血管造影,若仍存在肿瘤染色则继续栓塞。术后予以必要的对症处理,包括加强保肝、抑酸护胃、止吐、营养支持等。
1.3 观察指标
检测术前、术后1 周和术后1个月患者的天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)、白蛋白、总胆红素、谷氨酸氨基转移酶(alanine aminotransferase,ALT)的指标水平。嘱咐患者经常到院复查,需每月1次检查,根据改良实体瘤疗效评价标准(mRECISET)对患者的状况进行评价[8],主要包括疾病进展(progressive disease,PD)、 部分缓解(partial response,PR)、 完全缓解(complete response,CR)和疾病稳定(stable disease,SD),客观缓解率=(CR 例数+PR 例数)/ 总例数×100%,疾病控制率=(CR+PR+SD)例数/ 总例数×100%。关注患者治疗期间的不良反应(如发热、疼痛、恶心呕吐等)情况。
1.4 统计学处理
采用SPSS 20.0 统计学软件进行分析。计量资料以(±s)表示,组间比较采用独立样本均数t检验;计数资料用n(%)表示。P< 0.05 为差异有统计学意义。
2 结果
2.1 介入治疗情况
20 例患者接受CalliSpheres 载药微球治疗,且治疗都已顺利完成,患者在经手术治疗后的平均住院时间为(5.97±0.29)d。
2.2 手术前后肝功能变化
与术前相比,术后1 周,ALT、AST 及总胆红素明显升高(P< 0.05);但白蛋白水平比较,差异无统计学意义(P> 0.05);与术前相比,在经手术治疗1 个月后,经检查肝功能指标基本恢复至正常水平,差异无统计学意义(P>0.05),见表1。
2.3 介入治疗效果比较
患者在经手术治疗1 个月后,疗效分别为疾病进展(PD)2 例、部分缓解(PR)11 例、疾病稳定(SD)5 例和完全缓解(CR)2 例,客观缓解率为65.0%(13/20),疾病控制率为90.0%(18/20)复查MRI 显示,相比治疗前,经DEB-TACE 治疗后右肝区的肿瘤实现完全坏死,见图1。 7例患者后续接受了靶免系统治疗。
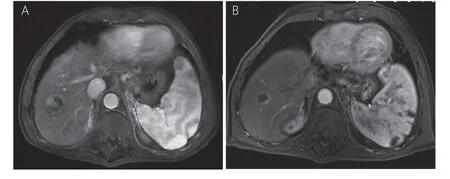
图1 1 例肝癌患者行DEB-TACE 治疗前后影像学表现
2.4 术后不良反应
术后主要的不良反应主要包括有轻度恶心呕吐、腹痛、发热,且有13 例患者经手术治疗后出现了腹痛,有5 例患者发热、还有6 例患者发生了恶心呕吐症状,在经对症治疗后,患者有所好转。且所有患者在术后都没有发生消化道及腹腔出血、胆汁漏合并感染等并发症。
3 讨论
肝细胞癌为全世界较为常见的一种恶性肿瘤,严重危及人们的生命,多因诊断晚和异质性而预后差[9]。研究显示,临床相关特征和患者的预后效果有密切联系[10]。
手术切除为肝癌治疗较有效的措施,然而仅25%的患者适合手术切除,即使接受切除手术的患者,仍有高达75%的复发率[11]。TACE 为临床近年来较常应用于肝细胞癌介入治疗的一项技术,该技术通过将有关抗肿瘤药物和碘油水乳栓塞试剂注射到肿瘤的供血动脉中,使其在肿瘤组织中呈现低氧、高毒性,同时还能进一步杀死肿瘤细胞。据相关研究显示,TACE 碘油的沉积与患者的预后效果有很大联系;同时,TACE 治疗还可作为包括不适合手术在内的中期肝癌患者的一线选择[12]。作为TACE 的新一代技术之一,DEB-TACE 的原理是将化疗药物装载在微球上,当注入肿瘤时,它将可持续地释放药物超过2 周[13]。DEBTACE 已被证明其有效性,能够延长患者生存期,并且化疗栓塞综合征发生较少[14]。因此,笔者开展了这项研究,以进一步探讨其在Child-Pugh 评分8 分肝癌患者中的有效性与安全性。
维持肿瘤内部的药物浓度是肝癌介入治疗中的关键。CalliSpheres 载药微球可作为新型的栓塞剂与化疗药物进行混悬,应用到TACE 的治疗中,实现药物在肿瘤内部持续释放[15]。与碘油相比,CalliSpheres 栓塞微球属于一类新型TACE 栓塞材料,有较高的安全性和较大的可载药量,同时还具有缓释效应,在一定程度上可以使药物长期稳定地释放[16]。本研究结果显示,针对Child-Pugh 评分8 分的肝癌,选用CalliSpheres 可载药微球治疗起效果较好。本研究表明,对肝癌施以CalliSpheres 栓塞微球TACE 治疗治疗1 个月后客观缓解率为65.0%(13/20),疾病控制率为90.0%(18/20)。
晚期肝癌患者的肝功能降低,通常被认为是决定治疗方案的关键[14]。肝功能不良会限制晚期肝癌患者的治疗选择。一些潜在疾病,如肝硬化、酒精性肝炎或病毒性肝炎等均可导致肝功能异常。本研究显示,与肝功能相关的实验室指标,大多数在化疗栓塞治疗后快速恶化,并在首次介入术后约1 个月恢复。
疼痛、恶心呕吐和发热是肝癌患者经DEB-TACE治疗后常见的几种不良反应。一项研究显示,疼痛、发烧、恶心、呕吐的发生率分别为63.3%、34.7%、18.4%、28.6%[17]。在另一项研究中也报告了包括疼痛(96%)、呕吐(16%)和发热(77%)在内的不良反应,该研究用CalliSpheres 微球治疗肝癌患者[18]。本研究中,疼痛、恶心、呕吐和发热发生率分别为13 例(65%)、6 例(30%)、5(25%)。与以前的研究相比,本研究中观察到的发热的发生率较低,这可能是因为对过敏反应进行了预防性的治疗,因此,发热在本研究中可能比较温和。与传统的碘油相对比,对于原发性肝癌的治疗,采用载药微球栓塞术可获得良好的疗效,从而在很大程度上减少并发症发生。本研究20 例患者均未出现严重并发症(如胆汁漏合并感染、肝功能衰竭、肿瘤破裂出血、肝脓肿等)。
目前的研究存在若干局限性。首先,本研究中的样本量相对较小,因此有必要进行更大的样本量进一步研究,以验证CalliSpheres 载药微球TACE 治疗Child-Pugh 评分8 分肝癌患者的安全性和有效性。其次,作为一个现实的研究,可能会出现一些复合因素,因此需要进一步的随机对照试验验证。最后,这是一个单中心的研究,这可能会导致患者的选择偏倚,进一步的多中心研究是必要的。
综上所述,CalliSpheres 载药微球应用于TACE 对治疗Child-Pugh 评分8 分肝癌具有良好的效果,是一种临床上积极和安全的治疗选择,但进行大量的随机对照试验证实仍然是必要的。当然,CalliSpheres 载药微球较传统的TACE 优势明显,本文研究结果为进一步研究这种动脉化疗栓塞治疗方法提供了依据。

