某院药品不良反应上报工作改进实践*
黄 娟,汪渝婷,彭 颖,张 静,李 旭,曾明辉△,杨 勇
(1. 四川省邛崃市医疗中心医院,四川 成都 611530; 2. 四川省医学科学院·四川省人民医院,四川 成都 610072)
目前监测药品不良反应(ADR)的方式包括自愿报告和主动监测。后者常用的有直接观察法、病历审查法和触发工具法。美国健康促进研究所于2009年推出全面触发工具(GTT,第二版),GTT 为监测药品不良事件(ADE)的方法,可提高护理过程的安全性。触发工具法是在病历审查法的基础上衍化发展而来的新型ADE 监测方法。首先建立一套和ADE 相关联的指标体系,包括ADE 相关的临床表现、对症治疗措施或特异性的实验室检查指标。审查者(医师、护士、药师)通过识别随机病例中的相关指标,再和ADE 进行关联,最终确认ADE是否发生,从而获得其真实发生率。触发器是检测ADE的线索。如触发器“肾上腺素”,提示患者可能发生了过敏性休克,然后对病历相关内容进行审查,以确认是否发生了ADE。运用触发管理工具对患者病历进行回顾性审查,确定可能的ADE,以提高审查效率和准确率[1-2]。四川省邛崃市医疗中心医院(下文以“我院”代指)为省、市ADR 监测哨点医院,为寻找行之有效的ADR 上报机制,我院以改善ADR 报告上报工作为切入点,利用质量管理工具和触发管理工具,各进行了1 轮持续改进工作,探讨了2 种管理工具在医院ADR 上报工作改进中的应用价值。现报道如下。
1 资料与方法
1.1 第1 轮改进
基于PDSA[计划(P)-实施(D)-学习(S)-处理(A)]循环并采用鱼骨图、甘特图等质量管理工具对收集数据进行整理、统计与分析。其中采用鱼骨图进行原因分析后,选择评分大于80%的条目为主要原因。第1轮改进时间为2017年1月至2019年12月。
原因分析:全面分析2016年医院ADR 上报情况后,发现存在的问题主要为ADR 整体上报数量少,针对该问题,医院组织相关人员从人员、机器设备、方法等多方面进行分析[3],统计出可能导致医院ADR 报告数量少的原因(见图1)。筛选出的主要原因为临床药师参与度不足,医师对ADR 认识不到位,医院无ADR 上报平台。
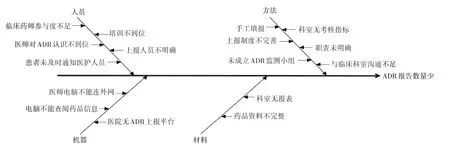
图1 我院ADR上报数量少原因鱼骨图Fig.1 Fishbone diagram of reason analysis for the small quantity of ADR reports in our hospital
计划制订:针对以上主要原因进行对策拟订,药学部工作人员经过头脑风暴,从可行性、经济性、效益性等方面对项目进行评价,并提出改进措施,主要措施有将指标分配到病区、每季度公布ADR 上报数量、完善ADR 上报流程等。利用甘特图制订计划时间表,确定各部分责任人,按计划实施。
实施与总结:2017年2月完成组织构架和制度的建设工作,主要为整理、统计和分析2016年我院ADR 上报情况。2017年3月至11月,按甘特图拟订计划(见表1)完成各项目标任务。其中,临床药师加强与临床科室的沟通,主要为督促临床科室主动、及时上报ADR,并给予必要的技术指导;多条途径收集ADR,主要指通过开放获取(OA)平台、微信群、QQ 群、电话等多条途径收集;每季度定期在药事管理会议上通报ADR 上报情况;召开专题讲座和举办宣传活动。2017年12月,总结ADR上报改进效果,建立标准化上报流程(见图2)。

表1 计划制订与实施甘特图Tab.1 Gantt chart of plan formulation and implementation
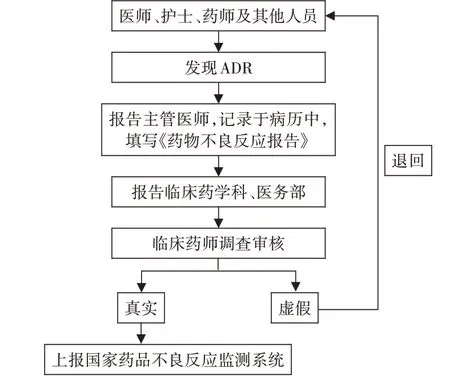
图2 ADR监测和报告流程图Fig.2 Flowchart of ADR monitoring and reporting
1.2 第2 轮改进
与2016年相比,医院2017年、2018年、2019年的ADR报告数量增多,但新的、严重ADR报告上报数量较少。药学部工作人员经过头脑风暴,查阅相关资料,运用触发管理工具进行第2 轮改进。第2 轮改进的目标为提高新的、严重ADR 上报数量,改进时间为2020年1月至2022年12月。
触发器:参考首都医科大学宣武医院研制的触发器[4],结合我院2016年至2019年的ADR 上报情况,得到14 条与实验室指标及用药相关的触发器[5],详见表2。
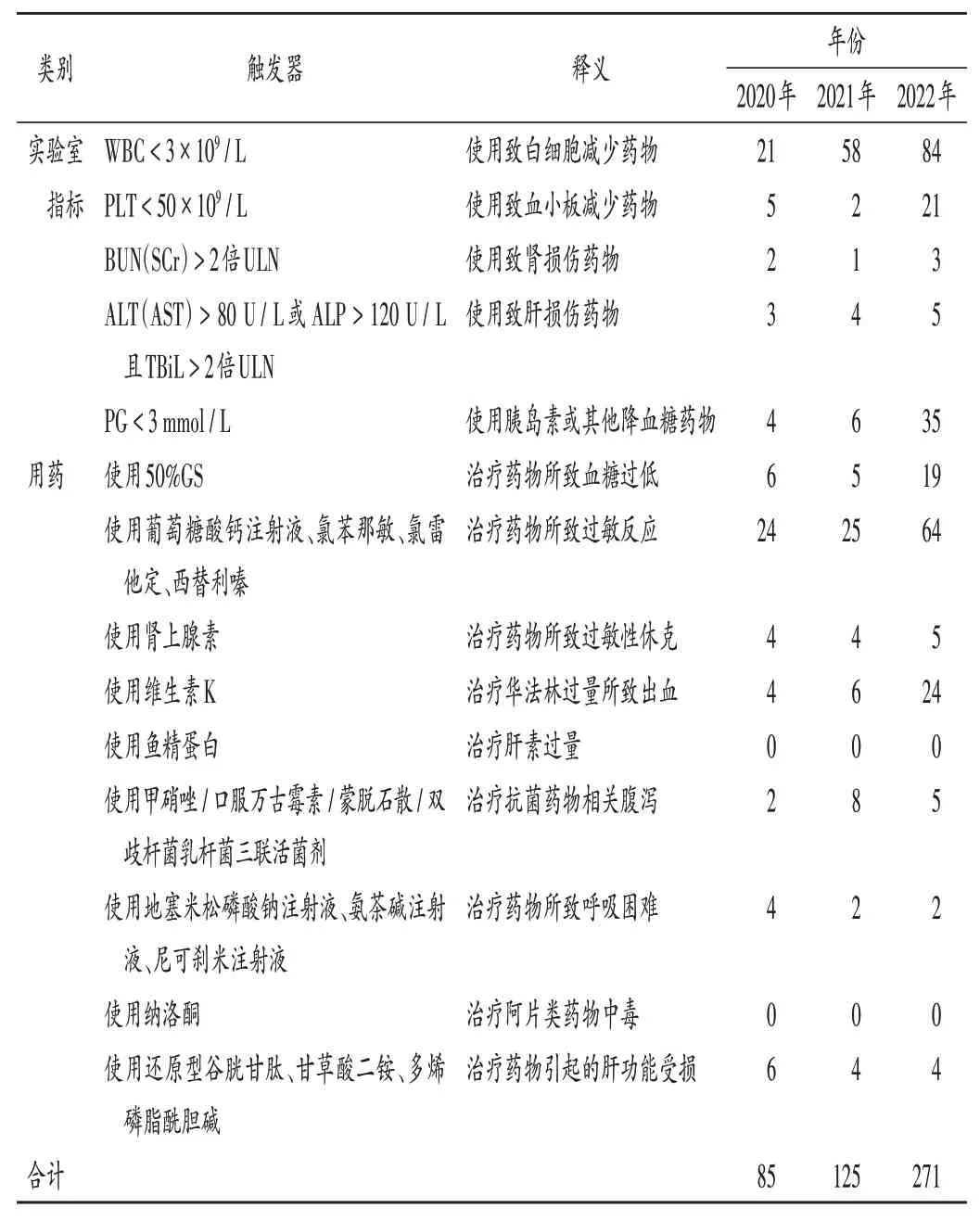
表2 触发器及其阳性频次Tab.2 Triggers and corresponding positive frequency
收集上报方式:各临床科室均配备专职临床药师1 名,负责合理用药及ADR 的监管。临床药师在进行临床科室审方、查房、会诊等药学监护时,发现触发器阳性时及时查看病历,并与责任医师、护士沟通,若确定为ADR,则及时上报。
1.3 统计学处理
采用GraphPad Prism 7.0 统计学软件及两因素方差分析法(Two-way ANOVA)对数据进行统计学分析。
2 结果
2021年、2022年触发器阳性频次均较2020年提升,详见表2。[其中2022年与2021年比较,差异有统计学意义(P<0.05)]。表2中,WBC为白细胞计数,PLT为血小板计数,BUN 为血尿素氮,SCr为血清肌酐,ULN 为正常值上限,ALT 为丙氨酸氨基转移酶,AST 为天门冬氨酸氨基转移酶,ALP 为碱性磷酸酶,TBiL 为总胆红素,PG 为随机血糖,GS 为葡萄糖注射液。2016年1月至2022年12月ADR 上报情况见表3,其中新的+ 严重ADR占比总体呈上升趋势。
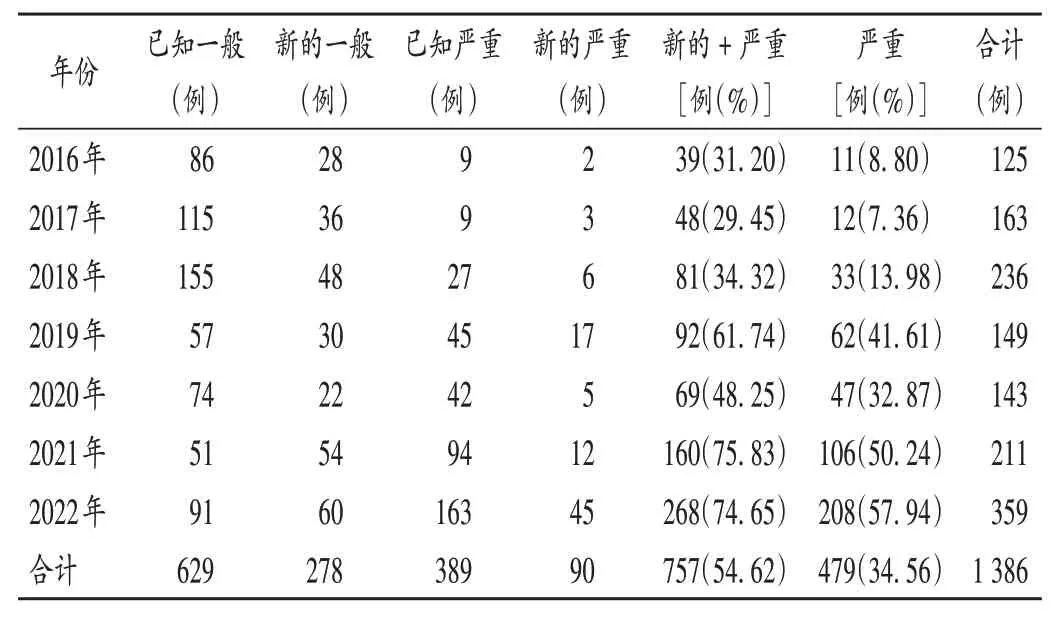
表3 2016年至2022年医院ADR上报情况Tab.3 ADR reporting in the hospital from 2016 to 2022
3 讨论
3.1 触发器的应用
2020年至2022年触发器“使用鱼精蛋白”和“使用纳洛酮”未触发。通过查找这2种药品的使用情况,发现其在我院的使用量均较低,主要为介入科和急诊科使用。介入科是在介入手术中使用鱼精蛋白[6],不易触发触发器。急诊科使用纳洛酮主要用于急性乙醇中毒[7],非药品所致,不会触发触发器。根据实际情况,医院在2023年ADR 收集实践中已删除这2 个触发器。在上报ADR 中除降糖药引起的低血糖反应外,也需关注非降糖药(糖皮质激素、抗菌药物等)引起的低血糖反应[8]。触发器中“使用甲硝唑/口服万古霉素/蒙脱石散/双歧杆菌乳杆菌三联活菌剂”可能治疗抗菌药物引起的相关性腹泻,若此触发器触发,临床药师需查看患者是否发生抗菌药物相关性腹泻[9]。触发器的应用不仅有利于收集ADR,亦可加强抗菌药物合理使用点评工作,促进其合理使用[10]。
除“实验室指标”触发器和“用药”触发器外,也可将“诊断”作为触发器,如诊断为急性上消化道出血,可能使用引起消化道出血药物;诊断为低血糖反应,可能使用胰岛素或引起血糖降低的药物;诊断为骨髓抑制,可能使用致白细胞减少的药物;诊断为肝功能异常,可能使用致肝损伤药物;诊断为肾功能异常,可能使用致肾损伤药物;诊断为过敏性皮炎,可能是药品导致的过敏反应。每个临床科室的专职临床药师在晨交班和医嘱审核时,查看该科室患者诊断,根据诊断作为触发器也可提升ADR上报质量,且可能大部分为严重ADR。但“诊断”触发器可能与“实验室指标”触发器、“用药”触发器有重复,使用50%GS或诊断为低血糖反应,可能是使用了胰岛素或其他降血糖的药物。“诊断”触发器还有待探索和完善。
3.2 PDSA 循环管理
以改善ADR 报告的上报情况为切入点,利用PDSA循环,通过计划的制订与实施,完善了ADR 监测与报告的组织架构,提高了医护人员的监测水平和素质,健全了奖惩机制,制订了ADR 监测制度和上报流程。PDSA循环管理提升了ADR 报告的上报数量;加强了医、药、护之间的沟通与交流,激发了药师学习和运用质量管理工具的热情,提升了其管理工具的运用能力;形成了PDSA 的良性循环机制;使持续质量改进逐渐成为员工的自觉习惯和医院文化的重要组成部分,也为PDSA 循环运用于医院药学质量管理奠定了基础。
3.3 触发管理工具
由于第1 轮PDSA 循环管理后,新的及严重ADR 报告仍较少,故第2轮运用触发管理工具改进ADR上报工作。我院触发管理工具的选择和应用参考文献[11-12]并结合医院工作情况,主要从“实验室指标”触发器和“用药”触发器入手。通过触发管理工具的应用,我院ADR 上报数量和质量均有所提升,且2020年至2022年新的和严重ADR 报告比例均逐年提升。但在上报过程中仍发现运用触发管理工具存在局限性,触发器条目数应包括但不限于本研究中的14 条触发器,如导致血钾、甲状腺激素水平异常的药物等尚未包括在内,还需进一步完善。
3.4 实践效果
我院以改善ADR 报告上报为切入点,利用质量管理工具和触发管理工具持续改进上报工作,完善了ADR 监测和报告的相关制度和流程,将ADR 上报工作标准化、流程化,全面提高了医院对ADR 发现、报告、预警和分析处理的整体能力。同时,药学相关人员运用2种管理工具的能力得到提升,医、药、护之间联系更紧密,提高了团队协作的能力。

