日照市193 例倍他司汀不良反应报告分析
房靖祥,刘 云,吴瑞强
(1. 山东省日照市市场监督管理局,山东 日照 276800; 2. 山东省日照市质量检验检测研究院,山东 日照 276800; 3. 山东省日照市莒县妇幼保健计划生育服务中心,山东 日照 276500)
倍他司汀为组胺H1受体激动剂,具有扩张血管作用,可促进脑干和迷路的血液循环,纠正内耳血管痉挛,减轻膜迷路积水,并有抗血小板聚集及抗血栓形成作用[1]。近年来,国内偶有倍他司汀引起严重神经毒性[2]、水肿[3]、声音嘶哑[4]、支气管痉挛[5]、窦性心动过速[6]、血管性水肿型药疹[7]的报道。为进一步明确倍他司汀药品不良反应(ADR)发生的特点,本研究中对山东省日照市上报国家药品不良反应监测系统的倍他司汀ADR 报告进行分析,为临床安全、合理使用该药提供参考。现报道如下。
1 资料与方法
收集山东省日照市药品不良反应监测中心2014年1月1 日至2023年1月1 日上报至国家药品不良反应监测系统涉及怀疑倍他司汀且已完成评价的ADR 报告。按国家药品不良反应监测中心报告质量评估标准进行规整,应用Excel 软件对ADR 报告的类型和来源、患者基本情况、给药途径、累及系统/器官及临床表现、转归等信息进行统计与分析。
2 结果
2.1 ADR 报告基本情况
共收集到有效ADR 报告193 份,其中,一般ADR 183 例(94.82%),含新的一般ADR 26 例(13.47%);严重ADR 10 例(5.18%),其中新的严重ADR 1 例(0.52%)。涉及患者193 例,其中男71 例,女122 例;患者年龄分布见表1。静脉滴注174 例(90.16%),静脉注射(不含静脉滴注)5例(2.59%),口服14例(7.25%)。
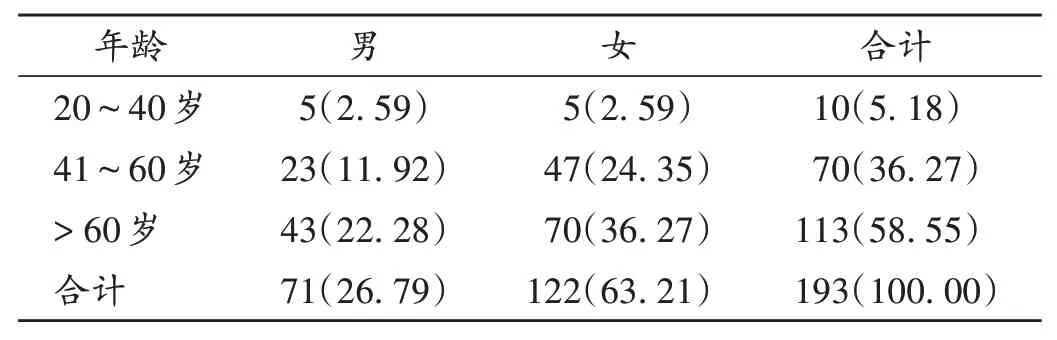
表1 患者年龄及性别分布[例(%),n=193]Tab.1 Distribution of patients′ age and gender[case(%),n = 193]
2.2 ADR 累及系统/器官及临床表现
共发生ADR 268例次。临床表现主要累及系统/器官为神经系统、胃肠系统、皮肤及皮下组织,并包括全身性疾病及给药部位各种反应等;ADR 主要表现为头痛、头晕、心悸、恶心、瘙痒、胸闷等。详见表2。
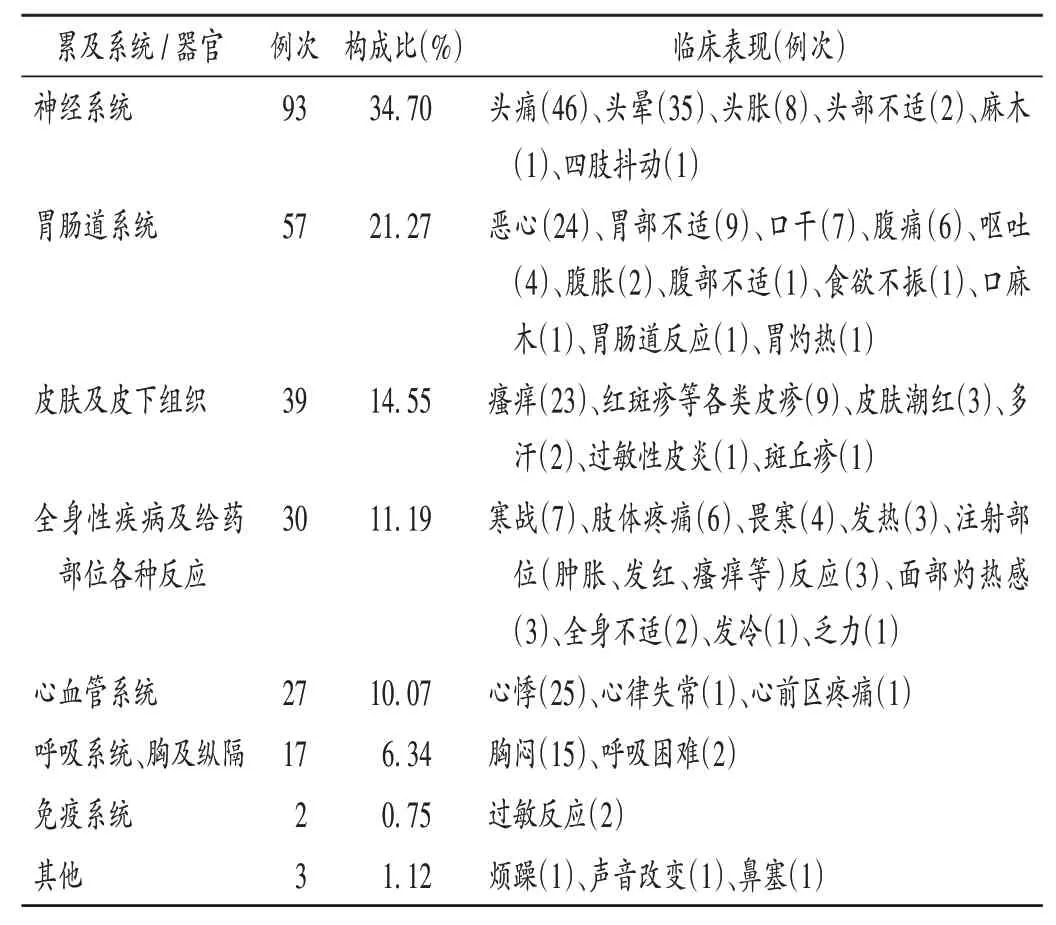
表2 ADR累及系统/器官及临床表现(n=268)Tab.2 Systems / organs involved in ADRs and clinical manifestations(n = 268)
2.3 严重ADR
倍他司汀所致严重ADR共10例。其中男2例,女8例;年龄30~87岁;主要表现为胸闷、呼吸困难;累及系统/器官主要为呼吸系统、胸及纵隔;给药途径除1 例为口服外,其余均为静脉滴注;发生时间为用药后6~50 min(2 例不详);3 例有合并用药,均为与丹参注射液合用;转归均为痊愈(7例)或好转(3例)。详见表3。

表3 严重ADR发生情况Tab.3 Incidence of serious ADRs
2.4 ADR 转归
193 例患者中,痊愈123 例(63.73%),好转66 例(34.20%),未好转1 例(0.52%),转归情况不详3 例(1.55%)。
2.5 关联性评价
根据《药品不良反应报告和监测工作手册》进行关联性评价,其中很可能71 例(36.79%),可能122 例(63.21%)。前者中一般ADR 64例,严重ADR 7例;后者中分别为119例和3例。
3 讨论
3.1 患者性别与年龄
女性患者多于男性,可能与该药物的适应证梅尼埃病女性发病率高于男性(1∶1~1.3∶1)有关[8],ZUCKER等[9]研究发现,由于药物潜在的生殖毒性,大多数药物临床试验曾排除女性参与,这可能导致获批药物更易诱发女性患者的ADR。倍他司汀ADR 以60 岁以上患者发生率最高。分析原因为,老年人因机体各系统功能全面或部分衰退,可能对相应种类的药物应答能力较弱[10],因此ADR 发生率高于一般成年人。另外,可能与疾病的发生年龄有关,提示老年患者在使用倍他司汀时,应加强药物治疗的监护,加强ADR 监测,减少ADR发生[11]。
3.2 给药途径
193 例ADR 中,静脉给药占92.75%;严重ADR 中90%为静脉滴注。静脉给药无首过效应,药效迅速且强烈,药物的pH、渗透压、毒素、杂质、微粒均可增加ADR的发生率[12],因此,医务人员应对静脉给药患者加强药学监护,促进患者用药安全[13]。
3.3 累及系统/器官及临床表现
倍他司汀ADR 主要累及系统/ 器官为神经系统、胃肠道系统、皮肤及皮下组织,主要临床表现为头痛、头晕、心悸、恶心、瘙痒、胸闷等。JECK-THOLE 等[14]在倍他司汀使用安全性的研究中回顾了该药上市35年以来ADR 的全球监测数据,其中神经系统ADR 主要包括头晕、头痛、失眠和烦躁不安,皮肤过敏反应通常包括轻度自限性皮疹、瘙痒和荨麻疹,胃肠道反应主要涉及恶心、呕吐或非特异性腹痛。本研究结果与之基本一致。
3.4 严重ADR
倍他司汀所致严重ADR 主要表现为胸闷、呼吸困难,累及系统/器官主要是呼吸系统、胸及纵隔。倍他司汀的药理作用是通过激动H1受体引起支气管平滑肌收缩[15]。杨湘君等[5]曾报道倍他司汀致支气管痉挛的病例。倍他司汀ADR发生时间均在1 h内(除2例不详外),最短为用药后6 min,说明倍他司汀致ADR多为速发型,因此,提示在用药初期就应密切观察患者的用药反应,一旦发现异常,应立即停药并给予对症处理。有3例合并丹参注射液用药的情况,提示尽量不要合并用药,联合用药可能也会诱发和增加ADR 发生[16]。但倍他司汀联合丹参注射液是否更易引发ADR,目前尚无有关报道。倍他司汀需经肾脏清除,高剂量的倍他司汀静脉滴注可能导致药物蓄积[2],10 例严重ADR 患者中有1 例肾功能较差,提醒肾功能较差患者的ADR风险可能会增加。
3.5 药品说明书警示力度不足
倍他司汀药品说明书中明确本品常见ADR有口干、胃部不适、心悸、皮肤瘙痒等,对于可能引起头痛、头晕、胸闷、呼吸困难等ADR 记载不全,有消化道溃疡史或活动期消化性溃疡也应慎用倍他司汀[4]。倍他司汀属组胺类药物,理论上抗组胺药可能削弱倍他司汀的疗效。
倍他司汀上市以来安全性较好,严重ADR 罕见[2],但使用过程中的ADR 也不可忽视,应对倍他司汀进行风险评估,结合已发现的ADR,药品生产厂家应修改完善药品说明书,增加累及神经系统、胃肠道系统、皮肤及皮下组织等ADR内容,增加禁忌和注意事项等内容。
3.6 合理用药
为促进临床合理使用倍他司汀,保障患者用药安全,临床医师应仔细阅读其药品说明书内容,在选择用药时应充分进行效益/风险评估,避免超适应证、超剂量及违反禁忌使用。应用倍他司汀前应详细询问患者过敏史,评估患者肝肾功能,有过敏史者要禁用,肝肾功能较差的患者要慎用,老年人使用要注意调节剂量,给药后要做好用药监护工作,若发生ADR 应及时予对症处理。本研究的不足之处在于,数据仅来源于日照市上报的数据,受上报人员认识和水平的制约,ADR 病例也可能存在漏报,样本量有一定的局限性,今后还需进一步扩大样本量深入研究。

