糖尿病综合管理中的药物相互作用调查与分析*
马雪辰,沈 珑,俞彬滨,曹莉华,施芳红△
(1. 青海省西宁市第三人民医院,青海 西宁 810005; 2. 上海交通大学医学院附属仁济医院,上海 200127;3. 浙江省台州市第一人民医院,浙江 台州 318020)
全球糖尿病地图显示,2021年全球糖尿病成年患者达5.37亿人,中国糖尿病发生率约为12.8%,有1.41亿成年糖尿病患者,居全球首位[1]。糖尿病为进展性疾病,其综合管理涵盖对血糖、血压、体质量和血脂的控制,更易存在多重用药情况[2]。据调查,糖尿病患者同时使用5~9 种药物的比例显著高于非糖尿病患者,且即使排除降糖药物影响,结果也一致[3]。多重用药会增加药物间的影响,潜在的药物相互作用(DDI)可能会加重病情。因此,了解糖尿病综合管理中常见DDI 及影响因素有利于临床安全用药,规避治疗风险。Lexicomp 为集药物和医疗信息于一体的专业数据库,其中通过Lexi -InteractTM数据库可筛选DDI 信息[4]。基于此,本研究中通过检索Lexi-InteractTM数据库,汇总糖尿病综合管理中的DDI,并收集上海某三级甲等医院2 型糖尿病(T2DM)并心肌梗死患者的病例资料,分析该类患者DDI的特点及影响因素,为临床合理用药提供参考。
1 资料与方法
1.1 糖尿病综合管理DDI 定义
选择的药物包括降血糖、降血压、调血脂及减重药物[分类标准参考《中国国家处方集(化学药品与生物制品卷)》[5]、《中国2 型糖尿病防治指南(2020年版)》[6]、《肥胖症基层合理用药指南》[7]、《高血压患者药物治疗管理路径专家共识》[8]]。通过Lexi- InteractTM数据库,查询糖尿病综合管理相关药物的DDI。按安全性等级分类整理(共分为5个等级:X级,避免联用,联用风险>收益,常为配伍禁忌;D级,考虑调整治疗,需评估风险获益,采取强化监测、经验性剂量调整或选择替代药物等措施;C级,需监控治疗,联用获益>风险,应合理监测或适当调整剂量;B级,无须调整,联用风险较小;A级,无相互作用[9]。分别统计每类药物各级DDI数量及平均数,并分析X级DDI数量较多的前3类药物。
1.2 患者资料收集
纳入标准:符合T2DM 诊断标准[6]及第4 版心肌梗死全球定义诊断标准[10],后者主要包括ST 段抬高型、非ST段抬高型心肌梗死,急性冠状动脉综合征,不稳定型心绞痛等;住院期间至少使用降血糖药、降血压药、调血脂药、减重药中的2 类及以上;至少使用1 种降血糖药物;合并用药超过5种。
排除标准:疾病诊断不明确;用药记录不完整;其他不符合纳入标准的情况。
资料收集:收集上海交通大学医学院附属仁济医院2021年8月至2022年8月收治的T2DM 并心肌梗死患者的资料。利用医院信息系统查询住院患者的病案号,以及基线数据[性别、年龄、身高、体质量、体质量指数(BMI)、疾病诊断、糖尿病病程],实验室指标[糖化血红蛋白、糖化白蛋白、空腹C肽、餐后C肽、空腹胰岛素、餐后胰岛素、肾小球滤过率(eGFR)等],院内合并用药情况。其中检测指标均为患者住院期间检测值,用药情况来自住院期间的长期医嘱。利用Lexi-InteractTM数据库筛选每例患者的DDI 情况,统计各级DDI 的数量,根据C,D,X 3类DDI总数分为低DDI组(≤5组DDI)和高DDI组(>5 组DDI),同时分析影响DDI的因素。本研究经上海交通大学医学院附属仁济医院伦理委员会批准[批件号KY〔2019〕076],患者签署知情同意书。
1.3 统计学处理
2 结果
2.1 糖尿病综合管理相关药物DDI
共纳入109 种药物,包括降血压药57 种,降血糖药32 种,调血脂药19 种,减重药1 种。DDI 总数依次为5 091组、1 086组、723组、15组,平均为89.32组、33.94组、38.05组、15组。
除减重药外,其余3类药物DDI总数最多的分别为钙通道阻滞剂(CCB)、磺脲类药物、他汀类药物。详见表1(其中TZD为噻唑烷二酮,DPP-4为二肽基肽酶4,SGLT2为钠- 葡萄糖协同转运蛋白2,GLP - 1 为胰高血糖素样肽-1,PCSK9为肝源性分泌型丝氨酸蛋白酶,ACEI为血管紧张素转化酶抑制剂,ARB为血管紧张素Ⅱ受体拮抗药,ARNI为血管紧张素受体脑啡肽酶抑制剂)。

表1 糖尿病综合管理相关药物DDI等级分布(DDI总数/平均数,组)Tab.1 Distribution of DDIs related to comprehensive management of DM by grades(total case / average case of DDIs)
2.2 糖尿病综合管理中避免使用的DDI
X级DDI总数排前3的药物分别是他汀类药物、CCB类药物及β受体拮抗药。他汀类药物均不能与夫西地酸和红曲米同时使用,其中辛伐他汀X级DDI数量最多,有17种药物应避免与其联用;CCB类药物均不能与溴哌利多和丹曲林钠同时使用,其中维拉帕米X级DDI数量最多,有32种药物应避免与其联用;β受体拮抗药均不能与卡巴拉汀和白桦树过敏原提取物同时使用。详见表2。

表2 糖尿病综合管理中避免使用的DDITab.2 DDIs to be avoided in the comprehensive management of DM
2.3 患者基线特征及DDI 情况
共纳入69 例患者,其中低DDI 组26 例,高DDI 组43例。由表3可知,两组患者仅慢性肾脏病(CKD)1-3期比例、糖化血红蛋白、糖化白蛋白、空腹血糖水平比较,差异有统计学意义(P<0.05)。详见表3(其中部分指标有部分患者未采集到)。
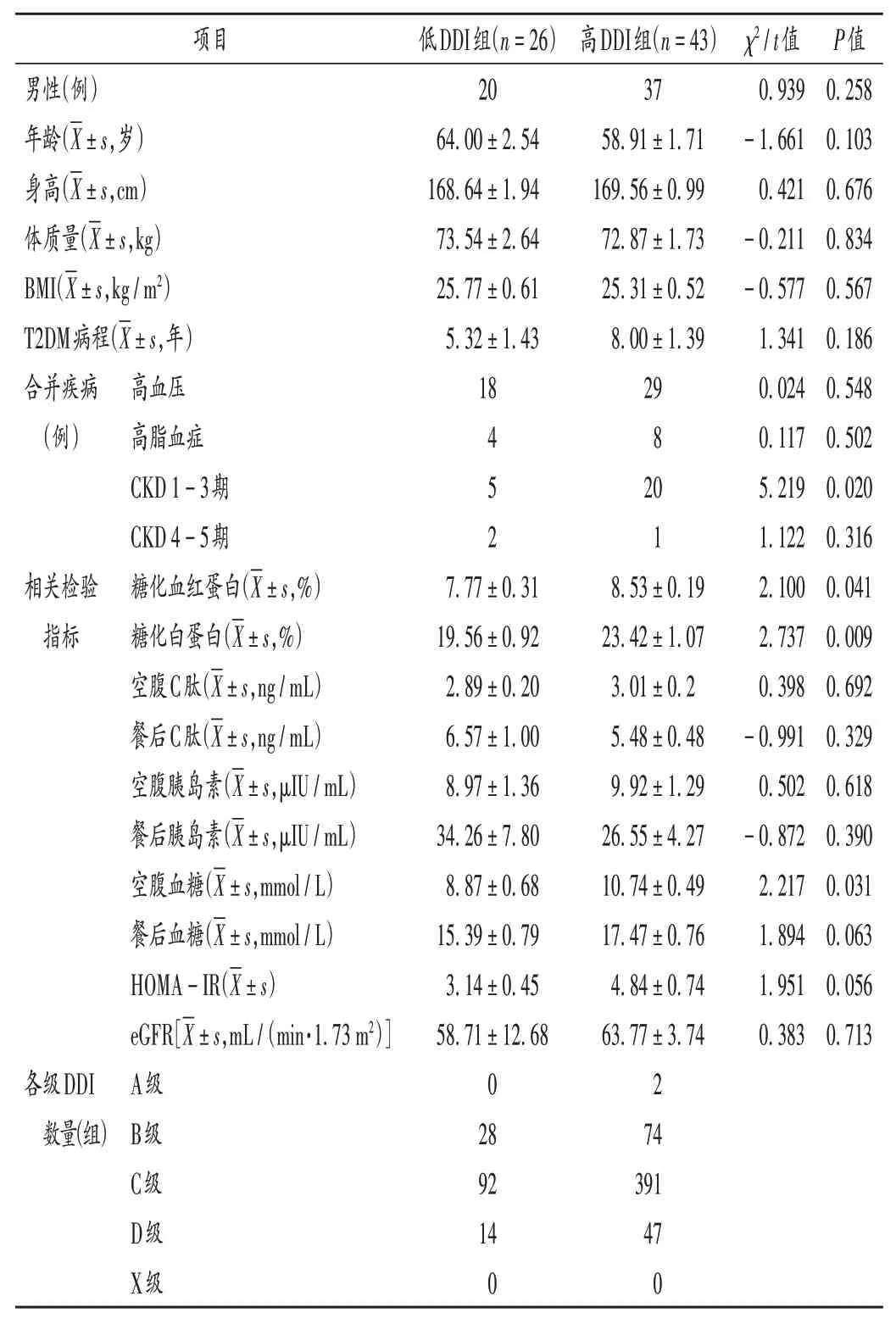
表3 两组患者一般情况比较Tab.3 Comparison of the patients′ general data between the two groups
2.4 影响患者DDI 相关危险因素分析
结果见表4(HOMA - IR 为胰岛素抵抗指数)。可见,患者合并用药数量、CKD 1 - 3 期、糖化血红蛋白、糖化白蛋白及空腹血糖为影响患者DDI 总数的危险因素。
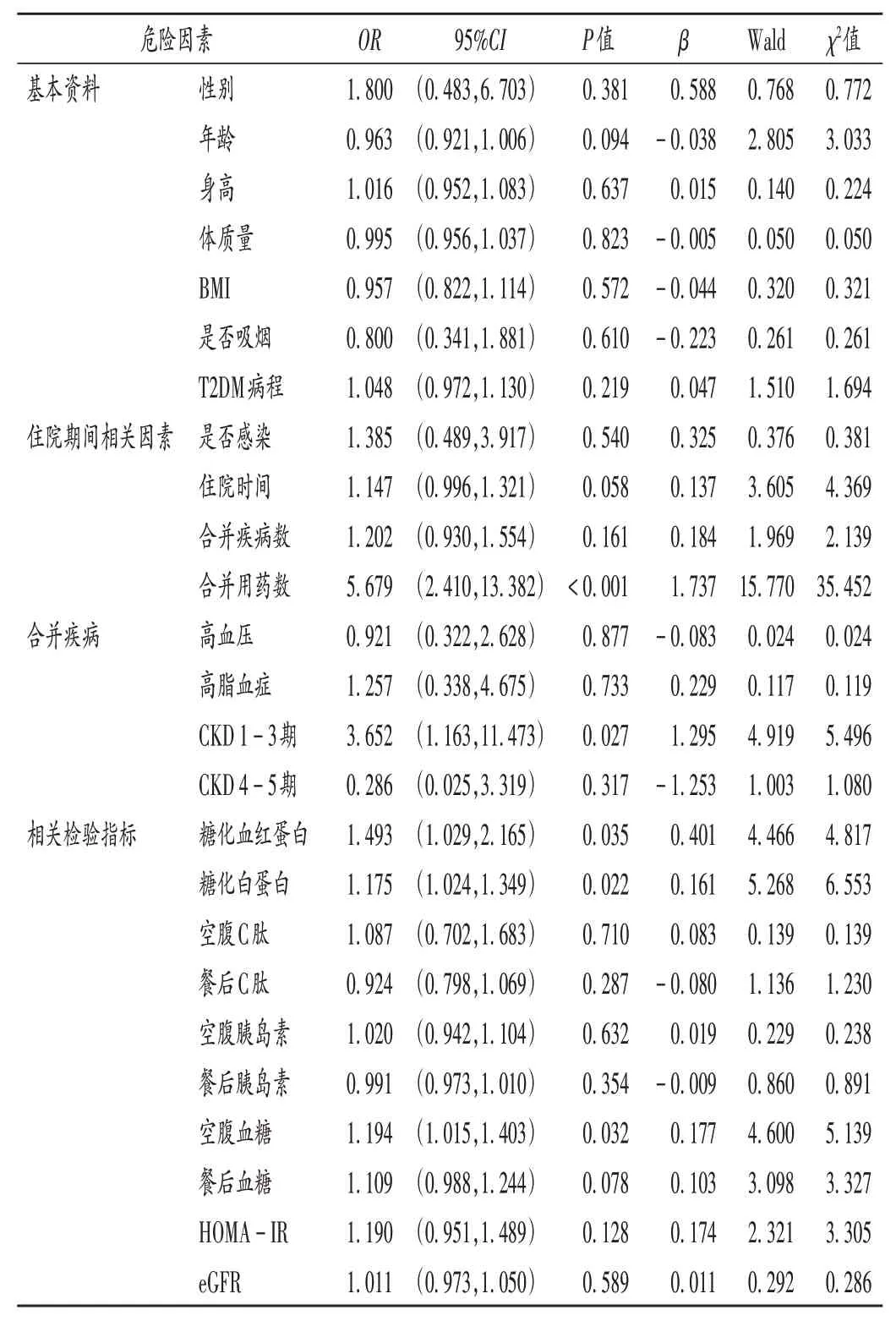
表4 患者DDI相关危险因素的Logistic回归分析Tab.4 Results of Logistic regression analysis of DDIs - related risk factors in patients
3 讨论
糖尿病患者常合并多种疾病,其中心血管疾病尤其心肌梗死是糖尿病致残致死的主要共患病[11-12]。因此,本研究中选择T2DM 合并心肌梗死的患者为研究对象。糖尿病患者的综合管理需涵盖血糖、血压、血脂和体质量[7],故本研究中统计了降血压药、降血糖药、调血脂药、减重药的DDI 分布情况,同时对纳入患者的DDI 情况进行分析,以探究可能引起DDI 的相关危险因素。
据报道,DDI 风险与合用药物种数有直接关联,与合用药数量≤5 种比较,合用药物数量> 5 种和> 8 种时,不良DDI 发生风险分别增加50%和100%[13]。因此,本研究中采用C,D,X 级DDI 总数> 5 组作为“DDI较多”的分界点,结果提示,患者合并用药数量、CKD 1-3 期比例及糖化血红蛋白、糖化白蛋白和空腹血糖水平为影响患者DDI 总数的危险因素。糖化血红蛋白是糖尿病诊断中的“金标准”,是糖尿病并发症风险的关键决定性因素;糖化白蛋白可比糖化血红蛋白更早地检测出平均血糖的变化[14-15]。糖化血红蛋白、糖化白蛋白及空腹血糖尽可能接近正常范围,有利于降低糖尿病并发症的风险,减少合并用药数量,减少DDI 发生的风险。
本研究结果显示,DDI数量由高到低依次是降血压药、降血糖药、调血脂药及减重药。高血压为常见慢性疾病,降血压药物品种多,使用广,常面临更多的DDI风险。减重药的DDI 数量最少,因为目前该类药仅纳入了原国家食品药品监督管理局唯一批准的化学减重药物奥利司他[8]。X级DDI 数量排前3 的药物分别是他汀类药物、CCB 类药物及β 受体拮抗药。他汀类药物中辛伐他汀是通过CYP3A4 代谢,CYP3A4 强抑制剂(如酮康唑、克拉霉素等)可减少辛伐他汀的消除,从而增加其血药浓度,相应的不良反应如横纹肌溶解的风险也会增加,应避免联用[16]。CCB 类药物中以维拉帕米X 级DDI 最多。文献报道1 例口服维拉帕米治疗的患者在静脉使用丹曲林钠后出现高钾血症并伴有血流动力学改变,由于丹曲林钠是防治恶性高热的唯一药物,因此建议冠状动脉搭桥期间易发生恶性高热的患者停用CCB类药物[17]。二氢吡啶类CCB 药物中尼索地平的X 级DDI 最多,该类药物与CYP3A4 强诱导剂(如利福平、卡马西平等)合用时,CYP3A4 强诱导剂会加快其代谢,降低血药浓度,引起血压升高或波动[9]。药师基于以上分析结果建议对于多重用药的糖尿病患者,在综合治疗时尽量选择同类药物中DDI 数量相对较少的药物联用。
本研究的局限性在于样本量相对较小,Lexi -InteractTM数据库筛选DDI时未纳入中成药和复方制剂,筛选药物存在局限性。
综上所述,糖尿病的综合管理提示,治疗时可考虑优先选择同类药物中DDI 数量相对较少的药物。除尽可能控制合并用药数量外,患者的糖化血红蛋白、糖化白蛋白、空腹血糖不仅可反映血糖控制水平,也是DDI 数量的相关危险因素,医务人员在糖尿病综合管理中应关注以上因素,减少因DDI 引起的药品不良事件。

