冷沉淀凝血因子融化后储存温度和时间对凝血因子的影响
王媛 刘国英 孔大为 李建斌 金新莉 张玉红 葛文超 成琳 刘佳璇 刘玉振
(河南省红十字血液中心,河南 郑州 450012)
冷沉淀凝血因子(cryoprecipitated antihemophilic factor,CAF)是新鲜冰冻血浆(fresh frozen plasma, FFP)在1℃~6℃融化后,分离出大部分的血浆,并将剩余的冷不溶解白色沉淀物在1 h 内速冻呈固态的成分血,主要组分是Ⅷ因子、血管性血友病因子、纤维蛋白原(简称Fbg)、纤维连接蛋白、Ⅴ因子和ⅩⅢ因子等,在甲型血友病、血管性血友病、先天性或获得性纤维蛋白原缺乏症、手术大出血、严重创伤及弥散性血管内凝血等患者治疗中取得了明显的效果,而血液质量是保障临床治疗效果的前提,由于CAF 中的Ⅷ因子不稳定,其含量与采集时间、制备方法、速冻温度、CAF 融化后的储存等有关[1-3]。 而CAF 融化后储存方法国内外标准差别太大,欧美是室温保存,我国是冷藏保存,另外,国内对于制备CAF 的原料FFP 报道较多[4-6],对于CAF 融化后储存温度及时间报道较少[7-8]。 鉴于以上原因,本研究大批量研究CAF 融化后储存不同的温度和时间对Ⅷ因子和Ⅴ因子的影响,为行业标准的制定提供参考依据,以保证临床输血及时、有效、安全,报告如下。
1 材料与方法
1.1 试剂与仪器
标准品(批号503298);质控品(批号507921、507795、 507788);Ⅷ因子试剂(批号560832A、560839、 560809、 560801); Ⅴ因 子 试 剂(批 号504995A、504990B); Fbg 试 剂(批 号565179 、565127、565092A、56571A);PT 试剂(批号568064、565798A、565796A);ATPP 试剂(批号558665A);OVBUFFER 缓冲液(批号569916);CaCl2溶液(批号563894A);清洗液(批号A2136),以上均由德国西门子SIEMENS 公司提供。 大容量低温离心机(美国西格玛);MBF-42 速冻机(卢森堡多美达);全自动CAF 制备仪(佛山沃塘医疗科技有限公司);恒温摇摆式水浴箱(美国科瑞特CT-4T.6C);ALS 多层速冻机(意大利Angelantonilife Science S.r.l 公司,山东威高代理);CS-2400 全自动血凝仪(日本Sysmex 公司);HSWS-600 电热恒温水浴箱(上海跃进医疗器械有限公司);50mL 转移袋(山东威高公司)。
1.2 CAF 制备
1.2.1CAF 制备原料
CAF 的制备原料是FFP,本中心制备CAF 均来源于400 mL 全血,对全血400 mL 采集时间>13 min进行标识,不能用于制备FFP,采集后储存于冷藏环境中,本站采用ACD-B 抗凝剂(含量100 mL)采血袋,最好在6 h 内完成上层血浆分离并速冻(下层红细胞加入100 mL MAP 保养液,制成悬浮红细胞,保存期由21 d 升为35 d),从血液采集到完成血浆分离最长时限不得超过18 h。 应当将FFP 快速冻结,建议在1 h 内将中心温度降至-30℃以下。 FFP 在-18℃以下储存,有效期为1 年。
1.2.2CAF 制备方法
1.2.2.1人工虹吸法
将FFP 袋置于1℃~6℃恒温摇摆式水浴箱中,另一空袋悬于水浴箱外,位置低于血浆袋,2 袋之间形成一定的高度落差。 血浆融化后,随时被虹吸至空袋中,当融化至剩下40~50 mL 血浆与沉淀物时,闭合导管,阻断虹吸。 转移至空袋的血浆,制成去CAF 的冰冻血浆。 将血浆与沉淀物混合,最终CAF容量控制在53(48~58)mL,制成CAF,宜在制备后1 h 内完成速冻,并且1 h 内将中心温度降至-30℃以下。 然后CAF 在-18℃以下储存,有效期为1 年。
1.2.2.2仪器虹吸法
打开全自动制备仪器,提前制冷到设定1℃~6℃,按“预温”按钮进行预先制冷,若制冷完成,按“启动”键开始制备,将FFP 在室温下放置5 min,待管路软化后上机制备,依次把血浆联袋放入制备盒中,按下“批量”按钮(所有袋同时进行称重),进入第二步操作,把三联袋分开,把空袋放入制备盒中,血浆袋放入水浴箱中,软管卡入夹管阀,按下该位置的确认按钮(称量空袋重量),同样操作其它血袋,如果是三联带,将2 个空袋都放入制备盒,全部血袋放置完毕后,仪器开始处理。 约30 min,当收集CAF 袋子剩余53(48~58)mL 时(仪器提前按重量进行设定),软管卡自动卡住,此时制备完成的位置会有声音和灯光提示,按一下提示灯光的按钮,取出该位置血袋,进行热合离断CAF 和血浆,宜在制备后1 h 内完成速冻,并且在1 h 内将中心温度降至-30℃以下。 在-18℃储存,有效期为1 年。
1.3 CAF 样本抽检
2021 年6 月—2023 年5 月,每月抽检4袋CAF,并于当月完成检测,2 年共抽检96 袋。
1.4 凝血因子检测
每月抽检储存在-18℃以下的CAF,在37℃水浴箱融化后称重,对外观有轻中度脂血予以标记,每袋融化后的CAF 和2 个50 mL 转移袋用无菌接驳机分装成2 袋两组CAF 各20 mL,1 组放置(4±2)℃(简称4℃)冰箱,另1 组放置(22±2)℃(简称22℃)电热恒温水浴箱中,放置时间段为0 h、4 h、8 h、12 h、24 h、48 h 各自进行无菌取样2 mL放入试管中,用加样枪在另1 试管中加入样品1 mL 和OVBUFFER 缓冲液3 mL 混匀,并及时在全自动血凝仪进行Ⅷ因子、Ⅴ因子以及Fbg 检测,打印结果留存记录,计算结果乘以4。 Ⅷ因子和Ⅴ因子计量单位均为IU/袋,Fbg 计量单位为mg/袋。
1.5 统计学分析
96 袋CAF 实验完成后,从其中随机选取60 袋无轻中度脂血CAF 实验数据进行分析,采用SPSS21.0 统计软件进行均值t检验,P<0.05 表示差异有统计学意义;P<0.01 表示差异有统计学意义。
2 结果
2.1 Ⅷ因子含量检测结果
融化后CAF 0h 检测Ⅷ因子、Ⅴ因子以及Fbg的平均值分别为(118.62±52.82)IU/袋、(41.19±10.37)IU/袋、(268.86±89.65)mg/袋,变异系数分别是44.53%、25.18%、33.34%,其中Ⅷ因子含量变异系数最大。 融化后CAF 中的Ⅷ因子含量,2 组储存结果比较,在4℃24h 及22℃48h,Ⅷ因子含量均有显著统计学意义(P<0.01),且在22℃储存,Ⅷ因子衰减速度更慢(表1)。

表1 CAF 融化后贮放不同的温度及时间对Ⅷ因子结果的影响(IU/袋,n=60)Table 1 Influence of different storage temperature and time on the results of FactorⅧafter CAF melting (IU/bag, n=60)
2.2 Ⅴ因子含量检测结果
融化后CAF 中的Ⅴ因子含量,两组储存结果比较,在4℃48h Ⅴ因子含量有统计学意义(P<0.05),22℃48hⅤ因子含量有显著统计学意义(P<0.01),且在22℃储存,Ⅴ因子衰减速度更快(表2)。
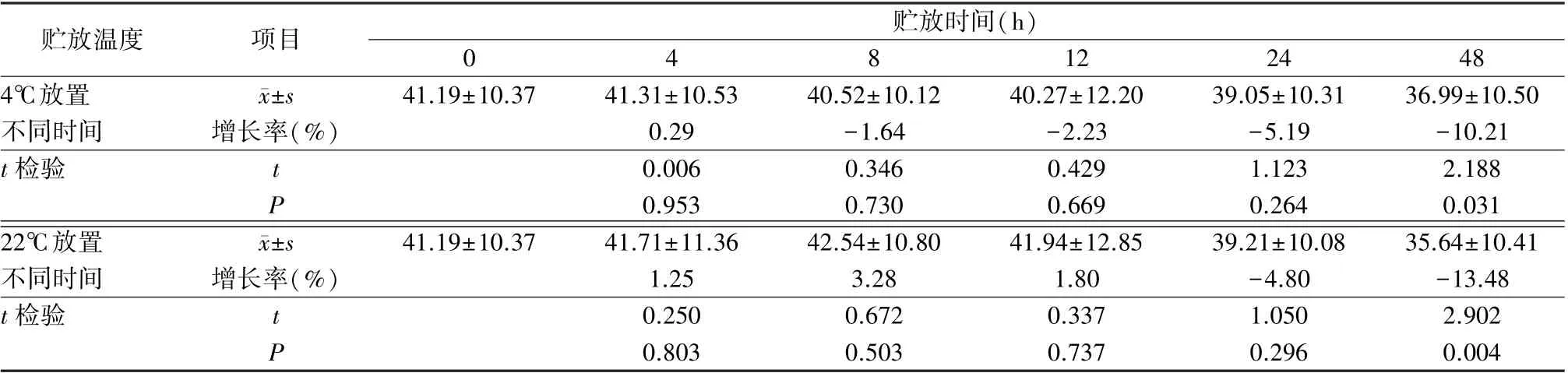
表2 CAF 融化后贮放不同的温度及时间对V 因子的影响(IU/袋,n=60)Table 2 Influence of storage temperature and time on V factor after CAF melting(IU/ bag, n=60)
2.3 Fbg 含量检测结果
融化后CAF 中的Fbg 含量,两组储存结果比较,各时间段与0h 含量比对均无统计学意义(P>0.05),说明Fbg 是比较稳定的凝血因子(表3)。
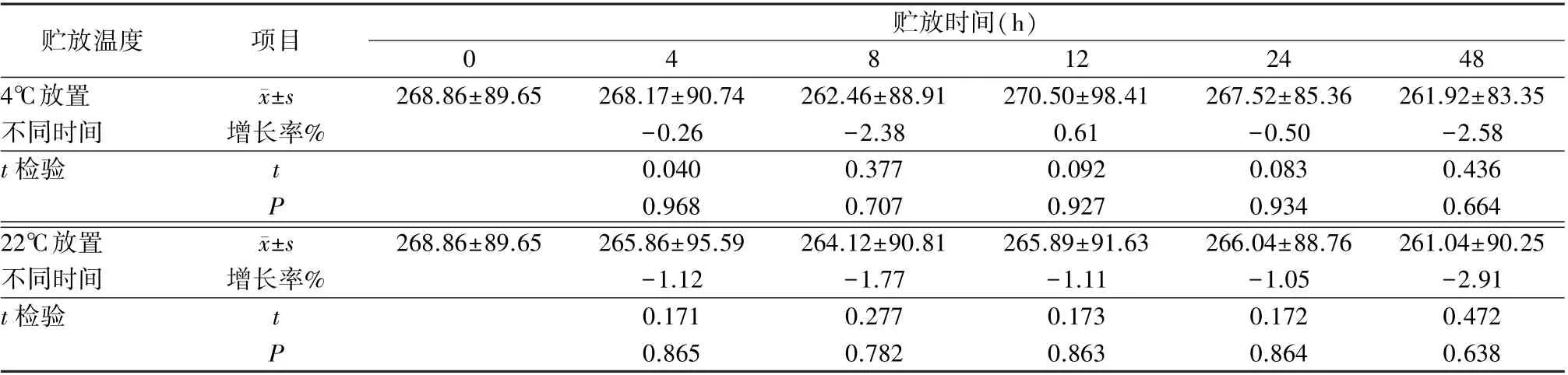
表3 CAF 融化后贮放不同的温度及时间对Fbg 的影响(mg/袋,n=60)Table 3 Effects of storage temperature and time on Fbg after melting CAF (mg/ bag, n=60)
3 讨论
CAF 是临床输血治疗的一种重要血液成分,主要用于预防和治疗出血性疾病。 如何避免融化后CAF 凝血因子下降,《美国AABB 技术手册》规定融化后的CAF 在20℃~24℃储存,在开放系统中汇集的,储存期为4 h,单袋或采用经FDA 批准的无菌接驳装置汇集的,储存期为6 h[9]。 《英国输血服务指南》规定CAF 一旦解冻,该成分不得再冷冻,应立即使用,如果延迟是不可避免的,在室温下储存,并在4 h 内使用[10]。 我国对融化后CAF 的储存规定:在2℃~6℃储存,储存期为24 h[11]。 CAF的制备原料是FFP,Cardigan 等[12]报道全血储存于4℃18~24 h 分离的血浆对于绝大多数需要输注FFP的患者是可以接受的。 Wilsher 等[13]发现全血储存于22℃24 h 分离的血浆中Ⅷ因子含量仍符合英国标准。 为了验证CAF 融化后的储存条件,本研究将CAF 融化后分成2 组,分别放置4℃和22℃储存,经过48 h 放置,检测凝血因子的变化。
本研究显示,60 份融化后的CAF 0 h 检测,Ⅷ因子、Ⅴ因子以及Fbg 的平均值分别是(118.62±52.82) IU/袋、(41.19±10.37) IU/袋、(268.86±89.65)mg/袋,变异系数分别是44.53%、25.18%、33.34%,其中Ⅷ因子含量变异系数最大,这可能与献血者血型、性别以及CAF 制备方法等差异相关[14-15],由于O 型Ⅷ因子含量最低,《英国输血服务指南》7.18 规定混合输注CAF,应来自O 型和非O 型CAF 的等量混合,国内对这方面没有规定。CAF 中的Ⅷ因子2 种(4℃和22℃)贮放温度24 h浓度下降率(20.46%和14.39%)低于文献报道[16],可能与本研究标本数量大和去除轻中度脂血样本等有关。
表1 显示,CAF 融化的2 组贮放温度Ⅷ因子含量均随贮放时间而下降。 4℃24 h 和22℃48 h 贮放与0 hⅧ因子含量比对,均有显著统计学意义(P<0.01),说明22℃贮放Ⅷ因子含量衰减率慢于4℃,原因可能是CAF 经过37℃融化后,其内部温度高于15℃以上,如果将融化后的CAF 重新放在4℃冰箱储存,随着时间延长超过12 h,CAF 袋内温度逐渐下降到4℃,这时的温度又达到Ⅷ因子重新析出临界温度,相当于反复冻融,导致析出的Ⅷ因子聚合体增加,从而使Ⅷ因子含量加速下降,这也验证了欧美国家CAF 融化后不冷藏而采取室温保存的规定;另外,如果制备CAF 原料FFP 中的血小板(英国规定血小板<60×109/L[17],我国没有相关规定)含量高,导致CAF 中的血小板浓度也高,过多的血小板在4℃聚集性增加,再加上和Ⅷ因子析出的白色物结合,激活凝血途径,导致细小纤维蛋白微聚物析出增多[18],从而导致Ⅷ因子含量下降。反观融化后的CAF 在22℃贮放可以克服上述缺点,阻止了Ⅷ因子析出和血小板聚集,大大延缓了Ⅷ因子含量下降率,因此,本研究CAF 融化后贮放于22℃与美国和英国贮放室温是接近的,而不是我国目前融化后CAF 在2℃~6℃储存24 h,因此,建议我国对融化后的CAF 储存方法进行改进,首选储存4℃,最长储存时间不超过12 h,次选储存22℃,最长储存时间不超过24 h。 表2 显示,融化后的CAF,2 组贮放温度Ⅴ因子含量均随贮放时间而下降,证明Ⅴ因子也是不稳定的凝血因子,与文献报道有一致的[19]也有不一致的[20]。 但Ⅴ因子下降速率没有Ⅷ因子明显,且4℃和22℃贮放24 h与0 hⅤ因子含量比对,均无统计学意义(P>0.05),当超过48 h 2 组贮放才均有统计学意义(P<0.05)。 4℃贮放Ⅴ因子含量衰减率要慢于22℃,原因是如果将融化后的CAF 重新放在4℃冰箱储存,CAF 中的Ⅴ因子在4℃时不会析出白色物质以及微聚物,从而不会导致Ⅴ因子下降速率增加。 表3显示,2 种贮放温度,Fbg 48 h 内与0 h 含量比对均无统计学意义(P>0.05),说明Fbg 是比较稳定的凝血因子。
综上所述,CAF 融化后储存22℃Ⅷ因子衰减速度比4℃更慢。 CAF 融化后应尽快输注,如果延迟不可避免;若延迟时间<12 h,采用4℃保存,若延迟时间超过12 h<24 h,采用22℃保存,这两种保存方法其实并不矛盾,是由CAF 中的Ⅷ因子在4℃析出白色物质这物理特性决定的。 将CAF 融化后由目前国标储存4℃24 h 缩短到12 h;或者由目前欧美标准22℃存放6 h 延长到24 h,这两种方法目的都是为了减少Ⅷ因子重新析出造成的反复冻融,从而导致Ⅷ因子失活,为临床和决策者对融化后CAF保存提供了理论依据,既保证了CAF 中的Ⅷ因子活性的安全有效性,又减少了血液资源的浪费。

