基于N端脑利钠肽前体、D-二聚体及降钙素原和临床病例资料构建AECOPD预后模型
何 萌 王 丽 詹江辉
河南省新乡市第二人民医院检验科 453000
慢性阻塞性肺疾病(Chronic obstructive pulmonary disease, COPD)是一种慢性、不可逆的阻塞性肺疾病。COPD的急性加重期(Acute exacerbation of chronic obstructive pulmonary disease, AECOPD)是病情进展的关键期,因感染等因素诱发,是以呼吸道症状恶化为特征的急性事件,典型症状为咳嗽加剧、呼吸困难加重、咳痰量变多、咳脓性黏稠痰。AECOPD患者易并发肺炎、慢性肺源性心脏病、低氧血症,已成为导致COPD患者最终死亡的重要原因。D-二聚体(D-dimer, D-D)是预测AECOPD患者预后的敏感指标,可反映机体炎症反应的严重程度。降钙素原(Procalcitonin, PCT)是一种降钙素前体物质,仅在炎症刺激作用下才可大量分泌和释放。N端脑利钠肽前体(N-terminal brain natriuretic peptide, NT-proBNP)是反映患者肺脏功能的准确指标。本研究拟观察重症AECOPD患者血清中NT-proBNP、D-D及PCT的表达水平,探讨三者联合检测对于患者预后的预测价值,对识别重症患者及潜在危险患者、指导临床策略的制定提供数据支撑,现报道如下。
1 对象与方法
1.1 研究对象 选取2018年1月—2022年10月我院接受住院治疗的AECOPD患者124例作为对象。电话随访1年,以全因死亡为终点,根据其出院后1年内的生存情况分为存活组(99例)和死亡组(25例)。按照相同标准选取2022年11月—2023年8月的45例AECOPD患者,设为验证集,行外部验证。
1.2 选择标准 纳入标准:(1)符合COPD诊断标准[1],同时符合AECOPD定义:短期内呼吸道症状加重,超出日常波动范围,需要改变药物治疗方案;(2)连续随访1年;(3)临床资料完整。排除标准:(1)伴随有尘肺、肺部切除术等影响肺功能疾病史的患者;(2)伴随有支气管扩张、支气管炎的患者;(3)伴随有恶性肿瘤疾病的患者。
1.3 方法 通过电子病历收集患者的临床资料,包括年龄、性别、住院时长、病程、身体质量指数(Body mass index, BMI)、上1年急性加重次数、吸烟指数、糖尿病、高血压、低蛋白血症、心功能不全、改良版英国医学研究委员会呼吸问卷(Modified version of British medical reseach council respiratory question-naire, mMRC)分级[2]、慢性阻塞性肺疾病自我评估测试评分(COPD assessment test, CAT)[3]、慢性阻塞性肺病全球倡议组织(Global initiative for chronic obstructive lung disease, GOLD)分级[4]、是否长期家庭氧疗(Long-term oxygen therapy, LTOT)、是否使用抗生素。(1)血压测量结果:用标准计量的台式水银柱血压计(山东喜翠商贸有限公司)测定收缩压(Systolic blood pressure, SBP)、舒张压(Diastolic blood pressure, DBP)。(2)呼吸道病原学检查结果:清洁口腔后,漱口3次,留取患者第2口深部痰,置于无菌痰盒中30min内送检,连续痰检3d。用autoSCAN-4微生物自动分析仪进行病原菌分析鉴定,根据美国临床实验室标准化委员会制定的标准进行结果判定。(3)实验室检查结果:出院前最后1次的血常规、生化全套结果。收集空腹静脉血3~4mL,检测包括NT-proBNP、D-D、PCT、血小板(Platelet, PLT)、谷丙转氨酶(Alanine aminotransferase, ALT)、谷草转氨酶(Aspartate aminotransferase, AST)、血红蛋白(Hemoglobin, Hb)、红细胞(Red blood cell, RBC)、白细胞(White blood cell, WBC)。采用贝克曼AU5800测定HbA1c,试剂盒未贝克曼试剂原装。采用全自动荧光免疫分析仪(安图A2000plus)检测NT-proBNP,采用沃芬Top700检测D-D,采用广州万孚检测PCT。全自动生化仪(迈瑞6800plus7)测定生化相关指标。全自动血细胞分析仪(XT1800i)测定血常规相关指标。(4)心脏彩超检查结果:应用美国GE公司的Vivid7超声仪行心脏彩超检查,测定射血分数(Ejection fraction, EF)、肺动脉压力、左心室增大、右心室增大、肺动脉增宽。

2 结果
2.1 基本情况 两组患者年龄、住院时长、BMI、上1年急性加重次数、mMRC分级、嗜麦芽窄食单胞菌检出、鲍曼不动杆菌检出、铜绿假单胞菌检出、肺炎克雷伯菌检出、肺炎链球菌检出、热带假丝酵母菌检出、LTOT以及抗生素使用情况的差异显著(P<0.05)。两组患者性别、病程、吸烟指数、糖尿病、高血压、低蛋白血症、心功能不全、SBP、DBP、CAT评分以及GOLD分级均无显著差异(P>0.05),见表1。

表1 两组患者临床资料比较
2.2 实验室检查结果 与存活组相比,死亡组患者NT-proBNP、D-D以及PCT的水平均更高(P<0.05)。两组患者PLT、ALT、AST、Hb、RBC以及WBC的水平均无显著差异(P>0.05),见表2。
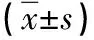
表2 两组患者实验室检查结果比较
2.3 心脏彩超检查结果 两组患者肺动脉压以及右心室增大的差异显著(P<0.05)。两组患者的EF、左心室增大以及肺动脉增宽均无显著差异(P>0.05),见表3。

表3 两组患者心脏彩超检查结果比较[n(%)]
2.4 多因素Logistic回归分析影响患者出院后1年内死亡的危险因素 以表1和2中两组差异具有统计学意义的指标为自变量,以患者出院后1年内死亡为因变量,多因素Logistic回归分析,结果显示,上1年急性加重≥2次、mMRC>2级、铜绿假单胞菌、无LTOT、NT-proBNP>1.1g/L、D-D>2.4mg/L、PCT>0.09g/L以及右心室增大,均为AECOPD患者出院后1年内死亡的独立危险因素(P<0.05),见图1。
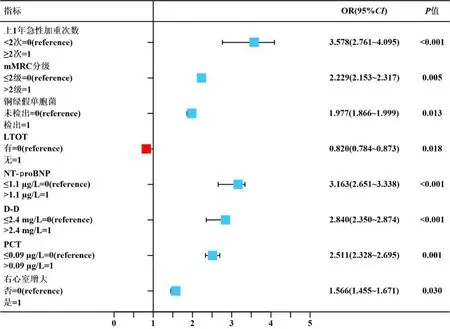
图1 影响AECOPD患者出院后1年内死亡的多因素Logistic回归分析森林图
2.5 NT-proBNP、D-D及PCT对AECOPD患者出院后1年内预后的预测价值 ROC曲线分析表明:NT-proBNP、D-D和PCT曲线AUC分别为0.817、0.805和0.789,具有较高诊断价值,且三者联合预测时AUC为0.830(P<0.001),表明联合诊断价值较三者更高,见表4和图2。
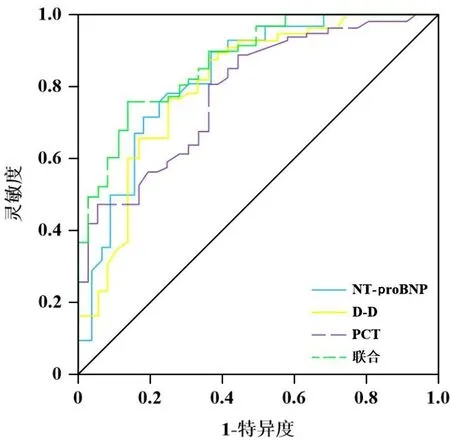
图2 各指标预测患者出院后1年内预后的ROC曲线
表4 患者氧化应激各指标的预测价值
2.6 建立患者出院后1年内死亡的风险评分模型 选取多因素Logistic分析中P<0.05的指标来构建出院后1年内死亡的风险评分模型,见图3,依据β值予以加权赋分:最终分值越高,则死亡风险越高。其中上1年急性加重≥2次赋予77分、mMRC>2级赋予48分、铜绿假单胞菌赋予41分、无LTOT赋予12分、NT-proBNP>1.1g/L赋予69分、D-D>2.4mg/L赋予63分、PCT>0.09g/L赋予55分以及右心室增大赋予27分。采用X-tile软件获取评分截断值,并将患者分为低(≤77分)、中(>77分且≤89分)、高风险(>89分)3组人群。
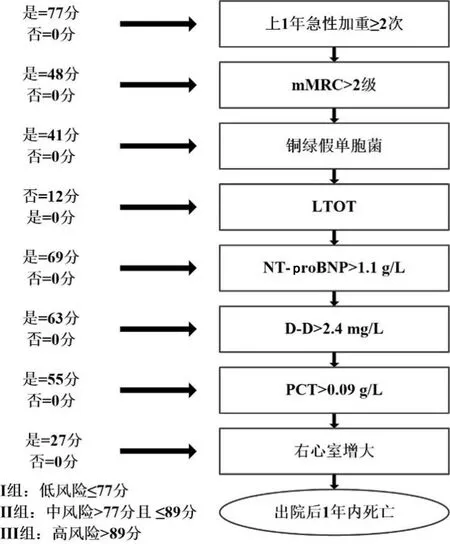
图3 风险评分模型
2.7 模型评价 采用Bootstrap法(原始数据重复抽样1 000次后)对风险评分模型进行内部验证,外部验证通过验证集验证。结果显示:训练集和验证集的C-index分别为0.821(95%CI:0.741~0.891)、0.805(95%CI: 0.721~0.884);两集的校正曲线均与理想曲线拟合良好,见图4。两集ROC的AUC分别为0.812(95%CI: 0.732~0.891)、0.806(95%CI: 0.734~0.887),见图5。风险评分模型的临床决策曲线显示阈值概率在1%~94%时,净获益率>0,见图6。
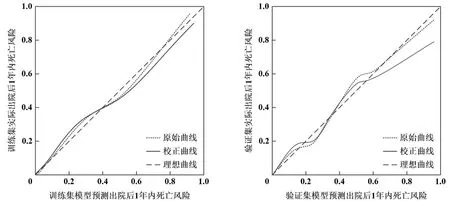
图4 模型的校正曲线验证图
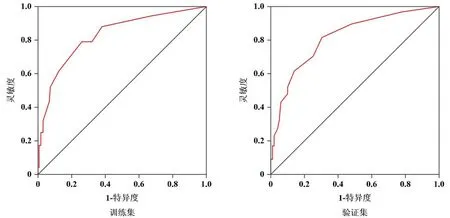
图5 模型的ROC曲线验证图
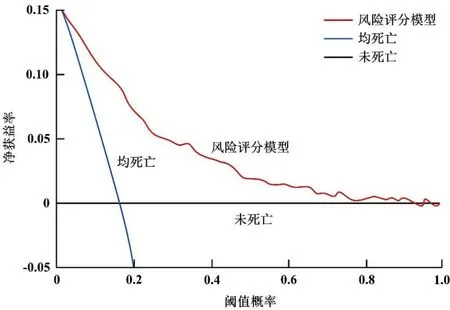
图6 模型的临床决策曲线
3 讨论
急性加重是COPD进展的重要阶段,导致患者额外治疗(例如住院)的呼吸道症状严重恶化,与患者肺功能下降、生活质量恶化和死亡率增加相关。因此,在临床上分析导致AECOPD患者死亡的危险因素,及时进行干预治疗,对改善患者预后、降低死亡率、提高生活质量至关重要。目前,临床上尚缺乏敏感度和特异度高的实验室指标对AECOPD患者的预后进行有效评价。已有学者研究提出,反映炎症感染反应的实验室指标NT-proBNP、超敏C反应蛋白、D-D、PCT等广泛用于临床[5],但关于三者联合检测在重症AECOPD患者预后预测中的价值研究涉猎较少,本研究拟探讨三者联合检测评估患者病情,以求寻找敏感指标早期诊断及监控重症AECOPD病情发展来指导治疗及改善患者预后。
AECOPD患者生活质量下降,频繁发作且多次住院,最终导致患者死亡。目前,相关学者分析AECOPD患者死亡原因,以期分析患者预后的影响因素,对患者实施早期干预及治疗。本研究结果显示,死亡组患者的血清NT-proBNP、D-D、PCT水平较存活组均显著上升。多因素Logistic回归分析结果显示,上1年急性加重≥2次、mMRC>2级、铜绿假单胞菌、无LTOT、NT-proBNP>1.1g/L、D-D>2.4mg/L、PCT>0.09g/L以及右心室增大,均为AECOPD患者出院后1年内死亡的独立危险因素。(1)重症AECOPD是患者不良预后的独立危险因素,死亡率与加重频率正相关。研究表明[6],与随访第1年相比,前1年的加重次数对于患者预后的预测价值更高。(2)mMRC分级是评估运动耐量的常用工具,准确度较高,可反映患者的呼吸困难程度。相关研究表明[7],呼吸困难与COPD病情恶化以及死亡率具有相关性,是预测患者死亡风险的独立危险因素。(3)细菌反复感染与COPD患者病情恶化以及预后不良有关,铜绿假单胞菌易造成患者严重感染。一项回顾性研究结果表明[8],与未检出铜绿假单胞菌的AECOPD患者相比,检出者30d再入院概率更高。另一项前瞻性研究表明[9],铜绿假单胞菌感染不仅会加重患者病情,其还与高死亡率有关。(4)LTOT是姑息治疗终末期COPD患者的重要组成部分。(5)脑钠肽是一种心脏神经激素,由心脏分泌并释放入血,NT-proBNP的半衰期长、含量高,且其表达水平不易受其他因素影响,是一项重要的心衰标志物,16%~60%的AECOPD患者血清NT-proBNP表达水平均有所上升[10](6)D-D是有效反映血栓形成及预后、血液高凝状态的特异性标志物。重症AECOPD患者因高碳酸血症、低氧血症及感染等因素可导致红细胞过度增多及血管内皮损伤,最终导致D-D水平显著上升。(7)正常情况下,血清PCT表达水平极低,当机体出现细菌感染时,其大量释放入血,血清PCT水平显著上升。(8)右心室增大是诊断COPD患者是否合并肺源性心脏病的指标之一,在临床上,两者具有相关性。三者联合预测时AUC为0.830(95%CI:0.801~0.859,P<0.001),灵敏度为95.15%,特异度为74.28%,表明联合预测价值较高。风险评分模型将患者分为低(≤77分)、中(>77分且≤89分)、高风险(>89分)3组人群。模型评价提示风险评分模型准确度高。
综上所述,上1年急性加重≥2次、mMRC>2级、铜绿假单胞菌、无LTOT、NT-proBNP>1.1g/L、D-D>2.4mg/L、PCT>0.09g/L以及右心室增大,均为AECOPD患者出院后1年内死亡的独立危险因素。NT-proBNP、D-D及PCT三者联合检测AECOPD患者出院后1年内预后情况具有的较高预测价值,临床上医生应该充分重视,严密监测三者水平的变化,采取积极的治疗措施,降低重症AECOPD患者的死亡风险。

