基于文献计量学的我国医院GCP中心相关研究可视化分析
袁汝奎,王明利,周安琴,陈美娟
(1.西南医科大学药学院,四川 泸州 646000;2.西南医科大学附属中医医院临床试验研究中心,四川 泸州 646000;3.西南医科大学附属中医医院临床药学,四川 泸州 646000)
临床试验机构(临床试验研究中心,GCP中心)是指具备相应条件,按照相应法规(《药物临床试验质量管理规范》《医疗器械临床试验质量管理规范》等)和临床试验相关技术指导原则等要求,开展药物、医疗器械、体外诊断试剂、特殊医用途配方食品临床试验的机构[1-2]。GCP中心在评估新药和治疗方案的安全性和有效性、推动医学科学的进步、优化临床实践和医疗决策、保护患者权益和安全以及促进跨学科合作和知识共享等方面具有重要性。GCP中心在医学研究和临床实践中发挥着不可替代的作用,为提高患者的生活质量和改善医疗水平做出了重要贡献[3-4]。
CiteSpace[5]是一种基于文献引用网络分析的可视化工具,用于探索学术研究领域的知识结构和发展趋势。它可以帮助研究人员发现关键的研究主题、研究热点、学术合作网络以及研究领域的演化过程。本文通过NoteExpress、CiteSpace 6.2.R1两个软件,整理归纳近20年来与GCP中心有关的文献,通过分析文献引用关系构建作者机构和关键词等网络图,旨在了解我国目前GCP中心研究现状、研究热点和未来发展趋势,为进一步开展GCP中心领域相关研究提供参考。
1 资料与方法
1.1 数据来源用计算机检索中国知网、万方数据库、维普网,检索条件如下:中国知网、万方数据库主题字段为“临床试验研究中心”或“GCP中心”;VIP数据库题名或关键词字段为“临床试验研究中心”或“GCP中心”;检索文献需为文献全文,检索时间段设置为2003年1月1日至2022年12月31日。
1.2 纳入与排除标准本研究纳入标准为临床试验研究中心相关的研究文献。本研究排除标准包括:①与主题不相关的文献;②重复发表的文献;③信息不完整的文献。
1.3 文献分析方法将获取的文献以NoteExpress软件格式导出,使用NoteExpress软件对文献进行排出整理,再以Refworks-CiteSpace格式导出,导入CiteSpace 6.2.R1软件。通过CiteSpace,研究人员可以进行一系列的分析,如共词分析、聚类分析、时间轴分析等,以深入了解领域内的研究动态和趋势。这些分析结果可以帮助研究人员发现新的研究方向、寻找合作伙伴、评估研究成果的影响力,并为科学决策提供支持[6]。
2 结果与分析
2.1 文献现状分析通过年度发文量可以了解GCP中心研究热度的变化。对文献进行年度发文量分析,结果如图1所示。基于药物、器械和特医食品等临床试验的重要性,GCP中心相关研究一直都备受关注。2003年已有53篇文献发表。近20年来与GCP中心相关文献的发文量更是逐年上升,2006年至2012年期间发文量相对平稳,自2013年开始发文量增长迅速,2013年至2022年平均发文量达300余篇。
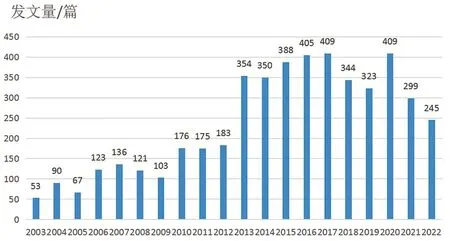
图1 近20年GCP中心相关文献年度发文量分布
2.2 期刊来源分析对文献期刊来源进行统计,选取发文量排名前20位的期刊进行分析,结果显示,有14本期刊是收录于北大中文核心目录,有5本期刊是收录于中国科技核心目录。文章收录前三的杂志分别为《中国新药杂志》(111篇)、《中国组织工程研究》(93篇)、《中国临床药理学杂志》(87篇)。关于GCP中心研究总体论文质量都很高,由此可知人们对GCP中心研究工作的重视性。
2.3 作者合作网络分析CiteSpace作者合作网络分析可以帮助研究人员了解学术界中的合作关系和团队合作的模式。通过分析作者之间的合作关系,可以揭示研究领域中的学术合作网络结构、合作伙伴的重要性以及合作的影响力。结果见图2、表1。由图表可知,作者网络分析有966个节点、2 539条连线,网络密度为0.005 4。依据普赖斯定律[7]对核心作者进行计算,若设该领域内发文量最多作者的论文数为Nmax,则在该领域发表[X](X =0.749 Nmax1/2)以上论文的作者被认为是领域内的核心作者。GCP中心相关研究发文量最高的学者是胡思源(40篇),即Nmax=40,则X=6.32,即认为发文量在7篇及以上的作者是该领域的核心作者。经统计,核心作者228位,发文量2 374篇,占总数的11.04%。发文量排名前三位的作者为胡思源(40篇)、李可欣(30篇)、李静(29篇)。由图2可以了解到,作者之间合作相对紧密,形成了胡思源-李新民-丁樱、李可欣-胡欣-赵紫楠、李静-黄慧瑶-吴大维、梁茂植-南峰-余勤等多个核心研究团队。
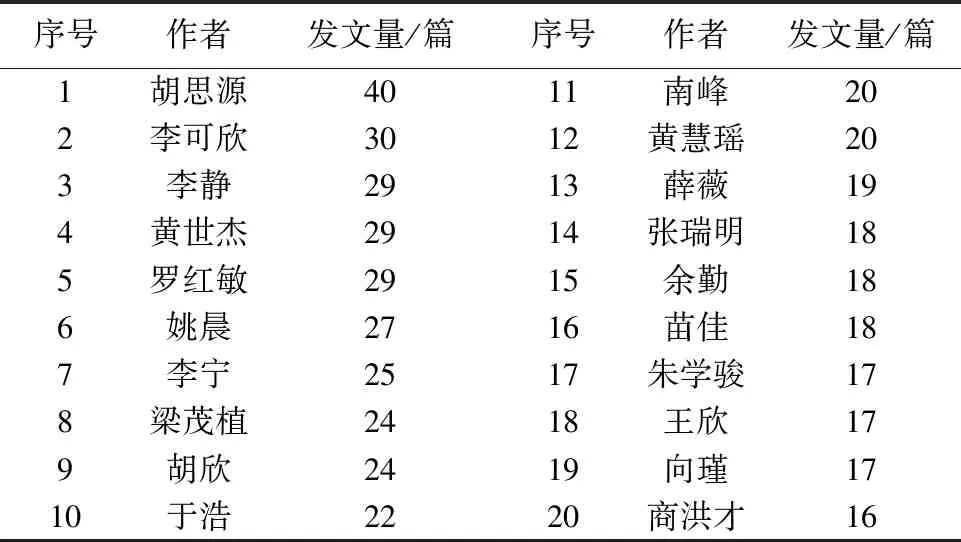
表1 GCP中心相关研究发文量排名前20位的作者
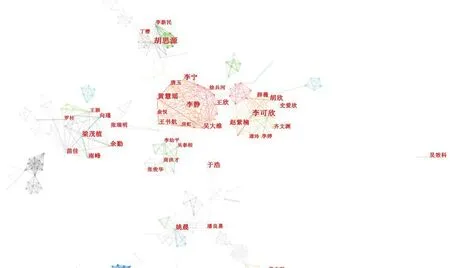
图2 GCP中心相关研究作者合作网络分析图
2.4 机构合作分析利用CiteSpace软件,对文献发文机构进行统计分析,提供一种全面的视角来理解学术界中的机构间合作关系和合作模式,为研究人员提供了有价值的信息,以促进学术合作和科学研究的发展,结果见图3。为保证临床试验得到的数据科学、真实、可靠,多中心研究是必要的研究方法。它可以扩大样本规模、提高研究的代表性、增加研究结果的可信度和效度,加强资源共享和经验交流,并提供多维度的数据分析和解释。多中心研究的应用有助于推动临床研究的发展,促进临床实践的优化和新药的研发。由图3可知,研究机构间具有明显的合作关系,机构间合作联系相对紧密。
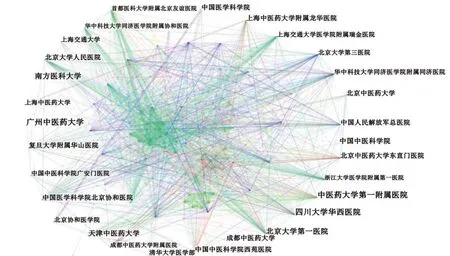
图3 GCP中心相关研究机构合作网络分析图
2.5 关键词共线分析关键词共线分析可以帮助研究人员发现文献中的主题和研究领域的重要方向。通过分析关键词的共现模式,可以识别出频繁共现的关键词组合,从而揭示出研究领域中的主题和研究热点。另外,通过关键词共线分析,可以了解研究领域中的知识结构和关键词之间的关系。通过分析关键词的共现网络,可以揭示出关键词之间的层次结构、关联性和重要性,帮助研究人员理解研究领域的知识体系和发展趋势。用CiteSpace 6.2.R1软件对关键词进行共现分析,结果见图4。其中关键词共现的节点有706个,连线有1 457条。中介中心性指标提供了一种衡量关键词重要性和影响力的方法,帮助研究人员识别关键词的作用、揭示关键词的影响力和认识研究领域的关键词演化过程。中介中心性取值在0~1之间,≥0.1说明其中心性较高。截取文献中排名前20位的高频关键词进行分析,结果见表2。高中介中心性的关键词包括:临床试验(0.68)、临床疗效(0.21)、安全性(0.11)。
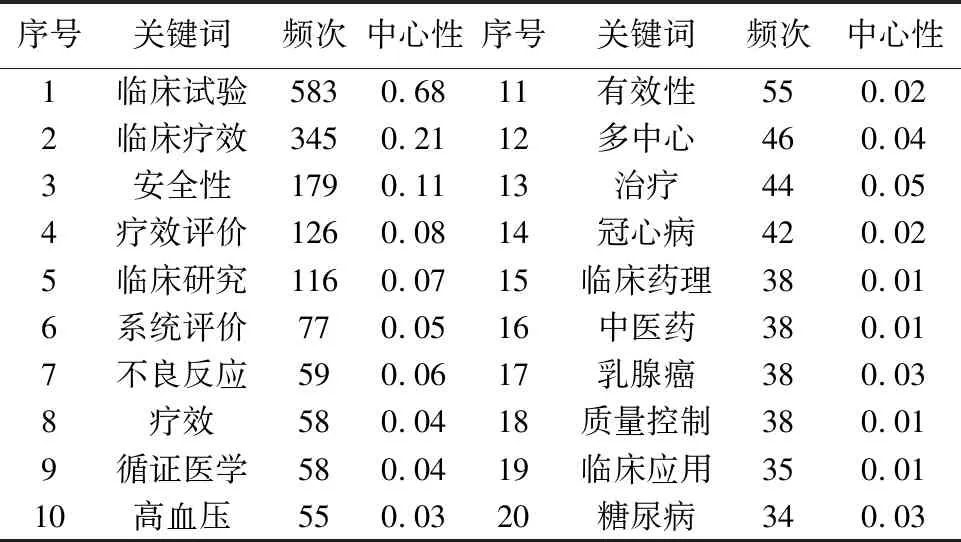
表2 GCP中心相关研究文献关键词共现分析结果
图4 GCP中心相关研究文献关键词共线图谱
2.6 关键词聚类分析关键词聚类分析可以帮助研究人员发现文献中的主题和研究领域的重要方向。通过将相似的关键词聚类在一起,可以识别出具有相似主题的关键词群组,从而揭示出研究领域中的主题和研究热点。用CiteSpace 6.2.R1对关键词进行聚类分析,了解GCP中心相关研究的主要内容。聚类模块值(Q值)>0.3,表明聚类结构显著;平均轮廓值(S值)>0.5,表明结果具有合理性;S值>0.7,表明结果可信,结果见图5。聚类图谱中Q值=0.551 4,S值=0.845 1,表明聚类板块结构显著且结果高效。图5中,#代表聚类。如#0应用聚类为红色,代表该聚类内容是近期GCP中心相关研究的研究热点,主要关键词聚类的代表领域前9位是临床试验、安全性、临床疗效、骨科植入物、治疗、临床研究、肿瘤、糖尿病、双盲法。具体关键词聚类的代表领域及其对应的关键词见表3。

表3 GCP中心相关文献关键词聚类前5位标签情况
2.7 关键词突现分析通过分析关键词的出现频率和突出程度,可以确定关键词在文献中的重要程度,从而帮助研究人员关注和理解研究领域的核心概念和关键问题。突现图谱中,“Strength”数值越大表明影响力越大。用CiteSpace 6.2.R1对关键词进行突现分析,结果见图6。

图6 GCP中心相关研究文献关键词突现分析图谱
由图6可知,近20年GCP中心的研究热点主要分3个阶段。第一阶段从2003年到2013年,该阶段主要以“循证医学”“双盲法”“临床试验”等关键词为研究热点。循证医学[8-9]是基于最新的临床研究证据,结合医生的临床经验和患者的价值观,制定最佳的医疗决策。GCP中心积极推广和应用循证医学的原则和方法,以确保临床试验设计的科学性和可靠性。双盲法[10]是临床试验中常用的控制偏倚的方法之一,旨在减少主观偏见的影响。GCP中心在临床试验中严格实施双盲法,即将试验参与者和研究人员分为接受治疗和接受安慰剂(对照组)的两组,双方不知道自己属于哪一组,以减少偏见对结果的影响。第二阶段从2006年到2018年,此阶段是GCP中心发展的快速期,研究热点呈现多元性。GCP中心在质量管理、技术应用、伦理要求和国际合作等方面取得了显著的发展。第三阶段从2018年到2022年,GCP中心开始注重质量管理、风险管理、伦理审查,2020年发布的《药品临床试验质量管理规范》[11]和《医疗器械临床试验质量管理规范》[12]等文件,旨在加强对临床试验的监管,并提高试验质量和安全性。
3 讨论
3.1 CiteSpace可视化分析CiteSpace可视化分析作为一种学术文献分析工具,为研究人员提供了一种全局的视角,帮助他们揭示学术领域的发展趋势、知识结构和研究热点。通过可视化地图、时间轴、演化路径和聚类分析,CiteSpace帮助研究人员理解学术领域的动态变化、核心概念和关键问题,促进学术交流和跨学科研究。CiteSpace可视化分析的综合作用在学术研究中具有重要的应用前景,将为研究人员提供新的思路和方法,推动学术领域的进一步发展[13]。本文结合CiteSpace可视化分析工具,能够更好地了解GCP中心研究领域的发展趋势、知识结构和研究热点,发现合作机会,评估研究结果的传播和影响力。这将有助于提升GCP中心的研究水平和影响力,推动临床试验研究的发展。
3.2 多中心研究作者合作网络分析结果核心作者间存在团队合作,机构合作分析也表明研究机构间合作联系相对紧密,可见多中心研究的应用有助于推动临床研究的发展,促进临床实践的优化和新药的研发。首先,多中心研究可以在不同地区、不同医疗机构之间进行,涵盖更广泛的受试者群体和临床实践背景。这样可以提高研究的代表性,结果更具普遍性和推广价值。其次,多中心研究可以招募更多的研究对象,扩大样本容量。这可以提高研究的统计学能力和可靠性,减少由于样本量不足导致的偏差。另外,通过多中心研究,可以同时在多个研究中心进行数据收集和分析,有效地减少研究时间和成本。同时,多中心研究还能够充分利用各个研究中心的研究设施和人力资源,提高研究的效率和质量。最后,由于不同地区和研究中心的人口特点和医疗条件不同,多中心研究可以帮助探索不同人群的反应差异。这对于了解药物的安全性、疗效和适应证范围等方面具有重要意义。因此,研究机构间具有明显的合作关系,机构间合作联系相对紧密[14-16]。
3.3 伦理性和合规性关键词共线分析显示高中介中心性的关键词包括:临床试验、临床疗效、安全性;关键词聚类分析表明代表领域前9位的是临床试验、安全性、临床疗效、骨科植入物、治疗、临床研究、肿瘤、糖尿病、双盲法;关键词突现分析显示研究热点主要分3个阶段:第一阶段以“循证医学”“双盲法”“临床试验”等关键词为研究热点;第二阶段是GCP中心发展的快速期,研究热点呈现多元性;第三阶段开始注重质量管理、风险管理、伦理审查。由此可见,随着对伦理学和合规性的关注不断增加,临床试验研究机构在近几年也加强了相关的监管和合规措施。研究机构更加重视保护受试者的权益和安全,确保研究过程符合伦理标准和法规要求。这种关注有助于提高研究的可信度和可持续发展。研究伦理要求GCP中心确保受试者的权益得到充分保护。这包括在试验开始前获得受试者的知情同意,确保试验过程中的风险和利益得到充分解释,以及确保受试者的隐私和数据安全得到保护。研究中心需要建立伦理委员会或伦理审查机构,审查和监督研究计划,以确保其符合伦理标准和法规要求[17-19]。
GCP中心需要遵守相关的法律、法规和行业准则。这包括国家、地区和国际上的伦理和法律要求,例如国际伦理指南、人体试验法规、数据保护法规等。GCP中心需要确保其研究过程和数据收集符合这些要求,并配备专业的合规人员来监督和管理合规事务[20]。
3.4 GCP中心的技术革新GCP中心在技术方面的革新对于提高研究效率、数据质量和研究结果的可靠性具有重要意义。电子数据捕获系统、远程数据采集和监测技术、生物标志物和分子诊断技术、人工智能和机器学习、虚拟试验和模拟技术等都是当前GCP中心关注和应用的技术创新领域。这些技术的应用有助于推动临床试验研究的发展,促进医学进步和患者获益[21-23]。
传统的纸质数据收集方式存在着数据录入错误、数据丢失和数据整理困难等问题。电子数据捕获系统通过电子化数据收集和管理,可以提高数据收集的准确性和效率。研究人员可以直接在电子系统中输入和管理数据,减少了人工录入错误的可能性,并且可以更方便地进行数据清理、整理和分析[24]。
随着科技的进步,越来越多的GCP中心采用远程数据采集和监测技术。这些技术包括远程医学图像、传感器技术、移动应用程序等,可以实时监测受试者的生理指标、症状和治疗反应。远程数据采集和监测技术提供了更精确、连续和客观的数据,减少了人为干预和主观评估的影响[23-24]。
4 结语
本文利用CiteSpace分析软件可视化地呈现了近20年我国GCP中心的整体动态、发展趋势及相关研究热点。结果显示,GCP中心研究机制越来越完善,研究工作越来越智能化、信息化。这对于推动医学科学的发展和改善患者的生活质量具有重要意义。通过不断的技术革新和创新方法的应用,GCP中心能够更准确地评估新药、治疗方案和诊断方法的有效性和安全性。同时,我们也必须认识到GCP中心所面临的挑战。研究过程中需要严格遵守伦理原则和法规要求,确保研究的安全性和可靠性。研究结果的传播和应用也需要与临床实践和决策制定密切结合,以实现科学研究和临床实践的有效衔接。

