HPLC多指标成分联合PCA、OPLS-DA及灰色关联度法的宫瘤消胶囊综合质量评价*
张希冉,贡磊磊,李轶凡,秦春雨,王志军
(1.首都医科大学附属北京妇产医院/北京妇幼保健院,北京 100026;2.河北中医学院药学院,河北 石家庄 050200)
宫瘤消胶囊(GLX)由党参、白花蛇舌草、牡丹皮、香附和莪术等中药经渗漉等加工工艺制备而成,现行标准为国家食品药品监督管理局国家药品标准WS-11329(ZD-1329)-2002-2011Z[1]。GLX具有活血化瘀、软坚散结之功效,用于子宫肌瘤属气滞血瘀证,证见:月经量多,夹有大小血块,经期延长,或有腹痛,舌暗红,或边有紫点、瘀斑,脉细弦或细涩。目前质量标准及相关文献[2-3]仅以单一成分为定量指标,不能满足中药现代化发展的需要,更不能保证产品质量及临床疗效。化学计量学[4-5]方法可通过对多成分的定量测定结果进行提取和降维,挖掘复杂数据间存在的内在关联关系,找出对质量控制具有显著贡献的主要成分。灰色关联度分析(GRA)法[6]基于灰色系统的灰色过程,根据各因素数列曲线形状相似程度进行发展态势分析,对各指标的综合评判值进行直观地表达,避免了用多个指标对其综合评判值的人为判断。本实验采用HPLC法同时检测GLX中党参炔苷、紫丁香苷、鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、圆柚酮、α-香附酮、莪术二酮和莪术醇的含量,运用化学计量学和GRA法对多组分定量检测数据进行分析挖掘,并通过SPSS 26.0和SIMCA 14.1统计学软件对其进行综合质量评价,以期为GLX的整体质量控制提供实验数据。
1 仪器与试药
丹皮酚(批号:110708-201908,含量以99.8%计)、莪术醇(批号:100185-201908,含量以99.9%计)、α-香附酮(批号:110748-202117,含量以99.8%计)、莪术二酮(批号:111800-202203,含量以99.8%计)、芍药苷(批号:110736-202246,含量以96.7%计)和紫丁香苷(批号:111574-202106,含量以94.3%计)由中国食品药品检定研究院提供;氧化芍药苷(批号:14062505,含量以99.9%计)、鸡矢藤次苷甲酯(批号:PRF8091244,含量以99.6%计)和车叶草苷酸(批号PRF8050928,含量以98.2%计)由成都普瑞法科技开发有限公司提供;党参炔苷(批号:CFS202201,含量以98.5%计)、车叶草苷(批号:CFS202102,含量以98.2%计)、香附烯酮(批号:CFS202101,含量以98.5%计)和圆柚酮(批号:CFS202201,含量以98.4%计)由武汉天植生物技术有限公司提供;15批GLX(规格:每粒0.5g,批号:221202,221104,221103,221102,221002,220907,220603,220602,220601,220502,211205,211204,211203,211201,211104,编号分别为S1~S15)来源于山东步长神州制药有限公司;乙腈(色谱级,天津市康科德科技有限公司)、磷酸(色谱级,美国Tedia公司),其余试剂为分析纯。
KQ-300DV型超声波清洗器(广州颖汉科技有限公司);Agilent 1200型HPLC仪(美国安捷伦科技公司);AB104.N型电子天平(上海托利-梅特勒仪器有限公司);色谱柱(规格250 mm×4.6 mm,5 μm,Dikmatech Diamonsil Plus C18柱)。
2 方法与结果
2.1 溶液的制备
2.1.1 混合对照品 精密称取党参炔苷、紫丁香苷、鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、圆柚酮、α-香附酮、莪术二酮和莪术醇对照品各适量,用50%甲醇制成含党参炔苷(0.192 mg/mL)、紫丁香苷(0.036 mg/mL)、鸡矢藤次苷甲酯(0.590 mg/mL)、车叶草苷酸(0.414 mg/mL)、车叶草苷(0.530 mg/mL)、氧化芍药苷(0.318 mg/mL)、芍药苷(0.452 mg/mL)、丹皮酚(0.940 mg/mL)、香附烯酮(0.374 mg/mL、)圆柚酮(0.042 mg/mL)、α-香附酮(0.176 mg/mL)、莪术二酮(0.252 mg/mL)和莪术醇(0.118 mg/mL)的混合母液。精密量取混合母液,用50%甲醇稀释20倍,即得。
2.1.2 供试品 取10粒GLX内容物,混匀,研细,取细粉约1.0 g,精密称定,经50%甲醇超声提取30 min,放冷,定容至25 mL,摇匀,过滤,取续滤液,备HPLC检测用。取按质量标准分别制备的缺党参、缺白花蛇舌草、缺牡丹皮、缺香附和缺莪术的阴性对照品,再依上法制成5个阴性对照品溶液,备HPLC检测用。
2.2 色谱条件及专属性试验 采用Dikmatech Diamonsil Plus C18色谱柱,流动相乙腈(A)-0.1%磷酸[7-10]梯度洗脱(0~9 min,17.0%A;9 ~17 min,17.0%→30.0%A;17 ~31 min,30.0%→33.0%A;31 ~45 min,33.0%→55.0%A;45 ~59 min,55.0%→65.0%A;59 ~71 min,65.0%→75.0%A;71 ~75 min,75.0%→17.0%A);检测波长为254 nm[11-13](0~27 min,党参炔苷和紫丁香苷)、235 nm[14-20](27~38 min,鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、圆柚酮和α-香附酮)和214 nm[21-22](38~65 min,莪术二酮和莪术醇);柱温:30 ℃,流速:1.0 mL/min,进样量:10 μL。混合对照品、供试品溶液色谱图见图1。结果GLX供试品中党参炔苷、紫丁香苷、鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、圆柚酮、α-香附酮、莪术二酮和莪术醇色谱峰的保留时间与对照品一致,且峰形尖锐,无杂质峰干扰。

图1 混合对照品(A)、GLX(B)、党参阴性对照品(C)、白花蛇舌草阴性对照品(D)、牡丹皮阴性对照品(E)、香附阴性对照品(F)和莪术阴性对照品(G)色谱图
2.3 方法学考察
2.3.1 线性关系考察用50%甲醇将上述对照品母液稀释4、10、20、40、100和200倍,摇匀,依法检测党参炔苷、紫丁香苷、鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、圆柚酮、α-香附酮、莪术二酮和莪术醇色谱峰,以峰面积(Y)对质量浓度(X)进行回归处理,结果见表1。

表1 GLX 中13 种成分回归处理结果
2.3.2 精密度、稳定性及重复性试验 在“2.2”项色谱条件下,重复进样同一份GLX(S1)供试品溶液6次,计算各成分峰面积的RSD值,结果党参炔苷、紫丁香苷、鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、圆柚酮、α-香附酮、莪术二酮和莪术醇峰面积RSD值依次为1.46%、1.83%、0.96%、1.15%、1.05%、1.35%、1.13%、0.73%、1.23%、1.79%、1.52%、1.41%和1.56%。取同一份GLX(S1)供试品溶液(室温存放),于制备后0、2、4、7、12、18、24和36 h进样,测得党参炔苷、紫丁香苷、鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、圆柚酮、α-香附酮、莪术二酮和莪术醇峰面积RSD值依次为1.69%、1.93%、1.37%、1.47%、1.54%、1.74%、1.54%、1.14%、1.35%、1.98%、1.73%、1.80%和1.88%,表明GLX供试品溶液36 h内稳定。取6份编号S1的GLX,各自按“2.1.2”项方法处理成供试品溶液,依法检测,记录峰面积,代入回归方程,用外标法计算党参炔苷、紫丁香苷、鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、圆柚酮、α-香附酮、莪术二酮和莪术醇含量,结果方法重复性良好,含量的RSD值依次为1.72%、1.98%、1.23%、1.48%、1.37%、1.59%、1.42%、1.02%、1.56%、1.92%、1.79%、1.67%和1.82%。
2.3.3 加样回收率试验 取已知13种成分含量编号S1的GLX内容物细粉9份,每份约0.5 g,精密称定,随机均分为3组,每组分别加入0.8、1.0、1.2 mL混合对照品溶液[党参炔苷(0.107 mg/mL)、紫丁香苷(0.019 mg/mL)、鸡矢藤次苷甲酯(0.398 mg/mL)、车叶草苷酸(0.311 mg/mL)、车叶草苷(0.372 mg/mL)、氧化芍药苷(0.229 mg/mL)、芍药苷(0.326 mg/mL)、丹皮酚(0.591 mg/mL)、香附烯酮(0.269 mg/mL)、圆柚酮(0.024 mg/mL)、α-香附酮(0.093mg/mL)、莪术二酮(0.152 mg/mL)和莪术醇(0.069 mg/mL)],按“2.1.2”项方法制得加样供试品溶液,低、中、高3个水平各平行3份,进样检测,得党参炔苷、紫丁香苷、鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、圆柚酮、α-香附酮、莪术二酮和莪术醇平均加样回收率分别为98.31%、96.81%、99.45%、97.89%、99.58%、98.65%、98.17%、100.10%、99.43%、96.91%、97.79%、97.95%和98.48%,RSD值分别为1.49%、1.44%、1.37%、1.46%、0.93%、1.24%、1.29%、0.86%、0.78%、1.48%、1.03%、1.20%和1.15%。
2.4 GLX样品含量检测 取15批GLX(S1~S15)依法制成的GLX供试品溶液,进样,每批样品检测3次,记录党参炔苷、紫丁香苷、鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、圆柚酮、α-香附酮、莪术二酮和莪术醇的峰面积,将13种成分峰面积代入“2.3.1”项回归方程,计算其在样品中的含量,结果见表2。

表2 15 批GLX 中13 种成分含量测定结果 (n=3)
2.5 GLX化学计量学质量评价
2.5.1 主成分分析(PCA) 将15批GLX中党参炔苷、紫丁香苷、鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、圆柚酮、α-香附酮、莪术二酮和莪术醇的含量数据导入SPSS 26.0软件进行PCA,由PCA结果(表3~4)可知,前2个主成分的累积方差贡献率为90.626%,其中主成分1的占比为74.364%。由载荷矩阵可知,主成分1的信息由紫丁香苷、鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、α-香附酮和莪术醇组成,党参炔苷、圆柚酮和莪术二酮对主成分2贡献度显著。为验证PCA的可信度,同时运用SIMCA 14.1软件对表2数据建立PCA模型,同样提取出2个主成分,其中R2X=0.906,表明模型稳定可靠,进一步分析得15批GLX样品PCA得分图(见图2)。由图2可知S1~S6位于得分图左上侧,S7~S10位于得分图左下侧,S11~S15位于得分图右下侧,批次相近的聚在一起。
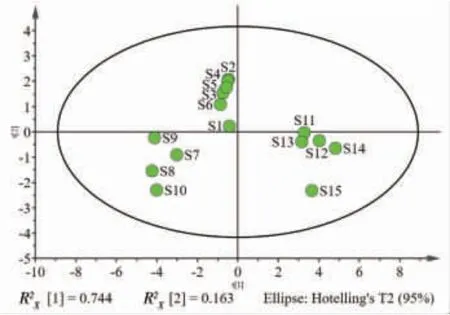
图2 15 批GLX 的PCA 得分图
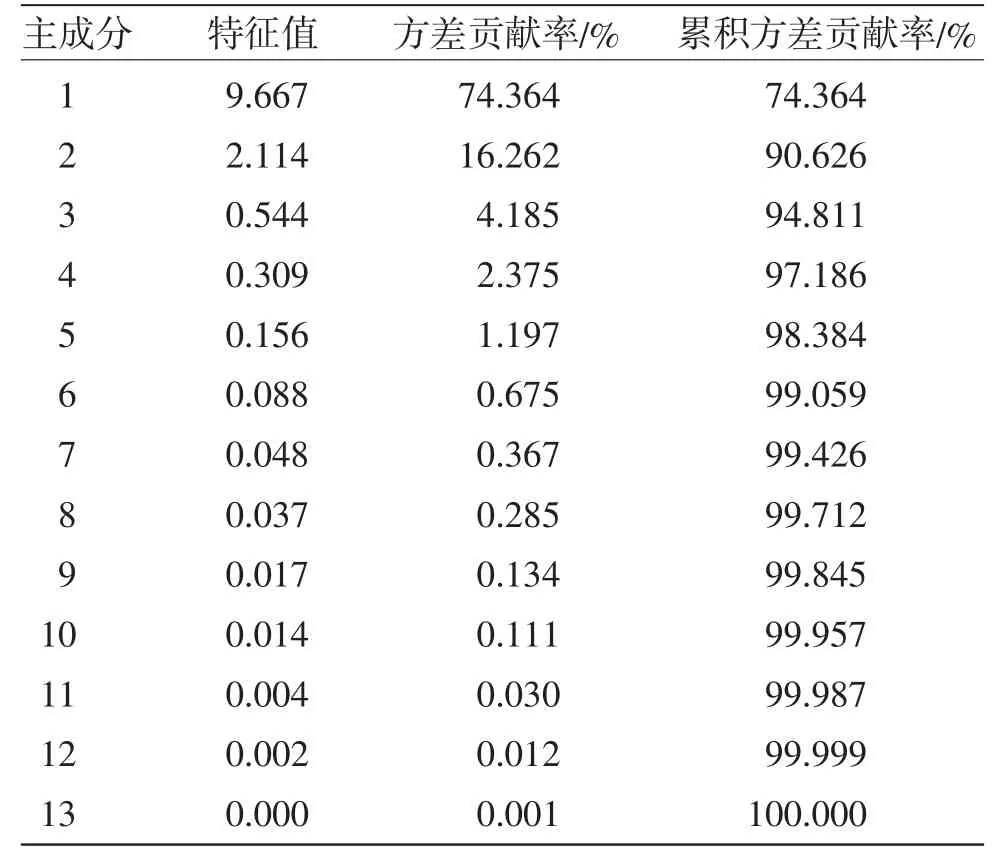
表3 特征值、方差贡献及累积贡献率
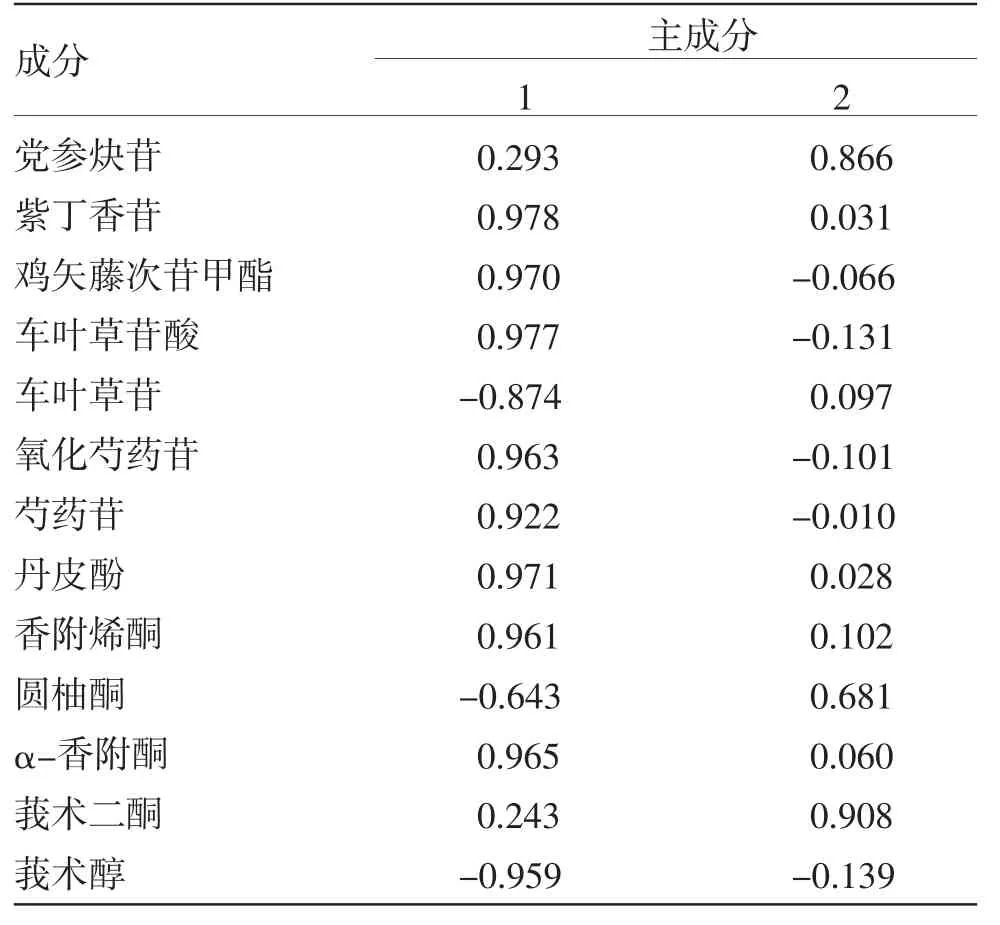
表4 GLX 中13 种成分的载荷矩阵
2.5.2 正交偏最小二乘法-判别分析(OPLS-DA) 为进一步比较GLX样品组间质量,发挖类间关异标记物,将表2数据导入SIMCA 14.1软件进行OPLS-DA,得OPLS-DA模型得分图(见图3),结果模型参数R2X=0.906,R2Y=0.878,Q2=0.776,均大于0.5,表明模型稳定可靠、预测能力良好。对OPLS-DA模型进行200次置换检验,得置换检验图(见图4),结果截距R2=0.072 2,Q2=-0.454,同时各成分散点的R2和Q2值均低于最右侧的R2和Q2值,由此表明OPLS-DA模型未过度拟合。根据模型变量重要性投影(VIP)图(见图5),以VIP>1为筛选标准,VIP值越大,对产品质量差异贡献度越大,结果有8个成分的VIP值>1,VIP值从大到小依次为VIP莪术二酮=1.370 2、VIP香附烯酮=1.313 7、VIP丹皮酚=1.282 8、VIP车叶草苷=1.139 1、VIP党参炔苷=1.119 1、VIP鸡矢藤次苷甲酯=1.110 5、VIP芍药苷=1.014 9、VIP氧化芍药苷=1.014 4,其次成分4(车叶草苷酸)的VIP=0.995 7,接近1,对GLX质量也有一定的影响。故这9个成分可作为影响GLX产品质量的差异标志物。
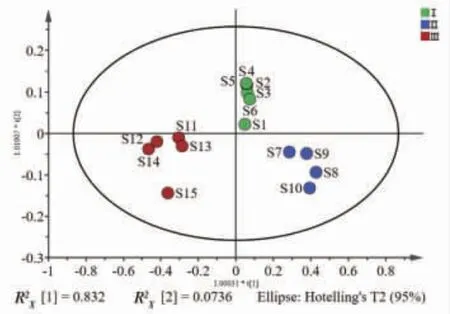
图3 15 批GLX 样品OPLS-DA 模型得分图
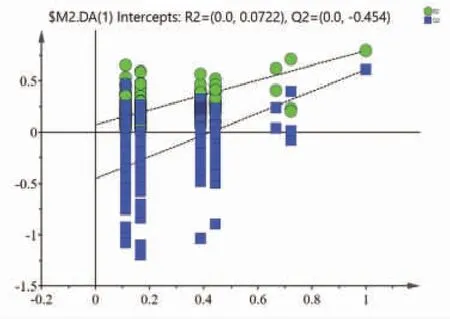
图4 OPLS-DA 置换检测结果图

图5 13 个测定指标的VIP 图
2.6 GRA
2.6.1 原始数据矩阵规格化 参考文献[23]采用均值变换法对表2中15批GLX中党参炔苷、紫丁香苷、鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、圆柚酮、α-香附酮、莪术二酮和莪术醇的含量数据规格化处理,处理后数据见表5。
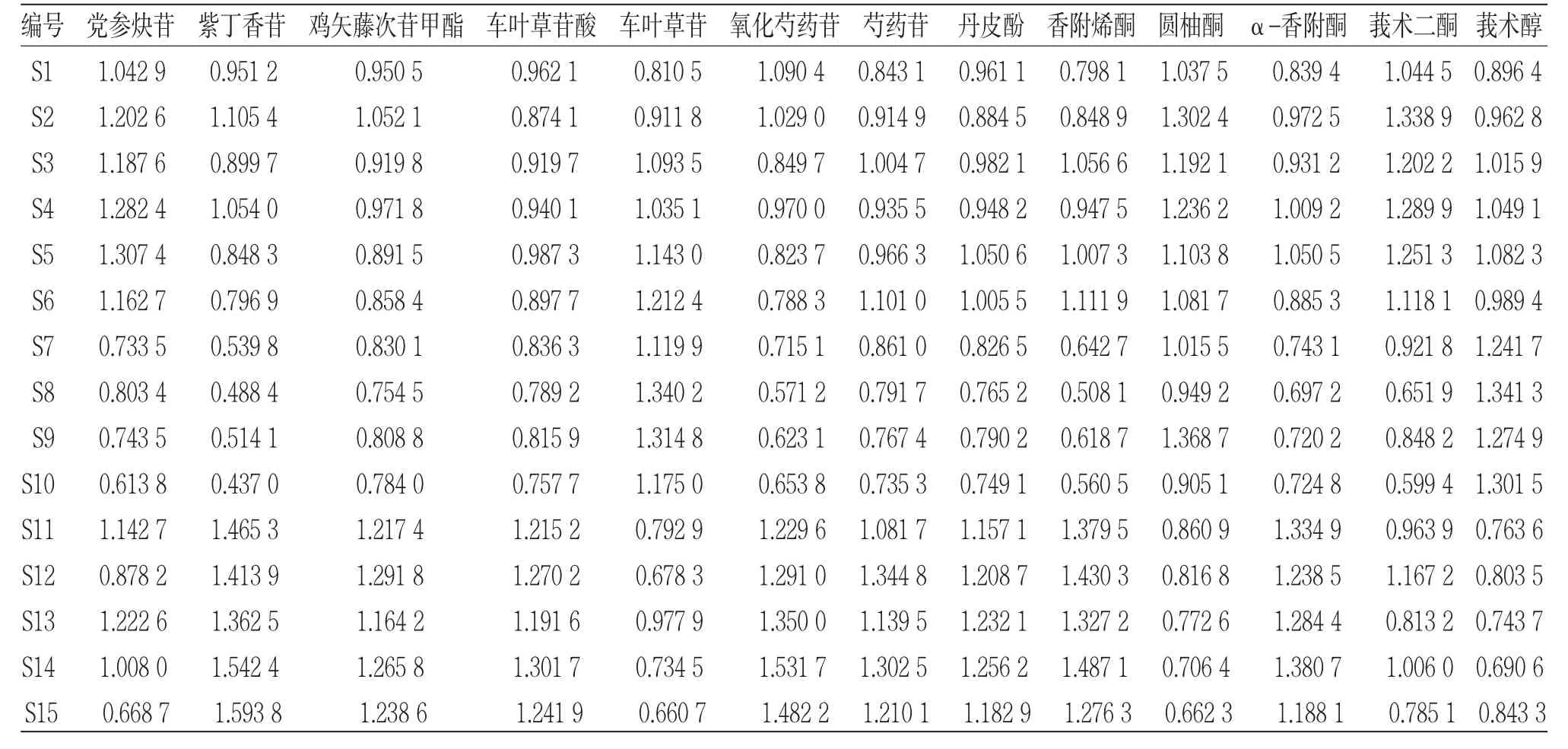
表5 GLX 中13 种成分含量数据规格化处理结果
2.6.2 计算关联系数 以表5中每一成分的最大值为最优参考序列,最小值为最差参考序列,结果最优参考序列为1.307 4、1.593 8、1.291 8、1.301 7、1.340 2、1.531 7、1.344 8、1.256 2、1.487 1、1.368 7、1.380 7、1.338 9和1.341 3,最差参考序列为0.613 8、0.437 0、0.754 5、0.757 7、0.660 7、0.571 2、0.735 3、0.749 1、0.5081、0.662 3、0.697 2、0.599 4和0.690 6。按文献[23]参考序列关联系数计算公式分别计算各成分与最优参考序列的关联系数(见表6)以及与最差参考序列的关联系数(见表7)。
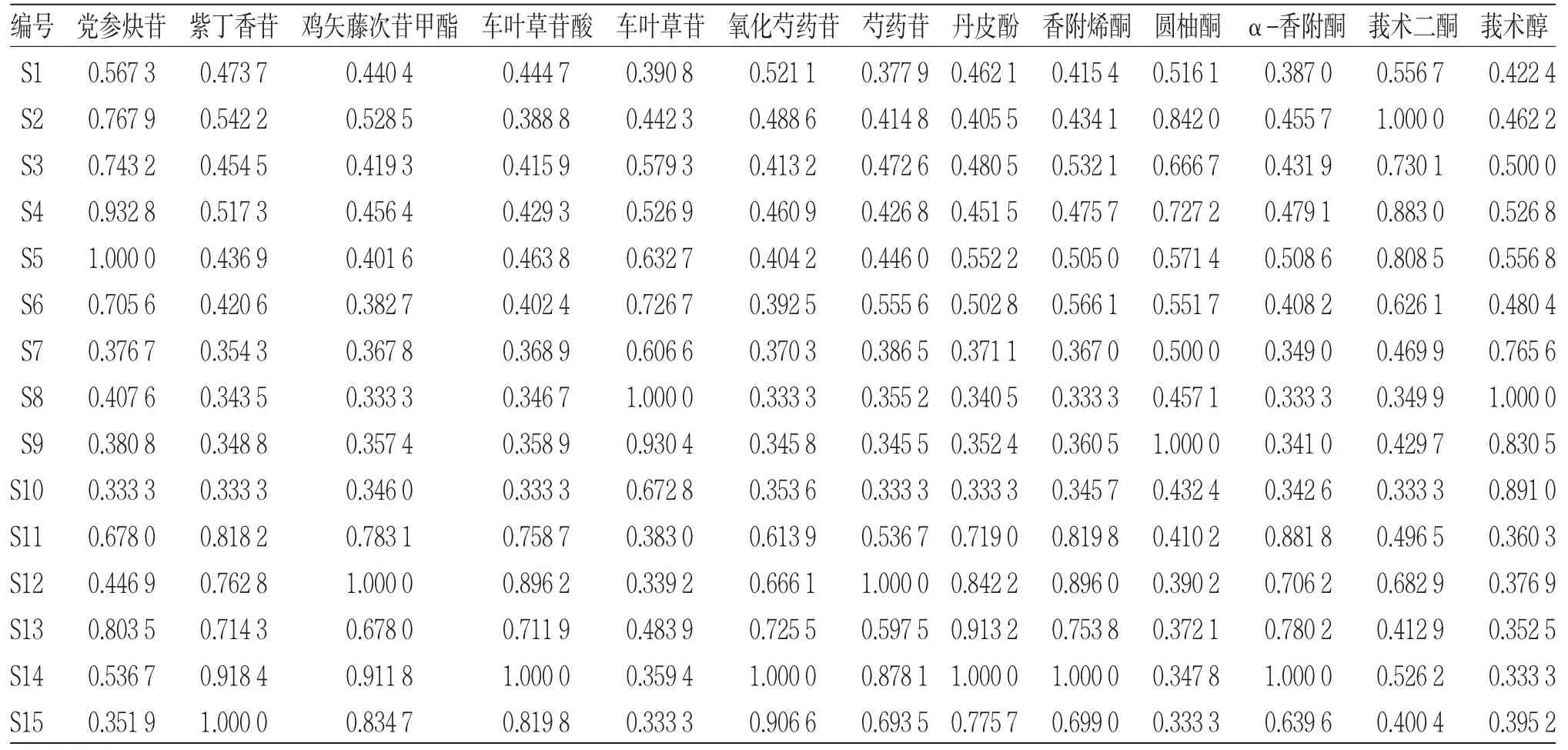
表6 各评价单元与最优参考序列的关联系数

表7 各评价单元与最差参考序列的关联系数
2.6.3 计算相对关联度关联度为每一批次GLX样品中各个成分关联系数的平均值,按文献[23]相对关联度计算公式计算相对关联度,结果与最优参考序列关联度、与最差参考序列关联度和相对关联度具体数据见表8。一般相对关联度介于0~1之间,数值越大,样品综合质量最优。15批GLX样品相对关联度0.330 2~0.606 8,S11~S15分别位于排名前5位,S1~S6位于排名中间位置,S7~S10位于排名后4位。
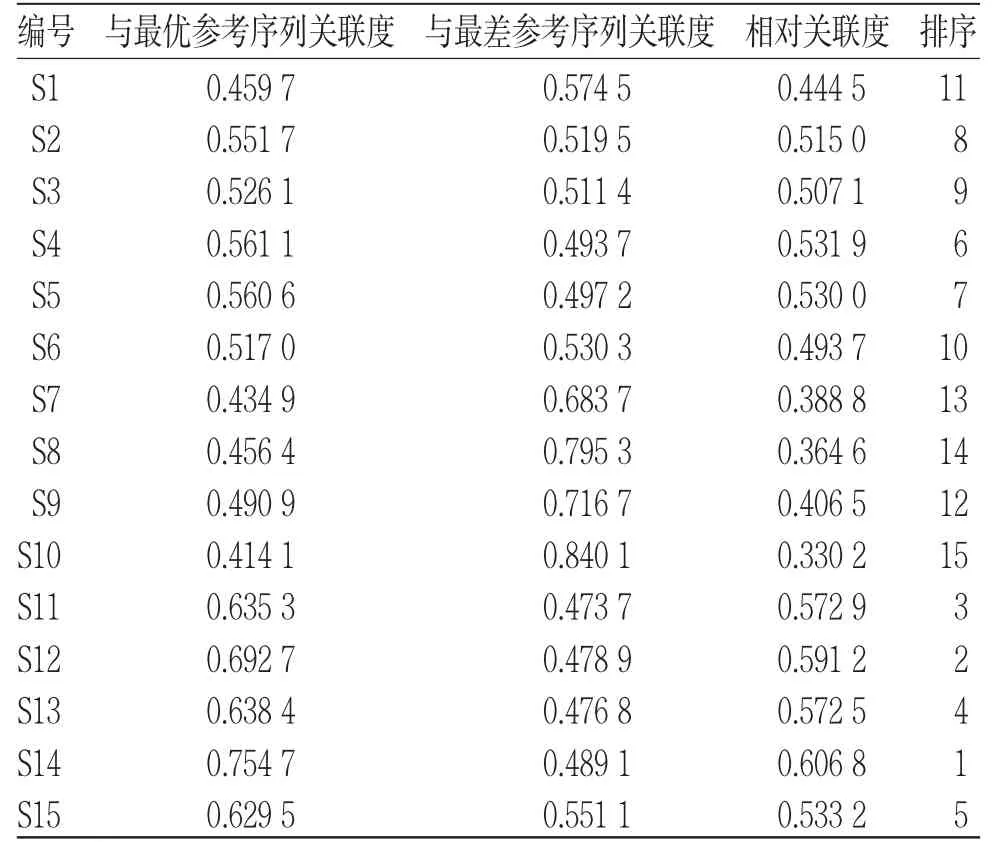
表8 15 批GLX 相对关联度排序结果
3 讨论
3.1 流动相选择 本试验考察了以乙腈为有机相,水、0.1%甲酸液、0.05%磷酸液、0.1%磷酸液、0.2%磷酸液为水相的流动相系统对GLX中的党参炔苷、紫丁香苷、鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、圆柚酮、α-香附酮、莪术二酮和莪术醇的响应值及分离效果。结果显示,以乙腈-0.1%磷酸液为流动相时,基线平稳,13种待测成分的检验用时短、峰形及峰纯度最优,响应值最大。
3.2 指标组分选择 GLX由牡蛎、香附(制)、三棱、莪术、土鳖虫、仙鹤草、党参、白术、白花蛇舌草、牡丹皮和吴茱萸11味中药材配伍而成。方中牡蛎味咸、涩,性微寒,软坚散结;香附味辛、微苦,性平,疏肝理气,调经止痛,两药合用,行气消癥,散结止痛,共为君药。三棱、莪术、土鳖虫破血逐瘀,消积止痛;党参、白术补气健脾,以资化源。各药相伍,祛瘀不伤正,扶正不留瘀,共为臣药。白花蛇舌草清热解毒,消肿止痛,伍仙鹤草、牡丹皮清热凉血,活血散瘀;佐少量吴茱萸温中散寒,防止苦寒伤脾阳,共为佐使。本方诸药相合,通补兼施,温清并用,共奏活血化瘀、软坚散结之功。本试验遵循中药质量标志物遴选原则,以君药、臣药和佐药为研究对象,选取香附活性成分香附烯酮、圆柚酮和α-香附酮,党参代表性成分党参炔苷和紫丁香苷,莪术主要成分莪术二酮和莪术醇,白花蛇舌草药效成分鸡矢藤次苷甲酯、车叶草苷酸和车叶草苷,以及牡丹皮特征成分氧化芍药苷、芍药苷和丹皮酚为指标成分。
3.3 质量评价结果分析 本试验采用HPLC法同步检测了GLX样品中13种化学组分含量,方法操作便捷,线性回归、精密度、重复性、稳定性及加样回收率均符合《中华人民共和国药典》要求,党参炔苷、紫丁香苷、鸡矢藤次苷甲酯、车叶草苷酸、车叶草苷、氧化芍药苷、芍药苷、丹皮酚、香附烯酮、圆柚酮、α-香附酮、莪术二酮和莪术醇的含量分别为0.123~0.262 mg/g、0.017 ~0.062 mg/g、0.639 ~1.094 mg/g、0.482 ~0.828 mg/g、0.600 ~1.217 mg/g、0.242 ~0.649 mg/g、0.573 ~1.048 mg/g、0.929 ~1.558 mg/g、0.340 ~0.995 mg/g、0.030 ~0.062 mg/g、0.152~0.301 mg/g、0.171~0.382 mg/g、0.104~0.202 mg/g。从含量检测结果来看,13种成分均存在一定差异,表明GLX多组分HPLC定量模式的应用对提升和稳定该制剂整体质量具有参考意义。以15批GLX样品中13种成分含量为质量评价变量,分别建立了PCA和OPLS-DA模型,对复杂的多维数据进行了降维,挖掘筛选出莪术二酮、香附烯酮、丹皮酚、车叶草苷、党参炔苷、鸡矢藤次苷甲酯、芍药苷、氧化芍药苷和车叶草苷酸对GLX质量影响较大,是影响GLX产品质量的主要标记物。同时本研究采用GRA技术,建立了GLX样品质量优劣评价模型,对评价对象进行质量排序,S11~S15分别位于排名前5位,相对关联度由大到小依次为0.606 8、0.591 2、0.572 9、0.572 5和0.533 2,S7~S10位于排名后4位,相对关联度由大到小依次为0.406 5、0.388 8、0.364 6和0.330 2,表明GRA模型可用于GLX样品质量优劣评价。
本试验所建立的HPLC多组分定量联合PCA、OPLS-DA等化学计量学以及GRA模型,操作便捷、结果准确、全面客观,所检测的13种分涵盖了处方中君、臣、佐药的大部分主要活性成分,可用于GLX综合质量评价,为该制剂质量控制提供参考。由于试验所用样品源于市场,样品数量不够大,其化学成分的差异性和关联性还需要更多批次的样品试验数据去研究。

