中枢和外周病理状态下全身麻醉敏感性的研究进展
王飒,徐赛红,俞卫锋,焦英甫
临床实践中常通过微量调整麻醉药物剂量应对个体敏感性差异,以保持稳定、安全的全身麻醉效果。但部分病理状态下麻醉敏感性的改变往往超越年龄、遗传等常见个体敏感性因素影响,令麻醉医师难以忽视。病理状态下的麻醉敏感性是在疾病自身病理生理学的基础上复合麻醉药物药效动力学和药代动力学的综合表型。疾病病理生理与麻醉药物互相作用,在部分疾病中观察到常规剂量的麻醉药物有促进疾病进展的风险[1],而疾病本身发生麻醉需求的变化可能是原因之一。不适当的麻醉剂量可能提高术中知晓、呼吸、循环系统过分抑制发生率,加重患者围术期风险,同时对疾病预后也产生不良的影响。
了解病理状态下麻醉敏感性的变化不仅能帮助临床麻醉医师实施精准麻醉,还尽可能地保障患者围术期安全并对远期预后产生积极的作用。同时从麻醉学的角度为病理状态下器官沟通机制的进一步诠释进行启发。
1 中枢神经系统疾病
中枢神经系统是麻醉药物发挥作用的主要靶器官,中枢病变的患者往往需要麻醉医师的更多注意。中枢病变不仅包括阿尔茨海默症、帕金森症等常见器质性病变;也包括睡眠障碍、抑郁、焦虑等精神类疾病。本部分就目前检索到的中枢神经系统疾病的麻醉敏感性相关研究进行一一总结。
1.1 睡眠障碍 睡眠与全身麻醉的共性和特性是麻醉领域的研究热点,睡眠障碍患者中枢神经系统的改变对麻醉药物的使用产生一定的影响。临床研究和动物实验中发现,睡眠障碍的存在可增强全身麻醉药物(静脉麻醉药物和吸入性麻醉药物)的敏感性[2-3]。Cao 等[2]使用Dixon 序贯法发现19 例睡眠障碍患者较19 例非睡眠障碍患者接受七氟烷麻醉的半数苏醒肺泡气浓度(MACawake)更高,与血清食欲素A水平升高有关。
1.2 阿尔茨海默症(Alzheimer’s Disease,AD) 目前尚无相关临床研究关注AD 患者的麻醉敏感性。多项动物研究分别检测了AD动物模型(3xTgAD小鼠[4]、A PP23 小鼠[5]及SAMP-8 小鼠[6])的全身麻醉药物敏感性,在不同的动物模型中得到的结论不尽相同。其中3xTgAD 小鼠对氟烷、异氟烷、七氟烷的MAC 值[4]及APP23 小鼠对异氟烷的MAC 值均较对照组升高[5]。在另外一项研究中使用了没有插入任何新的遗传片段、被认为可自然出现AD的病理特征的SAMP-8 小鼠进行研究,SAMP-8 小鼠对异氟烷、七氟烷和地氟烷的MAC 值显著低于对照组小鼠[6]。
1.3 自闭症 与AD 中表现类似,自闭症动物的麻醉敏感性受造模方法影响。Li 等[7]利用Shank3+/C突变小鼠模型研究一种特殊的自闭症 Phelan McDermid Syndrome 的麻醉敏感性,发现Shank3+/C突变小鼠异氟烷敏感性增高,且可能与前庭核中NR1 和脊髓中PSD95 表达下调有关。而由妊娠大鼠注射丙戊酸钠诱导的新生自闭症大鼠接受右美托咪定或丙泊酚麻醉时均表现为较对照组的翻正反射消失(loss of righting reflex,LORR)时间延长和翻正反射恢复(recovery of righting reflex,RORR)时间缩短[8],基因表达定量分析表明该模型的海马-氨基丁酸A 型受体( -aminobutyric acid type A receptor,GABAA)基因表达低于对照组,而N-甲基-M-天冬氨酸(N-methyl-D-aspartate,NMDA)基因表达高于对照组。临床研究为自闭症麻醉敏感性提供了更直接的证据:在接受听觉脑干反应测试时,自闭症患者对丙泊酚的需求量更高[9]。
1.4 罕见病 部分研究探索了一些罕见疾病中的麻醉敏感性。例如导致肌营养不良症1 型(Myotonic dystrophy type 1,DM1)中枢系统症状肌肉束蛋白样蛋白2(MBNL2)[10]。在标准地西泮剂量下,Mbnl2 KO 小鼠LORR 的比例也明显高与对照组。另外,导致线粒体疾病的Ndufs4 基因[11]也可影响麻醉药物的剂量。Nduf4 KO 小鼠吸入异氟烷的MAC 值明显低于其他组别,且更容易出现呼吸抑制。
1.5 中枢神经系统药物 临床上多种神经系统疾病患者可能接受抗癫痫药物的治疗。Ouchi[12]报道抗癫痫药物的数量和种类会影响丙泊酚的剂量需求,其中丙戊酸钠和氯巴扎姆可减少丙泊酚的剂量需求,而苯巴比妥则会增加异丙酚的剂量需求。目前中枢神经系统疾病的麻醉敏感性相关研究主要以动物研究为主,临床研究数量较少。而中枢神经系统疾病较为复杂,动物模型种类多,各有优势。不同动物模型得到的麻醉敏感性变化结论尚不能为临床提供直接指导,但仍能为疾病病理生理变化本身和麻醉药物机制的研究提供线索。而抑郁、焦虑等临床常见疾病的麻醉敏感性是否发生改变仍待解答。
2 外周疾病
近年来中枢-器官交互作用发展迅速,神经-内分泌-免疫网络、脑-肝轴、脑-心轴理论一定程度上解释了外周疾病麻醉敏感性变化的原因。本部分对部分系统性疾病、外周单器官病变以及肿瘤的麻醉敏感性进行综述。
2.1 外周系统性疾病
2.1.1 糖尿病 糖尿病是多器官、多系统代谢疾病,涉及消化系统、运动系统及中枢、周围神经系统。糖尿病对于镇痛、肌松、局部麻醉和全身麻醉药物均发生明显的改变,本文仅对其全身麻醉药物的改变进行总结。1993 年,Brain 等[13]观察到糖尿病可提高动物吸入性麻醉药物敏感性;Janicki 等[14]进一步研究发现糖尿病动物接受氟烷、异氟烷和恩氟烷麻醉时MAC 均有一定程度的降低。随后Ohsawa 等[15]发现糖尿病动物接受丙泊酚麻醉持续时间与对照组并无差异,而Leal 等[16]发现糖尿病动物中丙泊酚的药效动力学具体表现为丙泊酚起效剂量、总分布量和未结合分布量均降低,具体的机制可能与血糖-胰岛素平衡的中枢作用有关。动物研究显示胰岛素治疗可逆转糖尿病吸入性麻醉药物敏感性的现象[13,17],短时间的运动情况也可使其恢复,但急性高血糖并不会对大鼠MAC 造成影响[18]。这些结果直接或间接证明了胰岛素降低大鼠的异氟醚MAC,而与血糖浓度无关。
2.1.2 肥胖 体质量指数是临床较常使用的调整麻醉药物用量的指标之一,最近的研究也报道了中枢-脂肪代谢通路[19]。但多项临床试验和动物研究均表明,病理性肥胖或代谢综合征并不会改变全身麻醉药物的敏感性[20-21]。
2.2 单器官疾病
2.2.1 心脏疾病 近年来针对外周系统的药物在改善AD 患者的认知功能甚至预防AD 的发展方面取得了一定的进展[22],进一步揭示了脑-心轴的作用。动物研究报道了心脏疾病中的麻醉敏感性。在压力诱导的超负荷左心室肥大大鼠中,氟烷、异氟烷和七氟烷的MAC 值并无变化。而在充血性心力衰竭的大鼠中,氟烷和异氟烷的MAC 值显著增加,七氟烷并无变化[23]。
2.2.2 肝脏疾病 脑-肝轴是消化系统与中枢交流的关键机制[24]。作为麻醉药物的代谢中心,肝脏病变是否及如何影响麻醉药物得到了大量的研究。肝硬化的临床和动物研究中均观察到丙泊酚敏感性的增高,可能与肝纤维化程度、血氨浓度、抑制性及兴奋性神经递质失衡有关[25-26]。肝脏疾病的麻醉敏感性改变不仅是由于丙泊酚的肝内代谢途径受阻,以胆红素为代表的代谢物对于中枢的直接作用也是麻醉敏感性改变的重要机制之一。梗阻性黄疸的相关研究表明,胆红素可直接对中枢神经系统作用以改变麻醉敏感性。临床研究发现,梗阻性黄疸患者吸入性麻醉药物敏感性增加[27-28],胆红素对大脑神经递质释放过程的调节、对突触前膜Ca2+内流以及突触传递过程中抑制性神经递质GABA 和甘氨酸的释放可能是导致麻醉剂需求量减少的原因[29-30]。以脑-肝轴的角度阐释肝硬化、酒精性肝病等疾病的发病机制研究已得到一定进展,肝脏疾病的中枢变化对麻醉学的影响同样值得讨论。
2.2.3 胃肠道疾病 目前鲜少研究报道胃肠道疾病的麻醉敏感性是否改变,国内一项临床研究表明克罗恩病患者行无痛胃肠镜时对丙泊酚的需求量高于正常体检患者[31],但克罗恩病病程中反复经历丙泊酚诱导胃肠镜检查,克罗恩病自身病理生理是否影响全麻药物的效应和代谢等过程仍值得进一步研究。
2.3 外周器官衰竭 外周器官衰竭患者往往伴随神经和精神系统功能障碍,麻醉敏感性变化更为明显。与正常肾功能的患者相比,终末期肾病患者的七氟烷MACawake 值较低[32],终末期肝病患者的七氟烷MAC 值同样低于正常患者[33]。此类疾病普遍伴随神经毒性代谢产物的累积,如神经特异性烯醇化酶(neuronspe-cific enolase,NSE)、肌酐、尿素氮等,这些代谢产物可能通过影响麻醉药物中枢靶点如神经递质受体以改变麻醉药物的效力[34]。而从轻微病变逐渐发展至器官衰竭的过程中,此类代谢产物何时开始影响患者所需麻醉药物的种类及剂量仍值得探讨。
2.4 外周肿瘤 手术是肿瘤的重要治疗方法,麻醉药物可能增加肿瘤的侵袭、转移[1]。因此,按需给予对于肿瘤患者十分重要。随着肿瘤患病率的持续上升和早期诊断率的提高[35],接受麻醉的肿瘤患者日益增多,笔者认为有必要对此类情况进行归纳总结。近年来多项临床研究聚焦于肿瘤患者的麻醉敏感性,包括乳腺癌[36-38]、肺癌[39]、胃肠道肿瘤[40-42]、肝癌[43]及卵巢癌[44]等,从多项指标讨论了新辅助化疗是否影响麻醉药物的使用,见表1。而鲜少研究提及单纯荷瘤状态是否影响麻醉药物使用。在新辅助化疗影响麻醉敏感性的研究中,乳腺癌报道最多,术前新辅助化疗的乳腺癌患者对多种麻醉药物(丙泊酚、异氟烷、吗啡)的敏感性增高[37,45]。Linganna 等[37]认为紫杉类药物可能通过改变微管稳定性降低了对部分麻醉药物的敏感性,而在有些报道新辅助化疗药物并不影响丙泊酚的效应浓度(effect concentration,Ce)值[36]。
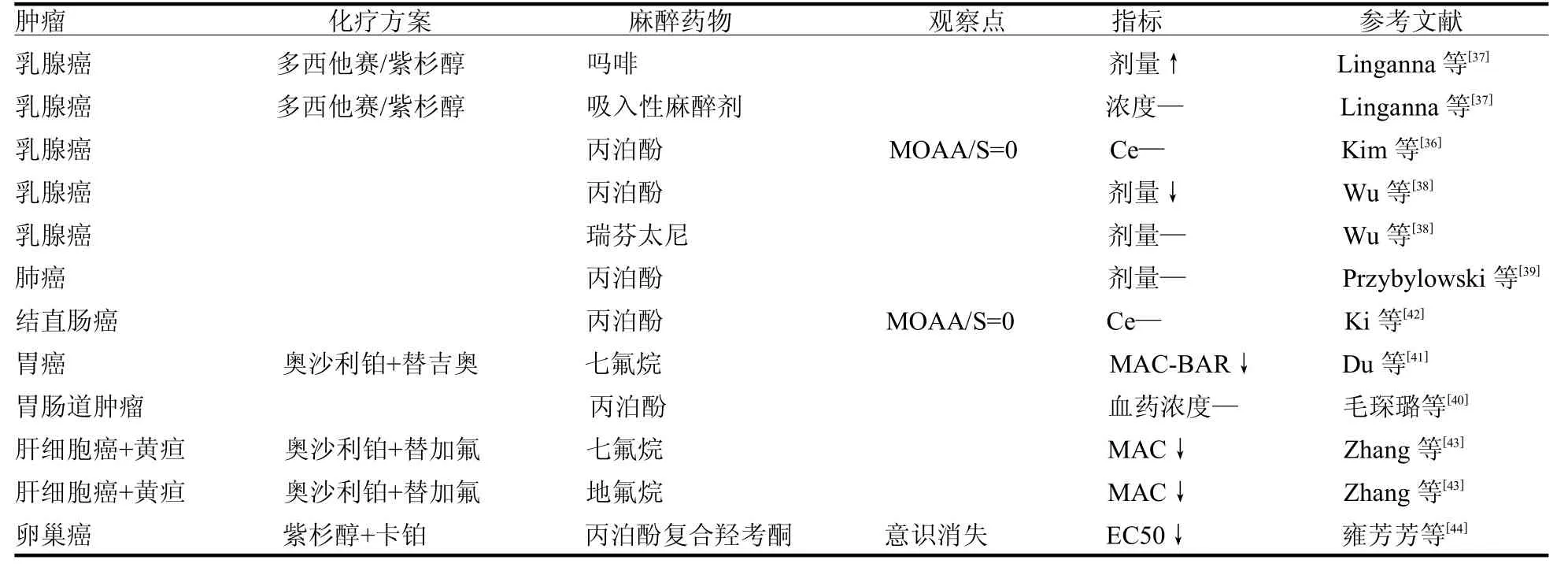
表1 肿瘤种类及新辅助化疗方案对麻醉药物用量的影响
化疗药物的肝肾功能损害及神经毒性常被提及[46],但其是否及如何影响麻醉药物的使用尚未清晰。Jung[47]认为此类研究单一地从化疗药物的神经毒性或现象来分析并不十分准确,科学地对肿瘤患者人群进行PK/KD 分析是改善麻醉药物临床安全性的关键。
3 总结
全身麻醉占据临床麻醉方法中的绝大多数。本文总结了中枢和外周不同病理状态下的全身麻醉药物敏感性情况,见图1。以中枢-外周器官互作出发的围术期脑保护逐渐进入人们视野,强调精准麻醉实施必要性的同时也显示出多器官系统性保护的重要性。
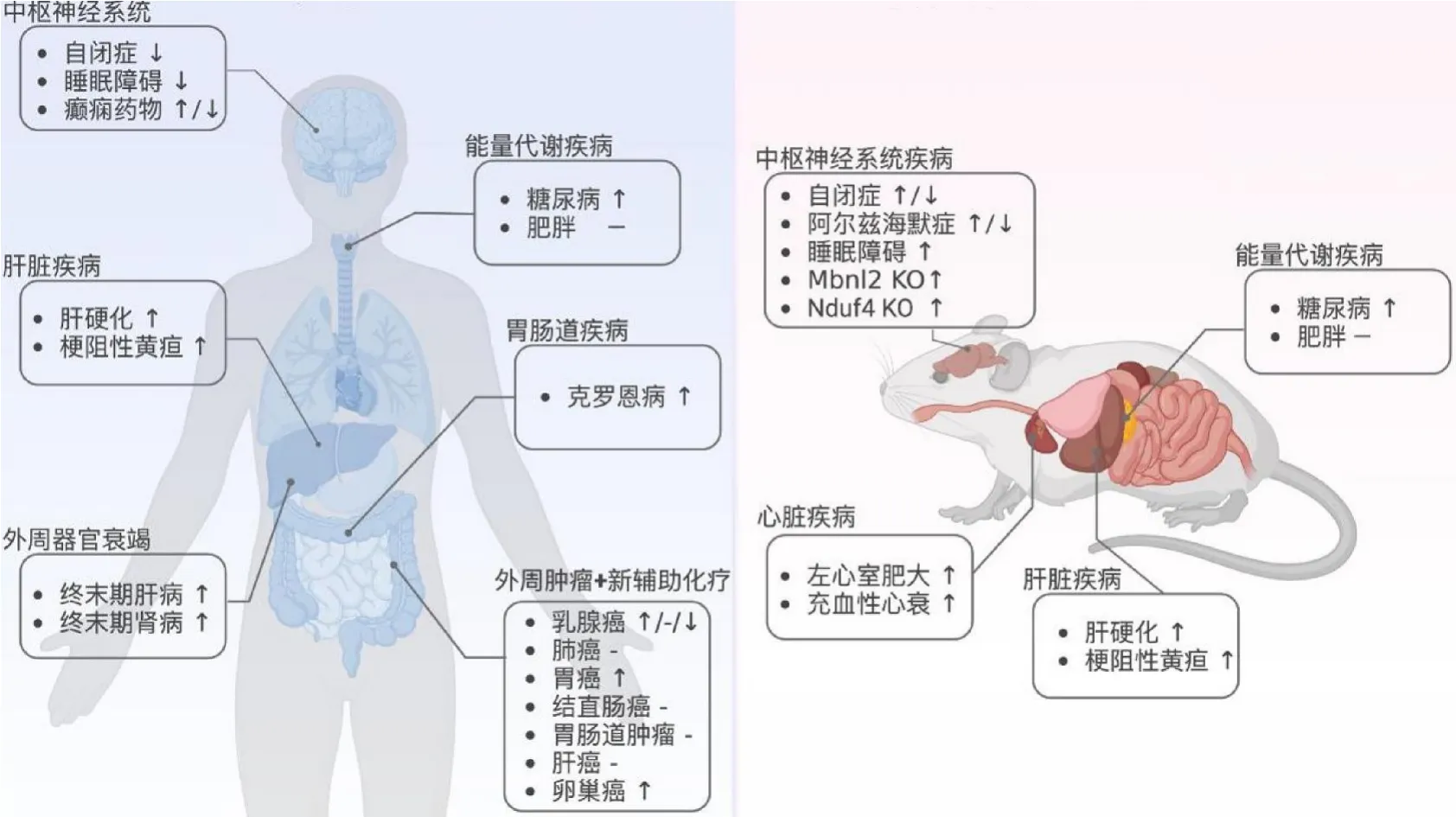
图1 中枢和外周病理状态下的麻醉敏感性
在目前发表的研究中,笔者注意到动物研究和临床研究麻醉敏感性结论相悖的现象,提示临床实际调查病理状态麻醉敏感性的重要性。而调查过程使用的评估方法和指标同样需要慎重选择。
麻醉科的目标不仅是完成术中麻醉和术后镇痛,如何改善患者预后是麻醉科同其他科室共同努力的方向。围术期脑保护是麻醉科需承担的任务之一,用合适的药物种类和剂量增强围术期脑保护、改善患者预后是麻醉医生的理想目标。另一方面笔者也看到一些研究从相对简单的病理状态出发加深人们对全麻机制的理解,此类研究很可能在未来开启全麻机制解析的新局面。
利益冲突 所有作者声明无利益冲突

